HIFU-гемиабляция у пациентов с локализованными формами рака предстательной железы
Автор: Абоян И.А., Галстян А.М., Бадьян К.И., Пакус С.М.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Экспериментальная урология
Статья в выпуске: 1, 2018 года.
Бесплатный доступ
Цель исследования. оценка онкологических и функциональных результатов HIFU-гемиаблации у пациентов с локализованными формами рака предстательной железы (РПЖ). Материалы и методы. Исследовательская работа основана на сравнительной оценке результатов лечения больных локализованным РПЖ методом HIFU в объеме тотальной аблации и гемиаблации. В период с 2011 по 2017 гг. в условиях хирургического отделения №1 МБУЗ КДЦ «Здоровье» г. Ростова-на-Дону проводилось лечение пациентов локализованным РПЖ высокоинтенсивным сфокусированным ультразвуком с использованием аппарата SONOBLATE 500 V5 TCM. Лечение проведено 250 пациентам. Все пациенты были разделены на две группы в зависимости от объема проведенной аблации. Пациентам 1-й группы (200 человек) выполнено лечение методом HIFU в объеме тотальной аблации предстательной железы (ПЖ), пациентам 2-й группы (50 человек) оперативное вмешательство проведено в объеме гемиаблации. Результаты. По данным наблюдения надир ПСА пациентов в исследуемых группах отмечен к 3 месяцам наблюдения и составил в первой группе-0,8нг\мл, во второй группе - 1,4нг/мл. В группе пациентов после тотальной аблации биохимический рецидив диагностирован у 28 %, в группе гемиаблации - у 20%. Гистологический рецидив заболевания выявлен у 12 % пациентов первой группы, в 10% случаев у пациентов второй группы. По данным исследования, функциональные результаты (индекс МИЭФ-5, IPSS, VAS, QOL) были достаточно высокими в группе пациентов после HIFU-гемиаблации. Заключение. HIFU-гемиаблация у пациентов с локализованными формами РПЖ при соблюдении строгих критериев отбора является высокоэффективным методом лечения, позволяющим добиться высоких функциональных и онкологических результатов.
Локализованный рак предстательной железы, высокоинтенсивный сфокусированный ультразвук, гемиаблация
Короткий адрес: https://sciup.org/142213142
IDR: 142213142
HIFU hemiablation in patients with localized prostate cancer
The aim of the study: was to evaluate oncological and functional results of HIFU hemiablation in patients with localized prostate cancer. Materials and methods. The study was based on comparative evaluation of the results of treating patients with localized prostate cancer with HIFU (complete ablation and hemiablation). Over the period of 2011-2017, 250 patients with localized prostate cancer underwent treatment with high intensity focused ultrasound using the SONOBLATE 500 V5 TCM system in the conditions of the department of surgery of the Clinical Center Zdorovie (Rostov-on-Don). All patients were divided into two groups, depending on the volume of ablation performed. The patients from the f irst group (n=200) underwent HIFU by complete ablation of the prostate; patients from the second group underwent hemiablation. Results. According to the screening, PSA nadir was observed by the third month of the trial (0.8 ng/ml in the first group and 1.4 ng/ml in the second). Biochemical recurrence was diagnosed in 28% of patients after complete ablation and in 20% of patients from the hemiablation group. Histological recurrence was observed in 12% and 10% of patients from the first and the second groups, respectively. According to the data obtained, functional results (IIEF 5 index and IPSS, VAS, QOL scales) were high enough in patients after HIFU hemiablation. Conclusion. HIFU hemiablation is a highly effective method for treating patients with localized prostate cancer, if strict selection criteria are applied. This helps to achieve successful functional and oncological outcomes.
Текст научной статьи HIFU-гемиабляция у пациентов с локализованными формами рака предстательной железы
ак предстательной железы (РПЖ) является наиболее часто выявляемым злокачественным новообразованием (ЗНО) в мире среди мужского населения и находится на третьем месте по распространенности среди всех ЗНО в целом. По данным мировой статистики в 2012 году самые высокие показатели заболеваемости РПЖ отмечены в Австралии и Новой Зеландии, самые низкие – в Южной и Центральной Азии, в Европе наиболее высокая частота РПЖ отмечена в Норвегии, самая низкая – в Албании [1,2].
По данным А.Д. Каприна и соавт. распространенность РПЖ в России за период с 2005 – 2015 гг. увеличилась в 3 раза. Из зарегистрированных в 2016 году 38 042 пациентов с диагнозом РПЖ доля больных с опухолевым процессом I стадии составила 11,4%, II стадии – 43,8%; III стадии – 27,4%; IV стадии – 15,9%. В 1,6% случаев стадия заболевания не была установлена. Летальность на первом году с момента установления диагноза составила 8%. Отношение показателей одногодичной летальности и запущенности онкологического процесса при РПЖ в 24 регионах России в 2015 г. равнялось или превышало 0,7 (среднероссийский показатель в
2014 г. 0,53). Индекс накопления контингента больных с РПЖ в России в 2015 г. составил 5,3% в сравнении с 3,8% в 2005 г. [3].
Благодаря широкому внедрению скрининга РПЖ в мире большая часть обнаруживаемых ЗНО предстательной железы (ПЖ) на сегодняшний день являются локальными [4].
В последние годы возросло количество публикаций, подтверждающих, что новые малоинвазивные методы лечения РПЖ позволяют предотвращать прогрессирование заболевания ПЖ и дают меньшее количество осложнений [5-8].
Следует отметить, что цель малоинвазивных стратегий лечения РПЖ, принимая во внимание биологические свойства злокачественных новообразований данной локализации, состоит в предотвращении прогрессирования заболевания, его лечении и контроле, сводя к минимуму побочные эффекты лечения [7,8].
Ультразвуковая аблация (HIFU) ПЖ является методом выбора лечения пациентов локализованным РПЖ и может быть использована также у пациентов, имеющих противопоказания для выполнения радикальной простатэктомии и у пациентов с доказанным местным рецидивом после проведенного ранее лечения. В настоящее время метод HIFU-гемиаблации может быть использован в качестве фокального лечения РПЖ. При этом онкологические результаты в отдаленном периоде сопоставимы с результатами тотальной аблации, а за счет сохранения ткани ПЖ, не подвергшейся ультразвуковой аблации, отмечены лучшие функциональные результаты [9,10].
Фокальная HIFU-гемиаблация РПЖ предполагает локальное прицельное энергетическое воздействие на опухолевый очаг с целью сохранения части ПЖ, не вовлеченной в опухолевый процесс [9]. Целью фокальной терапии РПЖ является выборочное разрушение очага злокачественного новообразования ПЖ с сохранением интактной ткани. Критерии и методы отбора кандидатов для фокальной терапии РПЖ могут варьировать в зависимости от объема образования, подлежащего разрушению, а также группы риска, к которой относится пациент [10, 11].
Группой ученых, учитывая гетерогенность характера РПЖ, объем поражения ПЖ, а также сопоставление уровня ПСА и объема ПЖ, разработано понятие «index lesion», которое является основополагающим при диагностике унифокального и унилатерального поражения, позво- ляя отобрать больных для выполнения фокального лечения установленного опухолевого очага [12,13].
Метод гемиаблации ПЖ был разработан для воздействия на одну из долей ПЖ при подтвержденном унифокальном, либо унилатеральном поражении с учетом верифицированного «index lesion» [14].
Основным условием эффективности фокальной терапии является обнаружение клинически значимого очага опухоли. Для этого необходимо применение комплекса высокоточных современных методов обнаружения РПЖ как в пораженной, так и в противоположной доле ПЖ, в частности мультипара-метрической магнитно-резонансной томографии (МпМРТ) (PIRADS-V2), новых схем выполнения промежностной биопсии ПЖ, гистосканирования и т.д. [15-17].
Таким образом, необходимо отметить, что в настоящее время ультразвуковая гемиаблация ПЖ имеет все возможности внедрения в клиническую практику, однако требуется проведение исследований, направленных на стандартизацию методики проведения данной процедуры, а также последующей оценки онкологических и функциональных результатов, с целью определения места данного метода в стратегии органосохраняющего лечения рака предстательной железы.
Целью работы явилась оценка онкологических и функциональных результатов HIFU-гемиаблации у пациентов с локализованными формами рака предстательной железы.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
В период с 2011 по 2017 годы в условиях хирургического отделения №1 МБУЗ КДЦ "Здоровье" г. Ростова-на-Дону проводилась HIFU-аблация у пациентов с локализованным РПЖ. Лечение проведено 250 пациентам, из них 200 больным выполнено лечение методом HIFU в режиме тотальной аблации (группа тотальной аблации), 50 пациентам лечение проведено в объеме HIFU-гемиаблации (группа гемиаблации).
Отбор пациентов для проведения фокальной гемиаблации проводился на основании Руководства Европейской ассоциации урологов 2013 г., согласно которому оптимальным кандидатом для данного вида лечения является пациент с локализованным РПЖ низкого и среднего риска с изолированным уни-фокальным или унилатеральным поражением. Предпочтение отдается пациентам с ПСА <10 нг/мл, суммой баллов по Глисону <7, клинической стадией РПЖ <Т2b, количеством положительных биоптатов <4 и процентным распространением опухоли <50% в одном био-птате. К потенциальным кандидатам могут быть отнесены пациенты с РПЖ низкого риска, которым показано активное наблюдение.
Диагноз РПЖ у всех пациентов был подтвержден морфологически после выполнения полифокальной биопсии ПЖ. Пациентам из группы гемиаблации выполнялась промежностная 24-точечная биопсия, при необходимости количество биопта-тов ПЖ увеличивалось.
Сравнение медиан в группах проводилось с помощью теста Манна-Уитни и теста Фишера. Различия признавались статистическими значимыми при p <0,05. Расчеты выполнялись в статистической программе R (версия 3,2 R Foundation for Statistical Computing, Vienna, Austria).
Лечение РПЖ с использованием высокоинтенсивного сфокусированного ультразвука проводилось на аппарате для HIFU терапии Sona-blate® 500 V5 ТСМ. Нами применялась разработанная в клинике методика гемиаблации РПЖ [18]. Этап планирования проводился с учетом данных предоперационной биопсии ПЖ, результатов Мп-МРТ и заключался в маркировке плана лечения. Диапазон планируемого лечения находился в границах от латерального контура пораженной доли до транзиторной зоны с отступлением от верхушки не менее 5 мм до базальных отделов. Производился интраоперационный контроль состояния капсулы ПЖ с целью оценки динамических изменений ее структуры при проведении лечения. Время аблации зависело от объема пораженной доли ПЖ. При проведении разметки зоны аблации латеральными границами являлись зона простатического отдела уретры и латеральная поверхность предстательной железы. Результат воздействия в каждой точке оценивался с помощью уровня температурной реакции тканей при этом в ходе лечения для достижения максимальной температуры тканей (между 65°C и 100°C) в зоне целевой аблации проводилась коррекция мощности акустического сигнала. Для визуальной оценки эффективности проведенной аблации тканей выполнялись сравнительные контрольные ультразвуковые сканирования ПЖ интактной и «пролеченной» долей ПЖ. При проведении гемиаблации нами использовались только стандартные циклы лечения. Важным моментом в процессе лечения являлась необходимость контроля за расстоянием от трансдьюсера ультразвукового проба до стенки прямой кишки.
При проведении процедуры гемиаблации использовалось программное обеспечение аппарата Sonablate – TCM (tissue control monitoring), созданное для получения обратной связи и контроля хирургом не только уровня поглощенной энергии, но и определения эффективности аблации. В зависимости от динамики изменяемых параметров производился подбор интервалов аблации. В связи с вариабельностью анатомии ПЖ, риском интраоперационного отека и изменением контура ПЖ в ходе операции нами производился промежуточный контроль положения ПЖ после аблации не более 25% заданного объема ткани.
В связи с отсутствием необходимости выполнения цистостомии, а также быстрой реабилитации пациентов после гемиаблации, выписку больных из стационара производили на 4 день после операции. Основным критерием оценки эффективности операции при послеоперационном мониторинге являлась динамика уровня ПСА. Контроль уровня ПСА осуществлялся каждые 3 месяца после лечения в течение первого года наблюдения, затем один раз в течение 6 месяцев наблюдения.
После проведенного лечения осуществлялся мониторинг функциональных результатов с использованием валидизированных шкал. Использовались следующие шкалы: визуальная аналоговая шкала (VAS), шкала оценки симптомов заболеваний предстательной железы с индексом качества жизни (IIPSS+QL) международный индекс эректильной функции (МИЭФ), а также шкала оценки удовлетворенности пациента перенесенным оперативным вмешательством (EPIC).
Биохимическая прогрессия оценивалась согласно критериям ASTROPhoenix (надир ПСА+2 нг/мл). При этом необходимо отметить, что в случае HIFU- гемиаблации, при наличии интактной ткани в доле предстательной железы, не подвергающейся воздействию, уровень ПСА не всегда может прогностически свидетельствовать о рецидиве заболевания. В связи с указанным выше, рекомендуем выполнение контрольной промежностной биопсии ПЖ пациенту после гемиаблации при динамическом увеличении уровня ПСА.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При проведении сравнительной возрастной характеристики пациентов значительных расхождений между группами не выявлено. Так, в группе тотальной аблации средний возраст пациентов составил 71,7 лет, в группе гемиаблации – 72,2 года, наибольшее количество больных в обеих группах были в возрасте 7074 лет (рис. 1).
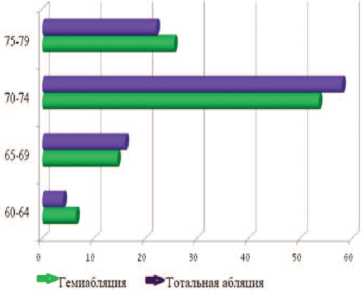
Рис. 1. Распределение пациентов в группах исследования по возрасту в %
При анализе зональной локализации РПЖ нами выявлено, что в обеих группах преобладали пациенты с новообразованиями в периферической зоне органа: 68,5% в группе тотальной аблации и 72% – в группе гемиаблации. Около 20% процентов опухолей у пациентов обеих групп локализовалось в пере-
Таблица 1. Распределение пациентов в группах исследования по стадиям заболевания согласно классификации TNM
|
TNM |
Группа тотальной аблации |
Группа фокальной гемиабла- |
||
|
Абс. число |
% |
Абс. число |
% |
|
|
T2аNх-M0 |
59 |
29,5 |
27 |
54 |
|
T2bNx-M0 |
43 |
21,5 |
23 |
46 |
|
T2cNx-M0 |
98 |
49 |
0 |
0 |
|
Всего |
200 |
100 |
50 |
100 |
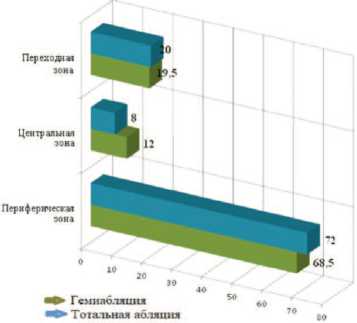
Рис. 2. Распределение пациентов (%) в группах исследования по локализации патологического процесса в различных зонах предстательной железы ходной зоне ПЖ. У меньшего количества пациентов очаг поражения диагностирован в центральной зоне ПЖ: у двух (12%) пациентов –в группе тотальной аблации ПЖ и у 4 (8%) – в группе гемиаблации (p>0,05) (рис. 2). Локализация опухоли не являлась критерием для выбора способа лечения.
Нами также проанализировано распределение пациентов, вошедших в группу тотальной абляции ПЖ, по стадиям заболевания согласно классификации TNM: стадия T2сNХM0 диагностирована у 98 (49%) пациентов, стадия T2аNХM0 – у 59 (29,5%), стадия T2bNХM0 у 43 (21,5%) пациентов. В группе пациентов, перенесших фокальную гемиаблацию ПЖ, у 27 (54%) человек диагностирована T2аNХM0 стадия заболевания, у 23 (46%) пациентов – T2bNХ-M0. (табл. 1)
Основные результаты доопера-ционного обследования пациентов обеих групп представлены в таблице 2. Группы пациентов имели сопоставимые показатели уровня ПСА, индекса Глисона, G опухоли. Имели место отличия объема ПЖ, очаговости поражения, а также результатов гистосканирования.
Проведена сравнительная оценка онкологических и функциональных результатов, полученных в 2-х группах. Медиана наблюдения составила 3 года. Мониторинг пациентов в исследуемых группах проводился с учетом динамики уровня ПСА, а именно nadir (отмеченного минимального его уровня в динамике). Данный показатель в группе с тотальной аблацией в среднем со- ставил 0,8 нг/мл, в группе гемиаблации – 1,48 нг/мл (p<0,001). Гистологический и биохимический рецидив отмечен у 12% и 28% группе тотальной аблации и 10% и 20% – в группе гемиаблации, соответственно.
Повторная биопсия выполнена всем пациентам в группе гемиаблации, а в группе тотальной аблации пациентам с биохимическим рецидивом согласно критериям Феникс, таких пациентов в группе тотальной аблации было 32 (16%).
В группе гемиаблации проведена оценка функциональных результатов лечения с использованием валидизированных шкал, являющихся субъективными шкалами оценки пациентом удовлетворенности проведенным лечением, ком-плаэнтности к лечению и адаптации пациента к дооперационным показателям жизни, выраженная в баллах у больных.
В группе пациентов после гемиаблации основные последствия лечения, связанные с неудовлетворенностью оперативным лечением, болевыми ощущениями, дизуриче-скими явлениями и другими ощущениями дискомфорта стабилизируются к 4 неделе послеоперационного наблюдения (рис. 3).
На рисунке 4 представлены показатели в динамике Международного индекса эректильной функции.
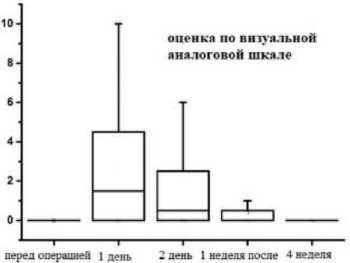
Рис. 3. Показатели шкалы VAS – Международной аналоговой шкалы адаптации пациента после перенесенного оперативного лечения в группе гемиаблации
В группе пациентов с гемиаблацией полученные данные показывают, что к 4-й неделе наблюдения показатели, связанные с эректильной функцией, могут достигать доопера-ционных параметров.
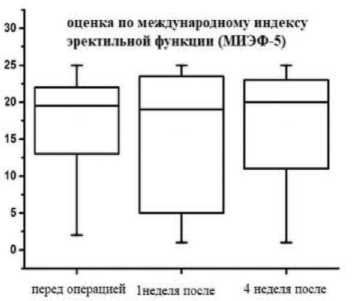
Рис. 4. Оценка в динамике показателей Международного Индекса Эректильной дисфункции (МИЭФ-5), выраженная в баллах в группе гемиаблации
На рисунках 5,6 представлены показатели качества мочеиспуска- ния пациентов в группе гемиаблации в динамике. Согласно оцениваемым шкалам в динамике через 4 недели расстройства мочеиспускания (IPSS), качество жизни (QоL), половой и мочевой функции по шкале (EPIC) у пациентов данной группы стабилизируются на дооперацион-ных показателях.
Таблица 2. Предоперационные показатели пациентов исследуемых групп
|
Показатель |
Группа тотальной аблации |
Группа фокальной гемиаблации |
|
|
Объем предстательной железы (см3) |
28,6 см3 |
42 см3 |
|
|
Очаговости поражения по данным Мп-МРТ |
Унифокальное |
84% |
85% |
|
Мультифокальное |
16% |
15% |
|
|
Индекс Глисона 6 (3+3) |
100% |
100% |
|
|
Grade 1 (ISUP 2014) |
100% |
100% |
|
|
Процент поражения в пределах биоптата |
50-80% |
0-50% |
|
|
Поражение одной доли по данным биопсии |
12% |
100% |
|
|
Перинеальная инвазия (процент пациентов) |
3% |
0% |
|
|
Уровень ПСА 0-10 нг/мл |
100% |
100% |
|
|
Гистосканирование |
2 и менее очагов в пределах каждой доли |
19% |
0% |
|
ПЖ |
2 и более очагов в пределах одной доли |
81% |
100% |
Оценка функциональных результатов также проводилась по Шкале EPIC, которая характеризует состояние половой функции, проявления дисфункции мочевой системы, выраженные в процентах. Оценка основных показателей функционирования мочевой и половой системы пациентов в группе гемиаблации согласно представленной шкале показывает относительно высокие показатели (80-100%) к 1 году наблюдения (рис. 7).
По данным комплексной оценки представленных ранее функциональных результатов лечения пациентов в группе гемиаблации можно говорить о том, что все пациенты
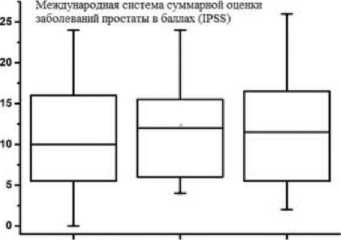
Рис.5. Оценка в динамике показателей, связанных с мочеиспусканием согласно опросника IPSS в группе пациентов с гемиаблацией перед операцией ] неделя после 4 неделя после
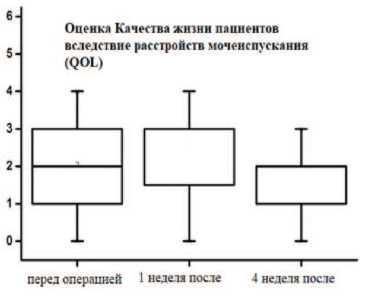
Рис. 6. Оценка в динамике показателей качества жизни пациентов QоL в группе гемиаблации

Рис.7. Оценка показателей половой функции в динамике у пациентов в группе гемиаблации (%)
остались удовлетворены проведенным вмешательством. Пациенты группы гемиаблации испытывали в послеоперационном периоде минимальные болевые ощущения, симптомы дизурии и умеренный болевой синдром. При этом эректильная функция у пациентов указанной группы соответствовала доопера-ционным показателям уже к году после лечения.
Представленные данные оценки функциональных результатов гемиаблации ПЖ и удовлетворенности проведенной операцией, говорят о высоких показателях данного вида вмешательства (рис. 8).
По данным наблюдения надир ПСА пациентов в исследуемых группах отмечен к 3 месяцам наблюде-
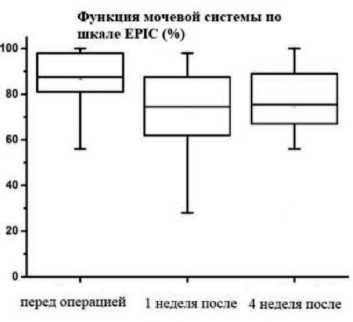
Рис. 8. Оценка в динамике функции мочевой системы у пациентов в группе гемиаблации (%)
ния и составил в первой группе – 0,8 нг/мл, во второй группе – 1,4 нг/мл. В группе пациентов после тотальной аблации биохимический рецидив диагностирован у 28%, в группе гемиаблации – у 20%. Гистологический рецидив заболевания выявлен у 12 % пациентов первой группы, в 10% случаев у пациентов второй группы. Сопоставление он-кологичес-ких показателей в обеих группах, HIFU-гемиаблация продемонстрировало сопоставимые результаты.
Таким образом, HIFU-гемиаблация у пациентов с локализованным РПЖ показывает высокие функциональные результаты, снижая сроки реабилитации после оперативного лечения.
ЗАКЛЮЧЕНИЕ
Резюме:
Цель исследования. оценка онкологических и функциональных результатов HIFU-гемиаблации у пациентов с локализованными формами рака предстательной железы (РПЖ).
Материалы и методы. Исследовательская работа основана на сравнительной оценке результатов лечения больных локализованным РПЖ методом HIFU в объеме тотальной аблации и гемиаблации. В период с 2011 по 2017 гг. в условиях хирургического отделения №1 МБУЗ КДЦ «Здоровье» г. Ростова-на-Дону проводилось лечение пациентов локализованным РПЖ высокоинтенсивным сфокусированным ультразвуком с использованием аппарата SONOBLATE 500 V5 TCM. Лечение проведено
Список литературы HIFU-гемиабляция у пациентов с локализованными формами рака предстательной железы
- Ferlay J, Soerjomataram I, Ervik M, et al. GLOBOCAN 2012 v1.0, Cancer Incidence and Mortality Worldwide: IARC CancerBase No. 11 . Lyon, France: International Agency for Research on Cancer; 2013. URL: http://globocan.iarc.fr(link is external), accessed December 2013.
- Ferlay J, Steliarova-Foucher E, Lortet-Tieulent J, Rosso S, Coebergh JW, Comber H, et al. Cancer incidence and mortality patterns in Europe: Estimates for 40 countries in 2012. Eur J Cancer 2013;49(6):1374-403 DOI: 10.1016/j.ejca.2012.12.027
- Каприн А.Д., Старинский В.В., Петрова Г.В. Состояние онкологической помощи населению России в 2016 году. М., 2017. 236 c.
- Patel MP, Schulman A, Shah KP, Anderson JB, Polascik TJ. Engaging the primary care community to encourage appropriate prostate cancer. Ther Adv Urol 2017;10(1):11-16 DOI: 10.1177/1756287217735799
- Ganzer R., Fritsche H.M., Brandtner A. Fourteen-year oncological and functional outcomes of high-intensity focused ultrasound in localized prostate cancer. BJU Int 2013;112:322-329 DOI: 10.1111/j.1464-410X.2012.11715.x
- Lukka H, Waldron T, Chin J. High-intensity focused ultrasound for prostate cancer: a systematic review. Clin Oncol R Coll Radiol 2011;23:117-127 DOI: 10.1016/j.clon.2010.09.002
- Ahmed HU, Hindley RG, Dickinson L, Freeman A, Kirkham AP, Sahu M, et al. Focal therapy for localised unifocal and multifocal prostate cancer: a prospective development study. Lancet Oncol 2012;13(6):622-32. doi: 10.1016/S1470-2045(12)70121-3
- Durand M, Barret E, Galiano M, Rozet F, Sanchez-Salas R, Ahallal Y, et al. Focal cryoablation: a treatment option for unilateral low-risk prostate cancer. BJU Int 2014 Jan;113(1):56-64 DOI: 10.1111/bju.12370
- Van Velthoven R, Aoun F, Marcelis Q, Albisinni S, Zanaty M, Lemort M, et al. A prospective clinical trial of HIFU hemiablation for clinically localized prostate cancer. Prostate Cancer Prostatic Dis. 2016;19(1):79-83 DOI: 10.1038/pcan.2015.55
- Taneja SS, Mason M. Candidate selection for prostate cancer focal therapy. J Endourol 2010;24(5):835-41 DOI: 10.1089/end.2010.0006
- Лумпов И.С., Амосов А.В., Крупинов Г.Е., Чиненов Д.В., Ганжа Т.М., Воробьев А.А. Гемиаблация локализованного рака простаты высокоинтенсивным фокусированным ультразвуком. Медицинский вестник Башкортостана 2017;12(3):97-99
- Ahmed H.U. The index lesion and the origin of prostate cancer.N Engl J Med 2009;361(17):1704-6 DOI: 10.1056/NEJMcibr0905562
- Huang CC, Deng FM, Kong MX, Ren Q, Melamed J, Zhou M. Re-evaluating the concept of "dominant/index tumor nodule" in multifocal prostate cancer. Virchows Arch 2014;464(5):589-94 DOI: 10.1007/s00428-014-1557-y
- Eggener S, Salomon G, Scardino PT, De la Rosette J, Polascik TJ, Brewster S.Focal therapy for prostate cancer: possibilities and limitations. Eur Urol 2010;58(1):57-64 DOI: 10.1016/j.eururo.2010.03.034
- Turpen R, Rosser CJ. Focal therapy for prostate cancer: revolution or evolution. BMC Urol 2009 Apr 23;9:2 DOI: 10.1186/1471-2490-9-2
- Hale Z, Miyake M, Palacios DA, Rosser CJ. Focal cryosurgical ablation of the prostate: a single institute’s perspective. BMC Urol. 2013;13:2 DOI: 10.1186/1471-2490-13-2
- Karavitakis M, Ahmed HU, Abel PD, Hazell S, Winkler MH. Tumor focality inprostate cancer: implications for focal therapy. Nat Rev Clin Oncol 2011;8(1):48-55 DOI: 10.1038/nrclinonc.2010.190
- Абоян И.А., Галстян А.М., Бадьян К.И., Пакус С.М. Способ лечения локализованного рака предстательной железы. Заявка на изобретение №2017146552/14(079560) от 27.12.2017. URL: http://www1.fips.ru/fips_servl/fips_ servlet?DB=RUPAT&DocNumber=2017146552&TypeFile=html


