Химическая модификация хлоранилинов при определении в воде методом газовой хроматографии
Автор: Груздев И.В., Алферова М.В., Кондратенок Б.М.
Журнал: Известия Коми научного центра УрО РАН @izvestia-komisc
Рубрика: Химические науки
Статья в выпуске: 4, 2010 года.
Бесплатный доступ
Для одновременного определения анилина и его хлорзамещенных (2- и 4- хлоранилины, 2,4- и 2,6-дихлоранилины, 2,4,5- и 2,4,6-трихлоранилины) в водных средах применен метод химической модификации, предполагающий получение их бромпроизводных, жидкостную экстракцию и газохроматогра- фическое определение с детектором электронного захвата. Изучены условия реакции бромирования в водной среде в присутствии бромид-ионов, определе- ны экстракционные и газохроматографические характеристики хлоранилинов и их бромпроизводных. Проведена оценка эффективности химической моди- фикации при определении хлоранилинов в воде в виде их бромпроизводных.
Хлоранилины, химическая модификация, бромпроизводные хлоранилинов, газохроматографический анализ
Короткий адрес: https://sciup.org/14992415
IDR: 14992415 | УДК: 543.544.43
Chemical modification of chloroaniline for determination in water by gas chromatography
The simultaneous determination of aniline and its chloroderivatives (2 - and 4- chloroaniline, 2,4- and 2,6-dichloroaniline, 2,4,5 - and 2,4,6-trichloraniline) in aqueous media has been carried out by a gas chromatography method. The analytical procedure involved their derivatization to bromoderivatives with bromine and further liquid-liquid extraction and gas chromatography-electron capture detector determination. The conditions of the bromination reaction in the presence of bromide ions, extraction and gas chromatographic characteristics of chloroanilines and their bromoderivatives were studied. The efficiency of chemical modification of chloroanilines was estimated.
Текст научной статьи Химическая модификация хлоранилинов при определении в воде методом газовой хроматографии
Актуальность исследований в области аналитической химии азотсодержащих ароматических соединений обусловлена тем, что в настоящее время в питьевой воде нормируется содержание 79 таких веществ. В особую группу распространенных и высокотоксичных веществ выделяют анилины. Их широкая распространенность связана с хорошей растворимостью в воде и активным промышленным применением. Так, ароматические амины всегда присутствуют в сточных водах предприятий по производству красителей, пестицидов и фармацевтических препаратов [1].
В почвах и природных водах хлоранилины могут образовываться при гидролитической или биохимической деструкции широко применяемых пестицидов и антисептиков [2, 3].
При попадании анилина в водоисточники, используемые для подготовки питьевой воды на стадии ее обеззараживания активным хлором, может происходить образование более токсичных хлор-замещенных анилинов [4].
Хлоранилины оказывают прямое токсическое действие на организм, поэтому их содержание в питьевой воде нормируется [5]. В питьевых водоисточниках концентрация хлоранилинов не должна превышать 50 мкг/дм3, а для водоемов, имеющих рыбохозяйственное значение, предельно-допустимые концентрации (ПДК) еще ниже – 0.1 мкг/дм3 [6].
Хроматографическое определение хлорани-линов непосредственно в воде осложнено их высокой гидрофильностью и полярностью. Поэтому для выделения анилинов из водной матрицы и их концентрирования используют различные варианты жидкостной [7-8] и твердофазной экстракции [9-13].
Для хроматографического анализа полученных экстрактов применяется высокоэффективная жидкостная хроматография с электрохимическим [14], амперометрическим [11] или фотометрическим детектированием [3, 7, 8]. При анализе экстрактов методом капиллярной газовой хроматографии используют пламенно-ионизационный [13], термоион- ный [9], а также масс-спектрометрический детекторы [10, 12]. Чувствительность прямых хроматографических определений анилинов составляет 0.55 мкг/дм3, что недостаточно, учитывая ПДК анилина – 0.1 мкг/дм3.
Наличие в молекулах хлоранилинов реакционно-способной аминогруппы, атомы водорода которой достаточно легко замещаются, позволяет получать их различные производные и достигать более высокой чувствительности определения. Наибольшее применение находят азот- [15], фосфор- [16] и галогенсодержащие [17-21] производные анилинов, получаемые для определения на селективных термоионном, пламенно-фотометрическом и электронозахватном детекторах соответственно.
Кроме того, аминогруппа анилинов характеризуется выраженным положительным мезомер-ным эффектом, поэтому производные хлоранили-нов можно получать не только по функциональной группе, но и по реакции электрофильного замещения атомов водорода бензольного ядра.
В данном исследовании в качестве реагента для получения производных хлоранилинов рассматривается молекулярный бром. Применение этого модифицирующего реагента имеет следующие преимущества:
-
1. Бромирование хлоранилинов в водной фазе протекает легко, поскольку вода проявляет свойства катализатора, поляризуя молекулы брома и генерируя электрофильные частицы [22].
-
2. Введение в молекулы атомов брома значительно повысит гидрофобность хлоранилинов, что обеспечит при жидкостной экстракции более полное их извлечение из воды в органическую фазу [23].
-
3. Применение для детектирования бром-производных хлоранилинов галогенселективного детектора электронного захвата (ДЭЗ) обеспечит максимально возможное по чувствительности их газохроматографическое определение [24].
Экспериментальная часть
Для приготовления стандартных растворов использовали образцы анилина, 2-хлоранилина, 3-хлоранилина, 4-хлоранилина, 2,4-дихлоранилина, 2,6-дихлоранилина, 2,4,5-трихлоранилина, 2,4,6-трихлоранилина (Riedel-de-Haen, PESTANAL®) с содержанием основного вещества ≥ 99 %. Остальные реактивы и растворители квалификации ч.д.а. или х.ч.
Газохроматографический анализ проводили на газовом хроматографе “Кристалл 5000” (Хрома-тэк) с электронозахватным детектором, совмещенным с системой сбора и обработки хроматографической информации “Хроматэк Аналитик 2.5”. Условия газохроматографического определения: кварцевая капиллярная колонка 30 м x 0.25 мм x 0.25 мкм (ZB-5, Phenomenex), газ-носитель – азот (ос.ч.), программирование давления газа-носителя: 80 кПа (7 мин) – 25 кПа/мин – 200 кПа, поддув детектора – 20 см3/мин, деление потока – 1:30. Температура детектора 320 0С, испарителя 320 0С, термостата колонок 180 0С.
Идентификацию бромпроизводных хлорани-линов и определение логарифмических индексов удерживания проводили на хромато-масс-спектро-метре TRACE DSQ (Thermo) в режиме полного ионного тока (энергия электронов 70 эВ). Условия определения: программирование температуры термостата колонок 50 °С – 5 °С/мин – 300 °С, кварцевая капиллярная колонка 30 м x 0.32 мм x 0.25 мкм (TR-1, Thermo). Газ-носитель – гелий, чистота 99.99 %, скорость потока через колонку – 1 см3/мин, деление потока – 1:50, температура испарителя 320 °С, интерфейса 250 °С, детектора 200 °С.
Значения рН и окислительно-восстановительного потенциала водных растворов брома определяли на приборе HI 8519N (Hanna Instruments) с использованием рН-электрода HI 1043 и ОВР-электрода HI 3220.
Обсуждение результатов
Получение бромпроизводных хлоранилинов. Молекулы хлоранилинов содержат заместители, по-разному взаимодействующие с электронным облаком ароматического ядра. Так, NН 2 -группа характеризуется положительным мезомерным эффектом (+М) и отрицательным индукционным (–I), причем определяющее влияние на поведение анилинов в реакциях электрофильного замещения оказывает именно +М-эффект. Взаимодействие аминогруппы с ароматической системой облегчает замещение атомов водорода в положениях 2, 4 и 6 ( орто - и пара -замещение). Атомы хлора, наоборот, характеризуются слабо выраженным +М-эффектом и значительным отрицательным индукционным эффектом (–I), но направляют заместители также в орто- и пара- положения [22].
Таким образом, анилин и 3-хлоранилин при бромировании образуют трибромпроизводные, 2- и 4-хлоранилин – дибромпроизводные, 2,4-, 2,6-дихлоранилин и 2,4,5-трихлоранилин – монобромпро-изводные. Одновременно с указанными хлоранили-нами определяется и 2,4,6-трихлоранилин, но поскольку положения 2, 4, и 6 уже заняты атомами хлора, это соединение бромпроизводного не образует.
Для проведения химической модификации следовых количеств органических соединений традиционно применяют большие молярные избытки модифицирующих агентов, что связано с отсутствием предварительной информации о качественном и количественном составе анализируемых проб и необходимостью поддержания высокой скорости реакции дериватизации [25]. При бромировании хлоранилинов (10 мкг/дм3) концентрация брома в воде составляла 0.0005 моль/дм3, что соответствует ~103-кратному избытку от расчетного стехиометрического соотношения.
При бромировании хлоранилинов в нейтральных и кислых водных растворах удается получить очень слабый аналитический сигнал, составляющий 5-10 % от теоретически возможного (рис. 1). Этот факт можно объяснить тем, что одновременно с бромированием хлоранилинов идет их окисление молекулярным бромом, редокс-потенциал которого достигает значений 0.9-1.1 В, и этот процесс является доминирующим.
Таким образом, для получения бромпроиз-водных хлоранилинов в воде окислительно-восстановительный потенциал брома необходимо сни- жать. Введение бромид-анионов позволяет значительно снизить редокс-потенциала водных растворов брома (рис. 1, зависимость 4), что связано с образованием в растворе ионов Br3- [26]:
Br 2 + Br - о Br 3 .
С увеличением концентрации бромид-анионов в растворе возрастает и устойчивость образующихся бромпроизводных (рис. 1, зависимости 1-3). При концентрации бромид-анионов 0.1-0.15 моль/дм3 редокс-потенциал раствора снижается до ~0.85 В, что позволяет получать бромпроизводные всех анализируемых хлоранилинов с количественным выходом. Важно также, что 2,4,6-трихлор-анилин, который без бромид-анионов полностью окислялся, при их введении сохраняется в водном растворе количественно (рис. 1, зависимость 5).
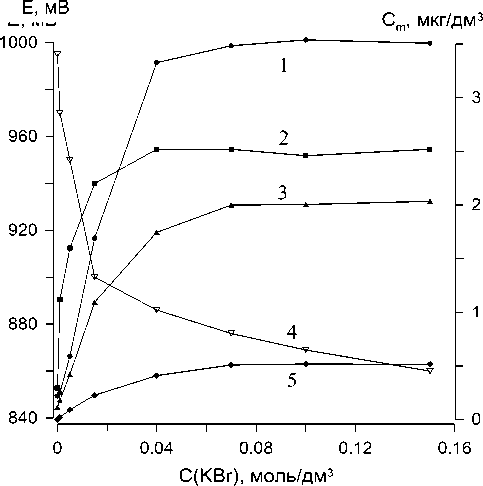
Рис. 1. Зависимость окислительно-восстановительного потенциала водного раствора брома (4) и концентрации бромпроизводных хлоранилинов в водном растворе (1-3) от концентрации бромида калия: 1 – 4,6-дибром-2-хлоранилин, 2 – 6-бром-2,4,5-три-хлоранилин, 3 – 4-бром-2,6-дихлоранилин, 5 – 2,4,6-трихлоранилин; С(Br 2 ) = 0.0005 моль/дм 3 , время бромирования 1 мин; исходная концентрация 2,4,6-трихлоранилина, 2,6-дихлоранилина, 2,4,5-трихлоранилина и 2-хлоранилина в воде – 0.5, 2.0, 2.5 и 3.5 мкг/дм 3 , соответственно.
Следует отметить, что получаемые аналитические формы хлоранилинов устойчивы как в воде, так и в органических растворителях (толуол), и концентрации бромпроизводных при температуре 20-25 ° С не изменяются, по крайней мере, в течение 24 час.
Экстракционное концентрирование бром-производных хлоранилинов. Метод газовой хроматографии, применяемый для разделения и детектирования бромпроизводных хлоранилинов, предполагает обязательную замену водной матрицы на менее активный органический растворитель. Одновременно с этим пытаются достичь селективного извлечения и максимальной степени концентрирования анализируемых соединений, поэтому от эффективности проведения жидкостной экстракции, в целом, зависит чувствительность определения анализируемых соединений [27].
Химическая модификация хлоранилинов в бромпроизводные значительно изменяет их экстракционные характеристики. Как и следовало ожидать, введение атомов брома, оказывающих гидрофобное действие, приводит к значительному увеличению коэффициентов распределения бромпроизводных, которые в системе толуол-вода характеризуются значениями в диапазоне от 3000 до 6000 (табл. 1).
Таблица 1
Коэффициенты распределения (D) и степень извлечения (R) хлоранилинов и их бромпроизводных
-
в экстракционной системе толуол/вода
Соединение
D
R, % (r = 25)
Хлоранилины
2-хлоранилин
53
14.7
3-хлоранилин
21
6.4
4-хлоранилин
8
2.4
2,4-дихлоранилин
423
58.0
2,6-дихлоранилин
1013
76.8
2,4,6-трихлоранилин
3951
95.4
2,4,5-трихлоранилин
2137
87.5
анилин
6
1.9
Бромпроизводные хлоранилинов
2-хлор-4,6-диброманилин
5334
99.5
3-хлор-2,4,6-триброманилин
5877
99.5
4-хлор-2,6-диброманилин
5051
99.4
2,4-дихлор-6-броманилин
3965
99.4
2,6-дихлор-4-броманилин
4081
99.3
2,4,5-трихлор-6-броманилин
5855
99.5
2,4,6-триброманилин
5470
99.4
Высокие значения коэффициентов распределения бромпроизводных хлоранилинов обеспечивают практически количественное извлечение анализируемых веществ из водной фазы в органическую, что значительно повышает чувствительность аналитических измерений. Степень извлечения вещества в органическую фазу (R, %) связана с D выражением [23]:
R = ——100% , D + r где r = Vв/Vo, Vo и Vв – равновесные объемы органической и водной фаз, см3.
Следует отметить, что введение атомов брома в хлоранилины приводит и к выравниванию их коэффициентов распределения, что позволяет с одинаковой эффективностью концентрировать все определяемые соединения. Экстракционное концентрирование самих же хлоранилинов сильно осложнено зависимостью их степени извлечения от числа атомов хлора в молекуле (табл. 1).
Газохроматографические свойства хлор-анилинов и их бромпроизводных. В табл. 2 приведены газохроматографические характеристики хло-ранилинов и их бромпроизводных: логарифмические индексы удерживания (RI) на стандартной неполярной полидиметилсилоксановой неподвижной фазе и относительные мольные отклики ДЭЗ [27]:
RMR an
MRi
MRan ,
где MR i и MR an – мольные отклики детектора электронного захвата на i- е соединение и анилин соответственно.
Введение атомов брома в молекулы хлор-анилинов не только значительно увеличивает (на 24 порядка), но и выравнивает значения RMR an . (табл. 2). Так, отношения RMR an 2,4,6-трибромани-лина, 4-хлор-2,6-диброманилина, 2,6-дихлор-4-бро-манилина и 2,4,5-трихлор-6-броманилина близки и составляют 1 : 0.83 : 1.06 : 1.09. Это принципиально важно для одновременного определения анилина и его моно-, ди- и трихлорзамещенных с применением ДЭЗ, поскольку при сходных концентрациях хлорани-линов их бромпроизводные будут иметь сравнимый по интенсивности аналитический сигнал (рис. 2).
Одновременное определение анилина и его хлорпроизводных в исходной форме с детектором электронного захвата невозможно, поскольку RMR an , например, анилина, 4-хлоранилина, 2,6-дихлоранилина и 2,4,5-трихлоранилина различаются более чем на четыре порядка: 1 : 9 : 545 : 12130.
Определение хлоранилинов в виде их бром-производных не вызывает значительного увеличе-
Таблица 2
Газохроматографические характеристики хлоранилинов и их бромпроизводных
Соединение RMR an RI
Хлоранилины анилин 1 946
|
2-хлоранилин |
12 |
1093 |
|
3-хлоранилин |
15 |
1157 |
|
4-хлоранилин |
9 |
1160 |
|
2,4-дихлоранилин |
416 |
1286 |
|
2,6-дихлоранилин |
545 |
1202 |
|
2,4,5-трихлоранилин |
12130 |
1488 |
|
2,4,6-трихлоранилин |
22730 |
1367 |
|
Бромпроизводные |
хлоранилинов |
|
|
2,4,6-триброманилин |
217870 |
1646 |
|
2-хлор-4,6-диброманилин |
177530 |
1552 |
|
3-хлор-2,4,6-триброманилин |
237120 |
1872 |
|
4-хлор-2,6-диброманилин |
180360 |
1546 |
|
2,4-дихлор-6-броманилин |
151740 |
1455 |
|
2,6-дихлор-4-броманилин |
231860 |
1461 |
|
2,4,5-трихлор-6-броманилин |
238660 |
1671 |
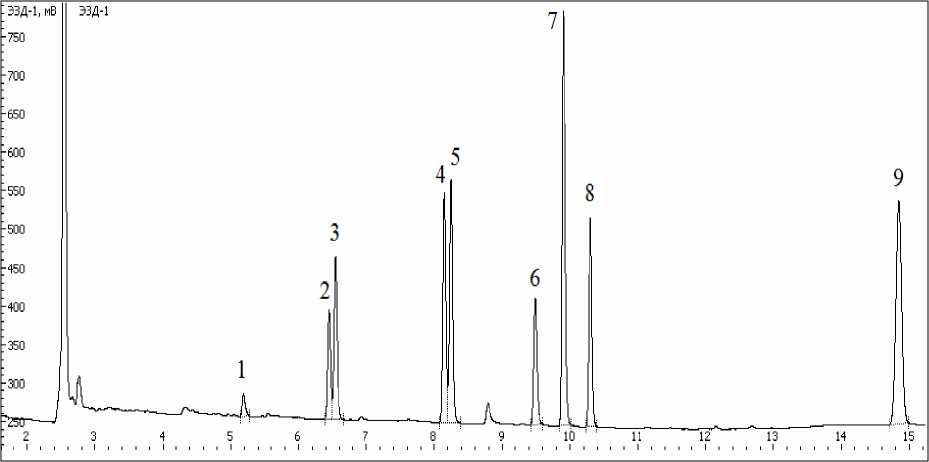
Рис. 2. Хроматограмма экстракта бромпроизводных хлоранилинов; исходная концентрация всех компонентов в водном растворе – 10 мкг/дм 3 : 1 – 2,4,6-трихлоранилин, 2 – 2,4-дихлор-6-броманилин, 3 – 2,6-дихлор-4-броманилин, 4 – 4-хлор-2,6-диброманилин, 5 – 2-хлор-4,6-диброманилин, 6 – внутренний стандарт, 7 – 2,4,6-триброманилин, 8 – 2,4,5-трихлор-6-броманилин, 9 – 3-хлор-2,4,6-триброманилин.
ния времени газохроматографического анализа – индексы удерживания (RI) возрастают только в 1.11.8 раза (табл. 2). Наибольший индекс удерживания имеет самый тяжелый компонент 3-хлор-2,4,6-триброманилин, который и определяет общее время анализа – 15 мин.
Оценка эффективности химической модификации хлоранилинов. Чувствительность определения хлоранилинов в воде возрастает в результате дополнительного введения в их молекулы атомов брома. Введение этих заместителей обеспечивает более эффективное экстракционное концен- трирование и детектирование ДЭЗ. Поэтому в качестве критерия оценки эффективности дериватиза-ции хлоранилинов нами предлагается обобщенный параметр Кхм, учитывающий как увеличение степени извлечения при экстракции, так и относительных мольных откликов ДЭЗ:
RMRan*R* К —-----------, хм RMR an R где RMRan и RMRan* – относительные мольные отклики хлоранилина и его бромпроизводного; R и R* – степень извлечения в экстракт хлоранилина и его бромпроизводного.
Параметр К хм характеризует возрастание чувствительности определения соответствующего хлоранилина при определении его в виде бромпро-изводного (табл. 3). Максимальный эффект получен для анилина – в виде бромпроизводного он определяется в миллион раз чувствительнее по сравнению с немодифицированной формой. Чувствительность определения монохлоранилинов возрастает более чем на пять порядков, дихлоранилинов – на два, 2,4,5-трихлоранилина – на порядок.
Высокая эффективность предлагаемой химической модификации позволяет снизить пределы обнаружения хлоранилинов до 0.005 мкг/дм3, что на порядок ниже минимального значения ПДК, установленных для этих соединений.
Разработанный способ был опробован для определения хлоранилинов в питьевой воде г. Сыктывкара (рис. 3). Обнаружены анилин и его моно-хлорпроизводные в концентрациях, не превышающих ПДК: Ст(2-хлоранилин) = 0.04 ± 0,01 мкг/дм3, Ст(4-хлоранилин) = 0.03 ± 0,01 мкг/дм3 и Ст(анилин) = 0.07 ± 0,03 мкг/дм3.
Таблица 3
Эффективность химической модификации хлоранилинов
|
Соединение |
К хм |
|
2-хлоранилин |
21000 |
|
3- хлоранилин |
35000 |
|
4- хлоранилин |
86000 |
|
2,4-дихлоранилин |
380 |
|
2,6-дихлоранилин |
430 |
|
2,4,5-трихлоранилин |
20 |
|
анилин |
1100000 |
Выводы
Для определения анилина и его хлорзаме-щенных (2- и 4-хлоранилины, 2,4- и 2,6-дихлорани-лины, 2,4,5- и 2,4,6-трихлоранилины) в водных средах применен метод химической модификации, предполагающий получение их бромпроизводных, жидкостную экстракцию и газохроматографическое определение с детектором электронного захвата. Бромирование хлоранилинов проводится в присутствии бромид-ионов, что позволяет получать бром-производные с количественным выходом и исключить их окисление. Изучены экстракционные и газохроматографические характеристики хлоранилинов и их бромпроизводных. Высокая эффективность предлагаемой химической модификации позволяет снизить пределы обнаружения хлоранилинов до 0.005 мкг/дм3, что на порядок ниже минимального значения ПДК, установленных для этих соединений.
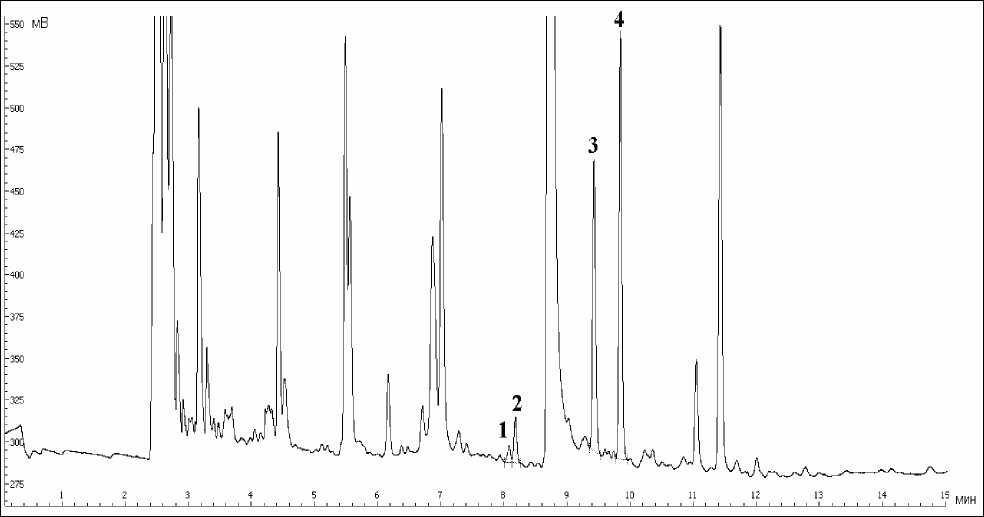
Рис. 3. Хроматограмма экстракта питьевой воды г. Сыктывкара. Пронумерованные пики соответствуют бромпроизводным: 1 – 4-хлоранилина, 2 – 2-хлоранилина, 4 – анилина; 3 – внутренний стандарт (4,6-дибром-1,2-диметоксибензол).
Список литературы Химическая модификация хлоранилинов при определении в воде методом газовой хроматографии
- Козубова Л.И., Морозов С.В. Органические загрязнители питьевой воды. Новосибирск: Изд-во СО РАН, 1993. Вып. 26. 167 с.
- Barcelo D., Hennion M. Trace determination of pesticides and their degradation products in water. Amsterdam: Elsevier, 1997. 434 p.
- Rasmussen H.; Omelczenko N.; Friedman S. Determination of chloroanilines in antibacterial soaps using cation-exchange chromatography with UV-detection//J. Chromatogr. A, 1996. Vol. 719. P. 434-437.
- Славинская Г.В. Влияние хлорирования на качество питьевой воды//Химия и технология воды, 1991. Т. 13. № 11. С. 1013-1022.
- СанПиН 2.1.4.1074-01. Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества. М.: Госкомсанэпиднадзор России, 2001. 111 с.
- Перечень рыбохозяйственных нормативов. М.: Изд-во ВНИРО, 1999. 304 с.
- Zapf A., Heyer R., Stan H. Rapid liquid-liquid extraction method for trace analysis of organic contaminants in drinking water//J. Chromatogr. A, 1995. Vol. 694. P. 453-461.
- Zhu L., Tay C., Lee H. Liquid-liquid-liquid microextraction of aromatic amines from water samples combined with high performance liquid chromatography//J. Chromatogr. A, 2002. Vol. 963. P. 231-237.
- Сониясси Р., Сандра П., Шлетт К. Анализ воды: Органические микропримеси. СПб: Теза, 1999. 248 с.
- Muller L., Fattore E., Benfenati E. Determination of aromatic amines by solid-phase microextraction and gas chromatography massspectrometry in water samples.//J. Chromatogr. A, 1997. Vol. 791. P. 221-230.
- Piangerelli V., Nerini F., Cavalli S. Determination of aromatic amines and phenols in environmental samples by selective SPE elution and HPLC with amperometric detection//Ann. Chim, 1997. Vol. 87. P. 571-582.
- Solid-phase microextraction of aromatic amines with an amide bridged calix[4]arene coated fiber/W.Wang, S.L.Gong, Q.H.Cao, Y.Y.Chen, X.J.Li, Z.R.Zeng//Chromatographia, 2005. Vol. 61. P. 75-80.
- Yan C.T., Jen J.F. Determination of aniline in water by microwave-assisted headspace solidphase microextraction and gas chromatography//Chromatographia, 2004. Vol. 59. P. 517-520.
- Lewin U., Efer J., Engewald W. High-performance liquid chromatographic analysis with electrochemical detection for residues of explosives in water samples around a former ammunition plant//J. Chromatogr. A, 1996. Vol. 730. P. 161-167.
- Skarping G., Renman L., Dalene M. Determination of aromatic amines as perfluorofatty acidamides using nitrogenselective detection//J. Chromatogr, 1983. Vol. 270. P. 207-218.
- Kijima K., Kataoka H., Makita M. Determination of aromatic amines as their N-dimethylthiophosphoryl derivatives by gas chromatography with flame-photometric detection.//J. Chromatogr. A, 1996. Vol. 738. P. 83-90.
- Dasgupta A. Gas chromatographic mass spectrometric identication and quantication of anilines after extraction from serum and derivatization with 2,2,2-trichloroethyl chloroformate, a novel derivative//J. Chromatogr. B, 1998. Vol.716. P. 354-358.
- Longo M., Cavallaro A. Determination of aromatic amines at trace levels by derivatization with heptafluorobutyric anhydride and gas chromatography electron-capture negative-ion chemical ionization mass spectrometry//J. Chromatogr. A, 1996. Vol. 753. P. 91-100.
- Mishra S., Singh V., Jain A., Verma K. K. Simultaneous determination of ammonia, aliphatic amines, aromatic amines and phenols at μgL-1 levels in environmental waters by solidphase extraction of their benzoyl derivatives and gas chromatography-mass spectrometry//Analyst, 2001. Vol. 126. P. 1663-1668.
- Schmidt T., Haas R., Steinbach K. Gas chromatographic determination of aromatic amines in water samples after solid-phase extraction and derivatization with iodine//J. Chromatogr. A, 1998. Vol. 810. P. 161-172.
- Weiss T., Angerer J. Simultaneous determination of various aromatic amines and metabolites of aromatic nitro compounds in urine for low level exposure using gas chromatography-mass spectrometry//J. Chromatogr. B, 2002. Vol. 778. P. 179-192.
- Агрономов А.Е. Избранные главы органической химии. М.: Химия, 1990. 560 с.
- Коренман И.М. Экстракция органических веществ. Горький: Изд-во Горьков. гос. ун-та, 1973. 158 с.
- Poole C. F., Zlatkis A. Sensitive derivatives for determination of organic compounds by electroncapture gas chromatography. Amsterdam: Elsevier, 1981. 151 p.
- Демьянов П.И. Химические методы получения производных при хроматографическом определении фенолов//Журн. аналит. химии, 1992. Т. 47. № 12. С. 1942-1962.
- Ксензенко В.И., Стасиневич Д.С. Химия и технология брома, йода и их соединений. М.: Химия, 1995. 379 с.
- Новак Й. Количественный анализ методом газовой хроматографии. М.: Мир, 1978. 179 с.


