Химиолучевая терапия больных раком слизистой оболочки полости рта и ротоглотки с использованием неравномерного дробления дневной дозы
Автор: Раджапова М.У., Мардынский Ю.С., Гулидов И.А., Медведев B.C., Семин Д.Ю., Иванова И.Н.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 3 (45), 2011 года.
Бесплатный доступ
Проведен анализ эффективности консервативного лечения 188 больных с морфологически верифицированным диагнозом первичного рака слизистой оболочки полости рта и ротоглотки. Использованы два метода лечения: стандартная лучевая терапия (2 Гр 5 раз в нед) и химиолучевое лечение (фракционирование дозы 1 Гр + 1,5 Гр с 4-6-часовым интервалом) до суммарной очаговой дозы 60 Гр. Полученные данные свидетельствуют, что химиолучевая терапия с дроблением дозы 1 Гр + 1,5 Гр оказалась более эффективной, чем стандартное лучевое лечение, по частоте объективных ответов и полных регрессий опухоли при отсутствии увеличения количества ранних лучевых реакций и поздних лучевых повреждений нормальных тканей. После химиолучевой терапии с дроблением дозы 1 Гр + 1,5 Гр частота объективных ответов (сумма полных и частичных регрессий) составила 97,8 %, после лучевой терапии стандартным облучением - 61,9 % (р
Рак слизистой оболочки полости рта и ротоглотки, химиолучевая терапия, дробление дневной дозы облучения
Короткий адрес: https://sciup.org/14055909
IDR: 14055909 | УДК: 616.31+616.321]-006.6+615.849+615.28
Chemoradiation therapy with the use of inhomogeneous daily dose distribution for patients with oral cavity and oropharyngeal cancer
The efficacy of conservative treatment of 188 patients with histologically-verified primary oral cavity and oropharyngeal cancer was analyzed. Two treatment methods were used: the conventional radiation therapy (2 Gy, 5 times a week) and chemoradiation therapy (dose fractions of 1 Gy + 1,5 Gy with 4-6-hour interval) up to a total dose of 60 Gy. The data obtained showed that chemoradiation therapy was more effective than the standard radiation therapy with regard to objective responses and complete tumor regressions. The rate of objective responses (the sum of complete and partial regressions) was 97,8 % after chemoradiation therapy and 61,9 % after the conventional radiation therapy (p
Текст научной статьи Химиолучевая терапия больных раком слизистой оболочки полости рта и ротоглотки с использованием неравномерного дробления дневной дозы
Консервативное лечение больных раком полости рта и ротоглотки является актуальной проблемой клинической онкологии. Основные неудачи терапии данной патологии связаны, в первую очередь, с лечением поздних (III–IV) стадий заболевания, частота которых крайне высока [4, 8]. Так, в 2008 г. у 69,7 % больных раком полости рта и ротоглотки диагностирован местнораспространенный опухолевый процесс III–IV стадии [7]. Быстрый инфильтративный рост опухоли, раннее лимфо- и гематогенное метастазирование, поздняя диагностика и, как правило, выраженные клинические проявления заболевания значительно ограничивают радикальность лечения и являются причиной высокой летальности, которая уже на первом году после установления диагноза достигает более 40 % [4].
Значительным прорывом в лечении плоскоклеточного рака головы и шеи стало открытие высокоэффективной комбинации препаратов платины и 5-фторурацила. На сегодняшний день химиолучевая терапия опухолей полости рта и ротоглотки является одним из перспективных направлений в практической онкологии [1, 2, 3, 5, 11, 12]. Однако недостаточная избирательность действия ионизирующего излучения по отношению к опухолевой ткани затрудняет подведение к опухоли доз, необходимых для полного излечения, из-за превышения толерантности нормальных тканей. Именно это обстоятельство диктует целесообразность применения при планировании химиолучевого лечения методик нетрадиционного фракционирования дозы во времени, усиливающих терапевтическую эффективность без увеличения риска возникновения тяжелых постлучевых осложнений в здоровых тканях.
Целью исследования являлось улучшение результатов лечения больных раком полости рта и ротоглотки путем использования химио-лучевой терапии с неравномерным дроблением ежедневной дозы облучения.
Материал и методы
Клинический материал представлен 188 больными с морфологически верифицированным диагнозом первичного рака слизистой оболочки полости рта и ротоглотки. В 98,1 % случаев это был плоскоклеточный рак различной степени дифференцировки, в 1,9 % – аденоки- стозный. Стадию заболевания устанавливали в соответствии с международной классификацией TNM (6-е издание, 2002 г.). При этом показатель запущенности (III–IV стадия) составил 74,5 % (табл. 1). Метастазы в регионарные лимфатические узлы были обнаружены у 92 из 188 (48,9 %) больных.
Пациенты в зависимости от метода лечения были распределены на 2 лечебные группы. В первой (контрольной) группе 97 больным проводилась стандартная лучевая терапия в самостоятельном варианте – разовая очаговая доза 2 Гр 5 раз в нед до суммарной очаговой дозы 60 Гр. Во второй группе 91 пациенту проводили одновременную химиолучевую терапию с неравномерным подведением ежедневной дозы облучения 1 Гр и 1,5 Гр с 4–6-часовым интервалом до СОД 60 Гр.
Дистанционная гамма-терапия в статическом режиме проводилась на гамма-терапевтических установках типа «Агат» и «Рокус-АМ». Первичную опухоль с лимфатическими узлами первого регионарного барьера облучали через противолежащие боковые поля. Границы и размеры полей облучения подбирали индивидуально в зависимости от локализации и степени распространенности опухоли и регионарных метастазов. Тактика по отношению к лимфоколлекторам шеи определялась наличием регионарных метастазов. Интактные лимфатические узлы облучали до суммарной очаговой дозы в диапазоне 44–46 Гр, метастатические – СОД 56–60 Гр. Пациентам с неполной регрессией регионарных метастазов выполнялось плановое иссечение лимфатических узлов через 4–5 нед после завершения противоопухолевой терапии.
Таблица 1
Распределение больных в зависимости от распространенности опухолевого процесса
|
Распространенность опухоли |
Метод лечения |
|
|
СЛТ |
ХЛТ |
|
|
Стадия I |
3 (3,1 %) |
1 (1,1 %) |
|
Стадия II |
23 (23,7 %) |
21 (23,1 %) |
|
Стадия III |
37 (38,1 %) |
13 (14,3 %) |
|
Стадия IV |
34 (35,1 %) |
56 (61,5 %) |
|
Количество больных |
97 (100 %) |
91 (100 %) |
Примечание: СЛТ – стандартная лучевая терапия, ХЛТ – одновременная химиолучевая терапия с дроблением дозы облучения 1 Гр + 1,5 Гр.
СИБИРСКИЙ ОНКОЛОГИЧЕСКИЙ ЖУРНАЛ. 2011. №3 (45)
Для проведения системной полихимиотерапии использовали цисплатин и 5-фторурацил. В первый день лечения, до начала лучевой терапии, внутривенно на фоне гипергидратации вводили цисплатин в дозе 100–120 мг/м2 в течение 30 мин, затем начинали внутривенное введение 5-фторурацила в дозе 3000 мг непрерывно в течение 72 ч при помощи инфузионного шприцевого насоса. Всего одновременно с лучевой терапией проводили 2 цикла полихимиотерапии с интервалом в 21 день. Расщепление курса лучевой и химиолучевой терапии использовали при развитии выраженных симптомов мукозита III степени.
Клиническую оценку состояния слизистой оболочки полости рта и ротоглотки (степень мукозита) и поздних лучевых повреждений в зоне облучения проводили в соответствии со шкалой RTOG/EORTC. Также фиксировали длительность перерыва, необходимого для регенерации слизистой оболочки, и величину СОД, которая была подведена к первичной опухоли до перерыва. Клиническую регрессию первичной опухоли оценивали эндоскопическим, рентгенологическим, ультразвуковым методами исследования в соответствии с рекомендациями ВОЗ.
Полученные данные обрабатывались с применением общепринятых методов вариационной статистики с использованием стандартных пакетов программ статистического анализа Statistica 6.0.
Результаты и обсуждение
Известно, что успех лучевой терапии определяется возможностью достижения полной стерилизации опухолевых клеток при сохранении допустимого уровня поражения нормальных тканей. Наряду с технической составляющей прогресса лучевой терапии не менее важным является биологическое направление её усовершенствования и повышения эффективности. Перспективным в этом плане представляется разработка методов расширения «терапевтического интервала» в радиочувствительности опухолей и попадающих в зону лучевого воздействия нормальных тканей. Применение нетрадиционных методов подведения дозы излучения является одним из возможных путей решения этой проблемы.
В настоящем исследовании в схеме химиолу- чевого лечения мы применили неравномерное дробление дневной дозы в виде гиперфракционирования в режиме 1 Гр + 1,5 Гр с временным интервалом между фракциями 4–6 ч. В качестве предпосылки использования данного режима облучения рассматривается более высокий репарационный потенциал медленно пролиферирующих, поздно реагирующих тканей по сравнению с быстро пролиферирующими, к которым относятся и опухоли [9, 10]. Так как при гиперфракционировании увеличивается количество сеансов облучения, которые проводятся с определенным интервалом между ними, возникает возможность с большей вероятностью воздействовать на опухолевые клетки в наиболее чувствительных фазах цикла клеточного деления. Вследствие этого усиливается лучевое повреждение опухоли. В то же время уменьшение величины разовой дозы приводит к смягчению лучевого эффекта для поздно реагирующих нормальных тканей, обладающих слабой репопуляционной способностью, но зато выраженным свойством восстановления сублетальных и потенциально летальных повреждений.
В ходе исследования нами была оценена безопасность и переносимость одновременной химиолучевой терапии с дроблением дневной дозы 1 Гр + 1,5 Гр по раннему и позднему местному токсическому эффекту – радиационному мукозиту и поздним лучевым повреждениям нормальных тканей и органов полости рта и ротоглотки. Следует отметить, что независимо от метода лечения острые лучевые реакции различной тяжести на слизистых оболочках возникали у 100 % пациентов. Однако при химиолучевой терапии с дроблением дневной дозы 1 Гр + 1,5 Гр была отмечена тенденция к снижению частоты тяжелых мукозитов III степени по сравнению со стандартной лучевой терапией – 40,5 % против 52,7 % случаев (р>0,05). Длительность перерыва, необходимого для регенерации слизистых оболочек, при двух способах терапии составила 10,4 ± 2,3 и 11,3 ± 4,1 дня соответственно (р>0,05). Следует отметить, что своевременная и адекватная терапия лучевых реакций слизистых оболочек позволила всем больным завершить запланированный курс радикального лечения.
Поздние лучевые повреждения нормальных
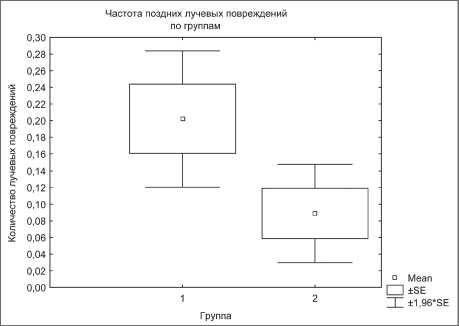
Рис. 1. Частота поздних лучевых повреждений нормальных тканей в зоне облучения. Примечание: 1 – стандартная лучевая терапия, 2 – одновременная химиолучевая терапия с дроблением дозы 1 Гр + 1,5 Гр
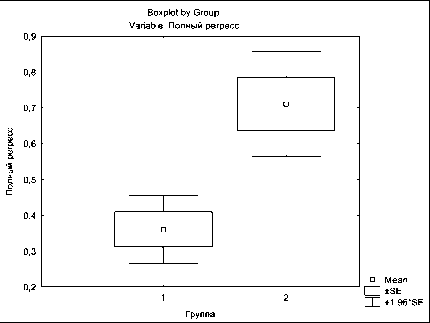
Рис. 2. Частота полных регрессий опухоли. Примечание:
1 – стандартная лучевая терапия, 2 – одновременная химиолучевая терапия с дроблением дозы 1 Гр + 1,5 Гр
тканей и органов полости рта и ротоглотки, возникшие в сроки более 3 мес после завершения терапии, были оценены у 90 пациентов после химиолучевого лечения и у 94 – после СЛТ. В 4 случаях имел место летальный исход от основного заболевания в течение 2 мес после окончания лечения, эти больные не были включены в анализ. Полученные данные свидетельствуют, что после ХЛТ с дроблением дозы 1 Гр + 1,5 Гр отмечается устойчивая тенденция к снижению частоты поздних лучевых повреждений нормальных тканей в зоне облучения, которые имели место у 8 (8,9 %) из 90 больных (рис.1), в то время как после лучевой терапии стандартным облучением эти осложнения возникли у 19 (20,2 %) из 94 пациентов (р>0,05). Остеорадионекрозы нижней челюсти были наиболее частым осложнением и развились у 24 из 184 больных – 13,0 %. При этом у 21 (87,5%) пациента остеорадионекрозы были III и IV степени тяжести и у 3 (12,5 %) – II степени тяжести.
После химиолучевой терапии в режиме 1 Гр + 1,5 Гр данное повреждение имело место у 8 (8,9 %) пациентов, а после стандартной лучевой терапии – у 16 (17 %) больных. После СЛТ также возникали повреждения в виде лучевой язвы, выраженного фиброза языка и атрофического фарингита (3,2 %).
Оценка кумулятивного погодового накопления поздних лучевых повреждений у 27 больных с постлучевыми осложнениями выявила его различный характер при сравниваемых методах лечения (табл. 2). После химиолуче-вой терапии с дроблением дозы 1 Гр + 1,5 Гр на протяжении первых двух лет отмечается своеобразная «стабилизация» накопления лучевых повреждений и лишь к 3-летнему сроку наблюдения их количество составляет 50,0 %, достигая 75,0 % интервального накопления к 4-му году наблюдения. После стандартного лучевого лечения на протяжении первого года развивается практически половина всех по-
Таблица 2
Кумулятивное накопление поздних лучевых повреждений нормальных тканей и органов полости рта и ротоглотки
|
Метод лечения |
Сроки развития повреждений |
||||
|
1 год |
2 года |
3 года |
4 года |
> 4 лет |
|
|
СЛТ |
9/19 (47,4 %) |
15/19 (78,9 %) |
16/19 (84,2 %) |
18/19 (94,7 %) |
19/19 (100 %) |
|
ХЛТ |
1/8 (12,5 %) |
1/8 (12,5 %) |
4/8 (50,0 %) |
6/8 (75,0 %) |
8/8 (100 %) |
|
Всего |
10/27 (37,0 %) |
16/27 (59,3 %) |
20/27 (74,1 %) |
24/27 (88,9 %) |
27/27 (100 %) |
Примечание: в числителе – количество накоплений, в знаменателе – общее число повреждений. СИБИРСКИЙ ОНКОЛОГИЧЕСКИЙ ЖУРНАЛ. 2011. №3 (45)
вреждений – 47,4 %, и в течение первых трех лет количество их достигает 84,2 %.
Сравнительная оценка непосредственной эффективности лечения показала, что после химиолучевой терапии с дроблением дозы 1 Гр + 1,5 Гр частота объективных ответов (сумма полных и частичных регрессий) составила 97,8 %, после стандартной лучевой терапии – 61,9 %, различия статистически значимые (р<0,001). При этом при химиолучевой терапии в режиме фракционирования дозы 1 Гр и 1,5 Гр полная регрессия опухоли отмечена у 60 из 91 пациента – 65,9 %, а после лучевой терапии стандартным облучением – у 35 из 97 – 36,1 % (рис. 2). Частичная регрессия опухоли получена у 29 (31,9 %) и 25 (25,8 %) больных соответственно. Стабилизация опухолевого процесса – у 2 (2,2 %) после ХЛТ и у 37 пациентов (38,1%) – после СЛТ.
При оценке эффективности лечения была отмечена зависимость частоты объективных ответов от величины очаговой дозы, подведенной к опухоли до перерыва. Так, в процессе химиолучевой терапии в режиме 1 Гр и 1,5 Гр до перерыва к опухоли подводится большая суммарная очаговая доза – 34,7 ± 6,2 Гр по сравнению со стандартной лучевой терапией – 30,2 ± 6,8 Гр (р<0,05). Это усиливает лучевое повреждение новообразования и уменьшает риск репопуляции опухолевых клеток. Следствием этого является достоверно большая частота объективных ответов (97,8 %) и полных регрессий опухоли (65,9 %) после химиолучевого лечения в режиме 1 Гр + 1,5 Гр по сравнению с лучевой терапией стандартным облучением – 61,9 % и 36,1 % соответственно. На основании полученных данных можно предположить более тесную корреляцию между режимом облучения 1 Гр + 1,5 Гр в схеме химиолучевого лечения и такими биологическими характеристиками опухоли, как репарация и репопуляция, что делает эту методику более эффективной по сравнению с лучевой терапией стандартным облучением.
Таким образом, одновременная химиолу-чевая терапия с дроблением ежедневной дозы
1 Гр + 1,5 Гр с высокой степенью достоверности оказалась более эффективной, чем стандартное лучевое лечение по частоте объективных ответов и полных регрессий опухоли при отсутствии увеличения количества ранних лучевых реакций и поздних лучевых повреждений нормальных тканей.
Выводы
Химиолучевая терапия с дроблением ежедневной дозы 1 Гр + 1,5 Гр с 4–6-часовым интервалом до суммарной очаговой дозы 60 Гр является эффективным и безопасным методом лечения больных раком полости рта и ротоглотки и имеет существенные клинические преимущества по сравнению со стандартной лучевой терапией.


