Хирургическое лечение регионарного рецидива рака желудка после комбинированного лечения с неоадъювантной химиолучевой терапией (клиническое наблюдение)
Автор: Скоропад Виталий Юрьевич, Костюк Игорь Петрович, Евдокимов Леонид Валерьевич, Титова Людмила Николаевна, Кудрявцев Дмитрий Дмитриевич, Агабабян Татев Артаковна, Куприянова Екатерина Ивановна
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Случай из клинической практики
Статья в выпуске: 2 т.17, 2018 года.
Бесплатный доступ
Актуальность. Рак желудка сохраняет ведущие позиции среди показателей онкологической заболеваемости и смертности в России и в мире. Несмотря на прогресс в диагностике, хирургическом и комбинированном лечении (расширение объема лимфодиссекции, применение адъювантной химиотерапии), общая пятилетняя выживаемость не превышает 25-30 %, а отдаленные метастазы и локо-регионарные рецидивы развиваются более чем у 50 % больных. Рецидивы заболевания связаны не только с уже имеющимися на момент операции микрометастазами; раковыми комплексами, не удаленными в процессе операции, но и с диссеминацией опухолевых клеток в процессе мобилизации желудка или при лимфодиссекции. Даже после выполнения радикального хирургического вмешательства прогноз остается крайне неблагоприятным. Стандартизированных методов лечения изолированных регионарных рецидивов до сих пор не разработано. Описание. Представлено клиническое наблюдение пациента 75 лет с диагнозом: Рак проксимального отдела желудка, по результатам морфологического заключения выявлена высокодифференцированная тубулярная аденокарцинома желудка. По поводу основного заболевания проведено комплексное лечение, на первом этапе выполнена неоадъювантная химиолучевая терапия (СОД 45 Гр по методике суперфракционирования), конкурентная химиотерапия по модифицированной схеме Capox, с последующей гастрэктомией и лимфодиссекцией D2. При контрольном обследовании выявлен изолированный регионарный рецидив рака желудка. На мультидисциплинарном консилиуме решено провести хирургическое лечение. Заключение. Тактика лечения при регионарном рецидиве рака желудка не стандартизована, при этом хирургическое лечение является методом выбора, особенно в тех случаях, когда больному уже была проведена неоадъювантная химиолучевая терапия. По данным литературы, медиана выживаемости таких пациентов не превышает нескольких месяцев. Ключевым моментом, определяющим эффективность неоадъювантной терапии, является достижение полного или выраженного лечебного патоморфоза, что, по данным зарубежных авторов, выражается в статистическом повышении показателя выживаемости по сравнению с хирургическим подходом. В связи с этим крайне важным представляется поиск иммуногистохимических, молекулярно-генетических маркеров, с помощью которых можно было бы прогнозировать ответ опухоли на неоадъювантную терапию для ее проведения только у потенциальных «респондентов»
Рак желудка, неоадъювантная химиолучевая терапия, регионарный рецидив, хирургическое лечение
Короткий адрес: https://sciup.org/140254167
IDR: 140254167 | УДК: 616.33-006.6-08-059-036.65-089 | DOI: 10.21294/1814-4861-2018-17-2-104-110
Surgical treatment of regional recurrence from gastric cancer after multimodal treatment with neoadjuvant chemoradiotherapy (a case report)
Background. Gastric cancer is the fourth most common cancer and the second leading cause of cancer-related death worldwide. Despite many advances in the diagnosis and treatment of gastric cancer, the overall five-year survival rate does not exceed 25-30 %, and distant metastases and loco-regional recurrence develop in more than 50 % of patients. Disease recurrence is not only associated with the presence of tumor micro-metastases at the time of surgery, but also with dissemination of tumor cells during mobilization of the stomach or lymph node dissection. Even after performing radical surgery, the prognosis remains extremely unfavorable. No standardized methods of treatment for isolated loco-regional recurrence have been developed yet. Cases of successful treatment of distant metastases and regional recurrence are sporadic. Case report. We present the case of a 75-year-old patient with histologically proven well-differentiated tubular adenocarcinoma of the stomach. The patient underwent neoadjuvant chemoradiation therapy (total radiotherapy dose was 45 Gy, modified Capox regimen) followed by gastrectomy and D2lymph node dissection. The control examination revealed an isolated regional recurrence of gastric cancer. It was decided to perform surgical treatment for isolated regional gastric cancer recurrence. Conclusion. There is no standardized approach to the treatment of regional recurrence of gastric cancer. Surgical treatment in such cases is a method of choice, especially for patients who previously received neoadjuvant chemoradiotherapy. According to the worldwide literature, the median survival of such patients does not exceed a few months. The key point that determines the effectiveness of neoadjuvant therapy is the achievement of complete or partial pathological response to therapy, thus demonstrating improved survival compared to surgery alone. Therefore, it is extremely important to search for immunohistochemical and molecular genetic markers for predicting tumor response to neoadjuvant therapy in order to administer it for only potential responders.
Текст научной статьи Хирургическое лечение регионарного рецидива рака желудка после комбинированного лечения с неоадъювантной химиолучевой терапией (клиническое наблюдение)
С учетом распространенности опухолевого процесса, на мультидисциплинарном консилиуме было принято решение о проведении на первом этапе лечения курса химиолучевой терапии. С 14.11 по 6.12.13 был проведен курс неоадъювантной химиолучевой терапии: СОД 45 Гр, разовая очаговая доза подводилась по методике суперфракционирования дозы 1 + 1,5 Гр с интервалом между фракциями 4 – 5 ч, что соответствует 84 ед. ВДФ, и изоэффективно 50 Гр классического фракционирования. Применяли статическое трехпольное облучение высокоэнергетическими фотонами на аппарате «Philips SL 20» с энергией тормозного пучка 6 МэВ. Продолжительность курса облучения составила 18 дней (с учетом выходных – 24 дня). Химиотерапия проводилась конкурентно следующими препаратами: капецитабин в дозе 1850 мг/ м2 per os за 2 приема с интервалом 12 ч в течение всего курса лучевой терапии; оксалиплатин в дозе 85 мг/м2 вводился внутривенно капельно в 1-й и 21-й дни. Лечение больной перенес удовлетворительно, наблюдалась гастроинтестинальная и гематологическая токсичность I ст.
Повторное обращение и госпитализация в МРНЦ 28.09.15. с жалобами на слабость, нарушение прохождения пищи, похудание. Ухудшение состояния отмечает с июля 2015 г. При осмотре состояние средней тяжести; больной истощен – при росте 180 см, вес – 52 кг (ИМТ=16 кг/м2). Ла-
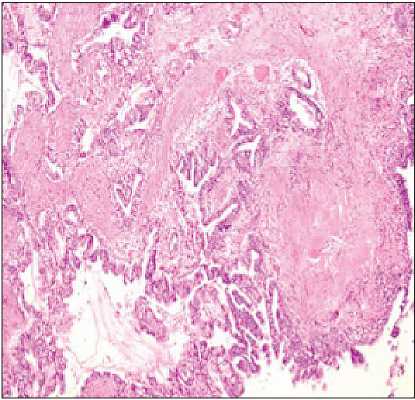
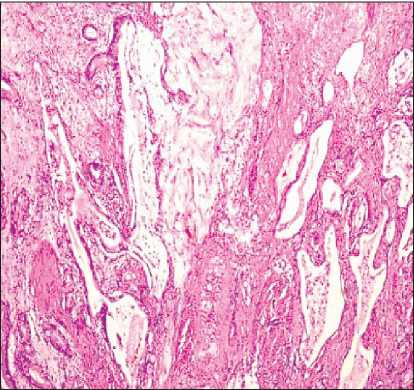
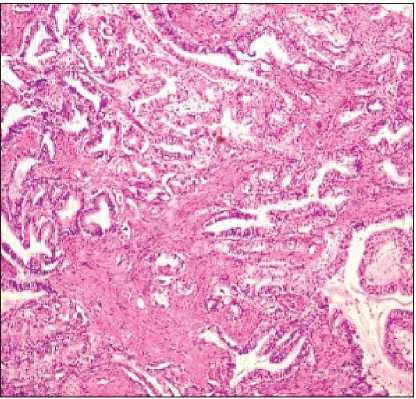
Рис. 3. Микрофото. Фрагменты препарата рецидивной опухоли: среди грубоволокнистой соединительной ткани стромы инвазивный рост аденокарциномы кишечного типа. Окраска гематоксилином и эозином, ×40
бораторно отмечается умеренный лейкоцитоз, увеличение общего билирубина (39,9 мкмоль/л) за счет непрямой (32,5 мкмоль/л) и прямой (7,4 мкмоль/л) фракций.
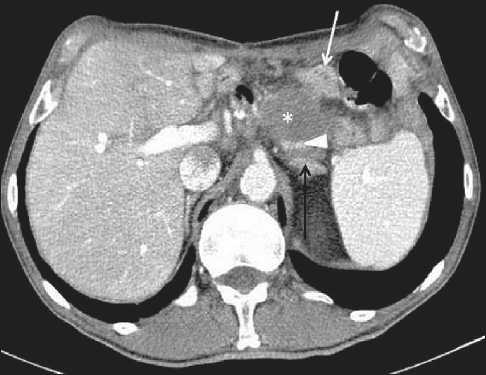
По данным СКТ органов брюшной полости, в зоне оперативного вмешательства, в поддиафрагмальном пространстве определяется рецидивная опухоль неправильной формы, с нечеткими контурами, неоднородной структуры за счет участков пониженной плотности, слабо накапливающая рентгеноконтрастное вещество, размерами 60×47×45 мм. Образование плотно, без четких границ прилежит к отводящей петле тонкой кишки, распространяется на стенку поперечноободочной кишки, тело поджелудочной железы и левый надпочечник (рис. 4).
Макропрепарат: органокомплекс, размерами 15×7×4 см, состоящий из прочно спаянных между собой плотной белесоватой опухоли (5×5×4 см), селезенки (9×6×3 см), дистальных отделов поджелудочной железы (7×1,6×1,5 см), надпочечника (4×0,8×1,5 см), фрагментов толстой (5 см длиной) и тонкой (7 см длиной) кишки, а также участка жировой клетчатки (6×3×10 см), покрывающей надпочечник и поджелудочную железу. Гистологическое заключение: опухоль представляет собой коллагенизированную фиброзную ткань, между волокнами которой многочисленные структуры железистого рака. Опухоль врастает в поджелудочную железу, надпочечник, стенку толстой кишки, прорастая ее до уровня слизистой оболочки, серозную оболочку тонкой кишки.
Больной выписан 28.10.15, в удовлетворительном состоянии, под наблюдение онколога по месту жительства, рекомендовано проведение химиотерапии. По сведениям Брянского ООД, умер в июне 2017 г. от прогрессирования опухоли.
Обсуждение
Данная работа проводилась в рамках выполнения тем государственного задания МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России за 2015–17 гг., промежуточные итоги выполнения нашли отражение в обобщающей публикации [15].
Список литературы Хирургическое лечение регионарного рецидива рака желудка после комбинированного лечения с неоадъювантной химиолучевой терапией (клиническое наблюдение)
- D'Angelica M., Gonen M., Brennan M.F., Turnbull A.D., Bains M., Karpeh M.S. Patterns of initial recurrence in completely resected gastric adenocarcinoma. Ann Surg. 2004 Nov; 240 (5): 808-816. DOI: 10.1097/01.sla.0000143245.28656.15
- Muratore A., Zimmitti G., Lo Tesoriere R., Mellano A., Massucco P., Capussotti L. Low rates of loco-regional recurrence following extended lymph node dissection for gastric cancer. Eur J Surg Oncol. 2009 Jun; 35 (6): 588-92. DOI: 10.1016/j.ejso.2008.12.012
- Lehnert T., Rudek B., Buhl K., Golling M. Surgical therapy for loco-regional recurrence and distant metastasis of gastric cancer. Eur J Surg Oncol. 2002 Jun; 28 (4): 455-61.
- Yoo C.Y., Noh S.H., Shin D.W. Choi S.H., Min J.S. Recurrence following curative resection for gastric carcinoma. Br J Surg. 2000 Feb; 87 (2): 236-42. DOI: 10.1046/j.1365-2168.2000.01360.x
- Dikken J.L., van de Velde C.J., Coit D.G., Shah M.A., Verheij M., Cats A. Treatment of resectable gastric cancer. Therap Adv Gastroenterol. 2012 Jan; 5 (1): 49-69. DOI: 10.1177/1756283X11410771


