Хроническая сердечная недостаточность. Распространенность, варианты течения и прогноз
Автор: Муркамилов И.Т., Айтбаев К.А., Юсупов Ф.А., Райимжанов З.Р., Юсупова Т.Ф., Солижонов Ж.И., Боймуродов Й.Р., Закиров О.Т., Хабибуллаев К.К.
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Медицинские науки
Статья в выпуске: 5 т.11, 2025 года.
Бесплатный доступ
Сердечная недостаточность (СН) — это клинико-функциональный синдром, обусловленный систолической и/или диастолической дисфункцией миокарда на фоне структурных или функциональных нарушений сердца, проявляющийся системной гипоперфузией тканей и венозным застоем при сохранённом кровенаполнении сердца (М.М. Миррахимов). В настоящее время миллиарды людей во всём мире находятся в группе повышенного риска развития СН. В общей популяции наиболее частыми причинами СН являются артериальная гипертензия, ишемическая болезнь сердца и сахарный диабет 2 типа. У мужчин основным этиологическим фактором является ишемическая болезнь сердца, тогда как у женщин — обменные и метаболические нарушения, ассоциированные с СН. Прогноз при СН остаётся неблагоприятным: смертность пациентов при острой СН III и IV функциональных классов составляет 44 и 85%, соответственно. Медиана дожития пациентов с I–II функциональными классами хронической СН составляет 8,4 года, тогда как при III–IV функциональных классах — всего 3,8 года. В данной статье представлено описание клинического случая хронической СН ишемической этиологии с низкой фракцией выброса левого желудочка у пациентки К., 1959 г.р., проживающего в сельской местности. Срок наблюдения после выписки из стационара составил 6 лет 9 месяцев (2473 дней). Публикация сопровождается таблицами и иллюстрациями, что способствует лучшему восприятию представленного материала.
Хроническая сердечная недостаточность, фракция выброса левого желудочка, распространённость, хроническая аневризма сердца, фибрилляция предсердий, фенотип, прогноз, электронный паспорт здоровья
Короткий адрес: https://sciup.org/14132417
IDR: 14132417 | УДК: 616-01/09.616-005 | DOI: 10.33619/2414-2948/114/32
Chronic Heart Failure. Prevalence, Clinical Course Variants, and Prognosis
Heart failure (HF) is a clinical and functional syndrome caused by systolic and/or diastolic myocardial dysfunction against the background of structural or functional cardiac abnormalities. It manifests as systemic tissue hypoperfusion and venous congestion while maintaining cardiac filling (M.M. Mirrakhimov). Currently, billions of people worldwide are at increased risk of developing HF. In the general population, the most common causes of HF are arterial hypertension, coronary artery disease, and type 2 diabetes mellitus. In men, the primary etiological factor is coronary artery disease, whereas in women, metabolic disorders associated with HF are more prevalent. The prognosis for HF remains poor: the mortality rate for patients with acute HF of functional classes III and IV is 44% and 85%, respectively. The median survival for patients with chronic HF of functional classes I–II is 8.4 years, while for those with functional classes III–IV, it is only 3.8 years. This article presents a clinical case of chronic HF of ischemic origin with reduced left ventricular ejection fraction in a female patient, K., born in 1959, residing in a rural area. The follow-up period after hospital discharge was 6 years and 9 months (2,473 days). The publication includes tables and illustrations to enhance the comprehension of the presented material.
Текст научной статьи Хроническая сердечная недостаточность. Распространенность, варианты течения и прогноз
Бюллетень науки и практики / Bulletin of Science and Practice Т. 11. №5 2025
УДК 616-01/09.616-005
Сердечная недостаточность (СН) — это клинико-функциональный синдром, обусловленный систолической и/или диастолической дисфункцией миокарда вследствие структурных или функциональных нарушений сердца. Она характеризуется системной гипоперфузией тканей и венозным застоем при сохранённом кровенаполнении сердца. Впервые такое определение СН было предложено академиком РАМН М. М. Миррахимовым в 1997 году. СН является полиэтиологическим и прогрессирующим заболеванием. По данным 2018 года, хронической СН страдали 37 миллионов человек во всём мире, а к 2022 году это число превысило 40 миллионов [1]. В Российской Федерации, согласно отчётам отечественных исследователей, число пациентов с СН превышает 7 миллионов, при этом ежегодно регистрируется около 170 тысяч новых случаев [2]. По данным И. В. Фомина, количество пациентов с хронической СН III–IV функциональных классов в России превысило 4,5 миллиона человек [3].
Распространённость хронической СН продолжает расти вследствие увеличения доли населения с хроническими инфекционными и неинфекционными заболеваниями, повышения средней продолжительности жизни и совершенствования методов лечения сердечнососудистых заболеваний (ССЗ). По прогнозным расчётам, к 2050 году распространённость хронической СН возрастёт на 60% по сравнению с 2010 годом, главным образом за счёт старших возрастных групп [4–6].
На данный момент каждый второй пациент с хронической СН повторно госпитализируется в течение шести месяцев после выписки, а каждый четвёртый — в течение 30 дней [7]. Риск повторной госпитализации особенно высок у пациентов с сахарным диабетом 2 типа (СД2), дилатационной кардиомиопатией, а также у лиц, перенесших аортокоронарное шунтирование (АКШ). Во всём мире несколько миллиардов человек имеют повышенный риск развития хронической СН. Наиболее распространёнными её причинами являются артериальная гипертензия (АГ), ишемическая болезнь сердца (ИБС), СД2, избыточная масса тела и ожирение, хроническая обструктивная болезнь лёгких, клапанные пороки сердца, миокардиты, хроническая болезнь почек (ХБП), дисфункция щитовидной железы, анемии, хроническая алкогольная интоксикация, перикардиты и иммуновоспалительные ревматические заболевания.
В Международной классификации болезней X пересмотра (МКБ-10) класс IX «Болезни системы кровообращения» включает рубрику I50 «Сердечная недостаточность», однако правожелудочковая сердечная недостаточность в ней не выделяется как отдельный диагноз. В клинической практике преимущественно описывается левожелудочковая сердечная недостаточность. Классификация СН по скорости развития симптомов и/или признаков миокардиальной дисфункции представлена на рисунке 1. Традиционно СН подразделяется на острую и хроническую формы. В клинической практике внутренних болезней острая СН может развиваться вследствие острого инфаркта миокарда (ОИМ), тампонады сердца, фибрилляции желудочков, а также длительной артериальной гипотонии на фоне гиперволемии.
Согласно классификации Thomas Killip и John T. Kimball, острая СН протекает стадийно, отражая степень и тяжесть снижения глобальной функции левого и/или правого желудочка [8]. Так, у пациентов с ОИМ и функциональным классом I острой СН при аускультации лёгких и сердца хрипы и третий тон сердца не выявляются, что свидетельствует о бессимптомной дисфункции левого желудочка (ЛЖ). II функциональный класс острой СН характеризуется появлением застойных хрипов в лёгких. III функциональный класс проявляется распространёнными застойными хрипами в лёгких (> 50% их поверхности), что часто сопровождается клинической картиной отёка лёгких (Риунок 1). IV функциональный класс соответствует состоянию кардиогенного шока и сопровождается такими симптомами, как спутанность сознания, слабый пульс на периферических артериях, нитевидная пульсация сосудов, олигурия, выраженный диффузный цианоз. По данным многочисленных исследований, смертность пациентов с острой СН при III и IV функциональных классах составляет 44–85% [9–11].

I — функциональный класс. Нет застойных явлений;
II — функциональный класс: умеренные застойные явления и/или умеренные признаки дисфункции правых отделов сердца;
III — функциональный класс: часто клиническая картина кардиогенного отека легких.
IV — функциональный класс: часто картина кардиогенного шока.
I — функциональный класс. Ограничение физической активности отсутствуют: привычная физическая активность не сопровождается быстрой утомляемостью, появлением одышки или сердцебиением. Повышенную нагрузку пациент переносит, но она может сопровождаться одышкой и/или замедленным восстановлением сил.
II — функциональный класс. Незначительное ограничение физической активности: в покое симптомы отсутствуют, привычная физическая активность сопровождается утомляемостью, одышкой или сердцебиением. III — функциональный класс. Заметное ограничение физической активности: в покое симптомы отсутствуют, физическая активность меньшей интенсивности по сравнению с привычными нагрузками сопровождается появлением симптомов.
IV — функциональный класс. Невозможность выполнить какую-либо физическую нагрузку без появления дискомфорта; симптомы ХСН присутствуют в покое и усиливаются при минимальной физической активности.
Рисунок 1. Классификация сердечной недостаточности по скорости развития
Хроническая СН — один из наиболее распространённых синдромов среди пациентов с хроническими инфекционными и неинфекционными заболеваниями. Истинная распространённость хронической СН во всём мире может достигать нескольких миллиардов человек. Наибольшее число пациентов с этим синдромом сосредоточено в терапевтических стационарах. В клинической практике широко применяется классификация хронической СН, предложенная Нью-Йоркской кардиологической ассоциацией (NYHA, New York Heart Association) [12]. Согласно данной классификации, хроническая СН подразделяется на функциональные классы (Рисунок 1), что позволяет оценить выраженность симптомов и степень переносимости физической нагрузки [13]. Примечательно, что эта классификация охватывает как систолический, так и диастолический варианты СН (Рисунок 2).
Быстрый рост числа пациентов с хронической СН, различающихся по полу, возрасту, нозологическим формам, географическим особенностям и фенотипу заболевания, требует пересмотра существующей классификации. В последние пять лет этот вопрос активно обсуждается в научном сообществе [14, 15]. Классификация СН по нарушениям функции ЛЖ представлена на Рисунке 2. Частота встречаемости систолической и диастолической СН варьирует в зависимости от её этиологии. Так, на ранних стадиях АГ, ИБС и СД2 преимущественно выявляются нарушения расслабления ЛЖ, свидетельствующие о
Бюллетень науки и практики / Bulletin of Science and Practice Т. 11. №5 2025 диастолической дисфункции. Однако в большинстве случаев систолическая дисфункция ЛЖ предшествует развитию диастолических нарушений. Клиницисты чаще диагностируют СН именно на стадии систолической дисфункции ЛЖ, поскольку она сопровождается классическими симптомами заболевания. Согласно опубликованным исследованиям, хроническая СН часто сочетается с АГ — в 85,6% случаев. Одновременное наличие АГ и ИБС отмечается у 81,3% пациентов [16]. По данным российских исследований [2], распространённость хронической СН составляет 1% среди лиц в возрасте 50–59 лет и достигает 10% среди пациентов старше 80 лет. Примечательно, что около 80% пациентов, госпитализированных в терапевтические стационары с диагнозом, хроническая СН — это лица старше 65 лет.

Рисунок 2. Классификация сердечной недостаточности по нарушениям функции ЛЖ
В клинической практике также применяется классификация СН, предложенная Европейским обществом кардиологов (ЕОК, ESC — European Society of Cardiology) в 2008 году [17]. В её рамках выделяют следующие формы: острая декомпенсация хронической СН, острая СН при гипертоническом кризе, кардиогенный отёк лёгких, кардиогенный шок, острая СН при остром коронарном синдроме и правожелудочковая СН. Кроме того, используется и другая классификация СН (Таблица 1).
Таблица 1
ОБЩЕПРИНЯТАЯ КЛАССИФИКАЦИЯ СЕРДЕЧНАЯ НЕДОСТАТОЧНОСТЬ СН
|
По происхождению |
По первичному нарушению |
По пораженному отделу сердца |
По скорости развития |
|
Миокардиальная |
Кардиогенная |
Левожелудочковая |
Острая (застойный и гипокинетический тип) |
|
Перегрузочная |
Некардиогенная |
Правожелудочковая |
Хроническая |
|
Смешанная |
Тотальная |
Следует отметить, что различные существующие классификации СН были адаптированы на основе клинической классификации хронической СН, предложенной советскими исследователями (Таблица 2) [18].
Эхокардиография (ЭхоКГ) как неинвазивный метод диагностики заболеваний сердца широко применяется в клинической практике. Оценка глобальной функции ЛЖ играет ключевую роль в определении сроков развития и типов происхождения СН. Фракция выброса ЛЖ (ФВ ЛЖ) — важнейший интегральный показатель, используемый для определения фенотипа СН. Она рассчитывается по формуле: ФВ ЛЖ = (КДО ЛЖ — КСО ЛЖ) / КДО ЛЖ × 100%.
Бюллетень науки и практики / Bulletin of Science and Practice Т. 11. №5 2025
Таблица 2 КЛИНИЧЕСКАЯ КЛАССИФИКАЦИЯ ХРОНИЧЕСКОЙ СН по Н.Д. Стражеско и В.Х. Василенко, 1935г.
Стадии Клинические признаки
I Признаки СН: тахикардия, одышка, цианоз отсутствуют в покое. Признаки СН появляются при физической нагрузке
II Признаки имеются в состоянии покоя
-
II A Признаки застоя в одном круге кровообращения:
Левожелудочковая недостаточность — одышка, цианоз, тахикардия, приступы сердечной астмы, «застойные хрипы в легких».
Правожелудочковая недостаточность — одышка, цианоз, тахикардия, набухание шейных вен, увеличение печени, отеки.
IIB Тотальная. Застой в большом и малом круге кровообращения
-
III Постоянное присутствие признаков / симптомов СН. Наличие дистрофических изменений
внутренних органов: асцит, желтуха, снижение массы тела ≤ 18,5 кг/м2, трофические изменения и/или пигментация кожи
Примечание: СН – сердечная недостаточность
Согласно рекомендациям Российского кардиологического общества (РКО), хроническая СН по уровню фракции выброса ЛЖ подразделяется на: хроническую СН со сниженной фракцией выброса (≤ 40%); хроническую СН с умеренно сниженной фракцией выброса (41–49%); хроническую СН с сохранённой фракцией выброса (≥ 50%) [19].
Важно помнить, что даже при лёгких симптомах СН пациенты могут иметь высокий риск госпитализации и смерти [11]. В этом контексте исследователи выделяют предстадию СН — состояние, при котором у пациента отсутствуют симптомы и/или признаки хронической СН в настоящем и прошлом, но при обследовании выявляются структурные и/или функциональные изменения сердца, а также повышение уровня мозгового натрийуретического пептида. Расширение знаний о факторах риска и предшественниках хронической СН является важной задачей клинической кардиологии. Согласно многочисленным данным, в постсоветских странах основными причинами хронической СН считаются АГ, ИБС и СД2.
Патогенетические принципы лечения хронической СН подробно изложены в российском кардиологическом журнале [19]. Медиана дожития пациентов с I–II функциональными классами хронической СН составляет 8,4 года, а с III–IV функциональными классами — 3,8 года [20]. Патогенез острой и хронической СН детально описан в ведущих учебниках и реферативных журналах [4, 11].
Информация о пациенте. 29.05.2018 г. Пациентка К., 4. 03. 1959 г.р., рост 155 см, вес 43 кг, индекс массы тела (ИМТ) — 17,9 кг/м², площадь поверхности тела — 1,38 м².
Периферических (видимых) отеков нет. Частота дыхательных движений (ЧДД) — 20 в минуту, сатурация кислорода на атмосферном воздухе — 93%. Дыхание над легкими жесткое, хрипов нет. Тоны сердца ослаблены, ритм правильный, частота сердечных сокращений (ЧСС) — 125 уд/мин, артериальное давление (АД) — 105/70 мм рт. ст. Живот мягкий, безболезненный, печень и селезенка не пальпируются. Физиологические отправления самостоятельные, регулярные.
Anamnesis morbi. Повышений АД пациентка не отмечает. С 2016 г. появились приступы стенокардии больших напряжений. В марте 2018 г. впервые госпитализирована в областную больницу по месту жительства с клиникой ОИМ передне-перегородочной локализации с вовлечением верхушки и боковой стенки ЛЖ. В раннем периоде ОИМ осложнился кардиогенным шоком, формированием острой аневризмы сердца и
Бюллетень науки и практики / Bulletin of Science and Practice Т. 11. №5 2025 фибрилляцией предсердий. Из-за отсутствия доступа к интервенционной кардиологии специальные визуализирующие исследования для оценки проходимости инфаркт-связанной коронарной артерии не проводились. После выписки из стационара пациентка в амбулаторных условиях регулярно принимала бета-блокаторы, антиагреганты и статины. На фоне их приема в конце мая 2018 г. госпитализирована в блок кардиореанимации с клиникой острого коронарного синдрома и острой СН.
Результаты обследования: Общий анализ крови (ОАК): Hb — 125 г/л, Ht — 40,5%, эритроциты — 4,5×10¹²/л, тромбоциты — 277×10⁹/л, лейкоциты — 6,3×10⁹/л, СОЭ — 43 мм/ч. Биохимический анализ крови (БАК): глюкоза венозной крови натощак — 4,8 ммоль/л; АЛТ — 10 Ед/л, АСТ — 25 Ед/л; липидный спектр: общий холестерин (ХС) — 4,0 ммоль/л, ХС липопротеинов высокой плотности (ЛПВП) — 1,0 ммоль/л, ХС липопротеинов низкой плотности (ЛПНП) — 2,4 ммоль/л, триглицериды — 1,3 ммоль/л. Функция почек: креатинин — 67 мкмоль/л, расчетная СКФ — 91 мл/мин. Электролиты крови: натрий — 134,6–137,0– 133,9 ммоль/л, калий — 1,06–3,2–3,65 ммоль/л, кальций — 1,22–1,06–1,16 ммоль/л. Электрокардиография (ЭКГ): ритм синусовый, признаки субэндокардиального повреждения в отведениях V7-V9. Рубцовые изменения переднеперегородочной и боковой стенок ЛЖ. Средняя ЧСС пациентки К. за весь период наблюдения представлена на рисунке 3.
ЭхоКГ: размер левого предсердия (ЛП) — 3,5 см, конечно-систолический размер (КСР) ЛЖ — 3,5 см, конечно-диастолический размер (КДР) ЛЖ — 4,5 см, фракция выброса ЛЖ — 16% (Рисунок 9). Толщина межжелудочковой перегородки (МЖП) и задней стенки ЛЖ (ЗСЛЖ) составила 0,85 см.
Выявлены эффект спонтанного контрастирования крови в полости ЛЖ, гипо- и акинез средних и апикальных сегментов МЖП, передней стенки ЛЖ, верхушки ЛЖ, а также апикальных сегментов боковой и нижней стенок ЛЖ. Систолическое давление в легочной артерии — 50 мм рт. ст.
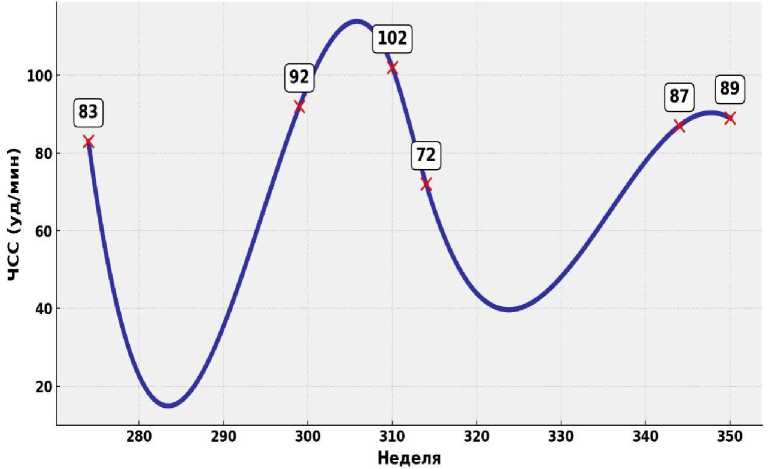
Рисунок 3. Динамика средней частоты сердечных сокращений пациента К., 1959г.р
Ультразвуковое исследование (УЗИ) внутренних органов выявило гемангиому печени, признаки холецистита, а также выпот в правой плевральной полости. По данным рентгенографии органов грудной клетки патологических изменений не выявлено. Рентгенологическое исследование верхнего отдела желудочно-кишечного тракта показало наличие грыжи пищеводного отверстия диафрагмы. Пациентка и её родственники отказались от проведения селективной коронароангиографии.
После выписки из стационара пациентка находилась под наблюдением кардиолога кафедры факультетской терапии, который осуществлял выезды на дом. Следует отметить, что из-за социальных и географических факторов пациентка не смогла приобрести лекарственные препараты для лечения хронической СН. В амбулаторных (домашних) условиях она начала приём ингибиторов ангиотензинпревращающего фермента, антагонистов минералокортикоидных рецепторов и антиагрегантов.
Аnamnesis vitae. Пациентка отрицает инфекционный гепатит, венерические заболевания, туберкулёз и аллергические реакции. Гемотрансфузий не проводилось. Вредные привычки отсутствуют. Акушерский анамнез: 4 беременности, 4 родов.
В 2020 году перенесла новую коронавирусную инфекцию, осложнённую двусторонней полисегментарной пневмонией тяжёлого течения с развитием дыхательной недостаточности. В связи с ограниченной возможностью госпитализации лечение проводилось в домашних условиях. Получала цефалоспорины (цефтриаксон) и антиагреганты. На ЭКГ неоднократно регистрировались эпизоды фибрилляции предсердий, в связи с чем пациентка принимала противоаритмические препараты III класса — блокаторы калиевых каналов (амиодарон), а также сердечные гликозиды (дигоксин) в таблетированной форме. Осенью 2020 года у пациентки обострился хронический панкреатит по диспепсическому типу. На ЭКГ сохранялся низкий вольтаж комплекса QRS (Рисунке 4), ритм синусовый, правильный. Отмечались нарушения процессов реполяризации в миокарде ЛЖ.
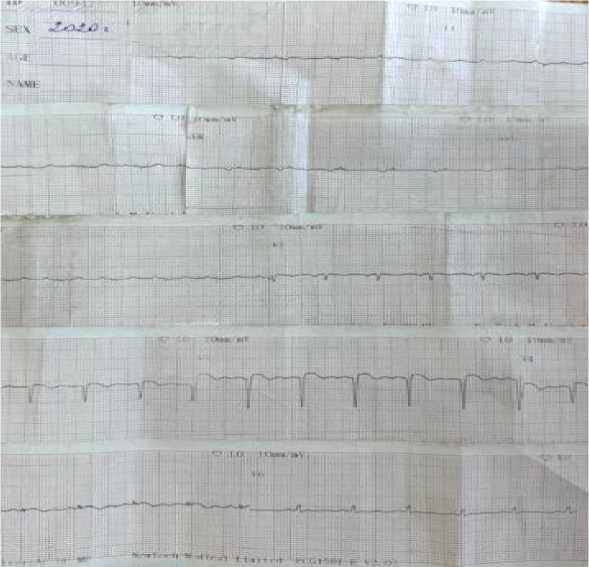
Рисунок 4. ЭКГ пациента К., 1959 г.р. На ЭКГ отмечены признаки фибрилляции предсердий. Низкий вольтаж комплексов QRS в отведениях от конечностей, отсутствие адекватного нарастания амплитуды зубца r в V1 по V6
У пациентки ЭКГ была зарегистрирована в домашних условиях (Рисунок 5) после вызова врача в связи с эпизодами острого респираторного заболевания (ОРЗ). В ходе лечения она принимала ингавирин, диазолин и амоксициллин.
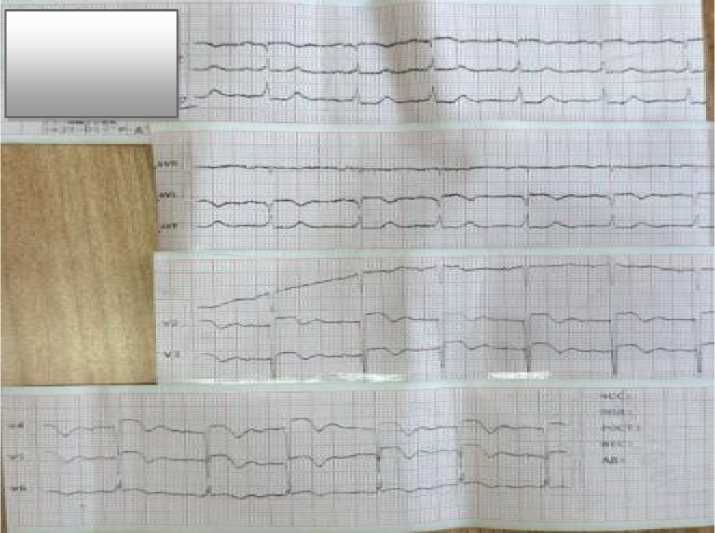
Рисунок 5. ЭКГ пациента К., 1959 г.р. На ЭКГ отмечены признаки замедления атриовентрикулярной проводимости. Косвенные ЭКГ признаки субэндокардиального повреждения (ишемия) в грудных отведениях на фоне хронической аневризмы сердца
В июне 2022 года у пациентки вновь обострился хронический панкреатит, что было связано с погрешностями в диете. На зарегистрированной ЭКГ (Рисунок 6, 7) основной ритм оставался синусовым. Примечательно, что до июня 2022 года симптомы хронической СН (ХСН) в покое у пациентки отсутствовали. Двигательный режим и уровень физической активности соответствовали II функциональному классу (ФК) ХСН.
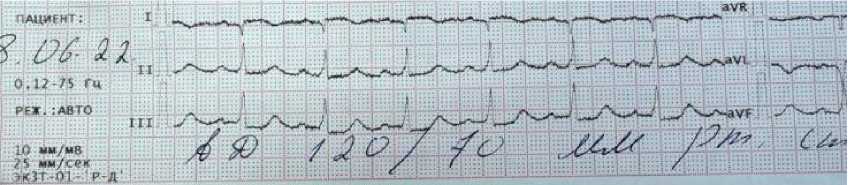
Рисунок 6. Электрокардиография пациента К., 1959 г.р.
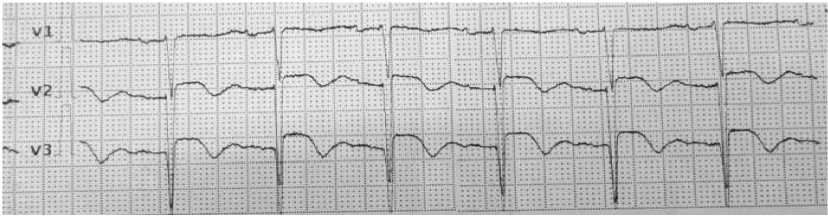
Рисунок 7. Электрокардиография пациента К., 1959г.р. На ЭКГ отмечены признаки хронической аневризмы сердца в грудных отведениях (V2-V3)
В октябре 2022 года на ЭКГ (Рисунок 8) у пациентки сохранялся синусовый ритм, отмечались признаки субэндокардиального повреждения (ишемии) в грудных отведениях на фоне хронической аневризмы сердца. При сборе анамнеза выяснилось, что пациентка нарушила диету, начав употреблять жирную и жареную пищу. Несмотря на рекомендации, она последовательно отказывалась от госпитализации по социальным мотивам.
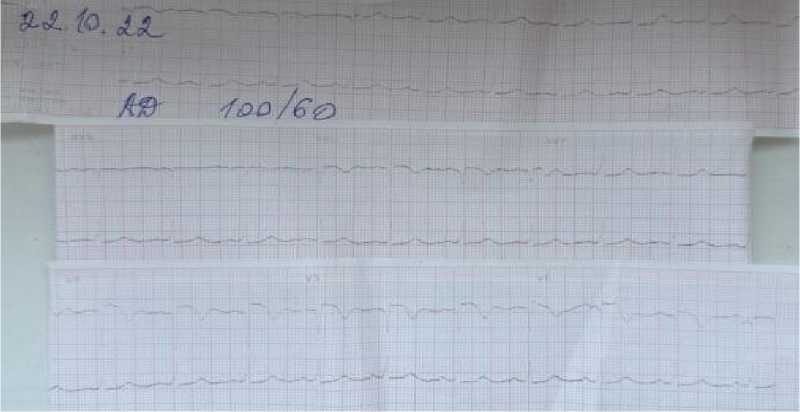
Рисунок 8. Электрокардиография пациента К., 1959 г.р. Основной ритм синусовый, правильный. Косвенные ЭКГ признаки субэндокардиального повреждения (ишемия) в грудных отведениях на фоне хронической аневризмы сердца
На Рисунке 9 представлены показатели эхокардиографии. Следует отметить, что в октябре 2023 года у пациентки в полости ЛЖ сформировался тромб размером 2,4×1,9 см, фиксированный к его верхушке. При ультразвуковом допплерографическом исследовании (УЗДГ) прецеребральных артерий выявлено утолщение комплекса интима-медиа сонных артерий (справа — 1,1 мм, слева — 1,1 мм). В обеих общих сонных артериях (правой и левой) зарегистрированы атеросклеротические бляшки, вызывающие стеноз просвета сосуда на 24% и 36% соответственно.
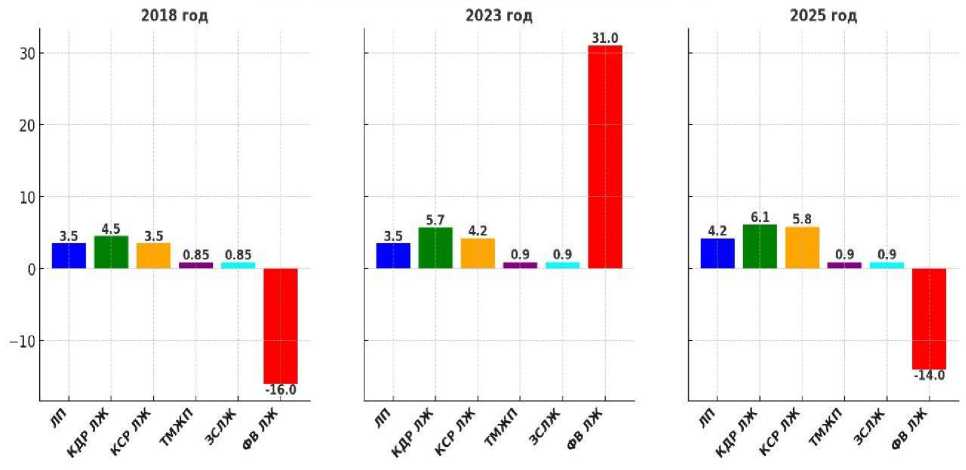
Рисунок 9. Параметры эхокардиографии в динамике пациента К., 1959 г.р
В июле 2024 г. пациентка прошла плановое обследование. ОАК: Hb — 135 г/л, Ht — 44%, эритроциты — 4,97х1012/л, тромбоциты 260х109/л, лейкоциты 6,44х109/л, СОЭ 36
мм/час. Биохимический анализ крови (БАК): глюкоза венозной крови натощак 6,04 ммоль/л, АлТ-21 Ед/л, AcT-30 Ед/л, С-реактивный белок 7,7 мг/л, сывороточный цистатин С 0,99 мг/л, Д-димер 0,29 мг FEU/л. Липидный спектр: общий ХС 5,16 ммоль/л, ХС ЛПВП 0,91 ммоль/л, ХС ЛПНП 3,72 ммоль/л, триглицериды 1,62 ммоль/л. Цитокиновый профиль: нтерлейкин-6 (ИЛ-6, (IL)) — 4,68 пг/мл. Функция почек: уровень креатинина в крови 63,7 мкмоль/л, расчетная скорость клубочковой фильтрации (СКФ) — 95 мл/мин, без отклонений.
бВ феврале 2025 года пациентка вновь прошла обследование (Рис. 9 и 10). ОАК: Hb — 128 г/л, Ht — 41,0%, эритроциты — 4,66×10¹²/л, тромбоциты — 270×10⁹/л, лейкоциты — 5,86×10⁹/л, СОЭ — 45 мм/час. ОАМ: выявлены следы белка, эритроцитурия. БАК: глюкоза венозной крови натощак — 5,89 ммоль/л. АлТ — 21 Ед/л, АсТ — 30 Ед/л. СРБ — 10,4 мг/л. Сывороточный цистатин C — 0,99 мг/л. Д-димер — 0,29 мг FEU/л. Липидный спектр: показатели без изменений по сравнению с предыдущим обследованием. Цитокиновый профиль: ИЛ-6 (IL) — 4,68 пг/мл. Функция почек: уровень креатинина в крови — 56,1 мкмоль/л, расчетная СКФ — 103 мл/мин, без значимых изменений.
А
Б
В
Г
Е
Д
Ж
З
И
К
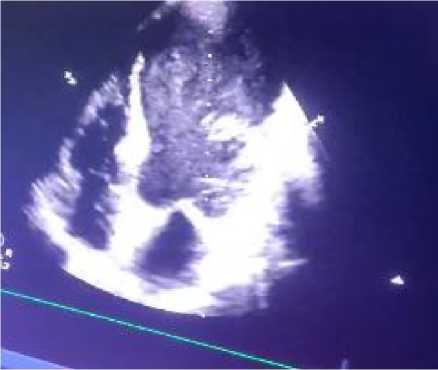
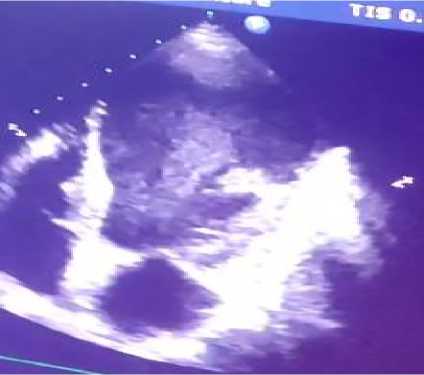
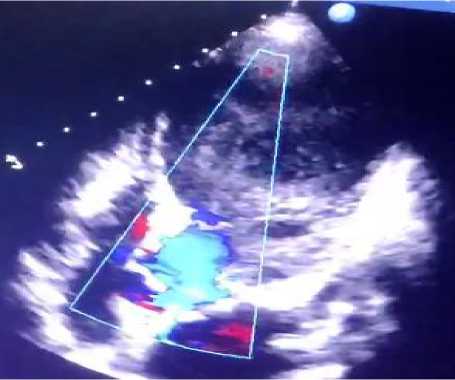
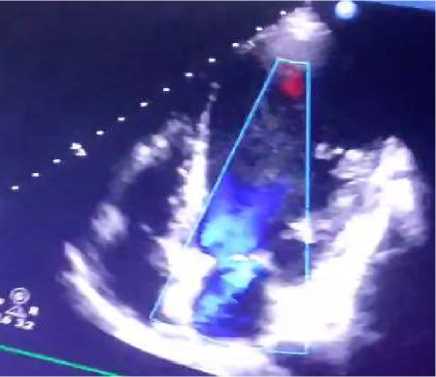
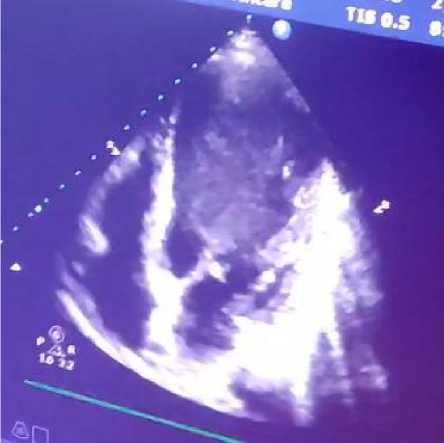
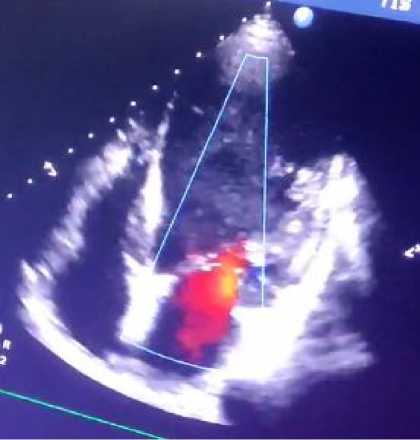
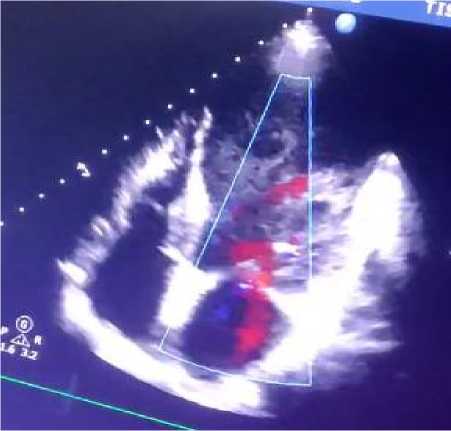
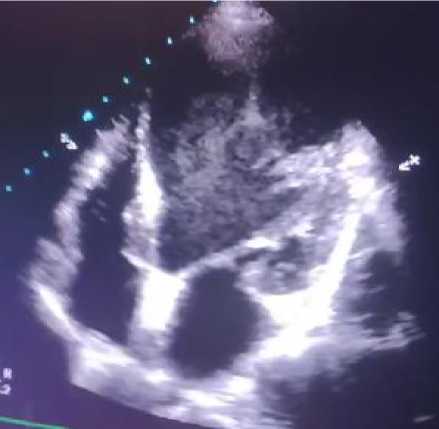
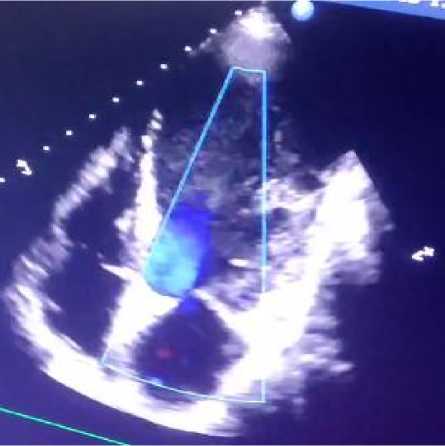
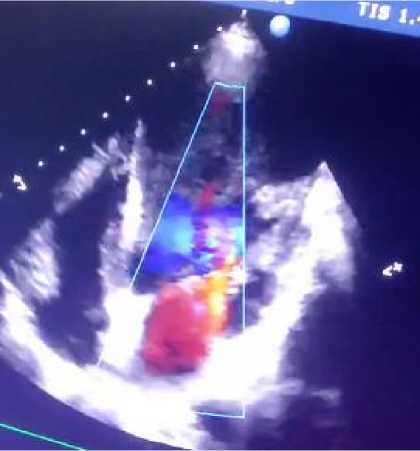
Рисунок 10. А-З. Апикальная, четырехкамерная позиция, В–режим. Визуализируется выраженное расширение полости ЛЖ и замедление кровотока в ней (цветной допплер)
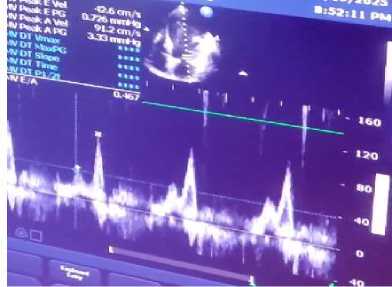
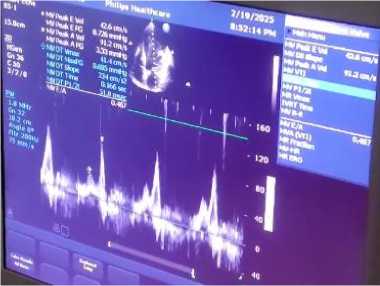
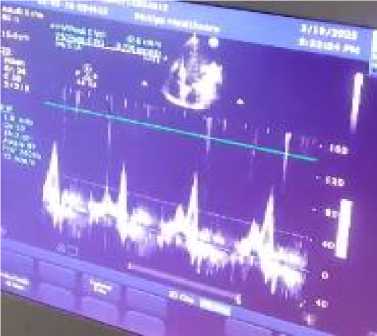
Рисунок 11. Оценка трансмитрального допплерографии
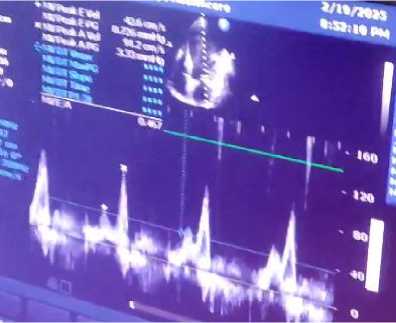
кровотока в режиме импульсно-волновом
Клинический диагноз: ИБС. Постинфарктный кардиосклероз. Аневризма сердца. Мультифокальный атеросклероз. ХСН II–III функциональных классов. Вторичная легочная гипертензия. Сопутствующие заболевания: хронический гастродуоденит, стадия ремиссии. Хронический холецистит в фазе неполной ремиссии. Хронический панкреатит в фазе неполной ремиссии. Лечение: эналаприл — 5 мг/сут., бисопролол — 1,25 мг/сут., верошпирон — 25 мг/сут., торасемид — 10 мг/сут., дигоксин — 0,125 мг/сут., аторвастатин — 20 мг/сут., ривароксабан — 10 мг/сут., ацетилсалициловая кислота — 150 мг/сут. На фоне терапии проявления ХСН субкомпенсированы: приступов сердечной астмы не отмечается, АД — 110/70 мм рт. ст. Пациентка продолжает наблюдаться на клинической базе кафедры факультетской терапии (Рисунок 10). На ЭКГ регистрируется синусовый ритм, картина аневризмы сердца (Рисунок 12).
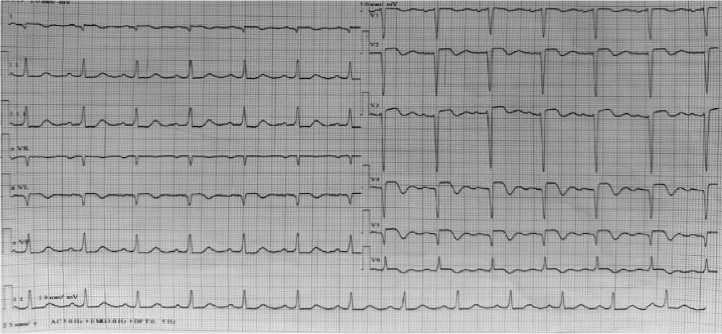
Рисунок 12. Электрокардиография пациента К., 1959 г.р. / дата регистрации 19. 02. 2025 г.
Бюллетень науки и практики / Bulletin of Science and Practice Т. 11. №5 2025
В настоящее время антропометрические показатели пациентки К., 66 года: рост — 155 см, вес — 54 кг, ИМТ — 22,4 кг/м², площадь поверхности тела — 1,52 м². Симптомов хронической СН в покое не отмечает. Срок наблюдения с момента выписки из стационара составил 6 лет 9 месяцев (2473 дней).
Обсуждение
В ходе амбулаторного наблюдения у пациентки К., 66 лет отмечались эпизоды нарушения возбудимости миокарда, в частности, фибрилляция предсердий, которая сама по себе является значимым фактором риска инсульта, увеличивая смертность от сердечнососудистых заболеваний и частых госпитализаций. Согласно многочисленным исследованиям, развитие фибрилляции предсердий у лиц пожилого возраста связано с рядом факторов риска, включая АГ, ХСН, ИБС и эндокринные нарушения [21, 22]. В одном из зарубежных исследований было установлено, что ХСН повышает риск фибрилляции предсердий в 8,5 раза у мужчин и в 14 раз — у женщин [23]. Очевидно, что присоединение фибрилляции предсердий при ХСН значительно ухудшает прогноз, особенно у женщин. Известно, что смертность пациентов с ХСН и низкой фракцией выброса ЛЖ выше, чем у пациентов с ХСН и сохранённой фракцией выброса, вне зависимости от возраста, пола и этиологии заболевания [24]. Так, средний уровень госпитальной и ранней летальности при ХСН составляет 20 и 11% соответственно [25].
Предикторами неблагоприятного исхода при ХСН являются пожилой возраст, наличие митральной регургитации, снижение экскреторной функции почек и III–IV функциональные классы. Примечательно, что у нашего пациента на протяжении всего периода наблюдения значимого ухудшения экскреторной функции почек не отмечалось. Важно подчеркнуть, что к 2025 году у пациентки К., 66 лет было зафиксировано выраженное снижение систолической функции ЛЖ (Рисунок 10, 11). Несмотря на значительное ухудшение сократительной функции ЛЖ, у пациента не наблюдалось отёков нижних конечностей. Вероятно, этому способствовали невысокий ИМТ, а также отсутствие АГ и СД2, что могло повлиять на клиническое проявление застоя в большом круге кровообращения. Имеются данные, свидетельствующие о тесной корреляции между течением и прогнозом ХСН и степенью снижения систолической функции ЛЖ, особенно у пациентов пожилого возраста [26, 27]. На выживаемость пациентов с ХСН значительное влияние оказывает приверженность к терапии. С возрастом приверженность к лечению снижается, что отмечалось и в нашем клиническом наблюдении. В одном из исследований было показано, что низкая приверженность к терапии, наряду с постинфарктным кардиосклерозом, может рассматриваться как фактор, способствующий прогрессированию дисфункции миокарда желудочков [28]. При отсутствии оптимального лечения ИБС у пациентов с ХСН наблюдается прогрессивное снижение фракции выброса ЛЖ, тогда как у пациентов, получающих адекватную терапию, темпы снижения фракции выброса ЛЖ замедляются [26, 27].
Ряд исследований свидетельствует о негативном влиянии коморбидности на когнитивные и адаптационные возможности пациентов с АГ и ХСН. Это способствует развитию депрессивно-ипохондрических состояний, сопровождающихся снижением мотивации и приверженности к лечению, что необходимо учитывать при междисциплинарном подходе к данной категории пациентов [16]. В исследовании Ж.Д. Кобалавой и соавт. (2020) отмечено, что триггерами декомпенсации ХСН являлись низкая приверженность к терапии, тахисистолическая форма фибрилляции предсердий, неэффективный контроль АД и бронхолёгочная инфекция [29]. У нашей пациентки также наблюдались эпизоды бронхолёгочной инфекции (Рисунок 13), а также неоднократные обострения симптомов хронического холецистита и панкреатита.
Рисунок 13. Присоединение бронхолегочной инфекции у пациента К., 1959 г.р.
Примечательно, что срок наблюдения за пациенткой К., 66 лет с момента её выписки из стационара составил 6 лет 9 месяцев (2473 дней). С учётом общей выживаемости пациентов с ХСН и низкой фракцией выброса ЛЖ можно предположить, что продление жизни пациентки было достигнуто благодаря применению традиционной фармакологической терапии. Согласно литературным данным, медиана дожития среди пациентов с ХСН III–IV функциональных классов составляет 3,8 года [20].
Следует отметить, что пациентка К., 66 лет в момент первого эпизода острого коронарного синдрома имела дефицит массы тела (ИМТ = 17,9 кг/м²). В процессе наблюдения и лечения масса тела увеличилась (ИМТ = 22,4 кг/м²). Как уже упоминалось, коррекция сопутствующих заболеваний, в частности, приём ферменто-заместительных препаратов и спазмолитиков при обострениях хронического холецистита и панкреатита, вероятно, оказала благоприятное влияние на качество жизни пациентки. Интересной особенностью данного клинического наблюдения является то, что пациентка К., 66 лет с 10 июня 2018 года находилась под амбулаторным наблюдением и лечением у одного специалиста-кардиолога. Несмотря на эпизод фибрилляции предсердий и низкую фракцию выброса ЛЖ (Рисунок 9 и 10), у пациентки не было выявлено прогрессирования симптомов хронической ишемии мозга. Следует также отметить, что пациентка ни разу не была повторно госпитализирована в стационар по поводу острой декомпенсации ХСН. Кроме того, она не имела возможности получать ингибиторы натрий-глюкозного котранспортера 2го типа (дапаглифлозин или эмпаглифлозин), длительный приём которых при ХСН с низкой фракцией выброса ЛЖ, согласно литературным данным, способствует улучшению сократимости миокарда, регрессу гипертрофии, улучшению диастолической функции ЛЖ, а также снижению жёсткости сосудистой стенки [30‒32].
Описанные и детально иллюстрированные результаты данного длительного клинического наблюдения за пациенткой К., 1959 г.р. представляют определённый научноклинический интерес для исследователей, так как полностью согласуются с принципами персонализированной медицины. Индивидуальный подход, учитывающий половые, возрастные, этнические, географические и социальные особенности, играет ключевую роль в улучшении общей выживаемости пациентов с ХСН вне зависимости от её фенотипа.
Cледует отметить, что не во всех регионах мира имеется достаточное оснащение клинико-диагностическими приборами, необходимыми для своевременной диагностики заболеваний внутренних органов, включая ХСН. В ряде случаев диагноз ХСН устанавливается исключительно на основании клинических и анамнестических данных. В таких ситуациях практикующим врачам важно опираться на фундаментальные диагностические критерии, позволяющие подтвердить или исключить синдром ХСН. Действующий алгоритм диагностики ХСН в клинической практике представлен на Рисунке 14. Врачам, независимо от профиля стационарного лечебно-профилактического учреждения, важно следовать поэтапному алгоритму диагностики и дифференциального подхода при обследовании пациентов с одышкой и/или сердцебиением (Рисунок 14). Чёткая маршрутизация таких пациентов в современных условиях значительно упрощает их ведение и оказывает существенное влияние на прогноз заболевания. Как уже отмечалось, рост числа пациентов с различными инфекционными и неинфекционными заболеваниями, на фоне которых развивается синдром ХСН, подчёркивает необходимость внедрения в клиническую практику концепции «электронного паспорта здоровья». Этот инструмент может способствовать более точному мониторингу состояния пациента, улучшению приверженности к лечению и повышению эффективности медицинской помощи.
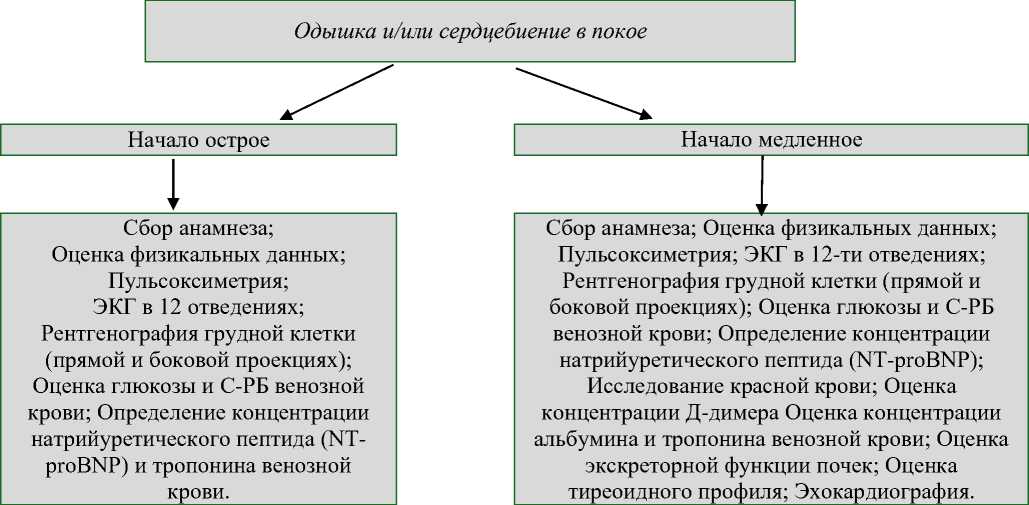
Рисунок 14. Алгоритм диагностического подхода при подозрении на СН в условиях реальной клинической практики
Обсуждая проблемы сердечной недостаточности, нам хотелось бы обратить внимание на аспекты терминологии, особенно в отношении функционального класса I. В клинической практике нередко возникает путаница при его идентификации. Дело в том, что I–II функциональные классы хронической СН зачастую не документируются должным образом или вовсе не фиксируются. Следует подчеркнуть, что в медицинской документации диагноз «СН I функциональный класс» не применяется, хотя в клинической практике такие обозначения, как «острая СН ФК-I» или «СН ФК-I», иногда встречаются. Однако они некорректны. Согласно современным представлениям, наличие острых очаговых изменений миокарда на ЭКГ при инфаркте миокарда уже свидетельствует о развитии острой СН, но в этом случае она классифицируется не как I, а как II функциональный класс, если имеются
Бюллетень науки и практики / Bulletin of Science and Practice Т. 11. №5 2025 клинические проявления. Аналогичный подход должен применяться и к хронической СН: функциональный класс I включает пациентов с высоким риском её развития (на основании данных ЭКГ, ЭхоКГ и других методов), но при наличии симптомов миокардиальной дисфункции диагноз сразу устанавливается как II функциональный класс. Ещё один важный аспект, на который следует обратить внимание при оформлении медицинской документации, — это корректность формулировок в разделе «сердечно-сосудистая система». В частности, нередко встречается выражение «тоны сердца приглушены». Однако с позиций пропедевтики внутренних болезней термин «приглушение» тонов сердца является некорректным, так как в медицинской терминологии он не используется. Правильной формулировкой является «ослабление тонов сердца» или «тоны сердца ослаблены». Кроме того, в клинической практике нередко допускаются неточности при описании выявленных изменений в организме пациента, особенно в разграничении понятий «симптом» и «признак». Симптом — это субъективные ощущения пациента, такие как боль, слабость или головокружение. В то же время признак — это объективные проявления заболевания, которые устанавливаются врачом и могут быть как клиническими (хрипы в лёгких, шумы в сердце, отёки, желтушность склер, увеличение печени, сухость кожи и т.д.), так и лабораторными (например, гипоальбуминемия — снижение концентрации альбумина, гиперкреатининемия — повышение уровня сывороточного креатинина, гиперпролактинемия — повышение уровня пролактина и т.д.).
Представленный клинический случай демонстрирует особенности течения хронической сердечной недостаточности с низкой фракцией выброса в реальной клинической практике. Развитие фибрилляции предсердий, приведшей к декомпенсации сердечной недостаточности и формированию внутриполостного тромба в левом желудочке на фоне аневризмы сердца, подчеркивает необходимость комплексного междисциплинарного подхода к ведению таких пациентов. Хроническая сердечная недостаточность ишемического генеза часто сопровождается эпизодами декомпенсации, обусловленными нарушениями ритма и/или проводимости миокарда, артериальной гипотонией и снижением качества жизни. Дальнейшие исследования должны быть направлены на оптимизацию лечения таких пациентов с применением современных молекулярно-генетических технологий, включая мРНК и некодирующие РНК, а также принципов персонализированной медицины.
Информированное согласие. От родственника пациента было получено письменное добровольное информированное согласие на публикацию описания клинического случая, результатов его обследования и лечения, а также его изображений в медицинском журнале, включая его электронную версию (дата подписания 20. 02. 2025 г.).
Вклад авторов: И.Т. Муркамилов — ведение пациентки с 2018 г по настоящее время, написание данной статьи, суммирование всех данных лабораторной и инструментальной диагностики; К.А. Айтбаев — редактирование статьи; Ф.А. Юсупов, Т.Ф. Юсупова, З.Р. Райимжанов, Ж.И. Солижонов., Й.Р. Боймуродов., О.Т. Закиров., К.К. Хабибуллаев — литературный обзор современных сведений и рекомендаций по ведению пациентов с данной патологией.
Прозрачность исследования. Исследование не имело спонсорской поддержки. Авторы несут полную ответственность за предоставление окончательной версии рукописи в печать.


