Иммунный статус и спектр цитокинов как прогностические признаки риска тяжелого течения заболевания и эффективности интенсивной терапии пациентов с коронавирусной инфекцией COVID-19
Автор: Садыков Валентин Фидаильевич, Полтавцева Римма Алексеевна, Чаплыгина Алина Вадимовна, Бобкова Наталья Викторовна
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Оценка риска в организации здравоохранения
Статья в выпуске: 4 (40), 2022 года.
Бесплатный доступ
Пандемия, вызванная новым штаммом коронавируса SARS-CoV-2 охватила весь мир, однако эффективных способов лечения этой тяжелейшей патологии до сих пор не создано. В настоящее время установлено, что риском тяжелого течения COVID-19 является не столько сам возраст пациента, сколько так называемые возрастные заболевания, в развитии которых прямо или опосредованно задействована ренин-ангиотензиновая система РАС. Вирус SARS-CoV-19 взаимодействует с одним из основных регуляторных элементов этой системы ACE2 и нарушает баланс двух ветвей РАС, что в итоге проявляется в росте уровня ангиотензина II, который через связывание с ангиотензиновым рецептором 1-го типа (AT1R) вызывает целый ряд патологических состояний, включая гипертонию, атеросклероз, сердечно-сосудистые заболевания, усиливает пролиферацию клеток, апоптоз, гибель эндотелиальных клеток сосудов и т.д., что нашло отражение во многих обзорах российских и зарубежных авторов. Однако другой, менее описанной, но не менее важной, мишенью действия ангиотензина II являются клетки врожденного и адаптивного иммунитета. Последствия этого взаимодействия подробно проанализированы в данном обзоре. При COVID-19 активируются дендритные клетки, увеличивается пролиферация макрофагов и инфильтрация нейтрофилов с дальнейшим включением в этот процесс CD4-лимфоцитов и других клеточных элементов системы адаптивного иммунитета. Гиперактивация иммунной системы сопровождается выбросом большого количества провоспалительных цитокинов, что и может привести к реализации цитокинового шторма. Картину усугубляет тормозное действие самого вируса на синтез сигнальных интерферонов на начальных этапах его интернализации в клетку. Отдельный раздел обзора посвящен проблеме прогнозирования риска развития тяжелого состояния и поиску его предикторов, используя анализ состояния РАС и соотношения клеточных элементов иммунной системы, что чрезвычайно важно для принятия решений об объеме необходимой медицинской помощи и стратегиях последующего лечения.
Covid-19, sars-cov-2, цитокиновый профиль, цитокиновый шторм, иммунные клетки, иммунодисрегуляция, фактор прогнозирования, иммунный статус, ренин-ангиотензиновая система (рас)
Короткий адрес: https://sciup.org/142236536
IDR: 142236536 | УДК: 615 | DOI: 10.21668/health.risk/2022.4.14
Immune status and cytokine spectrum as predictors of the risk of severe disease and performance indicators of intensive therapy in patients with coronavirus infection COVID-19
The pandemic caused by a new strain of the SARS-CoV-2 coronavirus has swept the whole world but effective methods for treating this severe pathology have not yet been created. It has now been established that a risk of a severe course of COVID-19 is not so much a patient's age itself, but so-called age-related diseases; the renin-angiotensin system (RAS) is directly or indirectly involved into their development. The SARS-CoV-19 virus interacts with one of the main regulatory elements of this system, ACE2, and disrupts the balance between the two RAS branches. This ultimately manifests itself in an increase in levels of angiotensin II, which, through binding to the angiotensin type 1 receptor (AT1R), causes a number of pathological conditions, including hypertension, atherosclerosis, and cardiovascular diseases, enhances cell proliferation, apoptosis, death of vascular endothelial cells, etc. This process has been described in many reviews by Russian and foreign authors. However, cells of innate and adaptive immunity are another less well-described but no less important target of angiotensin II. The consequences of this interaction are analyzed in detail in this review. With COVID-19, dendritic cells are activated, macrophage proliferation and neutrophil infiltration increase with further involvement of CD4-lymphocytes and other cellular elements of the adaptive immunity in this process. Hyperactivation of the immune system is accompanied with the release of a large amount of pro-inflammatory cytokines, which can lead to the occurrence of a cytokine storm. The picture is aggravated by the inhibitory effect produced by the virus itself on the synthesis of signaling interferons at initial stages in its internalization into the cell. A separate section in the review addresses the problem how to predict a risk of a developing serious condition and search for its predictors by analyzing the state of the RAS and ratios of key cellular elements in the immune system. This is extremely important for making decisions concerning the amount of necessary medical care and strategies for subsequent treatment.
Текст обзорной статьи Иммунный статус и спектр цитокинов как прогностические признаки риска тяжелого течения заболевания и эффективности интенсивной терапии пациентов с коронавирусной инфекцией COVID-19
Садыков Валентин Фидаильевич – анестезиолог-реаниматолог (e-mail: ; тел.: 8 (910) 468-63-98; ORCID: .
Полтавцева Римма Алексеевна – кандидат биологических наук, ведущий научный сотрудник (e-mail: ; тел.: 8 (916) 549-01-68; ORCID: .
Чаплыгина Алина Вадимовна – младший научный сотрудник лаборатории клеточных механизмов патологии памяти (e-mail: ; тел.: 8 (925) 927-63-14; ORCID: .
Бобкова Наталья Викторовна – кандидат биологических наук, заведующий лабораторией клеточных механизмов патологии памяти (e-mail: ; тел.: 8 (903) 184-52-77; ORCID: .
является важным звеном в функционировании ре-нин-ангиотензиновой системы (РАС), которой принадлежит центральная роль в поддержании гомеостаза в организме путем регуляции взаимодействия сердечно-сосудистой, дыхательной, системы водносолевого и углеводного обменов и регуляции кровяного давления [5]. SARS-CoV-2, взаимодействуя с АСЕ2-рецептором, вносит существенный дисбаланс в функционирование этой жизненно важной системы. При этом необходимо учитывать и тот факт, что вирус, проникая в клетки, не только начинает активно размножаться, но и влияет на ответную реакцию клетки на свое вторжение. К настоящему времени уже опубликовано достаточно много обзоров в России и за рубежом, освещающих эти две стороны действия вируса на организм хозяина, однако практически отсутствует анализ тесной взаимосвязи этих двух систем. Поэтому целью данного обзора явился анализ последствий нарушений РАС, вызванных SARS-CoV-2, на состояние элементов врожденного и адаптивного иммунитета, а также оценка возможности прогноза течения заболевания с учетом их изменений.
Физиология РАС и ее связь с иммунной системой организма. В норме РАС обеспечивает поддержание гомеостаза путем регуляции взаимодействия сердечно-сосудистой, дыхательной, системы водно-солевого и углеводного обменов и регуляции кровяного давления [5].
Классическая РАС состоит из двух ветвей, первая из которых включает ангиотензин / ренин / ангиотензин I / ангиотензин-конвертирующий энзим (АСЕ) / ангиотензин II (ANG II) и его рецепторы AT1R и AT2R. Взаимодействие ANG II с AT1R сопровождается повышением кровяного давления, констрикцией сосудов, повышением активности ADAM17 [6], что приводит к появлению циркулирующей формы TNF- α с последующей индукцией провоспалительных цитокинов, усилению пролиферации, инфильтрации и апоптозу [5, 7]. В настоящее время уже установлено, что риском тяжелого течения COVID-19 является не столько сам возраст пациента, сколько так называемые возрастные заболевания, в развитии которых прямо или опосредованно задействована активация 1-й ветви и высокий уровень ANG II [8].
Вторая ветвь РАС открыта относительно недавно и включает ACE2/ANG 1–7/рецептор Mas (Mas R) [9]. Ее функция направлена на подавление гиперактивации 1-й ветви. ANG- (1–7) через взаимодействие с Mas-рецептором вызывает торможение NF-κB-сигнального пути и, как следствие, оказывает противовоспалительное и антиапоптозное действие [10], а также активирует врожденный иммунитет. АСЕ2 является связующим элементом этих двух ветвей РАС и является ключевым ферментом, превращающим ANG II (1-8) – лиганд AT1R в ANG (1–7) с последующей активацией MasR [11]. По-видимому, вирус, вызывая снижение плотности
ACE2-рецепторов, приводит к дисбалансу активности двух ветвей РАС со снижением содержания ANG 1–7 и повышением активности ANG II со всеми вытекающими негативными последствиями, что и лежит в основе более тяжелого течения болезни у людей пожилого возраста с сопутствующими патологиями, для которых характерен исходно сниженный уровень экспрессии рецептора АСЕ2 [12]. Закономерно, что повышение соотношения уровней ACE/ACE2 является предиктором развития острого респираторного дистресс-синдрома, который можно предотвратить применением ANG 1–7 [13]. Однако широкое внедрение ANG 1–7 в клиническую практику ограничено его быстрым разрушением в организме и, возможно, сложностью его доставки в ткань легких и мозга при внутривенном введении. Недавно появились данные, что MasR может активироваться не только ANG 1–7, но и нейропептидом FF, аламан-дином, ангиотензинами III и IV, а также ангиопротек-тином и другими агонистами MasR, разработка которых представляет перспективное направление терапии COVID-19. В настоящее время на разных стадиях клинических испытаний находится более семи соединений, активирующих или усиливающих экспрессию MasR, а также агонистов этого вида рецепторов [14–19]. Из обзора литературы следует, что для лечения COVID-19 и других вирусных инфекций, возбудители которых используют ACE2, для коррекции нарушений РАС предпочтение следует отдавать стойким аналогам ANG 1–7, активирующим MasR.
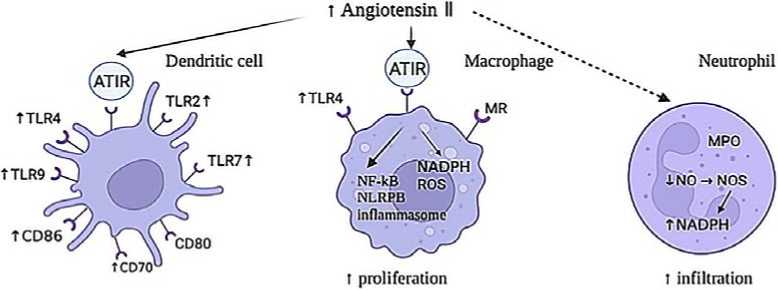
AT1R локализуется на мембранах многих клеток. Не составляют исключение и клетки, входящие в систему врожденного и адаптивного иммунитетов. На рис. 1 и 2 схематически представлены события, разворачивающиеся при COVID-19 на фоне повышенного уровня ангиотензина II.
В системе врожденного иммунитета наблюдается не только активация дендритных клеток, пролиферация макрофагов и инфильтрация нейтрофилов, но и усиление синтеза провоспалительных цитокинов на фоне повышения чувствительности мембранных Toll-like-рецепторов 2, 4, 7-го и 9-го подтипов, ответственных за узнавание микробных и вирусных патогенов. Сходные события происходят и с клетками адаптивной иммунной системы (см. рис. 2). Лимфоциты T4-helpers через выделение многочисленных провоспалительных цитокинов дополнительно активируют элементы этой системы, что происходит на фоне ослабления тормозного влияния со стороны Т-регуляторных клеток и снижения количества выделяемого противовоспалительного цитокина 10.
Установлено, что вирус SARS-CoV-2 может проникать в мозг и взаимодействовать с АСЕ2-рецеп-торами, локализованными на мембранах астроцитов и микроглии [20], где расположены также и многочисленные рецепторы AT1R и TLRs [21]. На рис. 3 схематично представлены последствия взаимодействия вируса с АСЕ2 и TLR на фоне повышенного
Innate immunity

Chemokines MCP- VCCR2 MCP-2/CCL8
Cytokines
Components of the RAS ACE
Renin secretion
TNFa
IL-10, IL-6, IL-12, IL-15, IL-17, IL-22
Рис. 1. Схема событий при COVID-19: избыток ангиотензина II действует на клетки врожденного иммунитета через рецепторы ATIR и TLR; повышается активность дендритных клеток, увеличивается пролиферация макрофагов и выработка АФК и NF-kB; нейтрофилы, хоть и не имеют прямого рецептора для взаимодействия, приобретают способность к инфильтрации и увеличивают производство NADPH
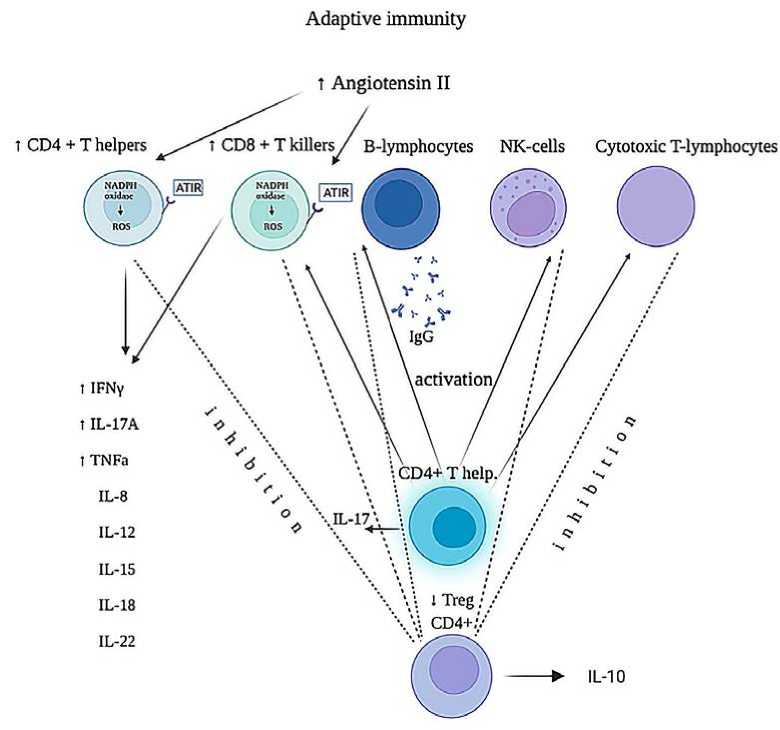
Рис. 2. Схема событий при COVID-19 с клетками адаптивной иммунной системы:
избыток ангиотензина II активирует CD4-лимфоциты, которые запускают дальнейший каскад реакций; при этом снижается количество регуляторных Т-клеток, осуществляющих тормозное влияние, в результате чего все клетки становятся гиперактивными, и запускается реакция цитокинового шторма
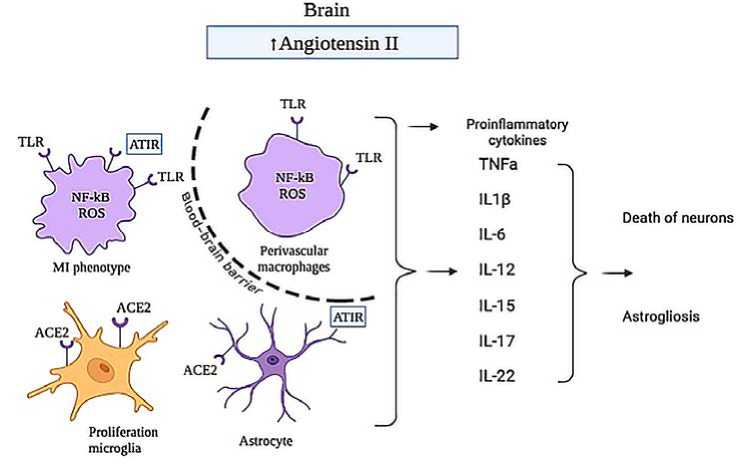
Рис. 3. Схема последствия воздействия вируса COVID-19: накопление ангиотензина II в мозге при блокаде ACE2-рецептора вирусом SARS-CoV-2 действует на рецепторы AT1R и TLR, что приводит к активации провоспалительного пути, выработке активных форм кислорода, синтезу многочисленных провоспалительных цитокинов и гибели нейронов на фоне астроглиоза
уровня ангиотензина II в мозге. Микроглия приобретает провоспалительный фенотип, соответствующий нейровоспалению, увеличивается проницаемость ГЭБ, происходит гибель нейронов и астроглиоз. Макрофаги в сосудистом русле активируются и через выделение активных форм кислорода и провоспалительных цитокинов, что повышает проницаемость ГЭБ и ведет к гибели нейронов, что впоследствии проявляется в виде разнообразных неврологических осложнений после выздоровления.
Важно отметить, что при использовании растворимого внемембранного sACE 2 в качестве лечебного средства для связывания вируса не наблюдалось значительного улучшения состояния у больных COVID-19, что, возможно, объясняется образованием иммунных комплексов «рекомбинантный sACE2+SARS-CoV-2», вызывающих у пациентов аутоиммунный ответ с образованием антител не только против вируса, но и против частей рецепторов ACE и ACE2 с последующим поражением всех органов и тканей, в которых экспрессируются эти рецепторы, с усугублением тяжести заболевания [22].
Механизм нарушения ответной реакции иммунной системы на заражение вирусом SARS-COV-2. На первый взгляд, взаимодействие SARS-CoV-2 мало отличается от такового для других вирусов: вначале связывается c эндосомальными Toll-like-рецепторами 3-го и 7-го типов и цитоплазматическими РНК-рецепторами, затем запускается каскад реакций врожденного иммунитета, происходит активация NF-κB- и IRF-путей, продукция интерферонов, интерлейкина-1 и -6, активируется адаптивный клеточный и, как следствие, гуморальный иммунитет. Однако SARS-CoV-2 запускает воспали- тельный каскад, не давая организму сформировать иммунный ответ, что сопровождается мощным выбросом провоспалительных цитокинов, усугубляет воспалительную реакцию и приводит к массивному повреждению различных тканей иммунными комплексами.
При более детальном анализе этого вопроса можно видеть, что коронавирус проявляет способность к активации синтеза альфа- и гамма-интерфе-ронов в клетке хозяина, а последние могут взаимодействовать с регуляторным сайтом, расположенным в промотере гена Ace2, что приводит к усилению синтеза АСЕ2, тем самым продлевая возможность дальнейшего распространения вируса в зараженном организме [23]. Поэтому перегрузка активированной вирусом интерфероновой системы стимуляторами иммунитета может привести к обратному эффекту – вызвать «цитокиновый шторм» и необходимость использования супрессоров иммунной системы [24], включая антитела к провоспали-тельным цитокинам или их рецепторам, таким как IL-6 и фактор некроза опухоли альфа (TNF-α) или их рецепторам. Предполагаемый механизм, приводящий к развитию «цитокинового шторма», заключается в поэтапном вовлечении ряда внутриклеточных сигнальных путей хозяина. Вошедшая в клетку вирусная РНК узнается эндосомальными РНК-рецепторами хозяина, TLR3 и TLR7, а также цитозольным сенсором РНК, RIG-I/MDA5, что вызывает активацию сигнального каскада NF-κB и IRF3 с транслокацией этих транскрипционных факторов в ядро и стимуляцией экспрессии интерферонов 1-го типа (альфа- и гамма-интерферонов) с последующим их выделением во внеклеточную среду. Интерфероны взаимодействуют с мембранными рецепторами IFNAR и активируют JAK-STAT-систему. Далее происходит фосфорилирование белков STAT1 и STAT2, которые благодаря комплексообразованию с IRF9 проникают в ядро, где стимулируют ряд генов (ISGs), на промоторе которых расположен элемент ISRE, регулирующий силу ответной реакции. Таким образом, коронавирус грубо вмешивается в формирование защитной реакции на этапе синтеза интерферонов и на этапе фосфорилирования СТАТ1. Первоначально задержанная стимуляция ISGs затем реализуется в гиперактивации экспрессии провоспа-лительных цитокинов [24]. Учитывая выраженную гиперреакцию иммунной системы пациентов, зараженных новой инфекцией COVID-19, можно полагать, что особую роль в определении раннего прогноза тяжести течения заболевания играет состояние иммунного статуса пациента.
Осложнения и предикторы тяжелого течения СOVID-19. Клиническая картина у больных новой коронавирусной инфекцией COVID-19 варьируется от легкой до тяжелой, при этом доля последней наряду с числом летальных случаев неуклонно растет по всему миру. В связи с этим возникает острая необходимость в надежных прогностических признаках тяжести течения данного заболевания [25]. На основании анализа обзоров по прогностическим факторам можно сделать вывод о наличии как минимум 49 переменных, представляющих ценную прогностическую информацию о смертности или тяжелом течении заболевания у пациентов с COVID-19. Выявленные переменные включают социально-демографические признаки, анамнестические данные о сопутствующих заболеваниях, результаты физикального осмотра, лабораторные и рентгенологические данные. Выбор наиболее информативных факторов уже на раннем этапе необходим для определения эффективной тактики лечения [26].
Наиболее ранними предикторами ухудшения состояния больных при COVID-19 являются повышенные значения IL-6, IL-10 и С-реактивного белка (CRP), а также снижение количества лимфоцитов [27]. Так, установлено, что при двусторонней пневмонии у 3–4 % пациентов отмечается развитие острого респираторного дистресс-синдрома (ОРДС), который у 3/4 таких больных сопровождается тромботической коагулопатией, в терминальных стадиях приводящей к тромбозам и «цитокиновому шторму», вызываемому системным выделением провоспалительных цитокинов: интерлейкинов IL-2, IL-6, IL-7, гранулоцит колоние-стимулирующего фактора, C-X-C motif хемокина 10 (CXCL10), хе-мокина (C-C motif) лиганда 2 (CCL2) и фактора некроза опухолей альфа (TNF- α ), при этом отмечается лейкопения, свидетельствующая о сниженном клеточном иммунитете [28].
В настоящее время уже не вызывает сомнения существование неразрывной внутренней связи между иммунитетом и секрецией цитокинов, высокие уровни которых на фоне низкого количества субпопуляций лимфоцитов были связаны с повышенным риском смерти от COVID-19. Была создана модель прогнозирования на основе IL-8 и количества CD4+ T-клеток и NK-клеток, показавшая хорошие результаты в прогнозировании смерти пациентов с COVID-19. При использовании порога 0,075 чувствительность и специфичность модели прогнозирования составляли 90,20 и 90,26 % соответственно. Среди всех переменных нейтрофилы, IL-6, CD3, -CD56, CD16-клетки и лейкоциты были четырьмя наиболее влиятельными факторами в тяжелых случаях, тогда как в легких случаях первыми пятью переменными были CD, CD56, CD16+ клетки, PD-1+ NK-клетки, NK-клетки, CD4+/CD8+и перфорин. Вместе с тем нейтрофилы внесли наибольший вклад в эту модель, что согласуется с более сильным воспалительным ответом у тяжелых пациентов с COVID-19. Кроме того, для определения хода развития болезни была продемонстрирована полезность измерения подмножеств NK-клеток на ранней стадии госпитализации [29]. Динамический мониторинг цитокинов и субпопуляций лимфоцитов дает потенциальную ценность для управления процессом болезни. Крупные метаанализы выявили отрицательную корреляцию между падением клеточного иммунитета и увеличением уровня провоспалительных цитокинов для прогнозирования перехода от легкой степени течения заболевания к тяжелой [28], при этом в периферической крови происходит значительное уменьшение лимфоцитов, моноцитов, CD4+T-клеток, CD8+ T-клеток, CD3-клеток, клеток CD19 и естественных киллеров (NK), а также увеличение интерлейкина-2 (IL-2), IL-2R, IL-4, IL-6, IL-8, IL-10, TNF-α и интер-ферона-гамма (INF-γ) [30]. Увеличение концентрации в крови плазмина и плазминогена также является биомаркером повышенной восприимчивости к SARS-CoV-2, поскольку протеаза плазмин может разрезать соответствующий сайт S-белка SARS-CoV-2, что повышает его вирулентность [31]. Мощным прогностическим фактором развития тяжелой формы COVID-19 является рост отношения нейтрофилов к лимфоцитам (NLR) и нейтрофилов к CD8 + Т-клеткам (N8R) [32].
Как уже указывалось, одним из ключевых признаков тяжелого течения заболевания при COVID-19 является патологическая гиперактивация иммунитета, где центральная роль отведена активации нейтрофилов. Протеомное профилирование плазмы поперечных и продольных когорт госпитализированных пациентов с COVID-19 выявило характерные признаки активации нейтрофилов, включая резистин, липокалин-2, фактор роста гепатоцитов, интерлейкин-8 и фактор, стимулирующий колонии гранулоцитов, которые были самыми сильными предикторами критического течения заболевания. Важным открытием стал факт, что сигнатура активации нейтрофилов была повышена уже в первый день госпитализации у тех пациентов, у которых впоследствии состояние ухудшилось до критического и требовало перевода в отделение интенсивной терапии. Исследователями было выдвинуто предположение, что высокие уровни G-CSF стимулируют экстренный гранулопоэз для увеличения продукции нейтрофилов, а IL-8 (CXCL8) управляет миграцией нейтрофилов в легкие и, возможно, другие ткани. Там нейтрофилы активируются и высвобождают RETN, LCN2, HGF, MMP8 и другие белки с антимикробными и другими воспалительными функциями, которые также вызывают значительные побочные повреждения легких, сосудистой сети и других органов [33]. Известно, что NK-клетки и Т-клетки играют жизненно важную роль в противовирусном иммунитете. Исследования больных с COVID-19 показали, что количество и частота CD4+Т-клеток, CD8+Т-клеток и NK T-клеток в тяжелых случаях были значительно ниже, чем в легких случаях. Значительно повышенные уровни экспрессии PD-1 и CD244 на CD8+Т-клетках указывают на истощение Т-клеток у пациентов с COVID-19 и на снижение экспрессии CD27 на CD8+Т-лимфоцитах в тяжелых случаях по сравнению с легким течением заболевания. Поэтому в качестве предиктора риска для выявления «тяжелых» пациентов эффективно использовать характеристики иммунных клеток и цитокинов.
Прогнозирование риска развития тяжелого состояния – чрезвычайно важная задача, поскольку может помочь в принятии решений об объеме необходимой медицинской помощи и стратегиях последующего лечения. Текущие исследования в этом направлении сосредоточены на ряде предикторов среди клинических и лабораторных данных (модели 4C Deterioration и 4C Mortality Score). Однако важно отметить, что ковариация между прогнозами 4C Deterioration и 4C Mortality не различалась по полу или этнической принадлежности, но ослаблялась у молодых возрастных групп [34]. Коллектив зарубежных ученых из Университета штата Аризона, Гарвардского университета и Национального центра биотехнологической информации (США) разработали математическую модель, позволяющую оценивать вероятность развития цитокинового шторма при COVID-19 в зависимости от интенсивности стимуляции выработки цитокинов иммунными клетками с использованием многочисленных параметров. К сожалению, о возможности развития острого респираторного дистресс-синдрома в ряде мест судят по более простым параметрам, таким как появление высокой температуры, уровню С-белка, снижению числа лимфоцитов, прогрессированию поражения легких, снижению сатурации. Данные исследований показывают, что в процессе оценки тяжести состояния и прогнозирования летального исхода должно учитываться влияние иммуногенетики пациента, а именно гендерных иммуногенетических различий. Так, в настоящее время уже доказано участие локуса AB0, генов HLA, регулирующих экспрессию последова- тельностей ДНК, кодирующих цитокины и хемокины [35]. Также было установлено, что пожилые люди мужского пола являются группой повышенного риска тяжелого течения заболевания, развития пневмонии с респираторным дистресс-синдромом и смерти. Возраст является ключевым фактором заболеваемости и смертности от COVID-19, поэтому понимание связанных с возрастом иммунных характеристик пациентов и состояния обеих ветвей РАС с анализом соотношения АСЕ/АСЕ2 важно для определения профилактических и терапевтических стратегий. Так, на основании исследования был выявлен ведущий характерный возрастной иммунный признак, связанный с тяжестью заболевания, а именно определены циркулирующие факторы – CXCL8, IL-10, IL-15, IL-27 и TNF-α – положительно коррелирующие с пожилым возрастом, более длительной госпитализацией и более тяжелой формой заболевания [36].
Выводы. Анализ многочисленных публикаций, посвященных различным нарушениям в функционировании РАС и иммунной системы при COVID-19, позволил прийти к заключению о существовании тесной взаимосвязи между этими системами. Связующим элементом является рецептор АСЕ2, играющий основную роль в интернализации вируса в клетку. Повышение уровня ангиотензина II в результате блокады АСЕ2-рецептора и взаимодействие с АТ1R-рецепторами, локализованными на ряде клеточных элементов врожденного и приобретенного иммунитетов, приводит к гиперактивации последних, что сопровождается синтезом и мощным выбросом во внеклеточное пространство большого количества разнообразных провоспали-тельных хемо- и цитокинов, что представляет угрозу развития цитокинового шторма. По-видимому, особенностью SARS-CoV-2 является его способность запускать воспалительный каскад до формирования защитного иммунного ответа из-за задержки синтеза интерферонов. Анализ литературы по предикторам тяжелого течения болезни позволил прийти к однозначному выводу, что величина соотношения уровней АСЕ/АСЕ2 и иммунный статус больного даже на начальных стадиях заболевания позволяют оценить риск тяжелого течения. Самое пристальное внимание следует уделять изменению состояния нейтрофилов. Таким образом, анализ представленных в обзоре материалов имеет значение не только для фундаментальной медицины, но и содержит данные для практической оценки прогноза течения заболевания и выбора оптимальной тактики лечения.
Финансирование. Работа выполнена при поддержке гранта РНФ (Проект № 18-15-00392).
Список литературы Иммунный статус и спектр цитокинов как прогностические признаки риска тяжелого течения заболевания и эффективности интенсивной терапии пациентов с коронавирусной инфекцией COVID-19
- The interacting physiology of COVID-19 and the renin-angiotensin-aldosterone system: Key agents for treatment / E.R. Lumbers, R. Head, G.R. Smith, S.J. Delforce, B. Jarrott, J.H. Martin, K.G. Pringle // Pharmacol. Res. Perspect. - 2022. -Vol. 10, № 1. - P. e00917. DOI: 10.1002/prp2.917
- Роль ренин-ангиотензин-альдостероновой системы во взаимодействии с коронавирусом SARS-CoV-2 и в развитии стратегий профилактики и лечения новой коронавирусной инфекции (COVID-19) / А.Я. Фисун, Д.В. Чер-кашин, В.В. Тыренко, К.В. Жданов, К.В. Козлов // Артериальная гипертензия. - 2020. - Т. 26, № 3. - С. 248-262. DOI: 10.18705/1607-419X-2020-26-3-248-262
- Qiu J. Covert coronavirus infections could be seeding new outbreaks // Nature. - 2020. DOI: 10.1038/D41586-020-00822-X
- A pneumonia outbreak associated with a new coronavirus of probable bat origin / P. Zhou, X.-L. Yang, X.-G. Wang, B. Hu, L. Zhang, W. Zhang, H.-R. Si, Y. Zhu [et al.] // Nature. - 2020. - Vol. 579, № 7798. - P. 270-273. DOI: 10.1038/S41586-020-2012-7
- Angiotensin-Converting Enzyme 2: SARS-CoV-2 Receptor and Regulator of the Renin-Angiotensin System: Celebrating the 20th Anniversary of the Discovery of ACE2 / M. Gheblawi, K. Wang, A. Viveiros, Q. Nguyen, J.-C. Zhong, A.J. Turner, M.K. Raizada, M.B. Grant, G.Y. Oudit // Circ. Res. - 2020. - Vol. 126, № 10. - P. 1456-1474. DOI: 10.1161/CIRCRESAHA.120.317015
- Reactive oxygen species and p38 mitogen-activated protein kinase mediate tumor necrosis factor a-converting enzyme (TACE/ADAM-17) activation in primary human monocytes / A.J. Scott, K.P. O'Dea, D. O'Callaghan, L. Williams, J.O. Dokpesi, L. Tatton, J.M. Handy, P.J. Hogg, M. Takata // J. Biol. Chem. - 2011. - Vol. 286, № 41. - P. 35466-35476. DOI: 10.1074/JBC.M111.277434
- Chappell M.C. Biochemical evaluation of the renin-angiotensin system: the good, bad, and absolute? // Am. J. Physiol. Heart Circ. Physiol. - 2016. - Vol. 310, № 2. - P. H137-H152. DOI: 10.1152/AJPHEART.00618.2015
- WHO Director-General's remarks at the media briefing on 2019-nCoV on 11 February 2020 [Электронный ресурс] // World Health Organization. - 2022. - URL: https: //www.who.int/director-general/speeches/detail/who-director-general-s-remarks-at-the-media-briefing-on-2019-ncov-on-11-february-2020 (дата обращения: 01.05.2022).
- Angiotensin-(1-7) is an endogenous ligand for the G protein-coupled receptor Mas / R.A.S. Santos, A.C. Simoes e Silva, C. Maric, D.M.R. Silva, R.P. Machado, I. de Buhr, S. Heringer-Walther, S.V.B. Pinheiro [et al.] // Proc. Natl Acad. Sci. USA. - 2003. - Vol. 100, № 14. - P. 8258-8263. DOI: 10.1073/PNAS.1432869100
- Suppressing inflammation by inhibiting the NF-kB pathway contributes to the neuroprotective effect of angiotensin- (1-7) in rats with permanent cerebral ischaemia / T. Jiang, L. Gao, J. Guo, J. Lu, Y. Wang, Y. Zhang // Br. J. Pharmacol. - 2012. - Vol. 167, № 7. - P. 1520-1532. DOI: 10.1111/J.1476-5381.2012.02105.X
- Santos R.A.S., Ferreira A.J., Simöes e Silva A.C. Recent advances in the angiotensin-converting enzyme 2-angiotensin( 1 -7)-Mas axis // Experimental Physiology. - 2008. - Vol. 93, № 5. - P. 519-527. DOI: 10.1113/expphysiol.2008.042002
- The pivotal link between ACE2 deficiency and SARS-CoV-2 infection / P. Verdecchia, C. Cavallini, A. Spanevello, F. Angeli // Eur. J. Intern. Med. - 2020. - Vol. 76. - P. 14-20. DOI: 10.1016/j.ejim.2020.04.037
- Acute respiratory distress syndrome leads to reduced ratio of ACE/ACE2 activities and is prevented by angio-tensin-(1-7) or an angiotensin II receptor antagonist / R.M. Wösten-Van Asperen, R. Lutter, P.A. Specht, G.N. Moll, J.B. van Woensel, C.M. van der Loos, H. van Goor, J. Kamilic [et al.] // J. Pathol. - 2011. - Vol. 225, № 4. - P. 618-627. DOI: 10.1002/path.2987
- Vascular relaxation, antihypertensive effect, and cardioprotection of a novel peptide agonist of the MAS receptor / S.Q. Savergnini, M. Beiman, R.Q. Lautner, V. de Paula-Carvalho, K. Allahdadi, D. Caires Pessoa, F. Pereira Costa-Fraga, R.A. Fraga-Silva [et al.] // Hypertension. - 2010. - Vol. 56, № 1. - P. 112-120. DOI: 10.1161/hypertensionaha.110.152942
- AVE 0991, a nonpeptide mimic of the effects of angiotensin-(1-7) on the endothelium / G. Wiemer, L.W. Do-brucki, F.R. Louka, T. Malinski, H. Heitsch // Hypertension. - 2002. - Vol. 40, № 6. - P. 847-852. DOI: 10.1161/01.HYP.0000037979.53963.8F
- Angiotensin-converting enzyme 2 activator diminazene aceturate prevents lipopolysaccharide-induced inflammation by inhibiting MAPK and NF-kB pathways in human retinal pigment epithelium / L. Tao, Y. Qiu, X. Fu, R. Lin, C. Lei, J. Wang, B. Lei // Journal of Neuroinflammation. - 2016. - Vol. 13, № 1. - P. 35. DOI: 10.1186/S12974-016-0489-7
- Liraglutide Enhances the Activity of the ACE-2/Ang(1-7)/Mas Receptor Pathway in Lungs of Male Pups from Food-Restricted Mothers and Prevents the Reduction of SP-A / J. Fandiño, A.A. Vaz, L. Toba, M. Romaní-Pérez, L. González-Matías, F. Mallo, Y. Diz-Chaves // Int. J. Endocrinol. - 2018. - Vol. 2018. - P. 6920620. DOI: 10.1155/2018/6920620
- A Novel Angiotensin-(1-7) Glycosylated Mas Receptor Agonist for Treating Vascular Cognitive Impairment and Inflammation-Related Memory Dysfunction / M. Hay, R. Polt, M.L. Heien, T.W. Vanderah, T.M. Largent-Milnes, K. Rodgers, T. Falk, M.J. Bartlett [et al.] // J. Pharmacol. Exp. Ther. - 2019. - Vol. 369, № 1. - P. 9-25. DOI: 10.1124/JPET.118.254854
- Within the Brain: The Renin Angiotensin System / L. Jackson, W. Eldahshan, S.C. Fagan, A. Ergul // Int. J. Mol. Sci. -2018. - Vol. 19, № 3. - P. 876. DOI: 10.3390/IJMS19030876
- COVID-19 - A Theory of Autoimmunity Against ACE-2 Explained / P. McMillan, T. Dexhiemer, R.R. Neubig, B.D. Uhal // Front. Immunol. - 2021. - Vol. 12. - P. 582166. DOI: 10.3389/fimmu.2021.582166
- The SARS-CoV-2 spike protein alters barrier function in 2D static and 3D microfluidic in vitro models of the human blood-brain barrier / T.P. Buzhdygan, B.J. DeOre, A. Baldwin-Leclair, H. McGary, R. Razmpour, P.A. Galie, R. Potula, A.M. Andrews, S.H. Ramirez // bioRxiv: The Preprint Server for Biology. - 2020. DOI: 10.1101/2020.06.15.150912
- TLR4 and AT1R mediate blood-brain barrier disruption, neuroinflammation, and autonomic dysfunction in spontaneously hypertensive rats / F.E. Mowry, S.C. Peaden, J.E. Stern, V.C. Biancardi // Pharmacol. Res. - 2021. - Vol. 74. -P. 105877. DOI: 10.1016/j.phrs.2021.105877
- Translating IL-6 biology into effective treatments / E.H. Choy, F. De Benedetti, T. Takeuchi, M. Hashizume, M.R. John, T. Kishimoto // Nature Reviews. Rheumatology. - 2020. - Vol. 16, № 6. - P. 335-345. DOI: 10.1038/S41584-020-0419-Z
- Evaluation of angiotensin-converting enzyme (ACE), its homologue ACE2 and neprilysin in angiotensin peptide metabolism / G.I. Rice, D.A. Thomas, P.J. Grant, A.J. Turner, N.M. Hooper // Biochem. J. - 2004. - Vol. 383, pt 1. -P. 45-51. DOI: 10.1042/BJ20040634
- Velavan T.P., Meyer C.G. Mild versus severe COVID-19: Laboratory markers // Int. J. Infect. Dis. - 2020. - Vol. 95. -P. 304-307. DOI: 10.1016/j.ijid.2020.04.061
- Prognostic factors for severity and mortality in patients infected with COVID-19: A systematic review / A. Izcovich, M.A. Ragusa, F. Tortosa, M.A.L. Marzio, C. Agnoletti, A. Bengolea, A. Ceirano, F. Espinosa [et al.] // PLoS One. - 2020. -Vol. 15, № 11. - P. e0241955. DOI: 10.1371/journal.pone.024195526
- Laboratory Biomarkers Predicting COVID-19 Severity in the Emergency Room / R. Assandri, E. Buscarini, C. Canetta, A. Scartabellati, G. Vigano, A. Montanelli // Arch. Med. Res. - 2020. - Vol. 51, № 6. - P. 598-599. DOI: 10.1016/j.arcmed.2020.05.011
- The role of cytokine profile and lymphocyte subsets in the severity of coronavirus disease 2019 (COVID-19): A systematic review and meta-analysis / H. Akbari, R. Tabrizi, K.B. Lankarani, H. Aria, S. Vakili, F. Asadian, S. No-roozi, P. Keshavarz, S. Faramarz // Life Sci. - 2020. - Vol. 258. - P. 118167. DOI: 10.1016/j.lfs.2020.118167
- Elevated Exhaustion Levels of NK and CD8 + T Cells as Indicators for Progression and Prognosis of COVID-19 Disease / M. Li, W. Guo, Y. Dong, X. Wang, D. Dai, X. Liu, Y. Wu, M. Li [et al.] // Front. Immunol. - 2020. - Vol. 11. -P. 580237. DOI: 10.3389/fimmu.2020.580237
- Longitudinal characteristics of lymphocyte responses and cytokine profiles in the peripheral blood of SARS-CoV-2 infected patients / J. Liu, S. Li, J. Liu, B. Liang, X. Wang, H. Wang, W. Li, Q. Tong [et al.] // EBioMedicine. - 2020. -Vol. 55. - P. 102763. DOI: 10.1016/j.ebiom.2020.102763
- Becker R.C. COVID-19 update: Covid-19-associated coagulopathy // J. Thromb. Thrombolysis. - 2020. - Vol. 50, № 1. - P. 54-67. DOI: 10.1007/S11239-020-02134-3
- Characteristics of SARS-CoV-2 and COVID-19 / B. Hu, H. Guo, P. Zhou, Z.-L. Shi // Nat. Rev. Microbiol. - 2021. -Vol. 19, № 3. - P. 141-154. DOI: 10.1038/S41579-020-00459-7
- A neutrophil activation signature predicts critical illness and mortality in COVID-19 / M.L. Meizlish, A.B. Pine, J.D. Bishai, G. Goshua, E.R. Nadelmann, M. Simonov, C.-H. Chang, H. Zhang [et al.] // Blood Adv. - 2021. - Vol. 5, № 5. -P. 1164-1177. DOI: 10.1182/bloodadvances.2020003568
- Risk stratification of patients admitted to hospital with COVID-19 using the ISARIC WHO Clinical Characterisation Protocol: development and validation of the 4C Mortality Score / S.R. Knight, A. Ho, R. Pius, I. Buchan, G. Carson, T.M. Drake, J. Dunning, C.J. Fairfield [et al.] // BMJ. - 2020. - Vol. 370. - P. m3339. DOI: 10.1136/bmj.m333934
- Relationship Between the ABO Blood Group and the Coronavirus Disease 2019 (COVID-19) Susceptibility / J. Zhao, Y. Yang, H. Huang, D. Li, D. Gu, X. Lu, Z. Zhang, L. Liu [et al.] // Clin. Infect. Dis. - 2021. - Vol. 73, № 2. - P. 328-331. DOI: 10.1093/cid/ciaa1150
- Age-severity matched cytokine profiling reveals specific signatures in COVID-19 patients / R. Angioni, R. Sánchez-Rodríguez, F. Munari, N. Bertoldi, D. Arcidiacono, S. Cavinato, D. Marturano, A. Zaramella [et al.] // Cell Death Dis. - 2020. -Vol. 11, № 11. - P. 957. DOI: 10.1038/S41419-020-03151-Z


