Иммунофармакологические аспекты применения хорионического гонадотропина
Автор: Заморина Светлана Анатольевна, Кочурова Софья Вадимовна
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Иммунология
Статья в выпуске: 4, 2019 года.
Бесплатный доступ
Представлены данные о роли хорионического гонадотропина (ХГ) в регуляции иммунной системы. Проанализированы эффекты ХГ в отношении функциональной активности дендритных клеток, основных субпопуляций Т-хелперов (Th1, Th2, Th17, Treg), Т-клеток иммунной памяти, а также В-лимфоцитов. Иммунофармакологический потенциал гормона тесно связан с его способностью модулировать функциональную активность перечисленных субпопуляций клеток иммунной системы. Помимо целевых эффектов ХГ, связанных с его действиями на уровне репродуктивных тканей, в обзоре рассмотрены перспективы в терапии аутоиммунных заболеваний и пострансплантационных осложнений. Эффекты ХГ на уровне иммунной системы имеют значение в связи с его применением в курсах подготовки к экстракорпоральному оплодотворению (ЭКО). Таким образом, благодаря плейотропному воздействию ХГ на организм и наличию нецелевых эффектов, спектр его применения имеет потенциал к расширению.
Хорионический гонадотропин (хг), дендритные клетки (dc), индоламин-2, 3-диоксигеназа (ido), т-хелперы (th), т-регуляторные клетки (treg), т- клетки иммунной памяти
Короткий адрес: https://sciup.org/147227114
IDR: 147227114 | УДК: 557.175.6 | DOI: 10.17072/1994-9952-2019-4-471-481
Immunopharmacological aspects of the chorionic gonadotropin application
The review presents data on the role of chorionic gonadotropin (CG) in the regulation of the immune system. The effects of CG on the functional activity of dendritic cells, the main subsets of helper T cells (Th1, Th2, Th17, Treg), memory T cells, as well as B cells were analyzed. The immunopharmacological potential of the hormone is closely related to its ability to modulate the functional activity of the listed immune cell subsets. In addition to the targeted effects of CG at the level of reproductive tissues, the review discusses the prospects for the possible use of the hormone in the treatment of autoimmune diseases and post-transplant complications. The effects of CG at the immune system are important also in connection with its use in preparation for in vitro fertilization (IVF). Thus, due to the pleiotropic effect of CG on the body, and the presence of non-target effects, the spectrum of its application has the potential to expand.
Текст научной статьи Иммунофармакологические аспекты применения хорионического гонадотропина
Хорионический гонадотропин (ХГ) – ключевой белковый гормон беременности, который модулирует процессы стероидогенеза у эмбриона и обладает мощным иммунорегуляторным потенциалом. ХГ небезосновательно считают «гормоном жизни и смерти» [Acevedo, 2002], а также «научным чудом» [Cole, 2012]. Группа молекул ХГ играет критическую роль как в процессах беременности, сопровождая развитие и рождение человека, так и в развитии некоторых видов онкологических заболеваний. В основе столь уникальных качеств гормона лежит, по-видимому, его аномально высокий заряд и длительный период полураспада in vivo (36 ч.) в сравнении с другими регуляторными молекулами [Сole, 2012]. Основным местом синтеза ХГ является синцитиотрофобласт; гормон продуцируется клетками трофобласта, пузырного заноса, де-структирующей хориоаденомы и хориокарциномы [Midgley, Pierce, 1962]. У человека к 9–11 неделе беременности концентрация ХГ достигает макси-
мума, затем она снижается и держится на одном уровне вплоть до родов [Cole, 2012].
ХГ способен секретироваться не только во время беременности, но и во время нормального менструального цикла в период окна имплантации секреторным эндометрием небеременных женщин [Ackermann, Alexander, 2009, 2011]. S. Schug с коллегами изучал возможность использования этого гормона как диагностического критерия для характеристики эндометрия лютеиновой фазы [Schug et al., 2019]. В этом исследовании выяснили, что с прогрессированием секреторной трансформации эндометрия и повышением экспрессии ХГ возрастало количество CD45-позитивных лимфоцитов. Это согласуется с тем, что ХГ действует как хемоаттрактант, например, для регуляторных Т-клеток (Treg) [Schumacher et al., 2009]. Также показана статистически значимая корреляция между экспрессией ХГ эндометрия, CD45-позитивной инфильтрацией лейкоцитов, концентрацией прогестерона в сыворотке и правильной секреторной трансформацией эндометрия, что позволяет предположить, что ХГ является возможным диагностическим критерием для характеристики эндометрия лютеиновой фазы.
Ключевую роль гормона в благоприятном развитии беременности подчеркивает тот факт, что полиморфизмы в структуре генов ( cgb5 и cgb8 ) β– субъединицы ХГ ассоциированы с рекуррентными самопроизвольными абортами [Rull et al., 2008]. Относительно недавно стало известно, что некоторые миссенс-мутации в структуре этих генов приводят к неадекватной сборке субъединиц гормона с последующей потерей его биологической активности, вследствие чего у носительниц таких миссенс-мутаций в анамнезе верифицируются реккурент-ные самопроизвольные аборты [Nagirnaja et al., 2012].
Как известно, вырабатываемый трофобластическими клетками, ХГ стимулирует инвазию цитотрофобластов и поддерживает рост плода и плаценты [Cole, 2010]. Эти данные согласуются с выводами, полученными C. Choux c соавторами в ретроспективном исследовании, включающем 149 одноплодных беременностей после ЭКО [Choux et al., 2019]. Было выяснено, что уровень материнского ХГ коррелирует со степенью инвазии плаценты. Так, недостаточная инвазия плаценты после переноса свежих эмбрионов, которая соотносится с увеличением частоты отслойки плаценты [Healy et al., 2010] и риском возникновения преэклампсии [Imudia et al., 2013], коррелировала с более низкими уровнями ХГ, и напротив, чрезмерная инвазия соответствовала более высоким уровням ХГ. Более ранние данные сообщают, что высокие уровни материнского ХГ соответствуют большему объему плаценты, и соответственно низкие уровни – меньшему объему [Hui et al, 2005].
Таким образом, очевидно, что ХГ имеет огромное значение в процессах репродукции и играет ключевую роль в формировании иммунной толерантности к полуаллогенному эмбриону.
ХГ как фармакологический препарат – целевые эффекты
ХГ как фармакологический препарат применяется при гипофункции половых желез, обусловленных гипоталамо-гипофизарными нарушениями [Клиническая …, 2017]. У женщин показанием к применению ХГ является ановуляторное бесплодие, ановуляторная дисфункция яичников, отсутствие или нарушение менструального цикла, недостаточность желтого тела, позднее половое развитие, привычный и угрожающий выкидыш, дисфункциональные маточные кровотечения. У мужчин это гипогонадотропный гипогонадизм, задержка полового созревания, гипогенитализм, гипоплазия яичек, адипозогенитальный синдром, гипофизарная карликовость с явлениями полового инфантилизма, нарушение сперматогенеза. У детей показанием к применению ХГ является крипторхизм. ХГ стимулирует синтез половых гормонов в яичниках и тестикулах, овуляцию, сперматогенез, обеспечивает функцию жёлтого тела; стимулирует развитие половых органов и вторичных половых признаков [Клиническая ..., 2017].
В настоящее время препараты ХГ получают из мочи беременных и выпускают в лиофилизированном виде в пузырьках по 5.000 или 10.000 МЕ для внутримышечного введения. В 2001 г. был начат выпуск препарата ХГ, полученного с помощью рекомбинантной технологии. Рекомбинантный ХГ (rec-hCG) доступен в шприцах-ручках, содержащих 250 мкг чистого ХГ, что эквивалентно приблизительно 6.750 МЕ ХГ в моче [Leao, Esteves, 2014].
В России на момент 2019 г. продаётся препарат ХГ производства Московского эндокринного завода под непатентованным названием «Хорионический гонадотропин», а также препараты: Прегнил (Pregnyl®) фирмы Organon, Профази (Profasi®) фирмы Industria Farmaceutica Serono, Хорагон (Choragon®) фирмы Ferring, и рекомбинантный препарат Овитрель (Ovitrelle®) фирмы Мерк Се-роно (Merck Serono ®).
Роль ХГ в регуляции основных субпопуляций клеток иммунной системы, формирующих толерантность
ХГ считается одним из основных факторов, формирующих иммунную толерантность во время беременности [Shumacher et al., 2013]. Он участвует в формировании необходимого баланса между субпопуляциями хелперных Т-лимфоцитов Th1/Th2 и Treg/Th17 в период беременности, модулируя также активность B-лимфоцитов, Т-клеток иммунной памяти и клеток моноцитарномакрофагального ряда [цит. по: Заморина, 2017].
Так, известно, что ХГ вовлекает в формирование иммунологической толерантности дендритные клетки [Wan et al., 2008]. В частности, ХГ в сочетании с липополисахаридами (ЛПС) в экспериментах на мышиных дендритных клетках повышал соотношение продукции ИЛ-10/ИЛ-12p70, снижал уровень ФНО-α и угнетал антиген-специфическую пролиферацию Т-лимфоцитов. В то же время, ХГ, в сочетании с ИФН-γ, снижал ИЛ-10 и ФНО-α, а также блокировал экспрессию MHC II. Помимо этого, ХГ повышал уровень мРНК индоламин-2,3-диоксигеназы (IDO) в этих клетках, что в перспективе ведет к угнетению Т-клеточной пролиферации. Известно, что высокий уровень IDO блокирует антифетальные клеточно-опосредованные иммунные реакции матери [Mellor, Munn, 2001]. Таким образом, ХГ формирует толерогенный фенотип дендритных клеток, что чрезвычайно важно в контексте взаимодействия мать-плод.
В условиях in vitro ХГ в высокой концентрации, соответствующей таковой в I триместре беременности, повышал ЛПС-индуцированную активность IDO в моноцитах [Заморина, 2017].
В 2018 г. было исследовано влияние ХГ на количество и фенотип различных подгрупп дендритных клеток человека и их способность индуцировать толерантность к плоду. Несмотря на то, что нативный ХГ в данном исследовании не оказывал значительного влияния на процесс созревания всех подмножеств дендритных клеток периферической крови, он, как и рекомбинантный препарат, снижал их способность секретировать ИЛ-8 и ИЛ-10, а также уменьшал экспрессию МНС II. На основании этого, авторы заключили, что наблюдаемое состояние неполной активации дендритных клеток имеет решающее значение для поддержания толерантности плода [Sauss et al., 2018].
Известно, что в клетках синцитиотрофобласта детектируется постоянный уровень мРНК IDO, который повышается под воздействием ХГ [Lei et al., 2007], при этом изолированные α- и β-субъединицы ХГ не оказывали стимулирующего эффекта. Важно отметить, что под воздействием ХГ повышалась не только экспрессия IDO, но и его ферментативная активность [Lei et al., 2007]. ИФН-γ, являясь индуктором IDO в различных тканях, оказывал синергичный с ХГ эффект на повышение уровня мРНК IDO в клетках синцитиотро-фобласта. Этими же авторами показано, что ХГ регулирует уровень IDO в клетках синцитиотро- фобласта, вовлекая ЛГ/ХГ-рецептор. Блокада синтеза рецептора приводила к отмене эффекта ХГ. Известно, что повышение уровня IDO в фетопла-центарной зоне приводит к отмене активации лимфоцитов. В то же время, неудачные беременности сопровождаются дефективной регуляцией IDO со стороны ХГ [Lei et al., 2007].
В период нормально протекающей беременности в иммунной системе матери цитотоксический ответ в отношении плода предотвращается посредством смещения баланса Th1/Th2 в направлении доминирования Th2-субпопуляции хелперных Т-лимфоцитов и подавления провоспалительных Th1-иммунных механизмов, в соответствии с которыми изменяется и спектр циркулирующих цитокинов [Saito et al. 2010]. Нарушение перестройки цитокинового баланса может быть причиной появления осложнений при беременности. Так, ХГ участвует в формировании необходимого баланса между субпопуляциями Th1/Th2, что было продемонстрировано при помощи оценки уровня ИЛ-4 и ИФН-γ в супернатантах культур клеток [Куклина, Ширшев, 2003]. При помощи серии экспериментов, при которых уровень данных цитокинов оценивался и на внутриклеточном уровне, эти данные получили дополнительное подтверждение [Замо-рина, 2017].
В исследованиях на мышах установлено, что ХГ способствует миграции Treg в фетоплацентар-ную зону, которая сопровождается их одновременной пролиферацией и повышает экспрессию мРНК IDO в клетках плаценты [Norris et al., 2011]. Важно отметить, что эффекты ХГ зависят от типа его молекулы: так, дисрегуляция (преобладание гипергликозилированного ХГ (h-hCG), расщепленного ХГ или свободной β-субъединицы) может приводить к развитию преэклампсии за счет снижения продукции ИЛ-10, уровня IDO, Treg и повышения Th17 [Norris et al., 2011]. У человека ХГ повышает содержание Treg-клеток на периферии и привлекает их непосредственно в зону фетопла-центарного контакта [Schumacher et al., 2009]. U.A. Kayisli с коллегами показали, что ХГ может быть ключевым фактором развития локальной иммунной толерантности, через апоптоз, опосредованный Fas/Fas-лигандом. ХГ повышает экспрессию fasL клетками эндометрия человека, тем самым участвуя в контроле инвазии трофобласта и также индуцируя апоптоз Т-лимфоцитов [Kayisli et al., 2003].
Установлено, что во время беременности происходит увеличение пула Treg периферической крови за счет пролиферации естественных Treg, а также за счет индукции адаптивных Treg [Shumacher, 2009]. Не исключено, что повышение содержания Treg в периферической крови на ранних сроках нормально текущей беременности свя- зано именно с действием данного гормона [Heikkinen et al., 2004]. Подтверждением служит тот факт, что у женщин, проходящих подготовку в цикле ЭКО и принимающих ХГ по определенным схемам, в периферической крови повышается уровень Treg [Koldehoff et al., 2011].
Одним из наиболее значимых механизмов формирования иммунологической толерантности является поддержание баланса между Treg и субпопуляциями Т-хелперов 17го типа (Th17) [Wang et al., 2010]. Treg играют важную роль в супрессии иммунного ответа, в том числе секретируют ИЛ-10 – противовоспалительный цитокин, который подавляет пролиферативный ответ Т-клеток на антигены и митогены, продукцию всех провоспали-тельных цитокинов, а также секрецию активированными моноцитами ИЛ-1β, ФНО-α и ИЛ-6. Так, установлено, что ХГ в концентрациях, соответствующих II-III и I триместру (10 и 100 МЕ/мл, соответственно) увеличивал количество Treg и стимулировал секрецию этими клетками ИЛ-10. В отношении Th17 показано, что ХГ снижал количество этих клеток в культуре СD4+-лимфоцитов, одновременно снижая способность этих клеток секретировать ИЛ-17А [Заморина, Ширшев, 2013]. Помимо этого, гормон достоверно снижает экспрессию хемокинового рецептора CCR6, необходимого для направленной миграции Th17 в очаг воспаления [Maddur et al., 2012].
Довольно интересно, что в исследованиях in vitro ХГ не оказывал влияния на уровень рекомбиназы RAG-1 в регуляторных субпопуляциях Т-хелперных клеток человека (Treg, Th17) [Ширшев и др., 2019]. Из этого следует, что регуляторные эффекты ХГ, по-видимому, не затрагивают процессы ревизии Т-клеточного рецептора Treg и Th17.
Известно, что в материнском кровотоке в период беременности циркулируют отдельные клетки плода, небольшие фрагменты ворсин хориона и микрочастицы синцитиотрофобласта [Germain et al., 2007]. Наличие антигенной стимуляции запускает сложный многоступенчатый процесс дифференцировки клеток адаптивного иммунного ответа, при этом наивные лимфоциты после взаимодействия со специфическим антигеном дифференцируются в эффекторные клетки, и часть из них приобретают свойства клеток памяти [Geginat, Lanzavecchia, Sallusto, 2003].
Однако исследований, посвященных дифференцировке Т-клеток в клетки памяти при беременности, крайне мало. Нашими работами установлена роль ХГ в регуляции активности Т-клеток иммунной памяти, ассоциированная с подавлением экспрессии активационных маркеров CD28 и CD25 на этих клетках. Депрессивные эффекты ХГ реализовались только на уровне CD4+-лимфоцитов, не затрагивая субпопуляцию CD8+ [Раев и др., 2017]. В то же время ХГ не влиял на экспрессию маркера пролиферации CD71 наивными Т-клетками и Т-клетками памяти. Установлено, что ХГ угнетал экспрессию мРНК гена hTERT в наивных Т-клетках (CD45RA+) и Т-клетках иммунной памяти (CD45RO+), что приводит к снижению репликативного потенциала клеток. Так, ХГ снижал число пролиферирующих Т-клеток иммунной памяти, оцениваемых по фенотипическим признакам методом дифференциального гейтирования. Параллельно оценивали экспрессию генов U2af1l4, Gfi1, hnRNPLL, регулирующих альтернативный сплайсинг гена Ptprc, кодирующего CD45, поскольку именно по этому маркеру дифференцируются Т-клетки иммунной памяти. Установлено, что ХГ стимулировал экспрессию генов U2af1l4, hnRNPLL, ответственных за сборку CD45RO в Т-клетках иммунной памяти, но снижал экспрессию Gfi1 в этих клетках. В целом, ХГ способствует дифференцировке Т-клеток иммунной памяти за счет повышения экспрессии CD45RO, но снижает их функциональную активность, связанную с экспрессией CD25 [Zamorina et al., 2018].
В 2016 г. T.E. Keiffer с коллегами показали, что физиологическая беременность не влияет на количество периферических CD8+-лимфоцитов памяти (CD45RO+CD8+), но существенно регулирует функции CD4+-лимфоцитов памяти [Keiffer et al., 2016]. В частности, во время беременности достоверно повышается количество так называемых «эффекторных» Т-клеток памяти (CD45RO+CD4+CCR7-), а спустя 18 месяцев после родов показано повышение количества эффекторных (CD45RO+CD4+CCR7-) и центральных Т-клеток памяти (CD45RO+CD4+CCR7+) [Раев и др., 2017]. Авторы считают, что гипотеза о том, что во время беременности генерируются долгоживущие Т-клетки памяти, специфичные к фетоплацентар-ным антигенам, подтверждается этими исследованиями. Мы предполагаем, что белки и гормоны, ассоциированные с беременностью, являются одними из факторов, не позволяющих сформироваться и реализоваться иммунному ответу на фе-топлацентарные антигены. Особенно это касается ХГ, играющего важную роль в формировании иммунной толерантности в период беременности.
На данный момент мало сведений о роли B-лимфоцитов в формировании иммунной толерантности in vivo . Существует предположение, что В-клетки, продуцирующие ИЛ-10 (Breg), вовлекаются в формирование иммунной толерантности во время беременности у мышей и людей [Fettke et al., 2016]. Используя модельные клеточные системы для человека и мыши, эти же авторы показали, что фетальные трофобласты позитивно регулируют генерацию В-клеток, продуцирующих ИЛ-10.
Важно, что именно ХГ, но не прогестерон, эстроген или их комбинация, способствовал изменениям фенотипа В-клеток и увеличивал продукцию ими ИЛ-10, которая была отменена после блокирования ХГ антителами. Фенотип В-клеток, индуцированный ХГ, не был связан с усиленным галактози-лированием, сиалилированием или фукозилирова-нием подклассов IgG в Fc-регионе. В системе in vitro ХГ индуцировал синтез асимметрически гликозилированных антител в Fab-регионе [Fettke et al., 2016].
Относительно недавно установлено, что уро-
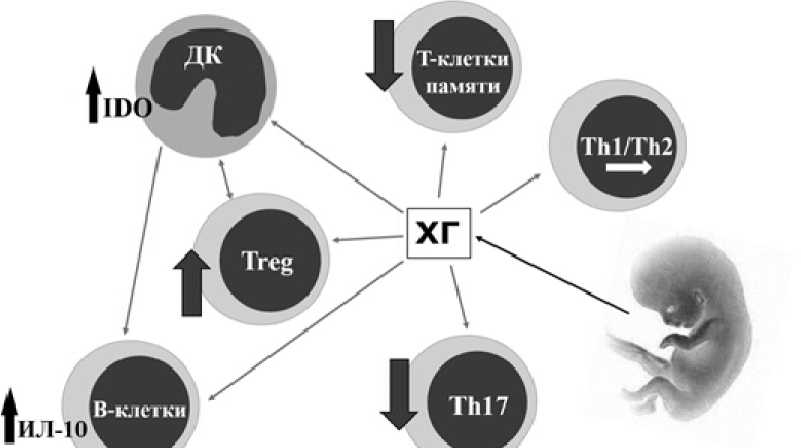
Влияние ХГ на ключевые субпопуляции клеток иммунной системы, ответственных за поддержание иммунной толерантности:
ДК – дендритные клетки, Treg – Т-регуляторные клетки, Th1 – Т-хелперы первого типа, Th2 – Т-хелперы второго типа, Th17 – T-хелперы 17го типа, IDO – индоламин-2,3-диоксигеназа, ИЛ-10 – интерлейкин 10
Иммунофармакологические аспекты применения ХГ – нецелевые эффекты
Благодаря наличию некоторых уникальных качеств, ХГ имеет высокий терапевтический потенциал. Однако, мы рассмотрим только иммунофар-макологические аспекты его действия.
В первую очередь, это связано с его применением в курсах подготовки к экстракорпоральному оплодотворению (ЭКО). Введение ХГ является „золотым‟ стандартом в стимулировании индукции овуляции как замещение лютеинизирующего гормона (ЛГ) в середине цикла [Leao, Esteves, 2014]. Исследования показывают, что клиническая эффективность нативных и рекомбинантных препаратов не различается. Так, в мета-анализе, включающем 11 рандомизированных контролируемых схем ЭКО с 1 187 женщинами M.A. Youssef и соавторы сравнили рекомбинантные препараты вень Breg у пациенток со спонтанным абортом ниже в сравнении со здоровыми беременными женщинами, что подчеркивает важную роль этих клеток в процессе беременности. Более того, ХГ, по-видимому, влияет на генерацию плазматических клеток, а также на их способность продуцировать специфический тип блокирующих (pregnancy-protective) антител [Shumacher, 2017].
В итоге становится очевидно, что ХГ участвует в регуляции основных параметров иммунной толерантности (рисунок) и играет ключевую роль в сохранении беременности.
ХГ с ХГ из мочи в отношении конечного созревания ооцитов. Не было обнаружено существенного различия при сопоставлении основного результата у этих двух препаратов: коэффициент продолжающейся беременности/частота живородящих родов [Youssef et al., 2011].
В настоящее время исследуется влияние препарата ХГ на приживаемость эмбрионов при ЭКО. M. Gao с коллегами в своей работе показали влияние разных концентраций ХГ на приживаемость и благоприятное протекание беременности при переносе эмбрионов [Gao et al., 2019]. Мета-анализ включал в себя 15 рандомизированных клинических испытаний с 2 763 участниками. Было обнаружено, что в группе исследований с применением ХГ в концентрации 500 МЕ, достигались оптимальные результаты беременности, в сравнении с теми работами, когда использовались концентрации 700 и 1000 МЕ. В целом этот мета-анализ показал, что у бесплодных женщин, получавших внутриматочную инъекцию ХГ перед переносом эмбрионов, наблюдались значительно более высокие показатели живорождения, продолжающейся беременности, имплантации, а также более низкая частота выкидышей.
Относительно недавно подтверждено, что ХГ влияет на исход беременности у женщин с рецидивирующей неудачей имплантации через регулирование хомингового предпочтения Treg [Diao et al., 2017]. Похожее исследование на данную тему, проведенное X. Liu с соавторами, также подтвердило данные о действии ХГ. Было выполнено проспективное когортное исследование для оценки влияния внутриматочного введения ХГ на исходы беременности в циклах переноса эмбрионов, с участием 153 человек (152 цикла). Пациенты в группе, получавшей ХГ, имели значительно более высокие показатели клинической беременности, имплантации и числа живорождений, чем в контрольной группе, у них также был значительно более высокий процент периферических Tregs, чем в контроле [Liu et al., 2019]. Важно отметить, что для повышения уровня рецептивности эндометрия в протоколе ЭКО гормон применяется внутрима-точно до пересадки бластоцисты [Makrigiannakis et al., 2017]. Помимо этого, описаны протоколы введения ХГ-обработанных аутологических моно-нуклеарных клеток периферической крови в полость матки перед внесением эмбриона для имму-нодуляции эндометрия, что повышает вероятность имплантации после неудачных попыток ЭКО [Makrigiannakis et al., 2017].
Кроме того, описаны удачные попытки применения ХГ в терапии состояний «трансплантат против хозяина», причем улучшение состояния пациентов сопровождалось повышением экспрессии IDO мононуклеарными клетками [Elmaagacli et al., 2014].
Аутоиммунные заболевания, такие как ревматоидный артрит и синдром Шегрена, имеют менее выраженную клиническую манифестацию во время беременности, за счет особого состояния иммунитета матери. Применение ХГ в моделях на животных имитирует преимущества беременности в контексте аутоиммунных заболеваний [Rao, 2016]. На основе рандомизированных клинических испытаний, сравнивающих применение ХГ с текущей терапией и/или плацебо, применение гормона может быть рекомендовано в терапии ревматоидного артрита, синдрома Шегрена, диабета 1 типа и анкилозирующего спондилоартрита, течение которых также улучшается во время беременности [Rao, 2016].
-
A. De и соавторы выяснили, что при воздействии на клетки адаптивного иммунитета ХГ способен вызывать аутореактивные ответы [De et al., 2018]. Такой эффект гормона был продемонстрирован в опытах с мышами, склонными к систем-
- ной красной волчанке (СКВ). Введение ХГ повышало общую аутореактивность с усиленным образованием аутоантител, также наблюдалось возрастание синтеза цитокинов, ассоциированных с СКВ. По мнению авторов статьи, эти результаты могут дать представление о связи между наличием более высоких уровней ХГ (или введением ХГ) с наличием или появлением гуморального аутоиммунитета.
В 1995 г. было замечено терапевтическое влияние ХГ на саркому Капоши, ассоциированную с ВИЧ первого типа [Борисова и др., 2017], с того же времени идёт обсуждение об анти-ВИЧ активности ХГ, точнее, его свободной β-субъединицы. На данный момент апоптотическое влияние ХГ на клетки саркомы Капоши объясняют его взаимодействием с рецептором TGF-β [Lee-Huang et al., 1999]. Также были выявлены компоненты препарата ХГ, влияющие на ВИЧ in vitro , ими оказались вещества, подобные уринарным формам лизоцима С, РНКазы U и РНКазы А. Эти ферменты обладают сильной противовирусной активностью и способны разрушать структуру ВИЧ [Lee-Huang et al., 1999; Abdallah et al., 2004].
Интересно, что ХГ применяется также в схемах наращивания мышечной массы в бодибилдинге как отдельно, так и совместно с анаболическими стероидами. Также показана полная неэффективность использования данного препарата при употреблении внутрь в составе пищевых добавок. В США с 6 декабря 2011 г. лекарства и пищевые добавки, содержащие человеческий ХГ, находятся под запретом [HCG Diet Products …, 2011].
Итак, благодаря терапевтическим свойствам ХГ и его широкому спектру воздействия на организм, возможно его применение в наиболее разнообразных областях медицины для лечения и профилактики различных патологий. В целом, ХГ является одним из факторов, способствующих поддержанию иммунологической толерантности при беременности и протектирует реакции, направленные на сохранение плода.
Список литературы Иммунофармакологические аспекты применения хорионического гонадотропина
- Борисова М.А., Моисеенко Д.Ю., Смирнова О.В. Хорионический гонадотропин человека: неизвестное об известном // Физиология человека. 2017. Т. 43, № 1. С. 97-110.
- Заморина С.А. Механизмы иммуномодулирующей активности хорионического гонадотропина: монография. Пермь: Стиль МГ, 2017. 168 с.
- Заморина С.А., Ширшев С.В. Хорионический гонадотропин - фактор индукции иммунной толерантности при беременности // Иммунология. 2013. Т. 34, № 2. С. 105-107.
- Клиническая фармакология и фармакотерапия: учебник / под ред. В.Г. Кукеса, А.К. Стародубцева. М.: ГЭОТАР-Медиа, 2017. 1024 с.
- Куклина Е.М., Ширшев С.В. Регуляция окислительной активности нейтрофилов хорионическим гонадотропином. Роль женских половых стероидных гормонов // Известия АН. Сер. биол. 2003. № 4. С. 399-404.
- Раев М.Б. и др. Влияние хорионического гонадотропина на конверсию фенотипа и экспрессию гена hTERT Т-лимфоцитами разной степени дифференцировки // Биомедицинская химия. 2017. Т. 63, № 6. С. 539-545.
- Ширшев С.В. и др. Влияние эстриола, хорионического гонадотропина и онкостатина М на экспрессию рекомбиназы RAG-1 в регуляторных субпопуляциях Т-лимфоцитов // Бюллетень экспериментальной биологии и медицины. 2019. Т. 167, № 1. С. 63-67.
- Abdallah M.A. et al. Human fetal non-gonadal tissues contain human chorionic gonadotropin/luteinizing hormone receptors // Journal of Clinical Endocrinology and Metabolism. 2004. Vol. 89, № 2. P. 952.
- Acevedo H.F. Human chorionic gonadotropin (hCG), the hormone of life and death: a review // Journal of Experimental Therapeutics and Oncology. 2002. Vol. 2, № 3. P. 133-45.
- Choux C. et al. Placental volume and other first-trimester outcomes: are there differences between fresh embryo transfer, frozen-thawed embryo transfer and natural conception? // Reproductive BioMedicine Online. 2019. Vol. 38. Iss. 4. P. 538-548.
- Cole L. A. Biological functions of hCG and hCG-related molecules // Reproductive Biology and Endocrinology. 2010. Vol. 8. № 102.
- Cole L.A. HCG, the wonder of today's science // Reproductive Biology and Endocrinology. 2012. Vol. 10. P. 24.
- De A. et al. Human Chorionic Gonadotropin Influences Systemic Autoimmune Responses // Front Endocrinol (Lausanne). 2018. Vol. 9. P. 742.
- DOI: 10.3389/fendo.2018.00742
- Diao L.H. et al. Human chorionic gonadotropin potentially affects pregnancy outcome in women with recurrent implantation failure by regulating the homing preference of regulatory T cells // American Journal of Reproductive Immunology. 2017. Vol. 77, № 3. P. 1-8.
- Elmaagacli A.H. et al. Human chorionic gonadotropin and indolamine 2,3-dioxygenase in patients with GVHD // Bone Marrow Transplant. 2014. Vol. 49, № 6. Р. 800-805.
- Fettke F. et al. Maternal and Fetal Mechanisms of B Cell Regulation during Pregnancy: Human Chorionic Gonadotropin Stimulates B Cells to Produce IL-10 While Alpha-Fetoprotein Drives Them into Apoptosis // Frontiers of Immunology. 2016. Vol. 7. P. 495.
- Gao M. et al. Intrauterine injection of human chorionic gonadotropin before embryo transfer can improve in vitro fertilization-embryo transfer out-comes: a meta-analysis of randomized controlled trials // Fertility and Sterility. 2019. Vol. 112, № 1.
- Geginat J., Lanzavecchia A., Sallusto F. Proliferation and differentiation potential of human CD8+ memory T-cell subsets in response to antigen or homeostatic cytokines // Blood. 2003. Vol. 101. P. 4260-4266.
- Germain S.J. et al. Systemic inflammatory priming in normal pregnancy and preeclampsia: the role of circulating syncytiotrophoblast microparticles // Journal of Immunology. 2007. Vol. 178. P. 5949-5956.
- HCG Diet Products Are Illegal / U.S. Food and drug. 2011.
- Hui P.W. et al. Maternal serum pregnancy-associated plasma protein-A and free β-human chorionic gonadotrophin in pregnancies conceived with fresh and frozen-thawed embryos from in vitro fertilization and intracytoplasmic sperm injection // Prenatal Diagnosis. 2005. Vol. 25. P. 390-393.
- Imudia A.N. et al. Elective cryopreservation of all embryos with subsequent cryothaw embryo transfer in patients at risk for ovarian hyperstimulation syndrome reduces the risk of adverse obstetric outcomes: a preliminary study // Fertility and Sterility. 2013. Vol. 99. P. 168-173.
- Kayisli U.A. et al. Human chorionic gonadotropin contributes to maternal immunotolerance and endometrial apoptosis by regulating Fas-Fas ligand system // Journal of Immunology. 2003. Vol. 171, № 5. P. 2305-2313.
- Koldehoff M. et al. Modulating impact of human chorionic gonadotropin hormone on the maturation and function of hematopoietic cells // Journal of Leukocyte Biology. Vol. 90(5). 2011. P. 1017-1026.
- Leao R., Esteves S. Gonadotropin therapy in assisted reproduction: an evolutionary perspective from biologics to biotech // Clinics. 2014. Vol. 69(4). P. 279-293.
- Lee-Huang S. et al. Lysozyme and RNAses as anti-HIV components in beta-core preparations of human chorionic gonadotropin // Proceedings of the National Academy of Sciences. 1999. Vol. 96, № 6. P. 2678.
- Lei Z.M. et al. Upregulation of placental indoleamine 2,3-dioxygenase by human chorionic gonadotropin // Biology of Reproduction. 2007. Vol. 76, № 4. P. 639-44.
- Liu X. et al. Intrauterine administration of human chorionic gonadotropin improves the live birth rates of patients with repeated implantation failure in frozen-thawed blastocyst transfer cycles by increasing the percentage of peripheral regulatory T cells // Archives of Gynecology and Obstetrics. 2019. Vol. 299, Iss. 4. P. 1165-1172.
- Мaddur M.S. et al. Th17 Cells: Biology, Pathogenesis of Autoimmune and Inflammatory Diseases, and Therapeutic Strategies // American Journal of Pathology. 2012. Vol. 181. P. 8-18.
- Makrigiannakis A. et al. The Role of HCG in Implantation: A Mini-Review of Molecular and Clinical. // International Journal of Molecular Sciences. 2017. Vol. 18. P. 1305.
- Mellor A.L., Munn D.H. Tryptophan catabolism prevents maternal T-cell from activating lethal antifetal immune responses // Journal of Reproductive Immunology. 2001. Vol. 52. P. 5-13.
- Midley A.R.J., Pierce G.B. Immunohistochemical localization of human chorionic gonadotropin // Journal of Experimental Medicine. 1962. Vol. 115. P. 289-294.
- Nagirnaja L. et al. Structural and functional analysis of rare missense mutations in human chorionic gonadotrophin β-subunit. // Molecular Human Reproduction. 2012. Vol. 18, № 8. P. 379-390.
- Norris W. et al. Review: hCG, preeclampsia and regulatory T cells // Placenta. 2011. Vol. 32, № 2. P. 182-185.
- Rao C.V. Potential Therapy for Rheumatoid Arthritis and Sjögren Syndrome With Human Chorionic Gonadotropin // Reproductive Sciences. 2016. Vol. 23(5). P. 566-571.
- DOI: 10.1177/1933719115597765
- Rull K. et al. Chorionic gonadotropin beta-gene variants are associated with recurrent miscarriage in two European populations. // Journal of Clinical Endocrinology and Metabolism. 2008. Vol. 93, № 12. P. 4697-4706.
- Saito S. et al. Th1/Th2/Th17 and regulatory T-cell paradigm in pregnancy // American Journal of Reproductive Immunology. 2010. Vol. 601, № 63. P. 601-610.
- Sauss K. et al. The pregnancy hormone human chorionic gonadotropin differentially regulates plasmacytoid and myeloid blood dendritic cell subsets // American Journal of Reproductive Immunology. 2018. e12837.
- Schug S. et al. Endometrial human chorionic gonadotropin (hCG) expression is a marker for adequate secretory transformation of the endometrium // Archives of Gynecology and Obstetrics. 2019. Vol. 299, Iss. 6. P. 1727-1736.
- Schumacher A. Human Chorionic Gonadotropin as a Pivotal Endocrine Immune Regulator Initiating and Preserving Fetal Tolerance // International Journal of Molecular Sciences. 2017. Vol. 18(10).
- Schumacher A. et al. Human chorionic gonadotropin attracts regulatory T cells into the fetalmaternal interface during early human pregnancy // Journal of Immunology. 2009. Vol. 9. P. 5488-5497.
- Schumacher A. et al. Human chorionic gonadotropin as a central regulator of pregnancy immune tolerance // Journal of Immunology. 2013. Vol. 190(6). P. 2650-2658.
- Zimmermann G., Ackermann W., Alexander H. Epithelial human chorionic gonadotropin is expressed and produced in human secretory endometrium during the normal menstrual cycle // Biology of Reproduction. 2009. Vol. 80, Iss. 5. P. 1053-1065.
- Zimmermann G., Ackermann W., Alexander H. Expression and production of human chorionic gonadotropin (hCG) in the normal secretory endometrium: evidence of CGB7 and/or CGB6 beta hCG subunit gene expression // Biology of Reproduction. 2011. Vol. 86(3), Iss. 87.
- Wan H. et al. Chorionic gonadotropin induces dendritic cells to express a tolerogenic phenotype // Journal of Leukocyte Biology. 2008. Vol. 83, № 4. P. 894-901.
- Wang W.J. et al. Increased prevalence of T helper 17 (Th17) cells in peripheral blood and decidua in unexplained recurrent spontaneous abortion patients // Journal of Reproductive Immunology. 2010. Vol. 84(2). P. 164-170.
- Youssef M.A. et al. Recombinant versus urinary human chorionic gonadotrophin for final oocyte maturation triggering in IVF and ICSI cycles // Cochrane Database of Systematic Reviews. 2011. Vol. 4. CD003719.
- Zamorina S.A. et al. The role of human chorionic gonadotropin in regulation of naïve and memory T cells activity in vitro // International Immunopharmacology. 2018. Vol. 54. P. 33-38.


