Иммунологические аспекты криотерапевтического воздействия в комплексном лечении врожденной косолапости у детей первого года жизни
Автор: Чугуй Е.В., Мельник Д.Д., Титова Е.Н.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: В помощь практическому врачу
Статья в выпуске: 4-1 т.24, 2009 года.
Бесплатный доступ
Воздействие на кожу сверхнизких температур у взрослых пациентов оказывает мощный иммуномодулирующий эффект. Влияние холода на детский организм недостаточно изучено. В связи с этим мы изучили динамику состояния специфического и неспецифического иммунитета у 60 детей первого года жизни с врожденной косолапостью до и после криотерапии. Выявление возможных нарушений являлось необходимым при применении локального криотерапевтического метода в комплексном лечении данного заболевания.
Криотерапия, врожденная косолапость, дети первого года жизни, иммуномодуляция
Короткий адрес: https://sciup.org/14919152
IDR: 14919152 | УДК: 617.586-007.5-053.1/.2-085.832.97]:612.017
Immunologic aspects of cryotherapeutic influence in complex therapy of congenital clubfoot in children of the first year of life
The influence of cold on childs organism is not studied enough yet. Therefore we studied dynamics of the status of specific and nonspecific immunity in 60 children of the first year of life having congenital clubfoot before and after cryotherapy. These investigations are necessary in using local cryotherapeutic method in complex treatment of the given disease.
Текст научной статьи Иммунологические аспекты криотерапевтического воздействия в комплексном лечении врожденной косолапости у детей первого года жизни
По признанию зарубежных и отечественных специалистов областями применения криотерапии являются воспалительные и дегенеративные заболевания суставов, заболевания позвоночника, колла-генозы, аутоиммунные, аллергические заболевания, депрессивные, гипоиммунные состояния и многие другие [4, 5, 7, 14]. Механизмы криогенного лечения представлены, прежде всего, рефлекторным компонентом, когда в ответ на резкое кратковременное охлаждение сверхнизкими температурами возникает спазм мелких сосудов, гипоксия и, как следствие, активация многих важных процессов: улучшение кровотока, обменных реакций [1, 10, 13]. Повышение местного неспецифического иммунитета является защитной реакцией организма на охлаждение [15, 18]. А обезболивающий эффект холодового воздействия был известен еще со времен Гиппократа. Учитывая описанные выше положительные моменты криохирургического лечения и биомеханические факторы формирования врожденной косолапости, мы сочли целесообразным сочетать криотерапевтический метод с ранней консервативной коррекцией этого заболевания [16].
Любой метод лечения, кроме положительного эффекта, может нести в себе нежелательное побочное действие [19, 20]. В некоторых случаях оно минимально, а иногда имеет значительные последствия. Легкое пощипывание при общем кратковременном охлаждении в криосаунах или дозированных локальных криоаппликациях с появлением местного отека в виде реакции тканей на холодовое воздействие не отражаются на общем состоянии организма у взрослых пациентов [2]. Однако у новорожденных и детей первых месяцев жизни, имеющих небольшую массу тела, могут возникать различные нарушения теплообмена, изменения гомеостаза, иммунитета в ответ на криовоздействие [11].
Воздействие на кожу сверхнизких температур у взрослых пациентов оказывает мощный иммуномодулирующий эффект. Влияние холода на детский организм недостаточно изучено [6, 8, 12, 17]. В связи с этим мы изучили динамику состояния специфического и неспецифического иммунитета у детей с врожденной косолапостью до и после криотерапии. Выявление возможных нарушений являлось необходимым при применении данного метода в комплексном лечении врожденной косолапости у детей первого года жизни.
МАТЕРИАЛ И МЕТОДЫ
Состав периферической крови и показатели неспецифического иммунитета подвержены значительным колебаниям также и в зависимости от климатогеографических условий проживания, возраста ребенка, режима жизни, питания, ухода, состояния здоровья и могут быть предметом контроля при проведении криотерапии у детей первого года жизни. Для объективной оценки данных показателей мы посчитали необходимым изучение аналогичных величин в контрольной группе условно здоровых детей такого же возраста (100 человек), находящихся в относительно одинаковых условиях. Основную группу составили 60 детей первого года жизни с врожденной косолапостью, которым в комплексном лечении патологии применялось локальное криотерапевтическое воздействие на мягкие ткани нижних конечностей сверхнизкими температурами (-196°). Забор крови проводили по обычной методике утром, натощак. Оценка морфологического состава периферической крови проводилась по общепринятым методикам. Полученные нами данные обработаны методом вариационной статистики, и результаты исследований использованы нами как стандарты для оценки результатов проведенной криотерапии у детей первого года жизни. Исследования морфологического состава периферического крови как до проведения криотерапии нашим пациентам, так и после нее на протяжении 2 месяцев не выявили каких-либо отклонений от нормы практически здоровых детей. Разница в показателях этих двух групп детей была статистически не достоверна. Дети, подвергавшиеся криоле-79
чению, были соматически здоровыми, и проводимое им локальное криовоздействие не вызывало каких-либо нарушений в состоянии организма и коррелировало с вышеуказанными показателями периферической крови.
Контроль специфического и неспецифического иммунитета в обеих группах детей проводили, исследуя содержание иммуноглобулинов M, G, A и лизоцима в сыворотке крови, выполняли расчет лейкоцитарного индекса интоксикации.
Иммуноглобулин М является пентамером, состоящим из пяти-, четырехцепочных структур. Из-за высокой молекулярной массы его называют макроглобулином. В онтогенезе он синтезируется раньше других классов и может продуцироваться в организме плода в ответ на внутриутробную инфекцию. Данный класс иммуноглобулинов появляется первым на самых ранних стадиях гуморального иммунного ответа.
Иммуноглобулин G является единственным из иммуноглобулинов, способных преодолевать плацентарный барьер, обеспечивая гуморальный иммунитет у детей первых месяцев жизни. При вторичном ответе иммуноглобулин G составляет основную массу антител, сравнительно легко выходит в межтканевое пространство и накапливается в тканевой жидкости, обеспечивая антибактериальную и антитоксическую защиту.
Иммуноглобулин А циркулирует в сыворотке крови в виде мономеров и димеров, обеспечивая защиту покровных тканей (местный иммунитет) путем предупреждения адгезии и всасывания патологических агентов (в том числе бактерий и вирусов). Другие классы иммуноглобулинов (Е, D) не имеют значения для проводимых нами исследований.
Определение иммуноглобулинов сыворотки крови (М, G, А) проводили по методу Mancini (1965) путем простой радиальной иммунодиффузии. Данный метод позволяет определить 0,003 мг/мл иммуноглобулина (ошибка не более 10%) и выявляет, как правило, высокий индивидуальный разброс интересующих нас компонентов. Поэтому при оценке количества иммуноглобулинов сыворотки крови большое значение имеет как сравнительный анализ рассчитанных показателей условно здоровых детей пер- мые сыворотки наших больных. Диаметры колец преципитации, получаемых в результате исследования, прямо пропорциональны количеству внесенного антигена. Замерив диаметры на калибровочной кривой, определяли содержание иммуноглобулинов в сыворотке крови обследуемых больных.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ
В результате наших исследований выявлено, что в контрольной группе условно здоровых детей (n= 100) в процессе становления иммунитета на первом году жизни ребенка наблюдается очень динамичная картина, представленная в таблице 1.
Динамика изменения количества иммуноглобулинов обусловлена вышеописанными характеристиками последних и их реакцией на смену условий жизни родившегося ребенка. Снижение содержания иммуноглобулинов G в сыворотке крови у детей первого года жизни обусловлено прекращением их поступления через плацентарный барьер. Но во втором полугодии происходит увеличение их количества в результате активации адаптогенных реакций ребенка после рождения.
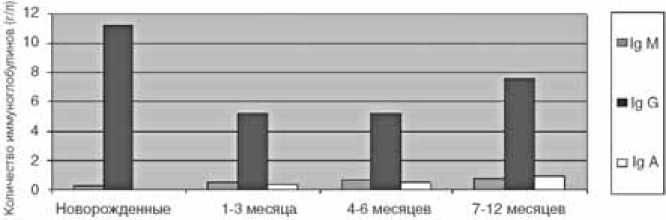
Содержание иммуноглобулинов А и М у условно здоровых детей имеет тенденцию к равномерному их увеличению (гистограмма №1).
Количество иммуноглобулина М в среднем у детей до года (контрольная группа) составило 0,57± 0,115, иммуноглобулина G – 7,35±0,762 и иммуно
Таблица 1
Содержание иммуноглобулинов в сыворотке крови условно здоровых детей первого года жизни (n=100)
вого года жизни и детей, получавших локальное холодовое воздействие на деформированную конечность в этом возрасте, так и динамическая характеристика данных на этапах криолечения. В процессе исследования в среду агар с предварительно внесенной моноспеци-фической сывороткой с антителами против иммуноглобулинов М, G, А вносили антиген – сыворотку с известным содержанием иммуноглобулинов (эталон) и испытывае-
Boipaci (мос)
Гистограмма №1. Динамика показателей иммуноглобулинов сыворотки крови здоровых детей первого года жизни
Наибольшее количество иммуноглобулинов М и G отмечалось к 28-му дню от момента начала лечения, иммуноглобулинов А – к 56-му дню. В то же время отмечено незначительное снижение показателей первых двух групп иммуноглобулинов (М и G) к 56-му дню, что свидетельствует об относительной устойчивости полученных изменений и напоминает модель нормальной иммунной защиты. Во время подсчета данных критериев учитывалась возрастная динамика количества иммуноглобулинов (изменчивость показателей в течение первого года жизни).
Анализ полученных результатов свидетельствует об адекватном реагировании иммунной системы де
Таблица 2
Содержание иммуноглобулинов в сыворотке крови у детей первого года жизни в процессе криолечения врожденной косолапости и после него (n=60)
Иммуноглобулин G составляет более 70% от всех сывороточных иммуноглобулинов и обеспечивает высокую напряженность иммунитета в ответ на любые токсины. Тем не менее в нашем наблюдении повышение данного иммунолобулина через 28 дней после криовоздействия не превышает значения 8,85+0,73=9,58 (г/л), что на 1,468 (г/л) больше, чем максимальное усредненное значение 7,35+0,762= 8,112 (г/л) и имеет тенденцию к снижению через 56 дней после криотерапии. Незначительное повышение количества исследуемых иммуноглобулинов в ответ на местное холодовое воздействие у детей первого года жизни свидетельствует об отсутствии гуморальных иммунных факторов, нарушающих гомеостаз наших пациентов на этапах криолечения врожденной косолапости, что позволяет использовать данный метод лечения более широко и в амбулатор- ных условиях.
Наиболее распространенным методом определения состояния неспецифических факторов защиты является исследование фагоцитарной активности нейтрофилов периферической крови. Локальное хо- лодовое воздействие сверхнизкой температуры на кожу ребенка опосредованно вызывает некоторую активность непатогенной и условно патогенной флоры, тем самым запускает цепочку активации фагоцитоза. Фермент гранул нейтрофилов – лизоцим – является основой бактерицидного действия крови. Количественное увеличение данного показателя всегда сопровождает нормальную защитную реакцию организма при воспалительных процессах. Поэтому в качестве показателя неспецифического иммунитета при криолечении врожденной косолапости у детей первого года жизни мы исследовали лизоцим сыво-
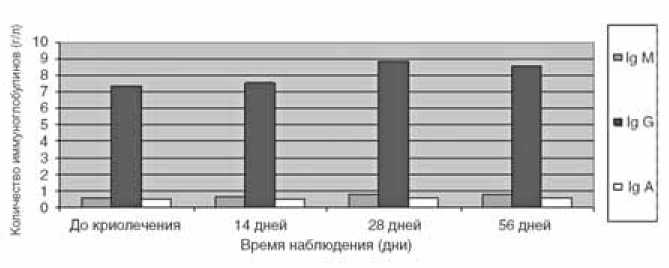
Гистограмма №2. Динамика показателей иммуноглобулинов в сыворотке крови у детей первого года жизни при криолечении врожденной косолапости
ротки крови.
Определение количества лизоцима проводили по методу В.Г. До-рофейчука (1968). В основе исследования лежит высокая чувствительность культуры микрококус лизодейтикус к воздействию лизоцима [9]. В присутствии последнего эталонная культура микрококка быстро растворяется и происходит просветление микробной взвеси. Стандартизацию полученного субстрата проводили на
ФЕКе, используя зеленый фильтр с длиной волны 5,4 мм. Суточная культура тест-микроба смывалась фосфатным буфером (рН 7,2-7,4). Смыв фильтровали через слой ваты, чтобы получить равномерную взвесь без кусочков среды и сгустков микробных тел. Полученную жидкость наливали на кюветы с рабочей длиной волны 3 мм, устанавливали зеленый светофильтр по левому барабану и определяли процент светопроницаемости. Постепенно, разводя взвесь буфером, доводили ее до светопроницаемости – 20%. В пробирку вносили 1,47 мл стандартизированной взвеси микрококка и 0,03 мл исследуемой сыворотки. Перед титрованием сыворотку инактивировали нагреванием в течение 30 минут при температуре 56°С, что способствовало разрушению комплемента, пропердина и других термолабильных начал, способных и в отсутствие лизоцима вызывать лизис микробных тел. После встряхивания пробирки смесь стандартизированного субстрата и сыворотки колориметрировали в тех же кюветах, в которых проводилась стандартизация микробной взвеси.
Пример. После часовой экспозиции в термостате процент светопроницаемости равен 61,8%, а в контроле – 23%. Следовательно, активность лизоцима равна 61,8 – 23 = 38,8%.
Для сравнительной оценки результатов исследования мы провели определение средних показателей активности данного фермента в сыворотке крови у 50 условно здоровых детей контрольной группы. Количество лизоцима в сыворотке крови в среднем составило 40,35±1,55%.
Динамическое исследование лизоцима сыворотки крови (до лечения, через 14 и 28 дней после лечения) было проведено у 30 детей основной группы, получавших криолечение врожденной косолапости (табл. 3). Полученные результаты позволили сделать вывод о том, что повышение активности неспецифического иммунитета является незначительным на протяжении 28 дней криотерапевтического воздействия (до 41,75±1,6%) и не свидетельствует о наличии воспалительных процессов в организме, требующих специального лечения.
При проведении криотерапевтического локального воздействия на мягкие ткани деформирован-
Таблица 3
Динамика активности лизоцима сыворотки крови у детей первого года жизни при проведении криолечения врожденной косолапости (n=30)
Для восстановления эластических свойств кожи в послеоперационном периоде после ахиллопласти-ки мы применили криодеструкцию рубцовой ткани у 15 детей основной группы. Площадь девитализации клеток в поверхостных слоях эпидермиса составляла 1-5 см2. В результате гибели тканей послеоперационного рубца после криовоздействия предполагается, что продукты распада девитализированных тканей (токсины) резорбцируются и становятся причиной интоксикации различной степени выраженности. Для контроля возможного явления у детей первого года жизни после криолечения мы использовали показатели формулы крови, которые позволяли вычислить лейкоцитарный индекс интоксикации (ЛИИ). Формула для определения ЛИИ была предложена Я.Я. Калифом в 1941 году и впервые опубликована в журнале «Врачебное дело» еще до Второй мировой войны. ЛИИ представляет собой эмпирический интегральный показатель, который отражает соотношение положительных и отрицательных факторов. Увеличение данного показателя происходит при интоксикациях, сопровождающих самые разнообразные процессы: инфекционные заболевания, сепсис, радиационные, химические, термические, механические повреждения, шоки и т.п. Расчет ЛИИ используется в практической медицине и при проведении научных исследований уже более 60 лет и производится по следующей формуле:
ЛИИ =
4Ми + 3Ю + 2П + С) х (Пл + 1) (Л + М) х Э + 1
,
где Ми – миелоциты, Ю – юные нейтрофилы, П – палочкоядерные, С – сегментоядерные, Пл – плазматические клетки, Л – лимфоциты, Мо – моноциты, Э – эозинофилы.
Для сравнительной оценки результатов произвели расчет ЛИИ у 50 условно здоровых детей контрольной группы: ЛИИ был равен 0,1-0,8. Исследования ЛИИ у 15 детей основной группы, получавших криолечение послеоперационных рубцов (после ранней ахиллопластики), проводились в течение трех дней после криодеструкции. Динамическое наблюдение выявило небольшое равномерное увеличение ЛИИ у наших пациентов на протяжении первых 36 часов (периода нарастания отека в области девитализированных тканей и предполагаемого всасывания продуктов распада). Через 48–60 часов исследуемый показатель уменьшался и к 72 часам приближался к исходным данным. Во всех наблюдениях при проведении криотерапии рубцовой ткани детям от 6 месяцев до 1 года показатель ЛИИ не превышал верхнюю границу нормы (0,8), определенной в группе
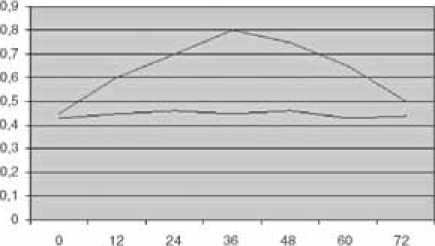
--ЛИИ при крио деструкции рубцов кожи после ранней ахиллотластик!
--ПИИ Пр* локалмюй криоторапни орождпнтюй косолапости
Время наблюдение (час)
График. Динамика показателя ЛИИ при криодеструкции рубцовых тканей у детей первого года жизни после ранней ахиллопластики и при локальной криотерапии тканей деформированной конечности
практически здоровых детей. Полученные результаты свидетельствуют о том, что девитализация патологической ткани послеоперационного рубца площадью 1-5 см2 после криолечения является местным ограниченным процессом, не приводящим к нарушению гомеостаза у наших пациентов, и исключает развитие интоксикации. Одновременно полученные данные о повышении уровня иммуноглобулинов и незначительном повышении активности лизоцима сыворотки крови в процессе криовоздействия свидетельствуют о достаточной напряженности общего и местного иммунитета, обеспечивающего тканевую защиту. Такая дополнительная защита способствует качественному заживлению криогенных ран под тонкой сухой корочкой, образованной девитализированными тканями. Процесс эпитализации под разрушенными участками рубца происходил без на-гноительных процессов. Таким образом, криодеструкция рубцовой ткани сверхнизкими температурами аппликационным способом с помощью пористых инструментов из никелида титана имеет право на существование как метод в амбулаторных условиях и применима даже для детей первого года жизни.
Расчет ЛИИ у детей основной группы, получавших локальное холодовое воздействие на мягкие ткани при коррекции врожденной деформации, мы провели с целью выявить болевую реакцию, ощущаемую при проведении криотерапии, которая могла бы вызвать нарушение гомеостаза в результате шока. Выполненные нами расчеты показали отсутствие какого-либо увеличения исследуемого показателя у данной группы пациентов (график).
Такой факт свидетельствует в пользу того, что криолечение вызывает вполне терпимые ощущения в момент его проведения, это позволяет использовать данный метод широкому кругу пациентов, в том числе и детям первого года жизни при консервативной коррекции врожденной косолапости.
ВЫВОДЫ
На основании полученных данных, указывающих на умеренное повышение функциональной активности иммунной системы у детей первого года жиз- ни в процессе криолечения врожденной косолапости и отсутствие симптомов интоксикации даже после криогенной девитализации клеток эпидермиса рубцово-измененной кожи (после ранней ахиллопластики), локальное воздействие сверхнизких температур на кожу ребенка можно рассматривать как эффективный способ искусственной иммунизации. Полученные данные подтверждают концепцию В.И. Коченова (2000) о том, что иммуностимулирующее действие криотерапевтических процедур несет мощный оздоравливающий эффект.
Список литературы Иммунологические аспекты криотерапевтического воздействия в комплексном лечении врожденной косолапости у детей первого года жизни
- Александров В.Я. Становление и развитие денатурационной теории повреждения и раздражения//Цитология, 1995, том 5, №12. -С. 1101-1121.
- Архаров А.М., Буткевич К.С., Головинцев А.Г. и соавт. Техника низких температур. -Москва, Энергия, 1975. -512 с.
- Билич Г.Л. Стимуляция регенерации и защитных механизмов в детской хирургии -Москва, «Медицина», 1976. -224 с.
- Боженков Ю.Г. Использование локального замораживания в клинической хирургии: обзор литературы//Хирургия, 1988, №4. -С. 145-148.
- Будрик В.В. Физические основы криометодов в медицине. Учебное пособие. -Москва, Издательство МГТУ им. Н.Э. Баумана, 2006. -130 с.
- Григорьева М.П., Говало В.И., Дедова В.Д., Малахов О.А. Иммунологическое исследование детей с заболеваниями опорно-двигательного аппарата//Актуальные вопросы травматологии и ортопедии. Сборник трудов ЦИТО, выпуск 23. -Москва, 1981. -С. 20-24.
- Дорохов С.Д. Регенеративная криотерапия//Медицинская криология. Выпуск 4. -Нижний Новгород, 2003. -С. 73-77.
- Дольницкий О.В. Экспериментальное исследование криохирургического метода и возможности его применения в детской хирургии -Автореферат кан. дис. -Москва, 1975. -32 с.
- Дорофейчук В.Г. Определение активности лизоцима нефелометрическим методом//Лабораторное дело, 1989, №1. -С. 28-30.
- Задорожный Б.А., Чень С.П., Кутасевич Я.Ф. Криогенное воздействие на кожу жидким азотом в эксперименте и клинике//Вестник дерматологии, 1976, №3. -С. 26-31.
- Машков А.В. Особенности иммунитета детского организма -Актовая речь 30 сентября 1965. -Москва, 1965.
- Пачес О.А. Криовоздействия в хирургии детского возраста//Хирургия, 1985, №7. -С. 129-133.
- Сандомирский Б.П., Волкова Н.А., Журавлев А.С. и соавт. Механизмы криостимуляции регенерации поврежденных тканей//Криобиология, 1985, №1. -С. 29-36.
- Чернышев И.С. Современные аспекты криомедицины//Медицинская криология. Выпуск 3. -Нижний Новгород, 2002. -С. 57-69.
- Чирва Г.И. Влияние многократных холодовых воздействий на физиологические показатели терморегуляции человека//Архив клинической и экспериментальной медицины. Том 10, №3, 2001. -С. 277-280.
- Чугуй Е.В., Баиндурашвили А.Г., Мельник Д.Д. Криолечение врожденной косолапости с использованием пористых проницаемых аппликаторов из никелида титана//Материалы с памятью формы и новые технологии в медицине. -Томск, 2007 -С. 105-109.
- Шафранов В.В., Цыганов Д.И., Романов А.В. и соавт. Криотерапия у детей. Некоторые терапевтические и практические аспекты//Детская хирургия, 1999, №3. -С. 35-44.
- Бабийчук В.Г., Козлов А.В., Бабийчук Л.В. Содержание противовоспалительных цитокинов в сыворотке крови людей после ритмических холодовых воздействий//Патология (научно-практический медицинский журнал), 2008, том 5, №3. -С. 42.
- Казмирчук В.Е. Интерпретация лейкограммы и иммунограммы согласно современным позициям//Внутренняя медицина (специализированный научно-практический журнал), 2007, №4. -Донецк. -С. 36-44.
- Черный В.И., Нестеренко А.Н. Нарушения иммунитета при критических состояниях: особенности диагностики//Внутренняя медицина (специализированный научно-практический журнал), 2007, №4. -Донецк. -С. 16-28.


