Иммунологические особенности остеоартроза крупных суставов различной этиологии
Автор: Чепелева Марина Владимировна, Швед Наталья Сергеевна
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 2, 2012 года.
Бесплатный доступ
Представлены данные по анализу особенностей иммунного статуса 159 больных с идиопатическим, гипопластическим, посттравматическим остеоартрозом коленного и тазобедренного суставов, коксартрозом - исходом АНГБ, остеоартрозом крупных суставов, развившимся на фоне ревматоидного артрита.
Иммунная система, остеоартроз
Короткий адрес: https://sciup.org/142121533
IDR: 142121533
Immunological special features of large jont osteoarthrosis of different etiology
The work deals with the data concerning analyzing the special features of immune status in 159 patients with idiopathic, hypoplastic, posttraumatic osteoarthrosis of the knee and the hip, coxarthrosis - the outcome of femoral head aseptic necrosis (FHAN), osteoarthrosis of large joints, developed through rheumatoid arthritis.
Текст научной статьи Иммунологические особенности остеоартроза крупных суставов различной этиологии
Диагностика и лечение тяжелых форм остеоартроза относятся к числу актуальнейших задач современной медицины.
Многие исследователи сходятся во мнении, что факторами, способствующими хронизации патологического процесса при остеоартрозе, являются нарушения в системе иммунитета, но их конкретные механизмы до конца не изучены [4, 5, 7, 8, 9]. Дан- ные об изменениях иммунного статуса при одних и тех же нозологических формах неоднозначны, противоречивы и не позволяют выработать единой концепции для их оценки.
Цель настоящего исследования – изучить влияние этиологического фактора на иммунный статус больных остеоартрозом крупных суставов.
МАТЕРИАЛЫ И МЕТОДЫ
Представленные в работе результаты получены при обследовании 159 пациентов с остеоартрозом II-III стадии в возрасте 29 лет – 72 года, из них 21 – с идиопатическим остеоартрозом тазобедренного сустава, 42 – с идиопатическим остеоартрозом коленного сустава, 12 – с гипопластическим остеоартрозом коленного сустава, 13 – с посттравматическим остеоартрозом тазобедренного сустава, 28 – с посттравматическим остеоартрозом коленного сустава, 32 – с исходом асептического некроза головки бедра (АНГБ) и 11 – с остеоартрозом крупных суставов, развившимся на фоне ревматоидного артрита. Пациенты с патологией тазобедренного и коленного суставов проходили плановое хирургическое лечение в ортопедических отделениях ФГБУ «РНЦ «ВТО» им. академика Г. А. Илизарова за период с 2004 по 2009 год.
Типирование лимфоцитов периферической крови осуществлялось методом лазерной про- точной цитометрии на цитометре «BECKMAN COULTER EPICS XL» (США) [3]. Т-лимфоциты (CD3+CD19-), Т-хелперы (CD3+CD4+), цитотоксические Т-лимфоциты (CD3+CD8+), В-лимфоциты (CD3-CD19+), натуральные киллеры (CD3-CD16+CD56+), натуральные киллеры / Т-лимфоциты (CD3+CD16+CD56+), CD3+HLA-DR, несущие маркеры поздней активации Т-лимфоцитов, идентифицировали с помощью моноклональных антител (МКАТ), меченых фикоэритрином (РЕ) и флуоресцинизотио-цианатом (FITC). Использовался набор МКАТ компании «Immunotech» (Франция). Количественное определение иммуноглобулинов классов А, М, G осуществлялось методом ИФА на иммуноферментном анализаторе BIO-TEK Instruments Inc, ELx808 (CША) с использованием набора реагентов ЗАО «Вектор-Бест» (Новосибирск), цитокинов IL-6, TNFα методом ИФА на иммуноферментном анализаторе BIO-TEK Instruments Inc, ELx808 (CША) с использованием диа- гностических тест-систем фирмы «BioSource Europe» (Бельгия). Определение уровня ЦИК проводилось методом преципитации 3,5 % ПЭГ (ММ 6000).
В качестве контрольных использовались иммунологические показатели 29 добровольцев аналогичного возраста, у которых отсутствовали клинические признаки остеоартроза. В обследуемую выборку не входили носители вирусов гепатитов В и С, лица с отягощенным аллергическим анамнезом. Забор крови осуществлялся из локтевой вены натощак.
Полученные данные были обработаны с помощью методов непараметрической статистики с использованием U-критерия Вилкоксона для не- зависимых выборок (Гельфгат Е. Л. с соавт., 2000; Гланц С., 1998; Гублер Е. В., 1978). Статистические гипотезы считали подтвержденными при уровне значимости pu<0,05. Учитывая применение непараметрических методов статистики, результаты исследования были представлены в виде медиан и интерквартильных размахов. При обработке полученных данных применяли программное обеспечение AtteStat 1.0, разработанное в информационно-вычислительном центре ФГБУ «РНЦ «ВТО» им. акад. Г. А. Илизарова» и выполненное как надстройка к «Microsoft Exсel» программного продукта «Microsoft Office» [1].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Анализ результатов исследования показал следующее: в синовиальной жидкости больных остеоартрозом, независимо от этиологии заболевания, наблюдалось увеличение содержания иммуноглобулинов классов А и G (IgА, IgG) (рис. 1, 2), выявлялся IgM, который, согласно литературным данным, отсутствует в синовиальной среде здорового сустава (рис. 3) [3]. Концентрация цитокинов в синовиальной жидкости больных остеоартрозом различной этиологии была существенно выше, чем в периферической крови (табл. 1, 2). Согласно литературным данным, дисбаланс цитокинов приводит к разрушению структурной и функциональной целостности хрящевого экстрацеллюлярного матрикса. Цитокины, необходимые в небольших количествах для поддержания гомеостаза, начинают в избытке выявляться в синовиальной жидкости, их повышенная продукция способствует прогрессированию патологического процесса, и, как следствие, развитию дегенеративно-дистрофических и воспалительных изменений в суставных тканях [2, 6]. В синовиальной жидкости больных остеоартрозом отмечалось увеличение содержания TNFα, являющегося одним из главных медиаторов костной резорбции и местной воспалительной реакции. Было выявлено повышение концентрации IL-6 – одного из наиболее активных цитокинов, участвующих в реализации иммунного ответа, для которого характерны не только провоспалительные эффекты, но и противовоспалительные свойства, опосредованные с одной стороны ингибицией продукции IL-1 и TNFα, а с другой стороны – активацией синтеза и секреции антагонистов провоспалительных цитокинов IL-1pa и растворимых рецепторов TNFα (табл. 1, 2).
Содержание Т- и B-лимфоцитов в периферической крови во всех группах не выходило за пределы нормативных границ (табл. 3). В то же время у пациентов с посттравматическим коксартрозом и гонартрозом было выявлено статистически значимое, в сравнении с показателями больных остеоартрозом другой этиологии, снижение количества CD3+CD19-, преимущественно за счёт популяции Т-хелперов (CD3+CD4+). Данные изменения мы расценили как пролонгированную иммунологическую реакцию на последствия травматического разрушения тканей сустава.
У пациентов с посттравматическим, гипопластическим, идиопатическим остеоартрозом, коксар-трозом – исходом АНГБ-соотношение CD3+CD4+ к CD3+CD8+ достоверно не отличалось от значений контрольной группы (рис. 4). У больных с остеоартрозом, развившимся на фоне ревматоидного артрита, наблюдалось увеличение данного индекса за счёт более высоких, чем в контроле, значений CD3+CD4+ и более низких значений CD3+CD8+.
В периферической крови больных идиопатическим, посттравматическим остеоартрозом, коксартрозом – исходом АНГБ, ревматоидным артритом отмечалось повышение содержания ЕКТ (CD3+CD56+CD16+) – особой категории лимфоидных клеток, биологическая роль которых реализуется через их цитотоксические эффекты. Увеличение абсолютного и относительного количества ЕКТ у этой категории пациентов может служить косвенным доказательством участия микроорганизмов в развитии патологических изменений в суставных и околосуставных тканях при остеоартрозе.
В периферической крови больных остеоартрозом крупных суставов независимо от этиологии заболевания мы обнаружили более высокие, чем в контрольной группе, значения лимфоцитов, экспрессирующих активационные маркеры (HLA-DR). Учитывая важнейшую роль HLA-DR – молекул в процессах антигенного распознавания и запуска каскада молекулярных процессов формирования специфического иммунного ответа, можно предположить, что увеличение числа Т-лимфоцитов, экспрессирующих эти гликопротеины, является отражением процессов системной активации клеток иммунной системы в ходе распознавания собственных антигенов соединительной ткани, а также микробных пептидов, которые при остеоартрозе могут рассматриваться как антигены эндогенного происхождения. Повышение количества CD3+HLA-DR клеток выявлялось у пациентов независимо от этиологии заболевания, что свидетельствует в пользу его патогенетической значимости, подтверждая участие аутоиммунных процессов в развитии патологических изменений при остеоартрозе.
Значительное повышение концентрации ЦИК, IgM и IgG наблюдалось у пациентов с ревматоидным артритом, что было обусловлено воспалительной реакцией и выраженным аутоиммунным компонентом (рис. 5) (табл. 4). Статистически значимое, в сравнении с показателями контрольной группы, увеличение уровня сывороточных ЦИК было выявлено также у пациентов с идиопатическим, посттравматическим остеоартрозом коленного и тазобедренного суставов, коксартрозом – исходом АНГБ. Однако, несмотря на достоверные отличия, у этой категории больных содержание ЦИК не выходило за пределы границ физиологической нормы.
Наиболее приближенными к значениям контрольной группы были показатели системы иммунитета у больных гипопластическим коксартрозом, так как для данной патологии свойственна, в первую очередь, ана-томо – биомеханическая неполноценность сустава с сохраненным гиалиновым хрящём и менее выраженными дегенеративными и воспалительными изменениями в синовиальной среде, чем при остеоартрозе другой этиологии. Наиболее выраженными были изменения иммунного статуса у пациентов с остеоартрозом, развившимся на фоне ревматоидного артрита, в основе патогенеза которого лежат генетически детерминированные аутоиммунные процессы, обусловленные дефицитом Т-супрессорной функции лимфоцитов.
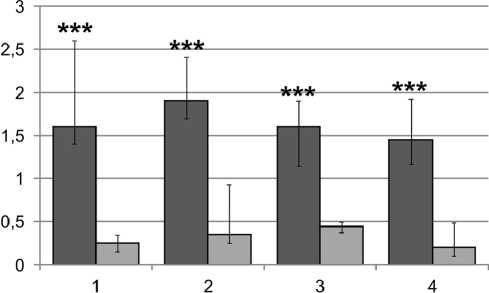
Рис. 1. Концентрация IgA в периферической крови (первый столбец) и синовиальной жидкости (второй столбец): 1 – идиопатический ОА крупных суставов; 2 – посттравматический ОА крупных суставов; 3 – остеоартроз – исход АНГБ; 4 – гипопластический ОА тазобедренного сустава; *** p<0,001 относительно значений синовиальной жидкости
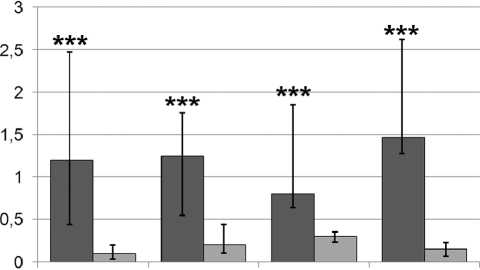
12 3 4
Рис. 2. Концентрация IgG в периферической крови (первый столбец) и синовиальной жидкости (второй столбец): 1 – идиопатический ОА крупных суставов; 2 – посттравматический ОА крупных суставов; 3 – осте-артроз – исход АНГБ; 4 – гипопластический ОА тазобедренного сустава; * - p<0,05, ** - p<0,01, *** - p<0,001 относительно значений синовиальной жидкости
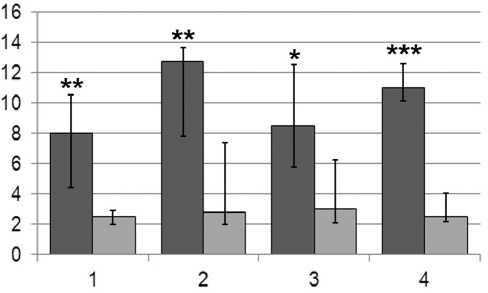
Рис. 3. Концентрация IgМ в периферической крови (первый столбец) и синовиальной жидкости (второй столбец): 1 – идиопатический ОА крупных суставов; 2 – посттравматический ОА крупных суставов; 3 – остеартроз – исход АНГБ; 4 – гипопластический ОА тазобедренного сустава; *** – p<0,001 относительно значений синовиальной жидкости
Уровень цитокинов в синовиальной жидкости у пациентов с ОА коленного и тазобедренного суставов различной этиологии (медианы значений показателей и интерквартильные размахи)
Таблица 1
|
Группы |
Показатели |
|
|
IL-6 (пг/мл) |
TNFα (пг/мл) |
|
|
Идиопатический ОА коленного сустава (n=15) |
128,6 (31,5÷291,0) |
6,04 (4,46÷15,7) |
|
Посттравматический ОА коленного сустава (n=10) |
159,4 (58,5÷315,0) |
8,43 (6,31÷9,84) |
|
ОА тазобедренного сустава - исход АНГБ (n=10) |
165,0 (27,9÷302,5) |
5,08 (2,54÷7,62) |
Примечание: * - p<0,05, **- p<0,01 относительно показателей контрольной группы.
Таблица 2
Уровень сывороточных цитокинов в периферической крови пациентов с ОА коленного и тазобедренного суставов различной этиологии (медианы значений показателей и интерквартильные размахи)
|
Группы |
IL-6 (пг/мл) |
TNFα (пг/мл) |
|
Контрольная группа (n=29) |
0,91 (0÷2,12) |
1,58 (0÷8,74) |
|
Идиопатический ОА тазобедренного сустава (n=21) |
0,1 (0÷0,9) |
1,3 (0÷9,04) |
|
Идиопатический ОА коленного сустава (n=42) |
0,1 (0÷2,3) |
3,3 (1,3÷5,2) |
|
Гипопластический ОА тазобедренного сустава (n=12) |
0 (0÷0,6) |
0 (0÷1,87) |
|
Посттравматический ОА тазобедренного сустава (n=13) |
0,14 (0,07÷0,21) |
2,6 (3,9÷5,2) |
|
Посттравматический ОА коленного сустава (n=28) |
2,25 (0,93÷2,52) |
3,6 (2,6÷6,01) |
|
ОА тазобедренного сустава - исход АНГБ (n=32) |
0,42 (0÷2,3) |
0,65 (0÷2,6) |
Примечание: * - p<0,05, **- p<0,01 относительно показателей контрольной группы.
Таблица 3
Показатели клеточного иммунитета у пациентов с остеоартрозом коленного и тазобедренного суставов различной этиологии
|
Значения |
Показатели |
||||||
|
СD3+CD19- |
СD3-CD19+ |
CD3+CD4+ |
CD3+CD8+ |
CD3-CD16+CD56+ |
CD3+CD16+CD56+ |
СD3-HLA-DR |
|
|
Контрольная группа (n=29) |
|||||||
|
% |
75,6 (71,3÷77,5) |
10,1 (8,0 ÷11,7) |
50,3 (43,4÷52,4) |
22,1 (17,1÷25,9) |
12,3 (11,1÷16,2) |
3,9 (2,7÷4,2) |
2 (1,2÷2,9) |
|
109/л |
1,32 (1,02÷1,41) |
0,14 (0,12÷0,21) |
0,79 (0,67÷0,92) |
0,35 (0,28÷0,52) |
0,24 (0,19÷0,26) |
0,05 (0,04÷0,08) |
0,03 (0,02÷0,04) |
|
Идиопатический ОА тазобедренного сустава (n=21) |
|||||||
|
% |
76,5 (72,8÷78,7) |
9,7 (6,6 ÷10,7) |
45,5 (41,7÷53,5) |
29 (26,6÷33,0) |
10,4 (8,9÷14,1) |
↑6,9** (4,0÷7,5) |
↑4,0** (2,9÷6,3) |
|
109/л |
1,07 (0,95÷1,41) |
0,14 (0,09÷0,18) |
0,71 (0,56÷0,86) |
0,38 (0,34÷0,5) |
0,16 (0,11÷0,28) |
↑0,1** (0,07÷0,15) |
↑0,06* (0,04÷0,1) |
|
Идиопатический ОА коленного сустава (n=42) |
|||||||
|
% |
74,4 (69,1÷76,3) |
9,9 (5,8 ÷13,6) |
44,6 (42,2÷53,5) |
28 (19,6÷32,8) |
12,6 (11,5÷14,9) |
↑6,8** (4,5÷8,4) |
↑5,9** (4,2÷6,7) |
|
1109/л |
1,21 (1,02÷1,47) |
0,19 (0,07÷0,26) |
0,77 (0,56÷0,98) |
0,43 (0,34÷0,49) |
0,19 (0,09÷0,28) |
↑0,09** (0,07÷0,19) |
↑0,09** (0,07÷0,12) |
|
Гипопластический ОА тазобедренного сустава (n=12) |
|||||||
|
% |
71 (67,5÷76,3) |
10,6 (4,9 ÷14,3) |
45,5 (41,9÷48,8) |
25,3 (20,4÷28,3) |
14,6 (8,3÷18,1) |
4,9 (2,4÷6,8) |
↑3,2* (2,1÷4,1) |
|
109/л |
0,9 (0,8÷1,1) |
0,18 (0,06÷0,22) |
0,54 (0,51÷0,8) |
0,27 (0,21÷0,32) |
0,19 (0,13÷0,23) |
0,06 (0,04÷0,09) |
0,04 (0,02÷0,05) |
|
Посттравматический ОА тазобедренного сустава (n=13) |
|||||||
|
% |
↓65,6** (64,6÷68,4) |
9,8 (7,2 ÷10,1) |
↓42,6* (37,4÷44,9) |
23,3 (19,6÷25,4) |
↑21,8** (18,6÷24,5) |
↑5,6* (5,4÷7,5) |
↑4,0* (2,6÷4,5) |
|
109/л |
0,91 (0,77÷1,06) |
0,12 (0,1÷0,14) |
↓0,65* (0,37÷0,69) |
0,26 (0,21÷0,5) |
0,34 (0,19÷0,43) |
↑0,1* (0,09-0,17) |
↑0,04* (0,04÷0,06) |
|
Посттравматический ОА коленного сустава (n=28) |
|||||||
|
% |
↓66,6** (53,9÷70,7) |
9,5 (8,4÷12,1) |
↓41,0** (34,9÷43,2) |
23,1 (19,1÷26,3) |
↑19,8* (15,6÷23,9) |
↑5,2* (4,4÷6,7) |
↑4,0* (3,2÷4,5) |
|
109/л |
1,07 (0,74÷1,23) |
0,16 (0,09÷0,18) |
↓0,62* (0,38÷0,7) |
0,39 (0,29÷0,47) |
0,26 (0,21÷0,29) |
0,08 (0,05÷0,09) |
↑0,06** (0,05÷0,11) |
|
ОА тазобедренного сустава - исход АНГБ (n=32) |
|||||||
|
% |
75,5 (72,1÷78,7) |
9,2 (7,3÷12,0) |
50,5 (42,4÷53,9) |
23,8 (18,5÷29,6) |
12 (6,2÷14,6) |
↑5,6* (4,0÷8,3) |
↑4,0** (3,7÷5,1) |
|
109/л |
1,36 (1,11÷1,46) |
0,18 (0,1÷0,23) |
0,86 (0,75÷0,98) |
0,39 (0,33÷0,49) |
0,19 (0,12÷0,26) |
0,06 (0,03÷0,11) |
↑0,06* (0,04÷0,11) |
|
ОА коленного сустава, развившийся на фоне ревматоидного артрита (n=11) |
|||||||
|
% |
76,1 (70,1÷78,2) |
8,3 (7,0÷11,8) |
55,1 (45,4÷56,8) |
19,2 (16,5÷22,6) |
14,5 (8,5÷16,1) |
↑6,1* (4,0÷8,3) |
↑4,0* (2,7÷5,5) |
|
109/л |
1,3 (1,01÷1,32) |
0,17 (0,1÷0,2) |
0,9 (0,7÷1,01) |
↓0,25* (0,19÷0,3) |
0,19 (0,09÷0,24) |
↑0,09* (0,07÷0,16) |
↑0,05* (0,04÷0,07) |
Примечание: * - p<0,05, **- p<0,01 относительно показателей контрольной группы.
Таблица 4
Уровень сывороточных иммуноглобулинов основных классов у пациентов с ОА коленного и тазобедренного суставов различной этиологии (медианы значений показателей и интерквартильные размахи)
|
Группы |
IgA (мг/мл) |
IgM (мг/мл) |
IgG (мг/мл) |
|
Контрольная группа (n=29) |
2,39 (1,87÷3,26) |
1,46 (0,79÷2,17) |
14,4 (10,9÷18,5) |
|
Идиопатический ОА тазобедренного сустава (n=21) |
2,03 (1,5÷2,99) |
1,5 (0,74÷2,46) |
10,6 (7,3÷12,7) |
|
Идиопатический ОА коленного сустава (n=42) |
1,47 (1,03÷2,07) |
0,85 (0,62÷1,5) |
7,6 (5,9÷13,7) |
|
Гипопластический ОА тазобедренного сустава (n=12) |
1,49 (1,26÷1,98) |
1,45 (1,21÷2,84) |
11,2 (8,9÷12,5) |
|
Посттравматический ОА тазобедренного сустава (n=13) |
1,58 (1,23÷1,86) |
1,58 (1,11÷2,89) |
11,7 (7,9÷17,1) |
|
Посттравматический ОА коленного сустава (n=28) |
2,17 (1,51÷3,96) |
1,03 (0,84÷1,72) |
17,3 (10,6÷24,8) |
|
ОА тазобедренного сустава - исход АНГБ (n=32) |
↓1,55* (1,08÷1,86) |
0,9 (0,7÷1,2) |
↓8,5** (5,6÷10,1) |
|
ОА, развившийся на фоне ревматоидного артрита (n=11) |
2,5 (2,05÷3,3) |
↑2,4* (2,08÷3,04) |
↑22,4* (17,9÷25,5) |
Примечание: * - p<0,05, **- p<0,01 относительно показателей контрольной группы.
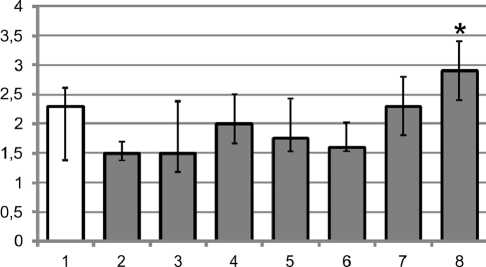
Рис. 4. CD4+/СD8+ у пациентов с ОА крупных суставов различной этиологии (у.е.): 1– контрольная группа, 2 – идиопатический ОА коленного сустава, 3 – идиопатический ОА тазобедренного сустава, 4 – гипопластический ОА тазобедренного сустава, 5 – посттравматический ОА коленного сустава, 6 – посттравматический ОА тазобедренного сустава, 7 – остеоартроз тазобедренного сустава – исход АНГБ; 8 – остеоартроз, развившийся на фоне ревматоидного артрита; * – p<0,05 относительно значений контрольной группы
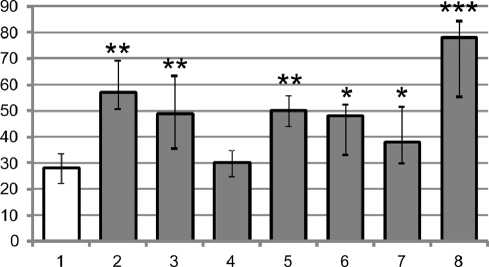
Рис. 5. Уровень ЦИК у пациентов с ОА крупных суставов различной этиологии (у.е.): 1– контрольная группа, 2 – идиопатический ОА коленного сустава, 3 – идиопатический ОА тазобедренного сустава, 4 – гипопластический ОА тазобедренного сустава, 5 – посттравматический ОА коленного сустава, 6 – посттравматический ОА тазобедренного сустава, 7 – остеоартроз тазобедренного сустава – исход АНГБ; 8 – остеоартроз, развившийся на фоне ревматоидного артрита; * – p<0,05, ** - p<0,01, *** – p<0,001 относительно значений контрольной группы
ЗАКЛЮЧЕНИЕ
Таким образом, этиология оказывает влияние на иммунный статус больных коксартрозом и го-нартрозом II-III стадии, что необходимо учитывать при лабораторном иммунологическом мониторинге
эндопротезирования или других видов хирургических вмешетельств, применяемых для лечения остеоартроза на поздних стадиях патологического процесса.


