Имплантационный метастаз рака гортани после наложения чрескожной эндоскопической гастростомы
Автор: Гузь Александр Олегович, Захаров Александр Сергеевич, Гарев Артм Владимирович
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Случай из клинической практики
Статья в выпуске: 3 т.16, 2017 года.
Бесплатный доступ
Развитие дисфагии у пациентов с плоскоклеточным раком головы и шеи является закономерным развитием опухолевого процесса. Адекватное энтеральное питание залог успешного лечения и реабилитации пациентов. Одним из возможных методов коррекции дисфагии является наложение чрезкожной эндоскопической гастростомы. Представлен наш опыт наблюдения и лечения пациентки с имплантационным метастазом рака гортани, после наложения чрезкожной эндоскопической гастростомы. Данный случай иллюстрирует редкое осложнение при наложении чрезкожной эндоскопической гастростомии, имплантационное метастазирование и опыт лечения данной пациентки. ЧЭГ является менее инвазивной процедурой, чем открытая гастростомия, она имеет ряд осложнений, такие как имплантационное метастазирование в области гастростомы. Знание этого осложнения и тщательный контроль со стороны онкологов, может обеспечить раннее выявление этого осложнения и раннее лечение.
Имплантационный метастаз, рак гортани, чрескожная эндоскопическая гастростома
Короткий адрес: https://sciup.org/140253985
IDR: 140253985 | УДК: 616.22-006-033.2-089.87-06-072.1 | DOI: 10.21294/1814-4861-2017-16-3-104-107
Implantation metastasis of laryngeal cancer after percutaneous endoscopic gastrostomy
Squamous cell head and neck carcinoma is frequently associated with dysphagia. An adequate enteral nutrition is the key to successful treatment and rehabilitation of these patients. Percutaneous endoscopic gastrostomy is the preferred route of feeding and nutritional support in head and neck cancer patients with dysphagia. We report a rare case of implantation metastasis of laryngeal cancer following percutaneous endoscopic gastrostomy. Our experience in treating this complication has been described. Percutaneous endoscopic gastrostomy is a less-invasive procedure than open gastrostomy. Percutaneous endoscopic gastrostomy can be accompanied by severe complications such as implantation metastasis at gastrostomy site. Careful monitoring can provide early detection of this complication and early treatment.
Текст научной статьи Имплантационный метастаз рака гортани после наложения чрескожной эндоскопической гастростомы
Злокачественные опухоли головы и шеи в структуре общей онкологической заболеваемости занимают менее 5 %. При этом на III-IV стадии плоскоклеточного рака головы и шеи приходится более 60 % случаев [1,2]. Из-за сложного анатомического строения аэро-дигестивного тракта рост опухоли зачастую приводит к нарушению приёма пищи и развитию дисфагии, что требует дополнительного лечения и коррекции. Хроническое недоедание наблюдается приблизительно у 20–57 % пациентов с плоскоклеточным раком головы и шеи [3]. Помимо этого, нарушение приёма пищи возникает в результате комбинированного лечения, и уровень нутритивного статуса прямо влияет на переносимость лечения и, как следствие, на его эффективность. Адекватное энтеральное питание является одним из важных компонентов терапии сопровождения при проведении лечения больных с плоскоклеточным раком головы и шеи. Одним из возможных вариантов современного лечения дисфагии и коррекции нутритивного статуса у онкологических пациентов является чрескожное эндоскопическое наложение гастростомы (ЧЭГ). Данная процедура технически несложная, малоинвазивная и хорошо переносится даже ослабленными пациентами. Одним из возможных видов «нехирургических» осложнений является имплантационное метастазирование.
Впервые данная клиническая ситуация описана S. Preyer et al. в 1989 г., когда пациенту, страдающему плоскоклеточным раком гортаноглотки, до начала лучевой терапии была произведена трахеостомия и наложена ЧЭГ [4]. В мировой литературе представлены единичные случаи имплантационного метастазирования при чрескожной эндоскопической гастростомии [5]. В 2013 г. A.T. Huang et al. [6] опубликовали обзор литературы, в котором описаны 42 случая имплантационного метастазирования плоскоклеточного рака головы и шеи при наложении чрескожной эндоскопической гастростомы (ЧЭГ). Авторы обобщают все опубликованные случаи начиная с 1989 г. по данным базы PubMed. Обзор показал, что среднее время появления метастазов после проведения ЧЭГ составляет 8 мес (3–22 мес). Средний возраст пациентов 56 лет, 89,9 % было мужчин. У 94 % пациентов были III–IV стадии заболевания. Средняя продолжительность
жизни после обнаружения метастазов в районе ЧЭГ составила 5,9 мес (1–19 мес). Общая смертность – 87,1 %, с выживаемостью больше года – 35 %. У 63 % пациентов одновременно с появлением имплантационных метастазов отмечена генерализация процесса с появлением новых очагов в лёгких и печени. Авторы делают вывод, что появление имплантационного метастаза является индикатором агрессивного проявления опухоли и неблагоприятного прогноза. В ГБУЗ ЧОКОД методика чрескожной эндоскопической гастростомы внедрена в клиническую практику с 2010 г. Всего наложено более 60 эндоскопических гастростом.
Представляем опыт лечения пациента с имплантационным метастазом рака гортани.
Пациентка Л., 25 лет, обратилась в Челябинский областной клинический онкологический диспансер 03.12.09 с жалобами на осиплость. При фиброла-рингоскопии (ФЛС) с биопсией выявлено поражение подскладочного отдела гортани больше слева, в виде экзофитного образования, которое занимает 1/3 окружности трахеи и распространяется на переднюю комиссуру. Гистологическое заключение: плоскоклеточный рак умеренной степени дифференцировки. УЗИ лимфоузлов шеи: справа в проекции нижней трети кивательной мышцы два округлых лимфоузла, диаметром 23 и 5 мм, в области яремной вырезки узлы до 14 мм. Пункционная биопсия. Цитологическое заключение: комплексы раковых клеток.
По результатам обследования установлен следующий диагноз: Рак подскладочного отдела гор-
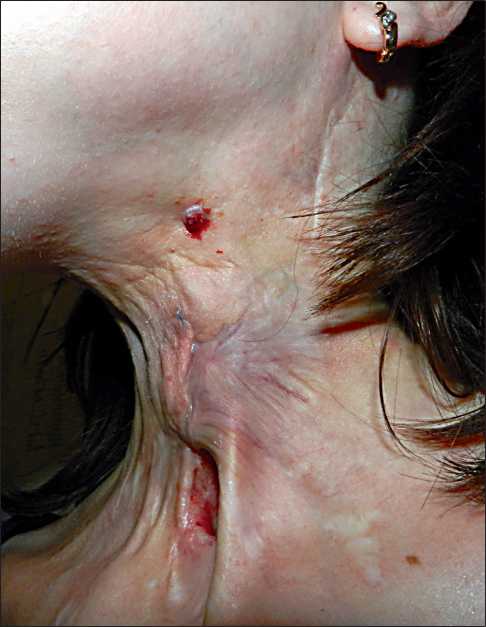
Рис. 1. Рецидив рака гортани в области глоточной воронки тани с метастазами в лимфоузлы шеи cT3сN2bM0, IVa ст. С учётом стадии заболевания, молодого возраста пациентки решено провести комплексное органосохранное лечение: 3 курса индукционной полихимиотерапии (ПХТ) по схеме PF с последующей конкурентной химиолучевой терапией. В период с 24.12.09 по 15.02.10 проведено 3 цикла индукционной химиотерапии по схеме PF (цисплатин 100 мг/м2; 5-фторурацил 1000 мг/м2). C 11.03.10 по 30.04.10 проведён курс конкурентной химиолучевой терапии в традиционном режиме фракционирования до СОД 60 изоГр на первичный очаг и лимфоузлы шеи до 46 изоГр, на фоне введения карбоплатина AUC 1,5 и цетуксимаба (нагрузочная доза 400 мг/м2 за 7 дней до начала облучения; затем еженедельно 2–8 нед – 250 мг/м2). На фоне лечения отмечен полный клинический ответ, по данным ФЛС и МСКТ.
В октябре 2010 г. (через 5 мес после завершения лечения) у пациентки вновь возникла осиплость и отмечено появление увеличенных лимфоузлов на шее с двух сторон. Произведена биопсия опухоли гортани, гистологическое заключение: плоскоклеточный рак низкой степени дифференцировки. 16.11.10 выполнена операция: расширенная ларингэктомия с резекцией верхней трети трахеи, классическая радикальная лимфаденэктомия справа 1 – 5 уровней, модифицированная радикальная лимфаденэктомия слева 1 – 5 уровня, гемитиреоидэктомия с перешейком справа, трахеостомия. Гистологическое заключение: низкой степени дифференцировки плоскоклеточный рак гортани, терапевтический патоморфоз опухоли II ст., язвенно-инфильтративная форма. По краям резекции опухолевого роста нет. Метастаз в лимфатический узел справа, диаметр узла 1,5 см, с полным замещением лимфоидной ткани, некрозом в центре опухоли, опухоль прорастает капсулу лимфоузла, врастает в прилежащие ткани.
Через 4 нед после операции у пациентки сформировался глоточный свищ, который закрылся самостоятельно через 3 мес. До августа 2012 г. у пациентки отмечалась ремиссия заболевания. В августе появились дисфагия за счёт наличия образования до 1,5 см в области глоточной воронки с переходом на трахею по верхнему краю трахеостомы (рис. 1).
30.08.12 пациентке произведена фиброга-стродуоденоскопия с биопсией и одновременное наложение чрескожной эндоскопической гастростомы. Гистологическое заключение: плоскоклеточный рак. Пациентке проведено 4 цикла ПХТ по схеме TPF (таксотер 75 мг/м2; цисплатин 100 мг/м2; 5-фторурацил 1000 мг/м2), на фоне чего отмечена стабилизация заболевания, что позволило в условиях МНИОИ им. П.А. Герцена (г. Москва) 18.02. 13 выполнить операцию: удаление опухоли мягких тканей шеи с резекцией шейного отдела пищевода, трахеи, пластикой перемещенным кожно-фасциальным лоскутом с грудной клетки, формирование оростомы, трахеостомы, эзофагостомы. Гистологическое заключение:
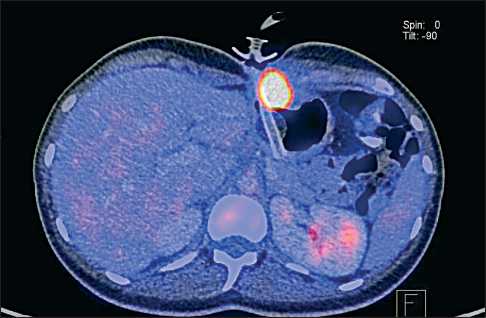
Рис. 2. ПЭТ-КТ. Слева от гастростомической трубки, в области мягких тканей брюшной стенки визуализируется гипо-денсное образование, размером 27×25 мм, накапливающее контрастное вещество инфильтративный низкодифференцированный плоскоклеточный рак с переваскулярной инвазией. Опухоль прорастает стенку пищевода почти полностью без инвазии в адвентицию, дерму, распространяется на трахеостомическое отверстие. В краях резекции пищевода, кожного лоскута, гортаноглотки, трахеи клеток опухоли не обнаружено. Послеоперационный период протекал без осложнений.
Продолжена таргетная терапия цетуксимабом. При контрольном ПЭТ-КТ (06.02.14): прогрессиро- вание заболевания с появлением солитарного метастаза в средостении на уровне LII, размером 30×26 мм, краниокаудально 34 мм, SUVmax-8,9, с инвазией в мембранозную часть трахеи на 1/3 полуокружность и адвентицию плечеголовного ствола на 1/3 окружности. Таргетная терапия прекращена. С паллиативной целью проведён курс конформной лучевой терапии на метастаз средостения в традиционном режиме фракционирования до СОД 40 Гр. После окончания ДЛТ назначена монотерапия гемцитабином.
Список литературы Имплантационный метастаз рака гортани после наложения чрескожной эндоскопической гастростомы
- Каприн Д.А., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2015 году (заболеваемость и смертность). М. 2017; 250.
- Какурина Г.В., Кондакова И.В., Чойнзонов Е.Л., Шишкин Д.А., Черемисина О.В. Особенности протеомы сыворотки крови больных плоскоклеточными карциномами головы и шеи. Сибирский онкологический журнал. 2013; 2: 62-66.
- McRackan T.R., Watkins J.M., Herri A.E. Effect of body mass index on chemoradiation outcomes in head and neck cancer. Laryngoscope. 2008; 118: 1180-1185.
- Preyer S., Thul P. Gastric metastasis of squamous cell carcinoma of the head and neck after percutaneous endoscopic gastrostomy - report of a case. Endoscopy. 1989; 21 (6): 295.
- Cappell M.S. Risk factors and risk reduction of malignant seeding of the percutaneous endoscopic gastrostomy track from pharyngoesophageal malignancy: a review of all 44 known reported cases. Am J Gastroenterol. 2007; 102: 1307-1311.
- Huang A.T., Georgolios A., Espino S., Kaplan B., Neifeld J., Reiter E.R. Percutaneous endoscopic gastrostomy site metastasis from head and neck squamous cell carcinoma: case series and literature review. J Otolaryngol Head Neck Surg. 2013; 42: 20. Review. DOI: 10.1186/1916-0216-42-20


