In silico и in vitro изучение антитирозиназной активности новых оснований шиффа - азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензотиофен-3-карбоксамида
Автор: Чиряпкин А. С., Кодониди И. П., Поздняков Д. И.
Журнал: Juvenis scientia @jscientia
Рубрика: Оригинальные исследования
Статья в выпуске: 3 т.9, 2023 года.
Бесплатный доступ
Введение. Гиперпигментация кожи является важной проблемой дерматокосметологии. Образующиеся пигментные пятна на кожных покровах человека, особенно на открытых участках тела, влияют на его психоэмоциональное состояние и социальную адаптацию, а в некоторых случаях являются и триггерами формирования заболеваний дерматологического профиля. Целью исследования является поиск новых эффективных и безопасных соединений с антитирозиназной активностью. Материалы и методы. В качестве объектов исследования выступают семь новых ранее синтезированных азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензотиофен-3-карбоксамида. Для in silico изучения молекулярных механизмов ингибирования тирозиназы исследуемыми соединениями использован метод молекулярного докинга. Ингибирующую активность тирозиназы определяли согласно методу, описанному Mapunya et al. (2012). Результаты. В ходе вычислительного эксперимента определены аминокислотные остатки активного сайта тирозиназы, с которыми взаимодействуют азометиновые производные 2-амино-4,5,6,7-тетрагидро-1-бензотиофен-3-карбоксамида. In vitro оценка антитирозиназной активности изучаемых соединений свидетельствует о том, что практически все анализируемые вещества уступают референтам по выраженности биологического действия, кроме соединения 1, которое превосходит по активности койевую и молочную кислоты. На основании значения LD50 соединения 1 оно было отнесено к 5-му классу токсичности по GHS-классификации. Заключение. В ходе проведенного исследования было установлено, что структура 1 по выраженности своей фармакологической активности превосходит койевую и молочную кислоты. Считаем целесообразным дальнейшие фармакологические исследования данного вещества.
Тирозиназа, азометины, 2-амино-4, 5, 6, 7-тетрагидро-1-бензотиофен-3-карбоксамид, молекулярный докинг, антитирозиназная активность
Короткий адрес: https://sciup.org/14128036
IDR: 14128036 | DOI: 10.32415/jscientia_2023_9_3_31-41
In silico and in vitro study of antithyrosinase activity of new schiff bases - azomethine derivatives of 2-amino-4,5,6,7-tetrahydro-1-benzothiophene-3-carboxamide
Introduction. Skin hyperpigmentation is an important problem of dermatocosmetology. The resulting pigment spots on the skin of a person, especially in open areas of the body, affect their psychoemotional state and social adaptation, and in some cases trigger dermatological diseases. The aim of the study is to search for new effective and safe compounds with anti-tyrosinase activity. Materials and methods. Seven new previously synthesized azomethine derivatives of 2-amino-4,5,6,7-tetrahydro-1-benzothiophene-3-carboxamide are the objects of research. To study in silico the molecular mechanisms of tyrozinase inhibition by the compounds under study, the method of molecular annealing was used. The inhibitory activity of tyrosinase was determined according to the method by Mapunya et al. (2012). Results. During the computational experiment, we determined amino acid residues of the active tyrosinase site, with which azomethine derivatives of 2-amino-4,5,6,7-tetrahydro-1-benzothiophene-3-carboxamide interact. In vitro evaluation of the anti-tyrosinase activity of the studied compounds indicated that almost all the analyzed substances were inferior to the referents in terms of the strength of biological action, except for compound 1, which was superior in activity to kojic and lactic acids. Based on the LD50 value of compound 1, it was assigned to the 5th class of toxicity according to the GHS classification. Conclusion. In the course of the conducted research, it was found that structure 1 surpasses kojic and lactic acids in the severity of its pharmacological activity. We consider it appropriate to further pharmacological studies of this substance.
Текст научной статьи In silico и in vitro изучение антитирозиназной активности новых оснований шиффа - азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензотиофен-3-карбоксамида
Гиперпигментация кожи является результатом чрезмерного диффузного или очагового отложения пигмента меланина в клетках эпидермиса, которое приводит к формированию на ней окрашенных участков коричневого цвета. Очаговая гиперпигментация может возникнуть, например, в случае проявления поствоспалительного процесса или мелазмы. Диффузная гиперпигментация, как правило, обусловливается метаболическими нарушениями, приемом лекарственных препаратов, онкологическими и аутоиммунными заболеваниями, а также может иметь инфекционную этиологию [1]. Гиперпигментация выступает важной проблемой дерматокосметологии, так как внешний облик человека влияет на его психоэмоциональное состояние и социальную адаптацию. K. França et al. (2017) установили, что 78% респондентов, у которых встречается гиперпигментация кожи лица, не способны наладить должный социальный контакт, 22% отмечают ухудшение качества жизни, а 10% нуждаются в квалифицированной психологической помощи [2]. Помимо психоэмоциональных проблем гиперпигментация кожных покровов может приводить к формированию у человека заболеваний. Аномально активные меланоциты выступают родоначальниками формирования меланомы, которая является злокачественной опухолью кожных покровов. Также патологически активный процесс формирования меланина может быть предрасполагающим фактором возникновения заболеваний дерматологического профиля, например, таких как, шейная пойкилодерма, лентигины и черный акантоз [3].
Меланогенез представляет собой важный биохимический процесс, продукт которого участвует в защите кожных и подкожных элементов тканей человека от пагубного воздействия ультрафиолетового излучения. Синтез меланина осуществляется тирозиназой — ферментным металлопротеидом, который относится к классу оксидоредуктаз. Субстратом для многоступенчатого биохимического каскада является тирозин, который через образование хинонов превращается непосредственно в меланин [4]. Тем самым, подавление активности тирозиназы напрямую снижает содержание кож- ного пигмента. Выделяют два основных подхода для терапии гиперпигментации: химический пилинг молочной кислотой и подавление активности тирозиназы [5]. Предварительные данные свидетельствуют об безопасности пилинга, в том числе при беременности и кормлении грудью [6]. В экспериментах in vitro обнаружено, что пилинг ингибирует ферменты, которые отвечают за разрушение коллагена и эластина, а не только выработку пигмента меланина. К тому же обнаружено, что трихлоруксусная кислота может синергически усиливать ингибирующее действие молочной кислоты [7].
Для снижения аномального меланогенеза осуществляется поиск и разработка ингибиторов тирозиназы. С доказанной эффективностью подавляют активность фермента такие соединения, например, как койевая, молочная, аскорбиновая и транек-самовая кислоты [8]. Койевая кислота обладает высокой биосовместимостью и образуется как метаболит жизнедеятельности плесневых грибов, относящихся к родам Aspergillus и Penicillium [9]. Высокой ингибирующей способностью фермента также обладает гидрохинон, но он относится к наиболее токсичным ингибиторам тирозиназы. Для снижения нежелательных эффектов от его использования рекомендуют в гель с ним добавлять изотретиноин [10]. Важно отметить, что применение ингибиторов тирозиназы не приводит к наступлению быстрого фармакологического эффекта, их действие в виде снижения уровня пигментации кожных покровов проявляется постепенно [8]. Таким образом, целенаправленный синтез новых высокоэффективных и безопасных соединений с антитирозиназной активностью является актуальной фармацевтической задачей.
МАТЕРИАЛЫ И МЕТОДЫ
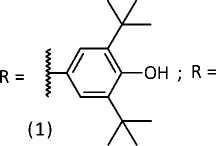
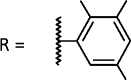
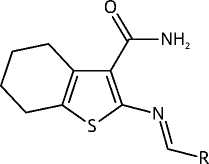
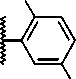
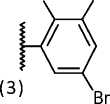
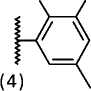
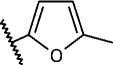
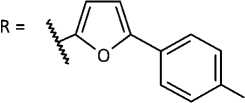
Объектами научного исследования выступают семь новых синтезированных азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензотио-фен-3-карбоксамида (рис. 1), которые получены нами на кафедре органической химии Пятигорского медико-фармацевтического института — филиала ВолгГМУ. Согласно данным фармакологического скрининга in vitro , они обладают антихолинэстераз-ной и антиамилоидной активностью, что обуслав-
Br
HO
OH
(2) NO2
OH O
R =
OH Br
NO
Рисунок 1. Структурные формулы азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензо-тиофен-3-карбоксамида.
ливает их гипотетическое применение для лечения болезни Альцгеймера. Структуры синтезированных соединений были подтверждены данными ИК-спектроскопии, 1H и 13C ЯМР [11–13].
Для ингибирования тирозиназы важным структурным элементом молекулы является наличие фенольного фрагмента, который, например, присутствует в таких ингибиторах фермента, как гидрохинон, резорцин и койевая кислота [14]. Таким образом, структуры с фенольными заместителями могут быть эффективными для ингибирования тирозиназы. Среди рассматриваемых азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бен-зотиофен-3-карбоксамида имеются соединения, которые удовлетворяют данное требование. Следовательно, они могут быть эффективными ингибиторами тирозиназы, что обуславливает целесообразность проводимых in silico и in vitro исследований.
Для проведения вычислительного эксперимента методом молекулярного докинга в качестве биологической мишени использована трехмерная виртуальная модель тирозиназы гриба Garicus bisporus из базы данных RCSB Protein Data Bank (rcsb.org) с идентификационным номером 2Y9X, структура которой достоверно установлена рентгеноструктурным анализом [15]. Грибная тирозиназа обладает широкой коммерческой доступностью по сравнению с тирозиназой человека, что позволяет активно использовать ее при разработке соединений-ингибиторов данного фермента [8]. При этом она обладает высокой гомологией с тирозиназой млекопитающих [16], в связи с чем ее можно рассматривать в качестве удобной мишени для поиска биологически активных соединений, применяемых для терапии заболеваний человека [8].
Пространственное построение структур анализируемых азометиновых производных 2-ами-но-4,5,6,7-тетрагидро-1-бензотиофен-3-карбокс-амида осуществлено в программе HyperChem 8.0.4 с последующей геометрической оптимизацией в программе ORCA 4.1. методом теории функционала плотности (UB3LYP) с применением базиса 6–311G** [17].
Молекулярный докинг проводился в программе Autodock 4.0 [18]. Моделируемые низкомолекулярные соединения обладали конформационной подвижностью, которая заключается в их способности менять в пространстве расположение структурных элементов молекулы относительно друг друга согласно их торсионным углам. Заряды всех атомов моделируемой системы рассчитывались алгоритмом Гастейгера (Gasteiger algorithm), и у них присутствуют только полярные атомы водорода. Заряд для двух атомов меди в активном сайте тирозиназы задавался вручную и равняется +2. In silico эксперимент проводился в кубической области моделирования, центр которой расположен по следующим координатам: x = –9,985, y = –27,898, z = –40,690. В итоге в программе Autodock 4.0 задавался поиск 200 энергетически выгодных конформаций образования комплекса лиганд-фермент с использованием ламарковской скоринговой функции подсчета энергии взаимодействия (Lamarckian GA 4.2). Аналогичным методом проводили вычислительный эксперимент тиенопиримидинов, где приводятся данные валидационной оценки данного протокола молекулярного докинга и обоснование предлагаемого дизайна ингибиторов тирозиназы [14].
Активность тирозиназы определяли согласно методу, описанному Mapunya et al. (2012) [19]. Изучаемые соединения растворяли в диметилсульфоксиде (ДМСО) до конечной концентрации 1000 µг/мл. Данный маточный раствор разбавляли 50 мМ калий-фосфатным буфером (рН 6,5) с получением двукратных разведений (500 µг/мл, 250 µг/ мл; 125 µг/мл и 62,5 µг/мл). Койевая кислота, гидрохинон и молочная кислота в аналогичном диапазоне концентраций использовались в качестве эталонов сравнения. Гидрохинон и койевая кислота были получены от Hunan Warrant pharmaceuticals (КНР), молочная кислота была предоставлена Sigma-Aldrich (Германия).
Ход анализа. В 96-луночный планшет вносили по 70 µл каждого серийного разведения и добавляли µл 30 тирозиназы (333 ЕД/мл в фосфатном буфере). Полученную смесь инкубировали при комнатной температуре в течение 5 минут. После инкубации добавляли 110 µл субстрата (2 мМ раствор L-тирозина) в каждую лунку и повторно инкубировали.
Оптическую плотность реакционных смесей регистрировали при 492 нм с помощью планшетного ридера Infinite F50 (Tecan). Все тесты выполнены в триплетном варианте. На основании полученных данных методом пробит-анализа рассчитывали показатель IC50 в моль/мл. Данные выражали в виде M (среднее значение) ± SEM (стандартная ошибка среднего), межгрупповые сравнения проводили методом ANOVA с пост-обработкой Ньюмена-Кейлса [19].
Острую токсичность азометинового производного 2-амино-4,5,6,7-тетрагидро-1-бензотио-фен-3-карбоксамида оценивали при пероральном введении методом «Up and Down», предполагающим проведение двух тестов: тест предельно переносимой дозы и основное тестирование (проводится в случае наличия летальности при проведении теста предельной дозы) [20]. В качестве биологической модели при изучении острой токсичности использовали мышей-самцов линии Balb/c массой 20–22 грамма, полученных из питомника лабораторных животных «Рапполово» (Россия, Ленинградская обл.). Исследование острой токсичности синтезированных веществ проводилось с соблюдением общепринятых норм экспериментальной этики, который изложены в Директиве 2010/63/ EU Европейского парламента и Совета Европейского Союза от 22 сентября 2010 года по охране животных, используемых в научных целях. Дизайн эксперимента был одобрен локальным этическим комитетом (протокол № 11 от 20.12.2019).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В результате проведенного вычислительного эксперимента были выбраны для анализа энергетически выгодные расположения азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензо-тиофен-3-карбоксамида в каталитическом сайте фермента, при которых их азометиновый заместитель расположен в сторону атомов меди в сужающемся кармане фермента. Такая локализация гидроксифенильного фрагмента моделируемых соединений позволяет им вступать во взаимодействие с атомами меди в активном сайте тирозиназы, как, например, гидрохинону, койевой и молочной кислотам.
Таблица 1
Значения минимальной энергии лиганд-ферментного взаимодействия моделируемых соединений с активным сайтом тирозиназы и информация о водородных связях
|
Соединение |
Энергия, ккал/моль |
Остаток аминокислоты |
Группа лиганда |
Длина связи (Å) |
|
1 |
-5,80 |
- |
- |
- |
|
2 |
-9,32 |
Val 283 |
C= O |
1,963 |
|
3 |
-7,33 |
Gly 281 |
N H 2 |
1,873 |
|
4 |
-6,93 |
Val 283 |
C= O |
2,201 |
|
5 |
-7,07 |
Val 283 |
C= O |
2,180 |
|
6 |
-6,77 |
Gly 281 |
N H 2 |
1,909 |
|
Ser 282 |
-N= |
2,050 |
||
|
7 |
-13,11 |
Val 283 |
-N= |
2,214 |
|
Гидрохинон |
-3,70 |
Met 280 |
O H |
2,134 |
|
Койевая кислота |
-4,46 |
Asn 260 |
O H |
2,117 |
|
Молочная кислота |
-7,22 |
- |
- |
- |
Согласно данным молекулярного докинга, анализируемые азометиновые производные 2-ами-но-4,5,6,7-тетрагидро-1-бензотиофен-3-карб-оксамида формируют связи со следующими аминокислотными остатками активного сайта фермента: His 259, Asn 260, His 263, Phe 264, Arg 268, Met 280, Gly 281, Ser 282, Val 283, Pro 284. В таблице 1 показаны минимальные энергии формирования лиганд-ферментного комплекса. Согласно этим данным, наиболее энергетически выгодные молекулярные комплексы образуют соединения 2 и 7. Структуры 2, 4 и 5 образовывают водородную связь между своими атомами кислорода карбонильной группы и Val 283. Атом водорода амидной группы структур 3 и 6 формирует водородную связь с Gly 281. Азот амидной связи веществ 6 и 7 может образовывать водородную связь с аминокислотным остатком Ser 282 и Val 283, соответственно. Атомы водорода гидроксильных групп гидрохинона формируют водородную связь с аминокислотным остатком Met 280, а койевой кислоты — с Asn 260.
На рисунке 2 показано расположение моделируемых соединений в активном сайте тирозиназы.
In vitro оценка способности азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензотио-фен-3-карбоксамида ингибировать тирозиназу сви- детельствует о том, что практически все изучаемые вещества уступают референтам по выраженности биологического действия. При этом наиболее перспективным соединением с антитирозиназной активностью является структура 1, которая превосходит по действию койевую и молочную кислоты. В тоже время показатель IC50 соединения 6 был статистически значимо выше такового у гидрохинона и койевой кислоты.
В ходе проведения тестирования было установлено, что при введении производного 2-ами-но-4,5,6,7-тетрагидро-1-бензотиофен-3-карбокс-амида под шифром 1 четырем последовательным животным в дозе 5000 мг/кг ( per os ) летального исхода отмечено не было. В связи с этим к проведению основного тестирования не приступали и за показатель LD50 принимали значение 5000 мг/кг. Основываясь на значении LD50, структура 1 была отнесена к 5-му классу токсичности по GHS-классификации [21].
Сопоставляя результаты вычислительного эксперимента и in vivo исследования изучения антитирозиназной активности азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензотиофен-3-карб-оксамида, можно предположить, что важную роль в процессе ингибирования фермента играет
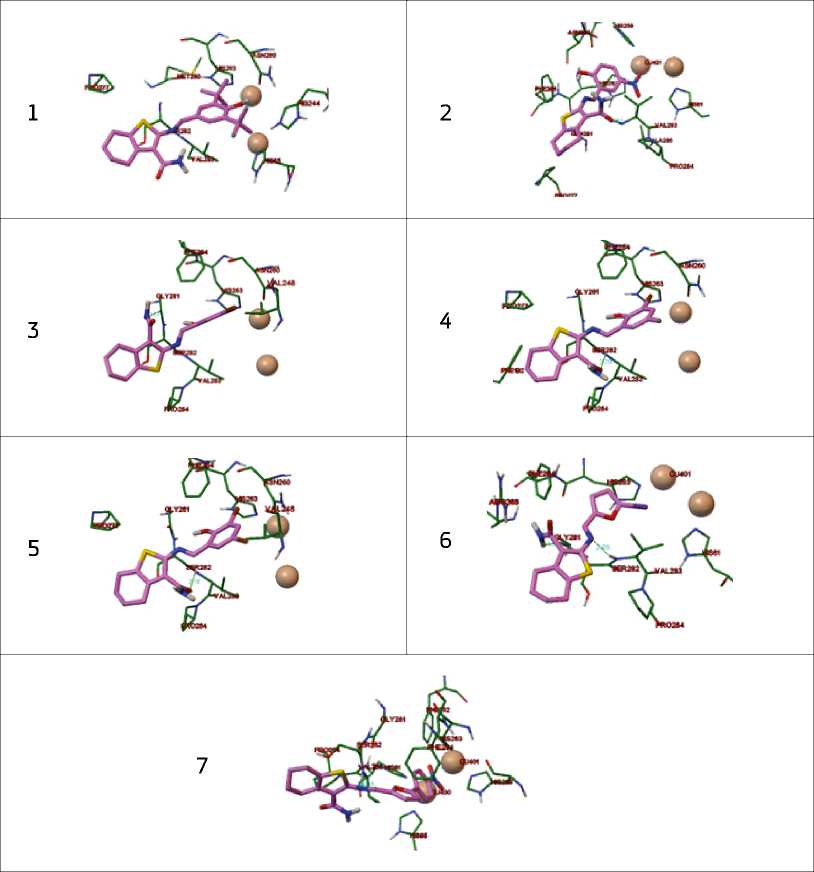
Рисунок 2. Локализация азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензотио-фен-3-карбоксамида в активном сайте тирозиназы.
взаимодействие лигандов с двумя атомами меди активного сайта тирозиназы. Такие молекулы, как гидрохинон, койевая и молочные кислоты в своей структуре содержат кислородсодержащие группировки — гидрокси- и/или карбоксильные группы, которые осуществляют химическое взаимодействие метал-лиганд с двумя атомами меди сайта связывания тирозиназы. Таким образом, для раз- работки молекул в качестве ингибиторов этого фермента целесообразно модифицировать выбранные для этой цели исследователями скаффолды, например, гидроксильными или карбонильными группами.
Проводилось in silico и in vitro изучение антитирозиназной активности целенаправленно синтезированных 5,6,7,8-тетрагидробензо[4,5]тиено[2,3-d]
Таблица 2
Влияние исследуемых соединений и референтов на изменение активности тирозиназы in vitro
|
Соединение |
IC50±SEM ммоль/мл |
|
1 |
0,26±0,064 *#Δ |
|
2 |
0,39±0,019*#Δ |
|
3 |
0,82±0,059*#Δ |
|
4 |
0,66±0,078*#Δ |
|
5 |
0,65±0,05*#Δ |
|
6 |
0,76±0,009*#Δ |
|
7 |
0,8±0,03*# |
|
Гидрохинон |
0,15±0,007 |
|
Койевая кислота |
0,32±0,005 |
|
Молочная кислота |
0,46±0,031 |
Примечание: * — статистически значимо относительно гидрохинона (критерий Ньюмена-Кейлса, p<0,05); # — статистически значимо относительно койевой кислоты (критерий Ньюмена-Кейлса, p<0,05); Δ — статистически значимо относительно молочной кислоты (критерий Ньюмена-Кейлса, p<0,05).
пиримидин-4(3H)-онов, которые получали путем гетероциклизации азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензотиофен-3-карб-оксамида. Биологическая активность обуславливается наличием в их структуре арильного радикала с гидрокси- и/или метоксигруппой, что согласуется с данными полученными нами в ходе исследования [14]. К тому же многие флавоноиды, например, такие как кемпферол, морин, лютеолин, кверцетин проявляют способность ингибировать тирозиназу, так как в их структуре присутствуют фенольные группы [22]. Синтезированы новые тетракетоны, которые по ингибирующей способности превзошли койевую кислоту и L-мимозин, что позволяет рассматривать кетогруппу в качестве возможного фармакофора для молекулярного конструирования антитирозиназных соединений [23]. Таким образом, можно выделить кислородсодержащие молекулярные группировки как важные структурные признаки соединений для ингибиторов тирозиназы. Синтезированные соединения содержат фенольные группы, за счёт чего предположительно и реализуется их антитирозиназное действие.
По результатам исследования можно пред- положить, что для целенаправленного синтеза ингибиторов тирозиназы можно использовать 3,5-ди-трет-бутил-4-гидроксифенильный фрагмент, так как азометиновое производное 2-ами-но-4,5,6,7-тетрагидро-1-бензотиофен-3-карбокс-амида с этой молекулярной структурой оказалось высокоэффективным ингибитором фермента. Возможно, что положительно на биологическую активность соединения 1 также сказывается высокая лиофильность трет-булиловых фрагментов, которая позволяет молекуле легче проникать в сайт связывания тирозиназы.
ЗАКЛЮЧЕНИЕ
В ходе проведенных исследований проанализировано семь азометиновых производных 2-ами-но-4,5,6,7-тетрагидро-1-бензотиофен-3-карбокс-амида на предмет наличия у них антитирозиназной биологической активности. Среди них соединением-лидером является структура 1, которая по выраженности своей фармакологической активности превосходит койевую и молочную кислоты, а также относится к 5-му классу токсичности по GHS-классификации, что позволяет судить о низкой токсичности соединения. Можно предположить, что ди-трет-бутил-4-гидроксифенильный фрагмент является перспективной химической группировкой для молекулярного конструирования соединений с антитирозиназным действием. Считаем целесообразным дальнейшие более углубленные медикобиологические исследования соединения-лидера.
Финансирование: Исследование выполнено при финансовой поддержке РФФИ в рамках научного проекта № 20-315-90060.
Список литературы In silico и in vitro изучение антитирозиназной активности новых оснований шиффа - азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензотиофен-3-карбоксамида
- Desai SR. Hyperpigmentation therapy: a review. J Clin Aesthet Dermatol. 2014;7(8):13-17.
- França K, Keri J. Psychosocial impact of acne and postinflammatory hyperpigmentation. AnBrasDermatol. 2017;92(4):505-509. DOI: 10.1590/abd1806-4841.20175645.
- Rigopoulos D, Gregoriou S, Katsambas A. Hyperpigmentation and melasma. J Cosmet Dermatol. 2007;6(3):195-202. DOI: 10.1111/j.1473-2165.2007.00321.
- Furue M, Tsuji G. Chloracne and Hyperpigmentation Caused by Exposure to Hazardous Aryl Hydrocarbon Receptor Ligands. International Journal of Environmental Research and Public Health. 2019;16(23):4864. DOI: 10.3390/ijerph16234864.
- Sarkar R, Bansal S, Garg VK. Chemical peels for melasma in dark-skinned patients. J Cutan Aesthet Surg. 2012;5(4):247-253. DOI: 10.4103/0974-2077.104912.
- Trivedi MK, Kroumpouzos G, Murase JE. A review of the safety of cosmetic procedures during pregnancy and lactation. International Journal of Women’s Dermatology. 2017;3(1):6-10. DOI: 10.1016/j.ijwd.2017.01.005.
- Bhardwaj V, Sharma K, Maksimovic S, et al. Professional-Grade TCA-Lactic Acid Chemical Peel: Elucidating Mode of Action to Treat Photoaging and Hyperpigmentation. Front. Med. 2021;8:617068. DOI: 10.3389/fmed.2021.617068.
- Zolghadri S, Bahrami A, Hassan Khan MT, et al. A comprehensive review on tyrosinase inhibitors. Journal of Enzyme Inhibition and Medicinal Chemistry. 2019;34(1):279-309. DOI: 10.1080/14756366.2018.1545767.
- Saeedi M, Eslamifar M, Khezri K. Kojic acid applications in cosmetic and pharmaceutical preparations. Biomedicine & Pharmacotherapy. 2019;110:582-593. DOI: 10.1016/j.biopha.2018.12.006.
- Chandra M, Levitt J, Pensabene CA. Hydroquinone therapy for post-inflammatory hyperpigmentation secondary to acne: not just prescribable by dermatologists. Acta Derm Venereol. 2012;92:232-235.
- Чиряпкин А.С., Кодониди И.П., Ларский М.В. Целенаправленный синтез и анализ биологически активных азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензотиофен-3-карбоксамида // Разработка и регистрация лекарственных средств. 2021. Т. 10. № 2. С. 25-31. [Chiriapkin AS, Kodonidi IP, Larsky MV. Targeted Synthesis and Analysis of Biologically Active Azomethine Derivatives of 2-amino-4,5,6,7-tetrahydro-1-benzothiophene-3-carboxamide. Drug development & registration. 2021;10(2):25-31. (in Russ.)]. DOI: 10.33380/2305-2066-2021-10-2-25-31.
- Chiriapkin AS, Kodonidi IP, Pozdnyakov DI. et al. Synthesis and QSAR of new azomethine derivatives as agents for the treatment of Alzheimer’s disease. Pharmacologyonline. 2021;3:563-584.
- Чиряпкин А.С., Кодониди И.П., Поздняков Д.И. Изучения антитирозиназной активности азометиновых производных 2-амино-4,5,6,7-тетрагидро-1-бензотиофен-3-карбоксамида // Вестник Воронежского государственного университета. Серия: Химия. Биология. Фармация. 2022. № 1. С. 110-116. [Chiriapkin AS, Kodonidi IP, Pozdnyakov DI. Studies of antithyrosinase activity of azomethine derivatives of 2-amino-4,5,6,7- tetrahydro-1-benzothiophene-3-carboxamide. Proceedings of Voronezh State University. Series: Chemistry. Biology. Pharmacy. 2022;1:110-116. (in Russ.)].
- Chiriapkin A, Kodonidi I, Pozdnyakov D. Targeted Synthesis and Study of Anti-tyrosinase Activity of 2-Substituted Tetrahydrobenzo[4,5]Thieno[2,3-d]Pyrimidine-4(3H)-One. Iran J Pharm Res. 2022;21(1):e126557. DOI: 10.5812/ijpr-126557.
- Ismaya WT, Rozeboom HJ, Wijn A, et al. Crystal Structure of Agaricus bisporus Mushroom Tyrosinase: Identity of the Tetramer Subunits and Interaction with Tropolone. Biochemistry. 2011;50(24):5477-5486. DOI: 10.1021/bi200395t.
- You Z, Wang Y-Q, He Q-X. Homology Modeling of Human Tyrosinase. J Southwest Univ. 2020;42:42-48.
- Brian JT. Hyerchem, release 2: molecular modeling for the personal computer. J Chem Inf Comput Sci. 1992;32:757-759.
- Morris GM, Huey R, W. Lindstrom W, et al. Autodock4 and AutodockTools4: Automated Docking with Selective Receptor Flexibility. J Comput Chem. 2009;30:2785-2791. DOI: 10.1002/jcc.21256.
- Mapunya MB, Nikolova RV, Lall N. Melanogenesis and antityrosinase activity of selected South african plants. Evid Based Complement Alternat Med. 2012;2012:374017. DOI: 10.1155/2012/374017.
- OECD № 425. Guidelines for the testing of chemicals Acute Oral Toxicity – Up-and-Down-Procedure (UDP).
- Globally Harmonized System of Classification and Labelling of Chemicals (GHS) Part 3 Health Hazards, United Nations, 2017.
- Kim YJ, Uyama H. Tyrosinase inhibitors from natural and synthetic sources: structure, inhibition mechanism and perspective for the future. CMLS, Cell Mol Life Sci. 2005;62: 1707-1723. DOI: 10.1007/s00018-005-5054-y.
- Khan KM, Maharvi GM, Khan MTH, et al. Tetraketones: A new class of tyrosinase inhibitors. Bioorganic & Medicinal Chemistry. 2006;14(2):344-351. DOI: 10.1016/j.bmc.2005.08.029.


