Инактивация тучных клеток нивелирует негативные последствия влияния высокой температуры на сперматогенез
Автор: Храмцова Ю.С., Садек А., Изместьева О.В., Юшков Б.Г.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Экспериментальная урология
Статья в выпуске: 4 т.18, 2025 года.
Бесплатный доступ
Введение. Одной из причин снижения мужской фертильности является чрезмерное перегревание яичек в результате различных причин. У пациентов с некоторыми формами мужского бесплодия наблюдается увеличение количества тучных клеток в семенниках, что указывает на связь этих клеток с данной проблемой и возможность коррекции нарушений сперматогенеза модуляцией состояния последних. Цель. Исследовать влияние инактивации тучных клеток препаратом кетотифен на сперматозоиды крыс на разных стадиях созревания при действии высокой температуры. Материалы и методы. Эксперимент проведен на 5 группах крыс самцов линии Wistar: 1) интактная, 2 и 3) контрольная и опытная группы многократного воздействия высокой температуры (48 суток, 43±1°C ежедневно 30 мин), 4 и 5) контрольная и опытная группы многократного воздействия высокой температуры + кетотифен. Оценивали спермограмму и сперматозоиды придатка, уровень тестостерона. Морфологические исследования сперматозоидов проводили с помощью ImageJ 1.53t. Данные статистически проанализированы с использованием GraphPad Prism 9.5.1. Результаты. У интактных животных наблюдаются различия морфофункциональных параметров эпидидимальных сперматозоидов и сперматозоидов нативного эякулята. У особей, подвергшихся многократному воздействию высокой температуры, отмечается значительное снижение концентрации, подвижности и агглютинации сперматозоидов на всех стадиях созревания, увеличивается процент дефектных клеток. Инактивация тучных клеток кетотифеном сохраняет параметры нативного эякулята и сперматозоидов придатка на уровне контроля, что свидетельствует о благоприятном влиянии применение препарата на нарушенный сперматогенез. Заключение. Инактивация тучных клеток препаратом кетотифен нивелирует негативные последствия влияния высокой температуры на сперматогенез.
Сперматогенез, сперматозоиды, высокая температура, тестостерон, семенник, придаток семенника, кетотифен
Короткий адрес: https://sciup.org/142246973
IDR: 142246973 | DOI: 10.29188/2222-8543-2025-18-4-26-36
Inactivation of mast cells eliminates the negative effects of high temperature on spermatogenesis
Introduction. Excessive overheating of the testicles, caused by various factors including pathologies, is one of the reasons for the decline in male fertility. In patients with some forms of male infertility an increase in testicular mast cells has been observed, suggesting a link between these cells and fertility issues. This raises the possibility of correcting spermatogenesis disorders by modulating mast cells activity. Objective. This study aims to investigate the effect of mast cell inactivation using mast cells blocker кetotifen on rat sperm at different maturation stages under high-temperature conditions. Materials and methods. The experiment involved 5 groups of male Wistar rats: 1) intact group, 2 and 3) control and experimental groups subjected to repeated high temperature exposure (48 days, 43±1°C for 30 min daily), 4 and 5) control and experimental groups exposed to high temperatures while receiving ketotifen. Ejaculate and epididymal sperm were evaluated using spermogram analysis, and testosterone levels were measured, and testosterone level measurements were performed. Morphological analysis of spermatozoa was conducted using ImageJ 1.53t. Statistical analysis was performed using GraphPad Prism 9.5.1. Results. Intact animals show differences in the morphological and physiological parameters of epididymal and ejaculate sperm. Repeated exposure to high temperature resulted in a significant decrease in sperm concentration, motility, and agglutination at all stages of maturation, while the percentage of defective cells increased. Mast cell inactivation maintains ejaculate and epididymal sperm parameters at control levels, indicating a beneficial effect of the drug on impaired spermatogenesis. Conclusion. Inactivating mast cells with mast cells blocker ketotifen effectively neutralizes the adverse effects of high temperatures on spermatogenesis.
Текст научной статьи Инактивация тучных клеток нивелирует негативные последствия влияния высокой температуры на сперматогенез
экспериментальная и клиническая урология № 4 2025
Многочисленные исследования показывают, что примерно половина всех случаев бесплодия связана с женским фактором, от 20 до 30% – с мужским и до 30% относятся к смешанным [1]. Соответственно, мужское бесплодие на сегодняшний день является серьезной проблемой, присутствующей у 50% бесплодных пар [2]. Мужской репродуктивный потенциал снижается ввиду различных факторов [3, 4], среди которых можно выделить повышение температуры мошонки, как одну из наиболее распространенных причин, вызывающих снижение фертильности у мужчин. Это в значительной степени связано с меняющимся образом жизни [1, 5].
Гипертермии способствуют производственные факторы, гиподинамия, ожирение, ношение тесного белья, а также патологические изменения в яичках (например, варикоцеле) и другое. Точное понимание механизма теплового воздействия на сперматогенез и его микроокружение, качество эякулята, а также поиск новых мишеней для возможной коррекции негативных последствий будут способствовать снижению его значения в общей доле мужского бесплодия, т. к. воздействие высоких температур является обратимым и предотвратимым фактором [6, 7].
Патологии различных органов и систем могут быть обусловлены как поражением его специфических клеток, так и их микроокружением. Тучные клетки – важные компоненты микроокружения мужских репродуктивных органов, участвующие в регуляции сперматогенеза. В последнее десятилетие появляются работы, свидетельствующие о повышенном количестве тестикулярных тучных клеток у мужчин с бесплодием [8, 9], а блокаторы этих клеток приводят к некоторым положительным эффектам при различных патологических состояниях [10, 11]. Это дает основание полагать, что инактивация тучных клеток может приводить к снижению негативных последствий влияния высокой температуры на сперматогенез.
В связи с этим цель настоящей работы – исследовать влияние инактивации тучных клеток препаратом кетотифен на сперматозоиды крыс на разных стадиях созревания при воздействии высокой температуры.
МАТЕРИАЛЫ И МЕТОДЫ
В качестве экспериментальных животных использовали 45 половозрелых самцов крыс линии Wistar массой 392,0±10,8 г возрастом 4 месяца. Во время эксперимента животных содержали в обычных условиях вивария при двенадцатичасовом световом дне, без специальной диеты и без ограничения питьевой воды.
Содержание,питание,уход и выведение животных из эксперимента осуществляли в соответствии с Правилами проведения работ с использованием экспериментальных животных (приказ № 755 от 12.08.1987 г.) и Федерального Закона РФ «О защите животных от жестокого обращения» от 01.01.1997 г. Исследование одобрено решением этического комитета ИИФ УрО РАН (№10-23 от 09.10.2023).
Все животные были разделены на 5 групп:
-
1) группа интактных животных (ИНТ), n=15;
-
2) контрольная группа многократного теплового воздействия (МТ (К)), n=10;
-
3) опытная группа многократного теплового воздействия (МТ (О)), n=10;
-
4) контрольная группа, получавшая препарат ке-тотифен (МТК (К)), n=5;
-
5) опытная группа многократного теплового воздействия, получавшая препарат кетотифен (МТК (О)), n=5.
Перед началом исследования у каждой особи методом окситоциновой стимуляции был произведен забор нативного эякулята и исследованы его характеристики с целью отбора в эксперимент только животных с нормальным сперматогенезом.
Многократное воздействие высокой температуры проводили [5 ] путем размещения животных в специально оборудованный термостат при температуре 43±1°C [12, 13] с сохранением доступа к воде и воздуху ежедневно на 30 мин в течение 48 суток (срок соответствует длительности 1 полного цикла сперматогенеза у крыс). Контрольная группа животных подвергалась тем же манипуляциям,но при выключенном термостате. На 24 сутки эксперимента было проведено промежуточное исследование нативного эякулята у животных обеих групп.
В 4 и 5 экспериментальных группах за 14 дней до воздействия высокой температуры и в течение 48 суток в ходе эксперимента животным ежедневно вводили препарат кетотифен 1 мг/кг внутрижелу-дочно через зонд.
У всех групп животных были взяты нативный эякулят и эпидидимальные сперматозоиды из головки придатка яичка для анализа спермограммы и оценки морфологических параметров сперматозоидов, а также кровь из бедренной вены для определения концентрации тестостерона в крови.
Забор нативного эякулята. Нативный эякулят получали методом окситоциновой стимуляции эякуляции [5,6]. Крыс наркотизировали эфиром, затем инсулиновым шприцом внутрибрюшинно вводили 0,2 мл раствора окситоцина концентрацией 5 МЕ/мл (Московский эндокринный завод, Россия). С полового члена крысы аккуратно отодвигали препуций и придерживали его до наступления эякуляции. Полученный эякулят с помощью дозатора собирали на предметное стекло,замеряли его объем,разводили в 2раза физиологическим раствором комнатной темпе-ратуры,после проводили оценку параметров спермо-граммы.
Забор эпидидимальных сперматозоидов. Для забора эпидидимальных сперматозоидов [14] у самцов крыс после их эвтаназии передозировкой диэтиловым эфиром оперативным методом выделяли придатки се-менников.Для извлечения семенной жидкости производили продольный разрез,отрезая головную часть придатка одинакового размера у всех крыс,затем ее помещали в пробирку и добавляли 2мл физиологического раствора температурой 37°C. Пробирку тщательно встряхивали и помещали в термостат при температуре 37°C на 10 мин. Затем пробирку повторно встряхивали и проводили анализ сперматозоидов.
Подсчет спермограммы. Микроскопическое исследование сперматозоидов в камере Горяева проводили при помощи светового микроскопа Leica DM2500 (Leica, Германия) при увеличении 40х15 по следующим показателям:
а) Концентрация сперматозоидов (млн/мл). В 1 мл эякулята проводили подсчет сперматозоидов в 5 больших квадратах, расположенных по диагонали слева сверху и направо вниз. Концентрацию рассчитывали по формуле:
С = (А ×250×2×1000)/5, где
С – концентрация сперматозоидов;
А – количество посчитанных сперматозоидов.
-
б) Содержание подвижных сперматозоидов (%). В случайно выбранном поле зрения было подсчитано общее количество клеток и количество подвижных клеток. Расчет процентного содержания подвижных клеток вели по формуле:
А=(В×100)/С, где
А – процентное содержание подвижных сперматозоидов;
В – количество подвижных сперматозоидов;
С – общее количество сперматозоидов.
-
в) Агглютинация сперматозоидов. Параметр оценивали по всей камере, для оценки использовали следующую классификацию:
(+ / 1 балл) – до 10–15% сперматозоидов склеены в небольшие агглютинаты;
(++ / 2 балла) – до 50% сперматозоидов склеены как в небольшие,так и в крупные агглютинаты;
(+++ / 3 балла) – массовая агглютинация, почти все сперматозоиды склеены в большие конгломераты.
-
г) Наличие лецитиновых зерен. Параметр оценивали по всей камере,для оценки использовали следующую классификацию:
1балл – малое количество;
-
2 балла – среднее количество;
-
3 балла – большое количество.
Для удобной регистрации полученных данных был разработан протокол исследования.
Оценка морфологических параметров сперматозоидов. Для морфологической оценки из эякулята и семенной жидкости эпидидимиса были приготовлены мазки. С помощью светового микроскопа Leica DM2500 (Leica, Германия), оснащенного камерой Basler acA1920-40um (B asler, Германия), проводили подсчет клеток для выявления процента сперматозоидов без дефектов. При этом визуально оценивали клетки на наличие дефектов головки,шейки и хвоста. Расчет вели на 100 клеток у каждой особи (всего проанализировали 3000 сперматозоидов) (рис. 1).
После проводили фотофиксацию сперматозоидов с помощью камеры и программы MultiMedia Catalog 2008–2020. На полученных фото в программе FIJI ImageJ 1.54f после соответствующей калибровки пикселей в микрометры проводили измерения следующих морфометрических параметров сперматозоидов: длина головки, мкм; ширина головки, мкм; площадь головки, мкм2; периметр головки, мкм; расстояние между апикальной частью головки и ее основанием, мкм; угол наклона головки, градусы; ширина основания хвоста, мкм; длина хвоста, мкм; соотношение хвоста к головке;шероховатость;линейность,%.
Шероховатость рассчитывали с использованием формулы:
R=4πA/P2 , где R – шероховатость, A – площадь головки, мкм2, P – периметр головки, мкм.
Линейность рассчитывали с использованием формулы:
L=C/H*100, где L – линейность, C – расстояние между апикальной частью головки и ее основанием, мкм, H – длина головки, мкм.
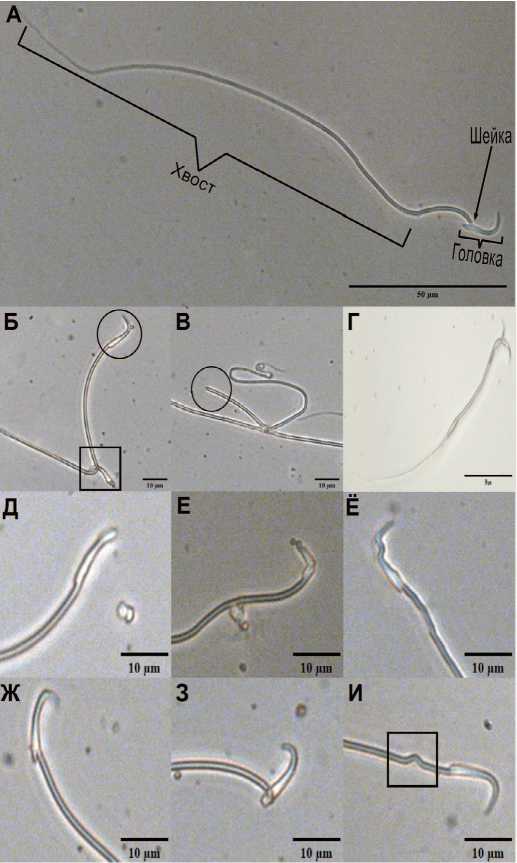
Рис. 1. Примеры дефектов сперматозоидов крыс. A – нормальный сперматозоид, Б – головка без хвоста и большой угол наклона головки, В – хвост без головки, Г – сперматозоид с двумя головками и дополнительными дефектами, Д – уплощенная головка, Е – булавочная головка, Ё – деформация головки, Ж – изогнутый угол наклона головки, З – патология шейки, И – изогнутый хвост. Без окрашивания, ув. х 400
Fig. 1. Examples of defects in rat spermatozoa. A – normal spermatozoon, Б – head without tail and large head tilt angle, В – tail without head, Г – two-headed spermatozoon with additional defects, Д – flattened head, Е – pinhead, Ё – head deformation, Ж – curved head tilt angle, З – neck pathology, И – curved tail. Unstained, magnification x 400
У каждой особи перечисленные параметры измеряли у 50 сперматозоидов. Всего было проанализировано 1650 сперматозоидов.
Концентрация тестостерона. Исследование концентрации тестостерона в сыворотке крови проводили с использованием автоматического иммунофермент-ного анализатора Lazurite (Dynex Technologies, США) и набора реагентов для количественного иммунофер-ментного определения общего тестостерона в сыворотке – Тестостерон-Имаксиз (IMAXIZ) (Vital Development, Россия).
Статистические методы. Все полученные данные были обработаны в программе GraphPad Prism 9.5.1. Показатели нативного эякулята и эпидидимисов при сравнении 2экспериментальных групп проанализированы с помощью непараметрического критерия Манна-Уитни, при сравнении 3 и более групп использовали непараметрический тест для независимых переменных Краскела-Уоллеса, а для точного определения отличий между каждой независимой группой проводили тест Данна для попарных сравнений с последующей коррекцией с помощью двухэтапного пошагового метода Бенджамини,Кригера и Екутиэли. Морфометрические параметры сперматозоидов при сравнении 2 экспериментальных групп анализировали с помощью параметрического t-критерия Уэлча, при сравнении 3 и более групп использовали однофакторный дисперсионный анализ (O ne-W ay ANOVA), для определения отличий между группами применяли апостериорный критерий Геймсу-Хоуэллу. Показатели нативного эякулята крыс до и после воздействия температуры сравнивали с помощью двухфакторного дисперсионного анализа Фридмана по рангам,а для попарных сравнений выборок применили критерий Вилкоксона для связанных повторных наблюдений. Различия считали значимыми при p<0,05. Данные в таблицах представлены, как М ± SE.
РЕЗУЛЬТАТЫ
При исследовании интактных крыс показаны различия эпидидимальных сперматозоидов и сперматозоидов нативного эякулята. Так, концентрация сперматозоидов в нативном эякуляте ниже, чем их концентрация в придатке. Снижаются также подвижность сперматозоидов и их способность к агглютинации. Наблюдается ряд различий в морфометрических параметрах. Нативные сперматозоиды имеют увеличенную головку, длину хвоста и шероховатость по сравнению с эпидидимальными сперматозоидами (табл. 1).
Многократное воздействие высокой температуры приводит к постепенному снижению всех параметров нативного эякулята в течение всего срока экспери-мента:концентрации и процента подвижных сперматозоидов, агглютинации, количества лецитиновых зерен. При этом в группе контроля параметры не из-меняются,что свидетельствует об изменении сперматозоидов именно под влиянием высокой температуры (табл. 2).
Снижаются и все параметры эпидидимальных сперматозоидов – концентрация, подвижность, агглютинация (агглютинация сперматозоидов у человека считается отрицательным показателем фертильности, но для крыс она играет важную роль в процессе оплодотворения),что свидетельствует о нарушении их созревания в придатках. Это подтверждается и увеличением количества клеток,имеющих самые разнообразные морфологические дефекты головки,
Таблица 1. Параметры сперматозоидов крыс интактной группы на разной стадии созревания Table 1. Sperm parameters of intact rats at different stages of maturation
б – отличия достоверны от соответствующего показателя придатка по t-критерию Уэлча ( p <0б05)
а – differences are significant compared to the corresponding parameter of epididymis according to the Mann-Whitney test ( p <0.05)
б – differences are significant compared to the corresponding parameter of epididymis according to Welch’s t-test ( p <0.05)
Таблица 2. Параметры нативного эякулята крыс при многократном воздействии высокой температуры на разные сроки эксперимента Table 2. Ejaculate parameters after repeated exposure to high temperature
в – отличия достоверны от соответствующего показателя группы 0 сут по двухфакторному дисперсионному анализу Фридмана по рангам с апостериорным множественным сравнением по критерию Вилкоксона ( p <0,05)
а – differences are significant compared to the corresponding parameter of the control group according to the Mann-Whitney test ( p <0.05);
в – differences are significant compared to the corresponding parameter of the 0 day group, based on to the two-way Friedman analysis of variance by ranks with post-hoc comparisons using the Wilcoxon test ( p <0.05)
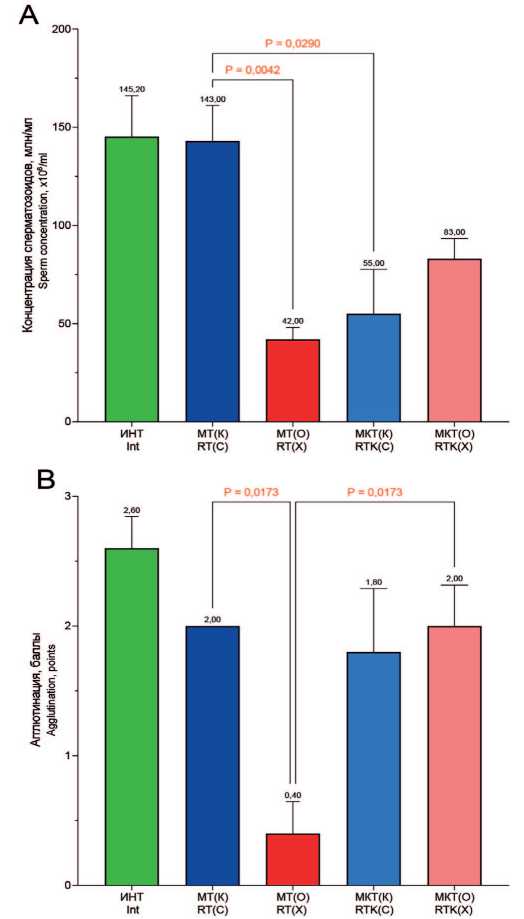
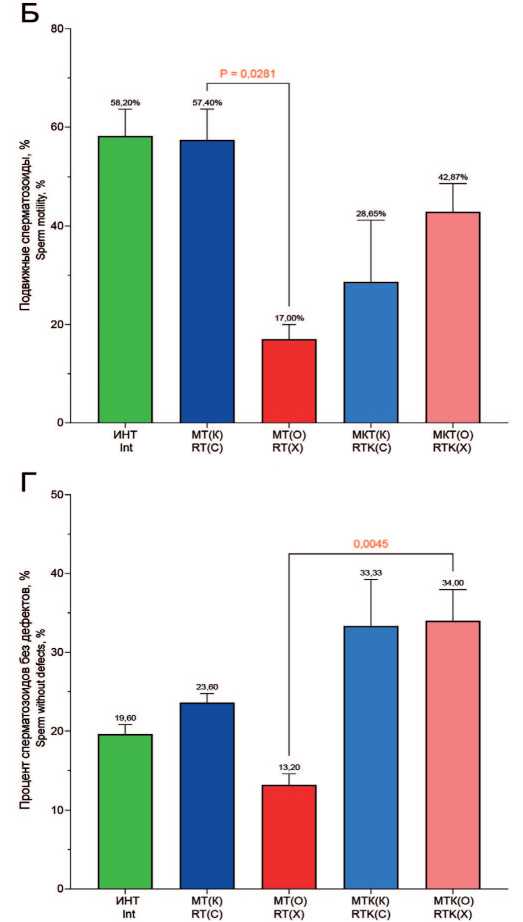
Рис. 2. Параметры эпидидимальных сперматозоидов крыс при многократном воздействии высокой температуры на фоне приема Кетотифена. Примечание: различия достоверны по критерию Краскела-Уоллеса с последующим анализом по критерию Данна и коррекцией по методу Бенджамини, Кригера и Екутиэли ( р <0,05)
Fig. 2. Epididymal sperm parameters of rats after repeated exposure to high temperature, with and without ketotifen intake. Note: differences are significant according to the Kruskal-Wallis test, followed by Dunn post-hoc test, with correction using the Benjamini, Krieger and Yekutieli method ( p <0,05)
шейки и хвоста (рис. 2). Многократное воздействие высокой температуры приводит к значительным изменениям морфометрических параметров сперматозоидов по сравнению с контрольной группой. Так, под действием температуры увеличиваются длина, пло-щадь,периметр головки,расстояние между верхней частью головки и ее основанием,ширина,основание и длина хвоста по сравнению с показателями контрольной группы (табл. 3).
Все описанные выше негативные изменения сперматозоидов на разных стадиях созревания под влиянием высокой температуры происходят на фоне сниженного уровня тестостерона в крови (рис. 3).
На фоне инактивации тучных клеток препаратом кетотифен отмечается сохранение практически всех параметров спермограммы на уровне контрольной группы При одновременном действии высокой температуры и препарата не отмечается снижение концентрации
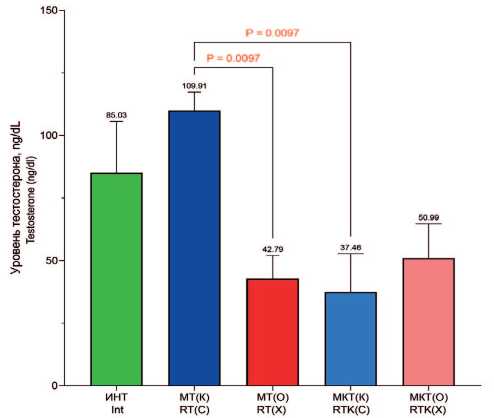
Рис. 3. Концентрация общего тестостерона в сыворотке крови крыс, нг / дл. Примечание: различия достоверны по критерию Краскела-Уоллеса с последующим анализом по критерию Данна и коррекцией по методу Бенджамини, Кригера и Екутиэли ( р <0,05)
Fig. 3. Total testosterone concentration in rat blood serum, ng/dl. Note: differences are significant according to the Kruskal-Wallis test, followed by Dunn post-hoc test, with correction using the Benjamini, Krieger and Yekutieli method ( p <0,05)
Таблица 3. Морфометрические параметры эпидидимальных сперматозоидов крыс при многократном воздействии высокой температуры на фоне приема Кетотифена
Table 3. Morphometric parameters of еpididymal sperm after repeated exposure to high temperature, with and without ketotifen intake
б – отличия достоверны от соответствующего показателя контрольной группы с приемом кетотифена по однофакторному дисперсионному анализу (One-Way ANOVA) с апостериорным множественным сравнением по критерию Геймсу-Хоуэллу ( p < 0,05)
в – отличия достоверны от соответствующего показателя опытной группы по однофакторному дисперсионному анализу (One-Way ANOVA) с апостериорным множественным сравнением по критерию Геймсу-Хоуэллу ( p < 0,05)
а – differences are significant compared to the corresponding parameter of the control group according to one-way ANOVA with post-hoc multiple comparisons using the Games-Howell criterion ( p <0.05)
б – differences are significant compared to the corresponding parameter of the control group receiving Ketotifen according to one-way ANOVA with post-hoc multiple comparisons using the Games-Howell criterion ( p <0.05)
в – differences are significant compared to the corresponding parameter of the experimental group according to one-way ANOVA with post-hoc multiple comparisons using the Games-Howell criterion ( p <0.05)
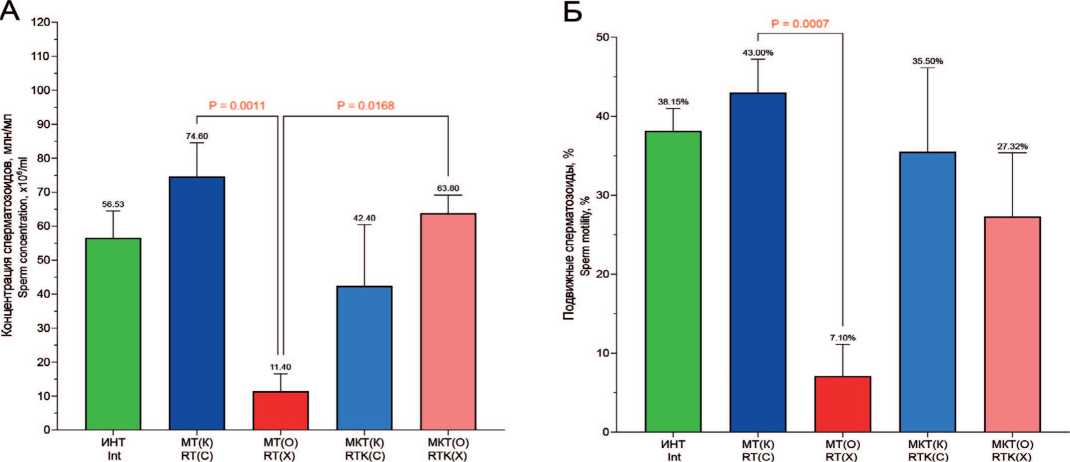
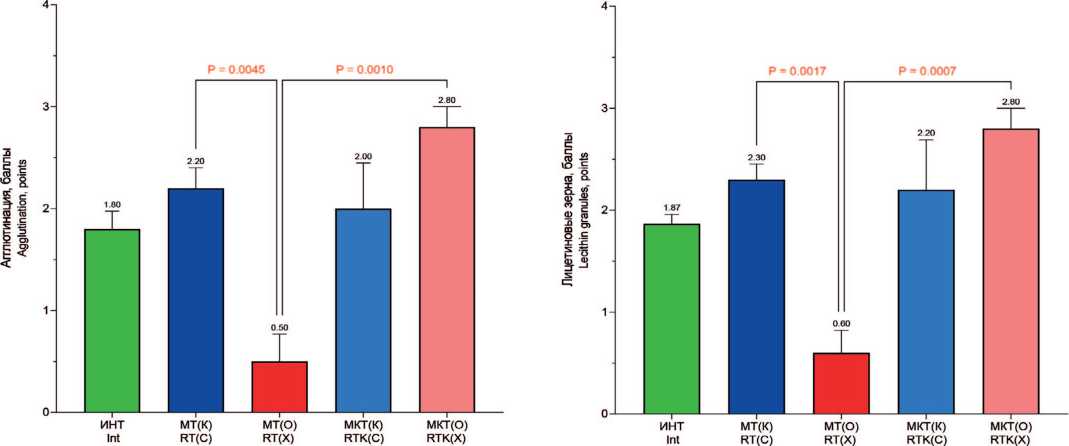
Рис. 4. Параметры нативного эякулята крыс при многократном воздействии высокой температуры на фоне приема Кетотифена. Примечание: различия достоверны по критерию Краскела-Уоллеса с последующим анализом по критерию Данна и коррекцией по методу Бенджамини, Кригера и Екутиэли ( р <0,05)
Fig. 4. Ejaculate parameters of rats after repeated exposure to high temperature, with and without ketotifen intake. Note: differences are significant according to the Kruskal-Wallis test, followed by Dunn post-hoc test, with correction using the Benjamini, Krieger and Yekutieli method ( p < 0.05)
сперматозоидов, их агглютинации, количества лецитиновых зерен. Процент подвижных сперматозоидов достоверно не изменяется, но отмечается положительная тенденция на его сохранение (рис. 4Б).
Применение препарата положительно влияет и на параметры сперматозоидов из придатка. Так, по сравнению с опытной группой не происходит снижения концентрации и агглютинации сперматозоидов Клетки сохраняют свою подвижность (рис. 2Б). Отмечаются изменения морфометрических параметров эпидидимальных сперматозоидов: уменьшается площадь головки,угол ее наклона,ширина хвоста,соот-ношение хвоста к головке и шероховатость по сравнению с опытной группы без приема препарата При этом длина хвоста остается без изменений.
Применение препарата без теплового воздействия также вызывает ряд изменений в сперматозоидах. Под воздействием препарата кетотифен наблюдается увеличение длины, ширины, периметра головки, расстояния между верхней частью головки и ее основанием, длины хвоста и линейности по сравнению с контрольной группой, не получавшей препарат. Также отмечается уменьшение угла наклона, ширины основания хвоста и шероховатости (табл. 3). Концентрация тестостерона в крови снижается в группе животных, принимавших препарат (рис. 3).
ОБСУЖДЕНИЕ
Половое созревание самцов крыс наступает через 40–60 суток после рождения [15, 16]. В эксперименте использованы крысы возрастом 4 месяца с полностью сформированной репродуктивной системой. Образование сперматозоидов у крыс,как и у большинства млекопитающих,происходит в извитых семенных канальцах яичка,расположенного в мошонке.Сформи-рованные сперматозоиды крыс имеют четкое разделение на части: головка (в форме крючка), шейка и хвост (рис. 1А), выделяются в просвет семенных канальцев и транспортируются до придатка яичка для дальнейшего созревания.
Показано, что концентрация эпидидимальных сперматозоидов выше концентрации сперматозоидов в нативном эякуляте. Это объясняется аккумуляцией сперматозоидов в придатке,поступающих из семенных канальцев.Далее эти клетки смешиваются с секретом добавочных желез, что и приводит к уменьшению их концентрации.В нативном эякуляте снижаются также подвижность сперматозоидов и их способность к агглютинации, что свидетельствует о функциональных изменениях сперматозоидов по мере их продвижения от головки придатка до хвоста.
Изменяются и все морфологические параметры сперматозоидов,в частности увеличивается площадь головки у сперматозоидов нативного эякулята. Это связано с процессом созревания сперматозоидов у млекопитающих, где клетки, хранящиеся в хвосте придатка яичка,имеют более развитые акросомы,чем сперматозоиды из головки придатка [17]. Модификации длины хвоста,шейки и угла наклона головки связаны с улучшением подвижности сперматозоидов. Это подтверждает и то, что созревание сперматозоидов происходит на протяжении всего пути по семявыносящим протокам и за их пределами (в половых путях самки).
Таким образом, эпидидимальные сперматозоиды из головки придатка крыс отличаются от сперматозоидов нативного эякулята по ряду морфофункциональных характеристик. Это подтверждают и подобные исследования,проведенные на других видах животных [18, 19]. Несмотря на то, что эпидидимальные сперматозоиды морфологически схожи со сперматозоидами эякулята и обладают большей подвижностью, они не способны к самостоятельному преодолению биологических и физиологических факторов в половых путях самки с последующим оплодотворением яйцеклетки, хоть и способны к оплодотворению in vitro [20].
Морфометрические показатели сперматозоидов интактных крыс неоднократно определяли разные группы исследователей. Например, группа ученых G. van der Horst с соавторами с помощью компьютерного анализа морфологии сперматозоидов (CASMA) крыс измерила ряд параметров и предложила их в качестве референтных значений [21]. Однако некоторые параметры морфометрического анализа сперматозоидов с использованием ImageJ, полученные в ходе дан- ного эксперимента, отличаются от их результатов Скорее всего, это связано с различными методами оценки,а также с возрастом,количеством животных в экспериментах и достаточно большим диапазоном нормальных значений морфометрических показателей сперматозоидов,что необходимо учитывать при проведении дальнейших исследований.
Действие высокой температуры сроком равным полному циклу сперматогенеза негативно влияет на сперматозоиды разных стадий созревания. Так, уменьшение концентрации сперматозоидов в нативном эякуляте происходит в результате структурных и функциональных изменений в клетках не только на стадии размножения сперматогоний,но и на других стадиях сперматогенеза.Это подтверждают авторы статьи, которые показали, что наиболее уязвимыми к тепловому повреждению у крыс являются сперматоциты и ранние округлые сперматиды.Снижение агглютинации и подвижности сперматозоидов свидетельствует о влиянии повышенной температуры не только на первые этапы сперматогенеза, но и на созревание сперматозоидов в эпидидимисах. Таким образом, повышение температуры влияет и на уже сформировавшиеся сперматозоиды, в результате чего может наблюдаться значительное снижение фертильности у самцов крыс.Длительное воздействие высоких температур может вызывать запуск усиленного апоптоза активно делящихся клеток под действием окислительного стресса,нарушения репарации ДНК и усиленную денатурацию белков [22].
Уменьшение содержания лецитиновых зерен в нативном эякуляте под действием высокой температуры свидетельствует о нарушении биохимических процессов, протекающих в добавочных железах, при этом изменяется состав их секретов,что в свою очередь может приводить к ухудшению не только показателей спермограммы, но и свойств эякулята в целом [23]. Изменение этих свойств значительно снижает устойчивость сперматозоидов в половых путях самки, что в разы снижает их фертильную способность. К тому же уменьшение лецитиновых зерен указывает на ухудшение липидного обмена,что приводит к дефициту выработки тестостерона необходимого для поддержания сперматогенеза (рис. 3).
Под воздействием высокой температуры изменяются практически все морфометрические показатели сперматозоидов. Увеличение размеров головки сперматозоидов у опытной группы может указывать на неполное формирование ее структуры,связанное с недостаточно плотной укладкой хроматина, что в итоге приводит к неполноценному оплодотворению, которое чаще всего сопровождается анеуплоидиями или вовсе отсутствием оплодотворения [24]. Изменение структуры основания хвоста может существенно снижать его способность к передвижению [25].
В качестве инактивирующего агента для тучных клеток был использован препарат кетотифен,который показал высокую эффективность как в наших предыдущих исследованиях [26], так и в исследованиях других ученых [10, 11]. Ранее нами было показано снижение функциональной активности тестикулярных тучных клеток под действием данного препарата.На-стоящее исследование демонстрирует положительное влияние инактивации тучных клеток на показатели как нативного эякулята,так и эпидидимальных сперматозоидов при нарушении сперматогенеза под действием высокой температуры. При воздействии препарата не отмечается снижение показателей спермо-граммы, что свидетельствует о сохранении оплодотворяющей способности сперматозоидов.
Изменения ряда морфометрических параметров также свидетельствуют о положительном эффекте инактивации тучных клеток. Уменьшение площади и угла головки указывает на правильное формирование ее структуры. Значение ширины основания хвоста, приближающееся к значениям интактной и контрольной групп, может указывать на улучшение подвижности сперматозоида. Восстановление соотношения хвост/головка и параметров шероховатости указывает на положительный эффект кетотифена в защите от теплового стресса. Однако некоторые параметры, такие как периметр головки,линейность и определен- ные характеристики хвоста сперматозоида,показали минимальное улучшение или его отсутствие.
В группе,получавшей кетотифен без воздействия высокой температуры, наблюдались некоторые потенциально негативные эффекты препарата, такие как снижение уровня тестостерона и концентрации сперматозоидов, увеличение длины хвоста. Это свидетельствует о неблагоприятном влиянии инактивации тучных клеток на сперматогенез в норме и об их необходимом участии в регуляции этого процесса.
ЗАКЛЮЧЕНИЕ
Длительное воздействие высоких температур приводит к ухудшению морфофункциональных характеристик сперматозоидов. Резкое снижение параметров спермограммы у особей, которых подвергали ежедневному нагреву в течение полного цикла сперма-тогенеза,подтверждает предположение о нарушениях развития клеток еще на стадии сперматогоний. Все это приводит к торможению сперматогенеза и,как следствие, к плавному, но значительному снижению фер-тильности.Инактивация тучных клеток препаратом кетотифен нивелирует негативные последствия влияния высокой температуры на сперматогенез, сохраняя большинство параметров нативного эякулята и сперматозоидов придатка.
ПТШТУРАШШПШ


