Индуцированный рак молочной железы у мужчины с первично-множественными злокачественными новообразованиями (клинический пример)
Автор: Каприн А.Д., Зикиряходжаев А.Д., Тыщенко Е.В., Сухотько А.С.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Случай из клинической практики
Статья в выпуске: 5 (65), 2014 года.
Бесплатный доступ
Представленное клиническое наблюдение полинеоплазии у мужчины с индуцированным раком молочной железы демонстрирует современные возможности лекарственной терапии первично-множественных злокачественных новообразований. Ключевые слова: ПМЗО, рак молочной железы у мужчин, лекарственная терапия.
Короткий адрес: https://sciup.org/14056467
IDR: 14056467 | УДК: 618.19-006.6-055.1
Induced breast cancer in a man with multiple primary cancer (a case report)
A case report of polyneoplasia in a male patient with induced breast cancer demonstrates current trends in drug therapy for multiple primary cancers. Key words: multiple primary cancers, breast cancer, drug therapy.
Текст научной статьи Индуцированный рак молочной железы у мужчины с первично-множественными злокачественными новообразованиями (клинический пример)
В настоящее время, по мере накопления наблюдений, предпринимаются попытки выяснить истинную частоту множественных опухолей. По данным литературы, за последние годы показатель роста первично множественных опухолей (ПМО) увеличился почти в 10 раз, частота их возникновения возросла до 13 % от общего числа впервые взятых на учет онкологических больных [10]. Только за последние 30 лет во всем мире описано несколько десятков тысяч наблюдений ПМО, что связано с улучшением диагностики, лечения, увеличением продолжительности жизни, увеличением числа больных с данной патологией [8, 11]. В России показатель заболеваемости первичномножественными злокачественными новообразованиями в 2005 г. равнялся 8,3, в 2010 г. – 11,2 на 100 тыс. населения [7].
Интерес к изучению полинеоплазий возрастал по мере накопления клинических наблюдений и экспериментальных исследований, позволяющих определить особенности развития и течения злокачественных новообразований. Первым до- кументированным наблюдением ПМО является описание Абу Али Ибн Синой (Авиценна) случая двустороннего поражения молочных желез. В России первые наблюдения ПМО данной области принадлежат А.А. Серебрякову (1849). В разное время этой проблемой занимались Г.Г. Непряхин (1926), Д.М. Абдурасулов (1977, 1982), А.В. Важенин (2000) [1, 2, 6].
Т. Бильрот в 1869 г. дал определение ПМО, в котором были следующие критерии [3]:
-
1) опухоли должны располагаться в разных органах;
-
2) должны иметь различную морфологическую структуру;
-
3) каждая опухоль должна давать собственные метастазы.
Это определение долгое время считалось классическим, но впоследствии оно было пересмотрено. В настоящее время большинство авторов придерживаются определения, предложенного S. Warren, O. Gates (1932) и впоследствии подтвержденного Н.Н. Петровым (1947). Считается, что обязательным
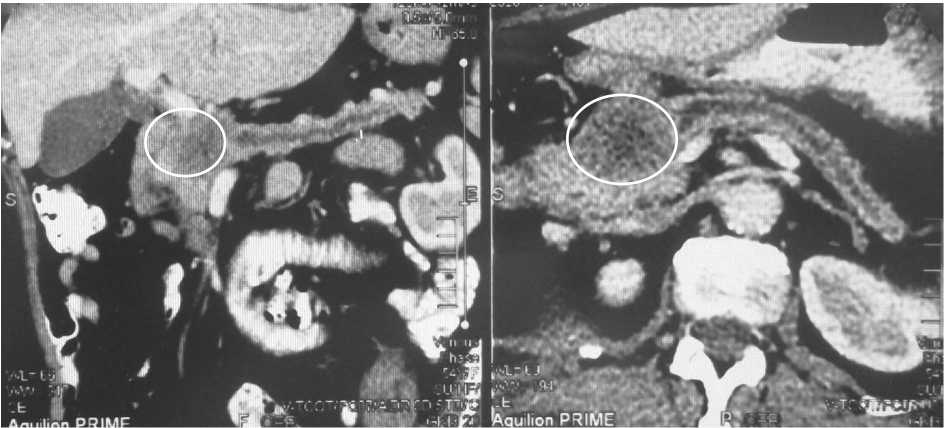
Рис. 1. КТ органов брюшной полости. Образование в головке поджелудочной железы размером 6,5×5 см
критерием для ПМО является то, чтобы эти опухоли не были ни метастатическими, занесенными по току лимфы, крови или по серозным полостям, ни отпечатками, развившимися от соприкосновения, т.е. должна быть доказанная их первичность, а не метастатическое происхождение [9].
Наиболее часто в практике наблюдается сочетание двух опухолей. Случаи тройной локализации опухолей встречаются в 5–8 % наблюдений. Наличие у одного больного четырех, пяти, шести и более опухолей встречается очень редко. Полинеоплазии чаще всего развиваются у лиц старше 50 лет, причем у мужчин в более пожилом, чем у женщин, в возрасте. Преобладание среди больных с ПМО лиц пожилого возраста, возможно, является следствием более благоприятного течения злокачественных опухолей в этой возрастной группе [5, 10, 12]. Особое место у мужчин с полинеоплазиями занимает первичный рак молочной железы (РМЖ), индуцированный эстрогенной терапией и лучевой терапией [4, 13].
Приводим следующее клиническое наблюдение.
Пациент Б., 83 лет. Диагноз: Первичномножественный метахронный синхронный рак: 1) Рак поджелудочной железы IV ст. (Т3NхМ1) c прорастанием в 12-перстную кишку, метастазами в забрюшинные лимфатические узлы. Состояние после полихимиотерапии (ПХТ) в 2007–2008 гг. (5 курсов по схеме гемзар + фторурацил + лейковорин). Прогрессирование процесса. Состояние после 3 курсов ПХТ по схеме оксатера в дозе 150 мг + ксе-лода в 2008–2009 гг. В настоящий момент полная регрессия. 2) Рак предстательной железы Т2сNхМх.
Состояние в процессе гормональной терапии (флутамид, золадекс). Стабилизация. 3) Рак левой молочной железы слева I ст. (Т1N0М0). Состояние после курса лучевой терапии на молочную железу, СОД 51 Гр, на над-, подключично-подмышечное поле слева, СОД 51 Гр в 2013 г. Прогрессирование процесса: внутрикожные метастазы в левой молочной железе.
Сопутствующая патология: Сахарный диабет II типа, ангиопатия нижних конечностей. ИБС, постинфарктный кардиосклероз. Артериальная гипертензия III ст. Системный остеопороз. Аутоиммунный тиреоидит. Эрозивный гастродуоденит. Хронический панкреатит.
Из анамнеза: пациент в течение 47 лет работал рентгенологом. В январе 2007 г. при КТ брюшной полости в проекции поджелудочной железы было выявлено объемное образование неправильной формы, размерами 3×2,9 см. При контрольном обследовании, в ноябре 2007 г., отмечена отрицательная динамика в виде увеличения образования в головке поджелудочной железы до 6,5×5 см, выраженная инфильтрация парапанкреатической клетчатки, сужение просвета и деформация двенадцатиперстной кишки (рис. 1). Тело и хвост поджелудочной железы без особенностей. В проекции правой доли печени (S7) подкапсулярно определялся участок сниженной плотности неправильной формы. Была выполнена ЭГДС с биопсией. Гистологическое заключение: аденокарцинома преимущественно высокой степени дифференцировки. По данным эндоскопической ультросонографии панкреатобилиарной зоны: на уровне луковицы и верхней трети горизонтальной ветви 12-перстной кишки стенки утолщены преимущественно за счет эпителиального компонента, просвет сужен. В луковице ДПК образование представлено только внутрипросветной частью, в верхней трети вертикальной ветви – с прорастанием в головку поджелудочной железы. В проекции головки поджелудочной железы определялись компрессия и объемное образование, распространяющееся из луковицы 12-перстной кишки. Тактика лечения обсуждена на консилиуме с участием хирургов, химиотерапевтов и радиологов. Учитывая распространенность процесса, была рекомендована химиотерапия препаратами гемзар, 5-фторурацил, лейковорин. В период с 24.01.2008 по 28.01.2008 проведен 1-й курс ПХТ, который осложнился аллергической реакцией на нижних конечностях. Тактика лечения повторно обсуждена на консилиуме, рекомендована смена схемы химиотерапии, с 27.03.2008 по 30.10.2008 проведено 5 курсов по схеме оксатера – 150 мг, кселода – 3 г, в 1–14-й дни. При контрольном обследовании 15.11.2008: по данным УЗИ брюшной полости имеются диффузные изменения печени, поджелудочной железы, головка железы не визуализируется. Гиперплазия простаты. Уровень ПСА: свободный – 4,24 нг/мл (N – 0–1,0), общий – 46,40 нг/мл (N –0–4,0). Клинически по периферии левой доли предстательной железы – участок хрящевой плотности, размерами 2,5×1,0 см. 17.12.2008 выполнена трансректальная сектантная биопсия простаты под УЗИ-контролем. Гистологическое заключение: аденокарцинома предстательной железы 8 баллов по Глиссону (4 + 4). Рекомендована антиандрогенная терапия препаратами: флутамид, золадекс. Через 2 мес при контрольном обследовании: по данным ЭГДС луковица 12-перстной кишки не деформирована, слизистая рыхлая, тусклая, с изменениями по типу «манной крупы». Органических изменений со стороны слизистой ДПК не выявлено. По данным КТ брюшной полости в перешейке поджелудочной железы определялось объемное образование размерами до 25 мм. Тактика лечения обсуждена на консилиуме, учитывая стабилизацию процесса в предстательной железе и прогрессирование в поджелудочной железе, рекомендована химиотерапия. С 22.04.2009 по 09.06.2009 проведено 2 курса химиотерапии по схеме гемзар + фторурацил + лейковорин. При контрольном обследовании выявлена отрицательная динамика в виде увеличения размеров опухоли панкреатодуоденальной области с 25 до 36 мм. С 25.06.2009 по 08.07.2009 проведено 3 курса химиотерапии по схеме оксатера – 150 мг + кселода. Полная регрессия, больной оставлен под динамическое наблюдение.
В феврале 2011 г. пациент самостоятельно обнаружил образование в левой молочной железе, обратился в городскую клиническую больницу. При обследовании в центральном квадранте левой молочной железы имелось узловое образование с неровными нечеткими контурами, диаметром 1,5×1 см (морфологическое заключение утеряно). Установлен диагноз: рак левой молочной железы I ст. (Т1N0М0).
Тактика лечения была обсуждена на консилиуме с участием хирургов, химиотерапевтов и радиологов. Учитывая начальную стадию заболевания и сопутствующую патологию, принято решение о проведении дистанционной лучевой терапии на молочную железу и регионарные зоны. С 10.05.2011 по 10.06.2011 проведена лучевая терапия на молочную железу, СОД 51 Гр, на над-, подключично-подмышечную зоны слева, СОД 51 Гр. При контрольном обследовании диагностирована регрессия образования в левой молочной железе, стабилизация по предстательной железе и поджелудочной железе.
В апреле 2013 г. больной самостоятельно прекратил прием препаратов флутамид и зо-ладекс. В августе 2013 г. отметил ухудшение мочеиспускания и появление мелких узловых образований на коже левой молочной железы. Для обследования самостоятельно обратился в МНИОИ им. П.А. Герцена, при котором диагностировано прогрессирование заболевания левой молочной железы в виде кожных сателлитов (рис. 2), узловые образования в ткани левой молочной железы не определяются. При исследовании поджелудочной железы: в ее головке имеется зона фиброзно-измененных тканей, данных за наличие опухолевого роста нет. При исследовании предстательной железы обнаружены явления выраженного фиброза без четких признаков наличия опухоли.
Выполнена открытая биопсия внутрикожного образования левой молочной железы. Гистологическое заключение: в дерме инфильтративный рост низкодифференцированной аденокарциномы. Иммуногистохимическое исследование: реакция с рецепторами эстрогенов – положительная (8 бал-
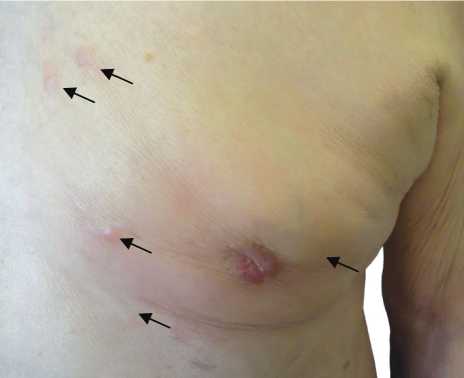
Рис. 2. Внутрикожные метастазы рака молочной железы слева (сателлиты)
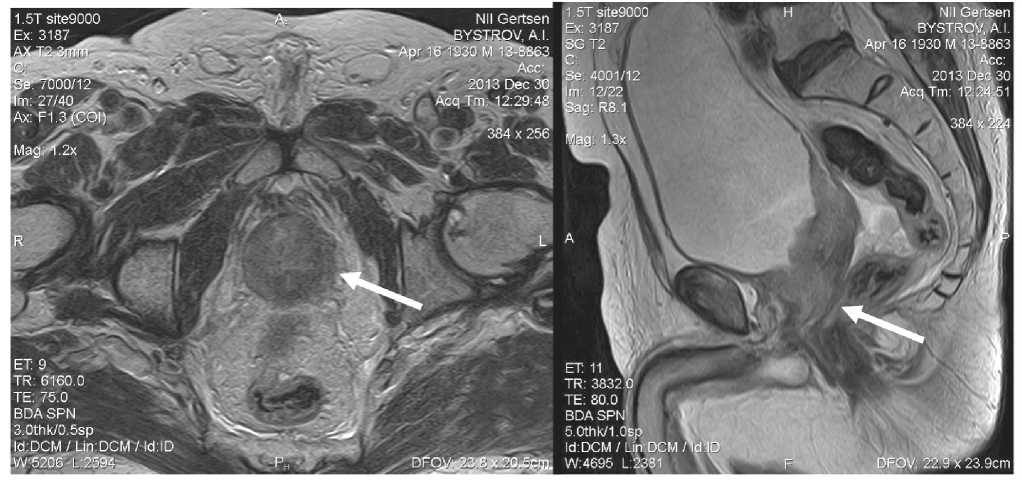
Рис. 3. МРТ органов малого таза. Опухоль предстательной железы
лов), реакция с рецепторами прогестерона – отрицательная, реакция с HER2/neu – отрицательная, экспрессия Ki67 – положительная в 5 % клеток. Тактика лечения обсуждена на консилиуме с участием хирургов, онкоурологов, химиотерапевтов и радиологов. Учитывая анамнез, сопутствующую патологию, рекомендовано продолжить гормонотерапию ингибиторами ароматазы, золадексом и абиротерон ацетатом.
В ноябре 2013 г. у больного на фоне гормональной терапии в режиме МАБ отмечается рост уровня ПСА до 40 нг/мл. Больной принимал препараты бикалутамид, флутамид в различных дозах без положительного эффекта. По данным УЗИ (15.11.2013): при исследовании шеи с обеих сторон очаговых образований не выявлено. В левой подмы- шечной области мелкое гипоэхогенное образование размерами до 4×4,5 мм. На грудной клетке слева визуализируются внутрикожные гипоэхогенные очаги диаметром до 5 мм. В надключичных, подключичных, правой подмышечной, парастернальных областях очаговых образований не выявлено. В августе 2013 г. пациенту рекомендована терапия тутабином, который был отменен из-за развития токсических реакций, задержки мочеиспускания. Была рекомендована гормонотерапия тамоксифеном либо анастразолом, которую пациент не получал. За последние 2 мес больной отмечает появление новых внутрикожных метастазов в области левой грудной железы. Учитывая возраст больного, выраженную сопутствующую патологию, увеличение уровня ПСА на фоне проводимой гормонотерапии, появление новых внутрикожных метастазов в области левой грудной железы, хирургическое лечение не показано, рекомендовано лекарственное лечение: октреотид депо 20 мг внутримышечно, 1 раз в 28 дней, гормональная терапия аналогами ЛГРГ длительно, ингибиторы ароматазы (аримидекс 1 мг/сут).
При контрольном комплексном обследовании 26.12.2013 по данным сканирования костей скелета выявлены множественные метастатические очаги; при МРТ (30.12.13): данные за рак предстательной железы с распространением на устья семенных пузырьков. Нельзя исключить начальную инвазию в парапростатическую клетчатку с вовлечением задней стенки мочевого пузыря. Определяются единичные лимфоузлы в малом тазу (рис. 3). При контроле ПСА (04.03.14): увеличение маркера уровня до 114,2 нг/мл. Учитывая прогрессирование рака предстательной железы на фоне проводимой терапии, показана терапия препаратом зитига (абиратерон) 1000 мг/сут и бисфосфонатами (бондронат – 50 мг/сут, per os).
Заключение
Самым распространенным вариантом РМЖ у мужчин является протоковый рак, при котором экспрессия ER и PR выявляется в 91 и 76 % наблюдений соответственно, что превышает данные показатели при раке молочной железы у женщин. В приведенном клиническом случае наблюдается индуцированный гормонотерапией и лучевой терапией первичный рак молочной железы у мужчины преклонного возраста. Гормональная терапия в лечении ПМО у мужчин, больных раком предстательной железы в сочетании с раком молочной железы, показала хороший результат. С момента первого обращения данного пациента прошло 7 лет, он социально активен.


