Индукция и репарация двунитевых разрывов ДНК в клетках линии V79 при длительном воздействии низкоинтенсивного Y-излучения
Автор: Озеров И.В., Бушманов А.Ю., Анчишкина Н.А., Гурьев Д.В., Пустовалова М.В., Сметанина Н.М., Архангельская Е.Ю., Воробьева Н.Ю., Осипов А.Н.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Генетика
Статья в выпуске: 4 т.9, 2013 года.
Бесплатный доступ
Цель: изучить закономерности изменений количества двунитевых разрывов (ДР) ДНК в клетках млекопитающих при длительном воздействии низкоинтенсивного у-излучения. Материал и методы. В работе использовали культуру фибробластов легкого китайского хомячка (линия V79). Облучение клеток у-лучами при мощности дозы 0,1 мГр/мин проводили на установке «Гамма-Панорама» (Cs-137). Для оценки изменений количества ДР ДНК использовали иммунофлуоресцентный анализ фокусов фосфорилированного гистона Н2АХ (у-Н2АХ). Частоту апоптотических клеток определяли методом «ДНК-гало». Для анализа продукции активных форм кислорода (АФК) использовали 5 (6) — хлорметил-2,7-дихлордигидрофлуоресцеиндиацетат. Результаты. Продемонстрировано, что при длительном низкоинтенсивном облучении клеток линии V79 в ранние сроки облучения (6-24 ч, дозы 3,6-14,4 сГр) наблюдается увеличение количества фокусов у-Н2АХ и продукции АФК, а в более поздние сроки (48-72 ч, дозы 28,8-43,2 сГр) снижение этих показателей практически до контрольного уровня. Статистически достоверных изменений доли апоптотических клеток при этом обнаружено не было. Заключение. Процессы, обусловливающие изменения количества ДР ДНК в клетках млекопитающих при длительном воздействии низкоинтенсивного у-излучения, по всей видимости, сопряжены с развитием оксидативного стресса и последующей активизацией антиоксидантных защитных систем клеток.
V-излучение, активные формы кислорода, апоптоз, двунитевые разрывы днк, клетки v79, низкая мощность дозы, фокусы v-h2ax
Короткий адрес: https://sciup.org/14917841
IDR: 14917841 | УДК: 577.2.043:539.1
Induction and reparation of double-strand DNA breaks in V79 cells continuously exposed to low dose-rate Y-radiation
Aim: to study the patterns of changes in the number of DNA double-strand breaks (DSB) in mammalian cells continuously exposed to low dose-rate y- radiation. Material and methods. Chinese hamster lung fibroblasts (V79) were used in this study. The y- irradiation of cells at a dose rate of 0.1 mGy/min was performed using the «Gamma-Panorama» unit (Cs-137). The fluorescence immunoassay of the phosphorylated H2AX-histone (y-H2AX) foci was used to investigate the DNA DSBs formation. Frequency of apoptotic cells was evaluated using «DNA halo» assay. 5 (6) — chloromethyl-2,7-dichlorodihydrofluorescein diacetate was used to estimate the reactive oxygen species (ROS) production. Results, it was showed that continuous low dose-rate irradiation of Chinese hamster V79 cells induces an increase of the y-H2AX foci number and ROS production rate at the early stages of exposure time (6-24 h, doses 3.6-14.4 cGy), while increasing exposition time and, therefore, the radiation dose (48-72 h, 28.8-43.2 cGy) caused a decrease in these endpoints to almost the control level. There was observed no significant changes in the frequency of apoptotic cells. Conclusion. It is assumed that the processes causing the DSB amount changes in mammalian cells continuously exposed to low dose-rate y-radiation are associated with the development of oxidative stress and subsequent activation of cellular antioxidant defense systems.
Текст научной статьи Индукция и репарация двунитевых разрывов ДНК в клетках линии V79 при длительном воздействии низкоинтенсивного Y-излучения
-
1 Введение. Большая часть повреждений, возникающих в ДНК клеток после воздействия ионизирующего излучения (ИИ), существенно отличается по своей химической природе от эндогенных повреждений [1]. Важнейшей характеристикой радиационно-индуцированных повреждений ДНК является их сложность и кластеризация [2]. Среди повреждений ДНК, вызываемых ИИ, двунитевые разрывы (ДР) ДНК являются наиболее критическими для дальнейшей
Ответственный автор — Осипов Андреян Николаевич Адрес: 123182, г. Москва, ул. Живописная, 46.
Тел: +79154373245.
судьбы клетки. Предполагается, что именно ДР являются основным триггером, запускающим процессы клеточного отклика на воздействие ионизирующего излучения [3]. Репарация ДР происходит довольно медленно, в то время как ДР, не устраненные в ходе репарации ДНК, приводят к серьезным цитогенетическим нарушениям, гибели клеток, инактивации генов супрессоров опухолей или активации онкогенов [4]. Основные закономерности индукции и репарации ДР довольно хорошо изучены при остром, кратковременном воздействии ИИ в различных дозах [5]. Однако в реальных условиях живые организмы, как правило, подвергаются не острому, а длительному / хроническому воздействию ИИ. К сожалению, существующие в настоящее время экспериментальные данные об особенностях изменения количества ДР в клетках млекопитающих при длительном / хроническом воздействии ИИ немногочисленны и крайне противоречивы [6].
Цель работы : изучение закономерностей изменений количества ДР ДНК в клетках китайского хомяка линии V79 при длительном воздействии низкоинтенсивного γ-излучения.
Материал и методы. В работе использовали культуру фибробластов легкого китайского хомячка (линия V79). Клетки обладают довольно высокой адгезивной способностью к лабораторному пластику. Клетки культивировали в стандартной полной среде DMEM, содержащей 10% фетальной телячьей сыворотки, 1 % L-глютамина и антибиотики (пенициллин и стрептомицин) в условиях стандартного СО2-инкубатора при 37°C в атмосфере с 5%-м содержанием CO2.
Облучение клеток при мощности дозы 0,1 мГр/мин проводили на специально переоборудованной для облучения культур клеток облучательной установке «Гамма-Панорама» (источник γ-излучения Сs-137).
Для анализа фокусов γ-Н2АХ использовали методику, описанную в работе [7]. Коротко: клетки на покровных стеклах фиксировали параформальдегидом (2% в трис-буфере, рН 7,4), промывали трис-буфером, пермеабилизировали холодным (–20°С) метанолом в течение 1 мин и помещали на 20 мин в трис-буфер, содержащий 4% фетальной телячьей сыворотки и 0,1 % Тритон-Х100. Слайды инкубировали с моноклональными антителами к белку γ-Н2АХ (Anti-phospho-Histone H2A.X Rabbit Monoclonal, Merck-Millipore) при 4°С в течение ночи, после чего промывали и инкубировали со вторичными антителами, конъюгированными с флуорохромом (Goat anti-Rabbit IgG (H+L), FITC conjugate, Merck-Millipore), при комнатной температуре в течение 1 ч ДНК окрашивали флуоресцентным красителем DAPI (0,5 мкг/мл, 5 мин). Визуализацию, документирование и обработку иммунноцитохимических микроизображений осуществляли на люминесцентном микроскопе Ахioscop-40 FL (СаrlZeiss), оснащенным видеокамерой высокого разрешения АxioCamMRс 5 (CarlZeiss) с помощью программы AxioVision 4.8 (CarlZeiss). Подчитывали не менее 100 клеток на точку.
Частоту апоптотических клеток определяли методом «ДНК-гало» [8]. Принцип метода состоит в том, что низкомолекулярные фрагменты ДНК, образующиеся в процессе апоптотической межнуклеосомной деградации ДНК, легко диффундируют в гель агарозы, образуя характерное «гало» вокруг ядерной области клетки. Коротко: 10 мкл суспензии клеток (1 млн клеток/мл) смешивали со 100 мкл 0,5%-го раствора легкоплавкой агарозы (тип IV) в фосфатно-солевом буфере при температуре 37ºC и наносили на предварительно покрытые 1 %-м слоем нормоплавкой агарозы предметные стекла. Лизис клеток проводили в холодном (4°С) лизирующем буфере (2,5 M NaCl, 100 мМ EDTA, 20 мМ Tris-HCl, pH 10,0, 1 % Triton X-100) в течение 2 ч. После окраски слайдов флуоресцентным красителем SYBR Green I (Invitrogen) анализ уровня клеточной гибели осуществляли на люминесцентном микроскопе Ахioscop-40 FL (Саrl Zeiss), оснащенном видеокамерой высокого разрешения АxioCam MRс 5 (Carl Zeiss).
Для анализа продукции активных форм кислорода (АФК) в клетках использовали краситель
5(6)-хлорметил-2,7-дихлордигидрофлуоресцеиндиа цетат (Invitrogen), считающийся маркером внутриклеточных АФК [9]. Этот препарат легко проникает через клеточную мембрану, в клетке гидролизуется эстеразами и далее окисляется до флуоресцирующего соединения. Суспензию клеток (1 млн/мл) в фосфатносолевом буфере (рН 7,4) инкубировали с препаратом в течение 60 мин. Измерения интенсивности флуоресценции проводили на флуориметре с длиной волны возбуждения 488 нм и эмиссией 525–530 нм.
Статистическую обработку результатов всех измерений проводили с помощью программы Statistica 7.0. Результаты представлены как среднее трех независимых экспериментов ± стандартная ошибка. Для оценки достоверности отличий использовали t-критерий Стьюдента.
Результаты. Для оценки изменений количества ДР ДНК использовали иммунофлуоресцентный анализ фокусов фосфорилированного корового гистона Н2АX (γ-Н2АХ). Фосфорилирование Н2АХ осуществляется киназами АТМ, АТR и DNA-PK в ответ на образование ДР и свидетельствует о его распознавании [10]. При этом образуются динамические микроструктуры, содержащие тысячи копий γ-Н2АХ, получивших в литературе название «фокусы γ-Н2АХ» [11]. Полагают, что один фокус γ-Н2АХ соответствует одному ДР ДНК [12]. Ранее нами было показано, что через 30 мин после острого облучения количество фокусов γ-Н2АХ в клетках линии V79 линейно зависит от дозы облучения [7].
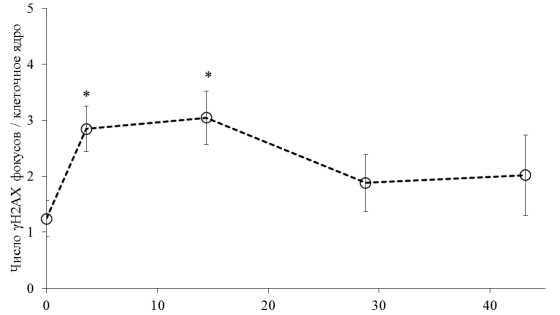
Предполагается, что «пороговой» дозой для индукции репарации ДР является доза в несколько сГр [13]. В связи с этим нами проведены исследования динамики изменений количества фокусов γ-Н2АХ в диапазоне доз 3,6–43,2 сГр при мощности дозы облучения 0,1 мГр/мин. Результаты исследований, представленные на рис. 1, свидетельствуют о том, что динамика изменений количества фокусов γ-Н2АХ при низкой мощности дозы существенно отличается от эффектов, наблюдаемых нами ранее на тех же клетках при облучении с высокой мощностью дозы (4000 мГр/мин) [7]. Если при облучении с высокой мощностью наблюдалось зависимое от дозы увеличение количества фокусов γ-Н2АХ, то при мощности дозы 0,1 мГр/мин характер изменений количества фокусов γ-Н2АХ необычен: в ранние сроки облучения (6–24 ч, дозы 3,6–14,4 сГр) наблюдается незначительное увеличение количества фокусов, в то время как увеличение времени и, соответственно, дозы облучения (48–72 ч, дозы 28,8–43,2 сГр) вызывало неожидан-
Доза, сГр
Рис. 1. Изменения количества фокусов γ-Н2АХ в клетках линии V79 при облучении с мощностью дозы γ-излучения 0,1 мГр/мин
П р и м еч а н и е : * — отличия от контроля достоверны, p<0,05
ное снижение количества фокусов γ-Н2АХ практически до контрольного уровня. Полученные результаты могут свидетельствовать в пользу гипотезы индуци-бельного характера репарации ДР в клетках млекопитающих при длительном воздействии низкоинтенсивного ионизирующего излучения.
Образование фокусов γ-Н2АХ происходит не только при индукции ДР повреждающими агентами, но и в процессе апоптоза. Показано, что киназа DNA-PK фосфорилирует гистон Н2АХ в процессе межнуклеосомной деградации хроматина [14]. В связи с этим было важно оценить возможный вклад апоптоза в индукции фокусов γ-Н2АХ при длительном низкоитенсивном облучении клеток. Результаты, представленные на рис. 2, показали, что при облучении клеток линии V79 при мощности дозы 0,1 мГр/ мин не отмечается увеличения доли апоптотических клеток в течение 72 ч облучения (рис. 2).
Другим процессом, индуцирующим образование фокусов γ-Н2АХ при длительном низкоинтенсивном облучении, является оксидативный стресс. Прямая индукция ДР при атаке ДНК свободными радикалами — довольно редкое событие, наблюдаемое при образовании близколежащих однонитевых разрывов (ОР) на противоположных нитях ДНК [9]. Известно, что соотношение ДР/ОР при атаке ДНК свободными радикалами составляет ~1/2000–1/3250, тогда как при воздействия ионизирующего излучения оно равно ~1/25. [9]. Однако ДР могут образовываться при коллапсе репликативных вилок, когда они достигают области однонитевого разрыва [10]. В результате фокусы γ-Н2АХ могут индуцироваться в клетках при повышенной продукции АФК. Действительно, результаты измерений продукции АФК в клетках линии V79, облученных при мощности дозы 0,1 мГр/мин, показывают, что характер изменений продукции АФК схож с изменением количества фокусов γ-Н2АХ в этих клетках (рис. 3).
Обсуждение. При анализе полученных нами результатов прежде всего обращает на себя внимание пороговость наблюдаемого эффекта. Снижение уровня ДР ДНК наблюдается после облучения в дозе ~15 сГр. Это наводит на мысль, что после достижения определенного количества ДР ДНК происходит активизация индуцибильных систем клеточного отклика на повреждения. Подобные результаты были получены нами ранее в экспериментах на мышах. Было показано, что при длительном воздействии низкоинтенсивного γ-излучения в дозах 14–43 сГр в начальные сроки облучения в клетках селезенки и лейкоцитах крови животных наблюдается незначительное увеличение количества ДР, после чего с увеличением продолжительности облучения и, соответственно, накопленной дозы, происходит неожиданное снижение их количества [6]. Результаты исследований Коллис и др. [15] свидетельствуют о том, что активация АТМ-киназы на повреждения ДНК и формирование фокусов γ-H2AX в клетках, облученных при низкой мощности дозы, значительно ниже, чем в клетках, подвергнутых облучению в эквивалентной дозе, но при высокой мощности дозы. Возможно, что активация систем клеточного отклика на повреждения ДНК при малом количестве ДР ДНК не происходит. Об индуцибильном характере отклика клеток на радиационно-индуцированные ДР ДНК свидетельствуют также результаты работы Грудзенски и др. [13]. Было показано, что первичные фибробласты человека не в состоянии репарировать ДР ДНК, возникающие в результате воздействия радиации в дозе
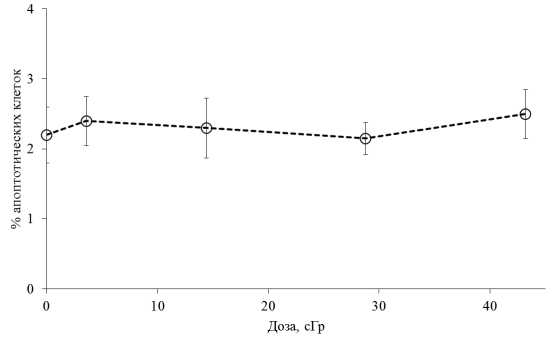
Рис. 2. Изменения доли апоптотических клеток в культуре клеток линии V79, облучаемой при мощности дозы 0,1 мГр/мин
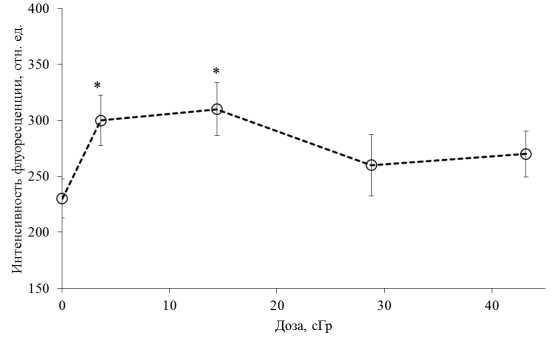
Рис. 3. Продукция активных форм кислорода в клетках линии V79 при облучении с мощностью дозы 0,1 мГр/мин П р и м еч а н и е : * — отличия от контроля достоверны, p<0,05
Заключение. Показано, что при облучении клеток китайского хомяка линии V79 с мощностью дозы 0,1 мГр/мин в ранние сроки облучения (6–24 ч, дозы 3,6–14.4 сГр) наблюдается увеличение количества фокусов γ-Н2АХ, а в более поздние сроки (48–72 ч, дозы 28,8–43,2 сГр) — снижение практически до контрольного уровня. Наблюдаемый эффект не сопровождается изменением доли апоптотических клеток, однако результаты измерений продукции АФК показывают, что их характер схож с изменением количества фокусов γ-Н2АХ в этих клетках. Сделано заключение о том, что процессы, обусловливающие изменения количества ДР ДНК в клетках млекопита- ющих при длительном воздействии низкоинтенсивного γ-излучения, по всей видимости, сопряжены с развитием оксидативного стресса и последующей активизацией антиоксидантных защитных систем клеток.
Список литературы Индукция и репарация двунитевых разрывов ДНК в клетках линии V79 при длительном воздействии низкоинтенсивного Y-излучения
- Jeggo P. A., Lobrich М. Contribution of DNA repair and cell cycle checkpoint arrest to the maintenance of genomic stability//DNA Repair (Amst). 2006. Vol. 5(9-10). P. 1192-1198
- Sutherland B.M., Bennett P. V., Sidorkina O., Laval J. Clustered damages and total lesions induced in DNA by ionizing radiation: oxidized bases and strand breaks//Biochemistry. 2000. Vol. 39 (27). P. 8026-8033
- Goodarzi A.A., Jeggo P., Lobrich M. The influence of heterochromatin on DNA double strand break repair: Getting the strong, silent type to relax//DNA Repair (Amst). 2010. Vol. 9 (12). P. 1273-1282
- Halazonetis T. D., Gorgoulis V G., Bartek J. An oncogene-induced DNA damage model for cancer development//Science. 2008. Vol. 319 (5868). P. 1352-1355
- Mladenov E., Iliakis G. Induction and repair of DNA double strand breaks: the increasing spectrum of non-homologous end joining pathways//Mutat. Res. 2011. Vol. 711 (1-2). P. 61-72
- Osipov A. N., Buleeva G., Arkhangelskaya E., Klokov D. In vivo y-irradiation low dose threshold for suppression of DNA double strand breaks below the spontaneous level in mouse blood and spleen cell.//Mutat. Res. 2013. Vol. 756 (1-2). P. 141-145
- Changes in the number of double-strand DNA breaks in Chinese hamster V79 cells exposed to y-radiation with different dose rates/K. V Kotenko, A.Y. Bushmanov, I. V Ozerov [et al.]//Int. J. Mol. Sci. 2013. Vol. 14, № 7. P. 13719-13726
- Singh N.P A simple method for accurate estimation of apoptotic cells//Exp. Cell Res. 2000. Vol. 256 (1) P. 328-337
- Osipov A.N., Lizunova E.Yu., Gur'ev D. V, Vorob'eva N.Yu. Genome Damage and Reactive Oxygen Species Production in the Progenies of Irradiated CHO-K1 Cells//Biophysics. 2011. Vol. 56, № 5. P. 931-935
- GammaH2AX foci analysis for monitoring DNA double-strand break repair: strengths, limitations and optimization/M. Lobrich, A. Shibata, A. Beucher [et al.]//Cell Cycle. 2010. Vol. 9 (4). P. 662-669
- A critical role for histone H2AX in recruitment of repair factors to nuclear foci after DNA damage/T.T. Paull, E. P. Rogakou, V Yamazaki [et al.]//Curr Biol. 2000. Vol. 10 (15). P. 886-895
- Sharma A., Singh K., Almasan A. Histone H2AX phosphorylation: a marker for DNA damage//Methods Mol. Biol. 2012. Vol. 920. P. 613-626
- Grudzenski S., Raths A., Conrad S., Rube C.E., Lobrich M. Inducible response required for repair of low-dose radiation damage in human fibroblasts//Proc. Natl. Acad.Sci. USA. 2010. Vol. 107 (32). P. 14205-14210
- DNA-PK phosphorylates histone H2AX during apoptotic DNA fragmentation in mammalian cells/B. Mukherjee, С Kessinger, J. Kobayashi [et al.]//DNA Repair (Amst). 2006. Vol. 5 (5). P. 575-590
- Evasion of early cellular response mechanisms following low level radiation-induced DNA damage/S. J. Collis, J.M. Schwaninger, A.J. Ntambi [et al.]//J. Biol. Chem. 2004. Vol. 279 (48). P. 49624-49632.


