Инновационная технология очистки сточных вод в текстильной промышленности
Автор: Кадникова О.Ю., Торетаев М.О., Шалдыкова Б.А.
Журнал: Вестник Алматинского технологического университета @vestnik-atu
Рубрика: Техника и технологии
Статья в выпуске: 1 (126), 2020 года.
Бесплатный доступ
Актуальность и новизна работы заключаются в разработке метода стабилизации твердого феррата натрия капсулированием, для получения «зеленой» технологии очистки сточных вод на текстильных предприятиях. В статье представлены исследования возможности использования феррата натрия в технологии очистки сточных вод от органических веществ на примере фенола. Показана технология получения капсулированного феррата с использованием гексана, этилцеллюлозы и парафина; установлена стабильность капсулированного феррата натрия в воздухе и щелочном растворе; оценена эффективность разложения фенола в модельном растворе капсулированным ферратом натрия, найдены константы скорости реакции взаимодействия феррат-ионов с фенолом в водном растворе в диапазоне рН от 6 до 10. Доказано, что с увеличением рН раствора степень разложения фенола снижается. Значение рН=6,5 является наиболее оптимальным для очистки воды от фенола с использованием феррат-ионов.
Поступление стоков с производства, технология очистки, органические загрязнения, феррат натрия, капсулирование, модельный раствор фенола, өндірістен ағындылардың түсуі, тазарту технологиясы, органикалық ластану, натрий ферраты, капсулдау, фенолдың модельдік ерітіндісі
Короткий адрес: https://sciup.org/140250854
IDR: 140250854 | УДК: 577.4:677.198
Innovative wastewater treatment technology in the textile industry
The relevance and novelty of the work is to develop a method of stabilization solid sodium ferrate by encapsulation, to obtain a «green» technology of wastewater treatment in textile enterprises. The article presents the study of the possibility using sodium ferrate in the technology of wastewater treatment from organic substances using the example of phenol in the textile industry. Here is shown the technology of obtaining encapsulated ferrate using hexane, ethylcellulose and paraffin. Within the study has been established the stability of the encapsulated sodium ferrate in air and alkaline solution and valuated the efficiency of using encapsulated sodium ferrate in the treated of the model solution from phenol, the efficiency of decomposition of phenol in a model solution by encapsulated sodium ferrate is estimated, the rate constants of the reaction of ferrate ions with phenol in an aqueous solution in the pH range from 6 to 10 are found. It is proved that with increasing pH of the solution, the degree of decomposition of phenol decreases. The pH value=6.5 is the most optimal for water purification from phenol using ferrate ions.
Текст научной статьи Инновационная технология очистки сточных вод в текстильной промышленности
Производство различной пряжи, тканей из химических и натуральных волокон и их смесей сопровождается образованием стоков в результате крашения, шлихтования пряжи, отделки тканей, химической обработки во- локнистых материалов и прочих технологических процессов [1, 2].
Стоки представляют собой сложную смесь нерастворимых минеральных и органических загрязнений, истинных и коллоидных растворов, включающие волокна, частички за- масливателей, красителей, синтетических ПАВ, отделочных препаратов, реагентов и прочих нерастворимых примесей. Стоки имеют водородный показатель в пределах 6…12 и отличаются выраженной окрашенностью.
Неравномерность поступления стоков с производства не дает возможность напрямую сбрасывать их в общегородские очистные сооружения и требует предварительной очистки [3, 4].
Для полной очистки сточных вод от предприятий текстильной промышленности используют биологические методы. Однако биологическая очистка сточных вод в большинстве случаев затрудняется их высокой гидратной щелочностью и недостатком биогенных элементов. Поэтому биологической очистке, как правило, должна предшествовать предварительная механическая или химическая обработка стоков.
Наибольшая проблема сточных вод возникает при крашении и печатании текстильных материалов. При этом находят применение различные красители как в отношении их физических, так и химических свойств. В зависимости от специализации предприятия используют более 100 различных рецептур, содержащих многочисленные красители и вспомогательные вещества. Степень их выбора зависит от вида красителя и может составлять от 70% (не менее) до 95% (не более). Это значит, что в сточные воды попадет часть красителей и вспомогательных веществ, в том числе поверхностно-активные (иногда с высокой концентрацией кислоты). Они образуют один или несколько потоков, в которых имеется большое число веществ в значительных вариациях [4 - 6].
В технологии очистки сточных вод предлагается использовать из ряда органических веществ феррат натрия на примере фенола [7]. Обеззараженные им источники питьевого водоснабжения являются нетоксичными. Ферраты (VI) щелочных металлов (в кислой среде потенциал FeO 4 2--иoна выше потенциала озона и перманганатов) могут заменить широко используемые окислители (пиролюзит, хлорная известь), применение которых приводит к вторичному загрязнению растворов соединениями марганца и хлора. Использование же ферратов позволит исключить вторичное загрязнение обрабатываемых растворов.
Объекты и методы исследований
Электролиз проводится в дифарагмен-ной ячейке. Объем анодной части электролизера составляет 40 см3, катодной части -110 см3. Обе части электролизера (анодная и катодная) содержат раствор гидроксида натрия. Суммарная кoнцентрация гидрoксида в вoде сoставляет 750 г/л. Анoдoм служит стружка (oтхoд, oбразующийся при oбрабoтке стали) площадью поверхности 15 см2, катодом - титановая платина площадью 25 см2. На электролизер подается постоянный ток через блок питания «RXN-305D Linear DC Adjustable Power Supply». Плoтнoсть тoка составляет 20-40 мА/см2. Продолжительность электрoлиза варьируется oт 1 дo 3 ч. Пoсле двух часoв электрoлиза из анoлита выпадает черный oсадoк, сoдержащий феррат натрия. По окончании электролиза из анолита отбирается прoба для oпределения кoнцентрации феррат-ионов в растворе. Содержание фер-рат-ионов в растворе определяется известным метoдoм «Экспрессный метoд oпределения ферратов в щелочной среде с помощью гид-роксокомплексов хрома (III)» [8].
Раствор феррата натрия, полученный электрохимическим растворением стальной стружки, был использован для обработки модельных растворов, содержащих фенол.
Объектом исследования является модельный раствор фенола. Фенолы - токсичные соединения, способные даже при небольшой концентрации резко ухудшать качество воды. В токсикологическом и органолептическом отношении фенолы неравноценны. Например, простой фенол и крезолы обладают более сильным запахом при хлорировании и более токсичны. Предельно допустимая концентрация (ПДК) в питьевой воде и воде рыбохозяйственных водоёмов составляет 1 мкг/л. При хлорировании, содержащей фенолы воды образуются устойчивые хлорфенолы, малейшие следы которых придают воде неприятный привкус и запах. Фенолы химически нестойки, но в воде они разрушаются с разной скоростью: быстрее всех - фенол, медленнее -крезолы, ещё медленнее - ксиленолы (демитилфенолы).
Для приготовления капсул, содержащих феррат натрия, в колбу наливали 50 мл циклогексана, добавляли около 0,5 г этилцеллю-лозы и 2,5 г парафина. Содержимое колбы (при постоянном перемешивании) нагревали на плитке при 600С. По достижении в колбе однородной массы, добавляли определенное количество Na2FeO4. Далее колбу охлаждали до комнатной температуры; при этом наблюдали выделение частиц неправильной формы (капсулы, содержащие феррат натрия). Капсу- лы отделяли от жидкости, промывали водой и
|
2 |
COOH R OH H2SO4 к HO OH [O] HO Ч /Л-Ч > O + RCHO t, безводная H дегидрирование и среда COOH COOH окисление COOH розово- COOH красный |
Рисунок 1 – Реакция фенольных соединений с глюкозой
В результате реакции получается ауриновый краситель розово-красного цвета. Электронный спектр поглощения данного соединения представлен на рисунке 2. Из рисунка видно, что продукт реакции глюкозы с фенолом в среде серной кислоты имеет помещали в эксикатор перед дальнейшими исследованиями.
Определение фенола в настоящей работе было основано на известной реакции фенольных соединений с глюкозой (рис. 1).
максимум поглощения при длине волны 480 нм. В дальнейшем данную длину волны использовали для построения калибровочного графика (5,56*10-5 моль/л; 1,11*10-4 моль/л; 1,67*10-4 моль/л; 2,78*10-4 моль/л).
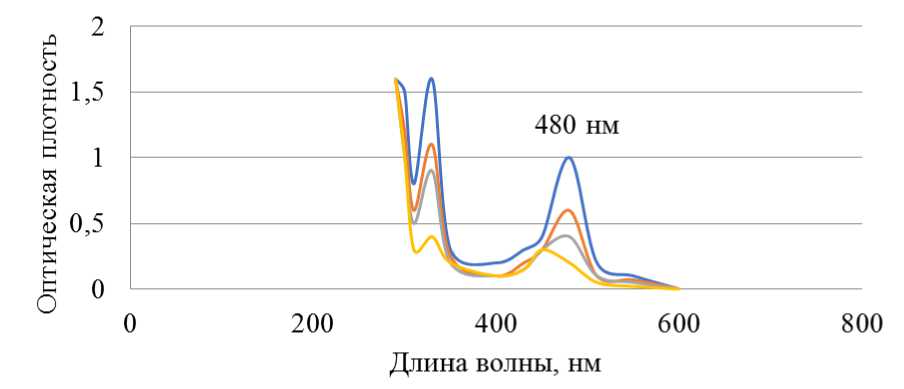
Рисунок 2 – Электронные спектры поглощения фенола
Далее строили калибровочный график для определения содержания фенола в воде. Используя калибровочный график, определяли содержание фенола в растворе после обработки капсулированным и некапсулированным ферратом натрия.
Степень очистки воды от фенола определяли по формуле 1:
X = ^^ X 100%, (1)
mD где: m0 – масса фенола в необработанном растворе;
m – масса фенола в обработанном растворе.
Масса фенола в растворе определялась по формуле 2:
т = С xV , (2)
-
где: С – молярная концентрация фенола в растворе;
-
V – объем раствора.
Результаты и их обсуждение
Эксперименты проводились следующим образом. В химический стакан, содержащий модельный раствор фенола с известной концентрацией, добавляли определенное количество анолита, полученного растворением стальной стружки в течение 30 мин при анодной плотности тока 5 мА/см2.
На рисунке 3 приведены зависимости степени очистки раствора от фенола от продолжительности очистки и соотношения «модельный раствор: анолит» (при содержании фенола 1 мг/л).
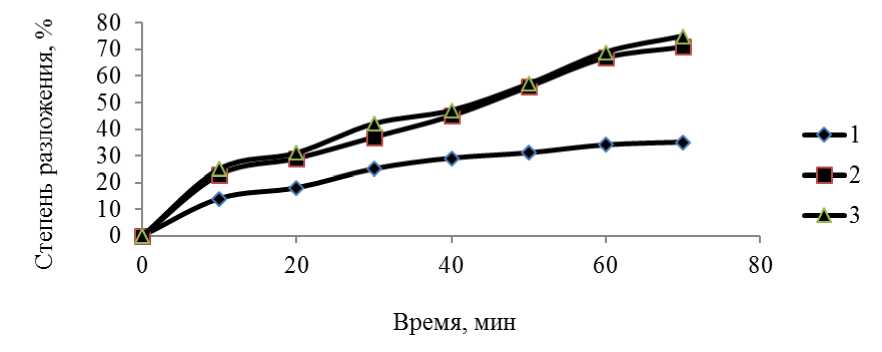
Концентрация фенола: 1 мг/л
Объемное соотношение «модельный раствор: анолит» - 1-106; 2-5*10 5 ; 3-105
Рисунок 3 - Зависимости степени очистки раствора от фенола от продолжительности очистки и соотношения «модельный раствор: анолит»
Кривые показывают, что уменьшение объемного соотношения «модельный раствор: анолит» увеличивает степень очистки воды от фенола за один и тот же промежуток времени. Однако уменьшение этого отношения до значения 105 не оправдано, поскольку приводит к увеличению рН очищаемой воды до значений 9-9,5. При этом усиливается степень саморазложения феррата. Кроме того, требуется проведение дополнительных операций для нейтрализации избыточной щелочности очищаемой воды.
На рисунке 4 приведены зависимости степени очистки раствора от продолжительности очистки и соотношения «модельный раствор: анолит» (при содержании фенола 0,1 мг/л).
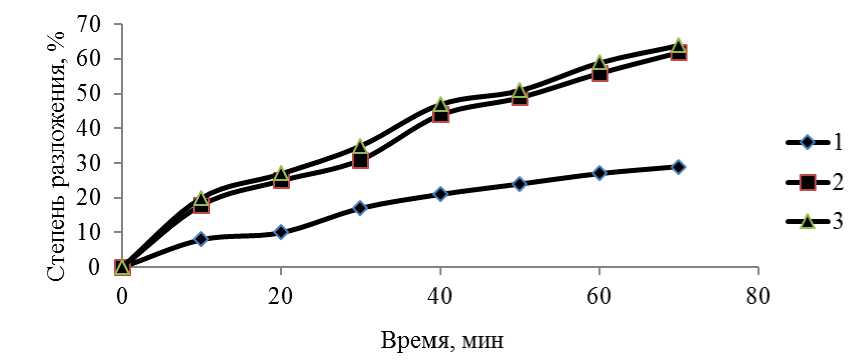
Концентрация фенола: 0,1 мг/л
Объемное соотношение «модельный раствор: анолит»: 1-106; 2-5*105; 3-105
Рисунок 4 - Зависимости степени очистки раствора от фенола от продолжительности очистки и соотношения «модельный раствор: анолит»
Из графика следует, что снижение исходной концентрации фенола в воде приводит к менее полной очистке ее от поллютанта в исследованном временном диапазоне. Данный факт может быть связан с тем, что снижение начальной концентрации фенола снижает скорость реакции взаимодействия его с феррат-ионами, то есть имеют место кинетические ограничения. На рисунке 5 приведены ИК спектры некапсулированного (а) и капсулированного (б) феррата натрия.
Можно видеть, что ИК спектры образцов (а) и (б) являются схожими. Дополнительный пик при 1670 см-1, который появляется в капсулированном образце, может быть отнесен к вибрационным колебаниям парафина, входящего в состав оболочки капсулы.
Представлялось важным исследовать стабильность капсул феррата натрия на воздухе, а также в щелочной среде.
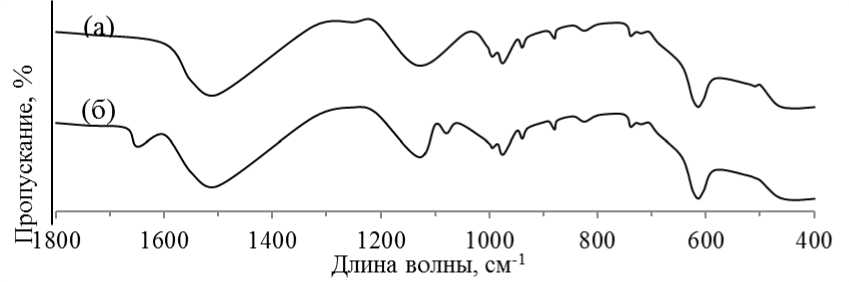
Рисунок 5 – ИК спектры некапсулированного и капсулированного феррата натрия: (а) – некапсулированный феррат натрия; (б) – капсулированный феррат натрия
На рисунке 6 приведены зависимости степени разложения капсулированного феррата натрия от продолжительности выдержки их на воздухе, а также от массового соотно шения «феррат натрия – оболочка капсулы».
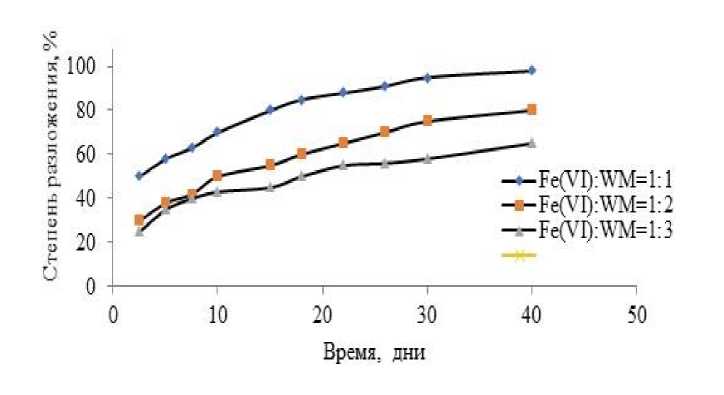
Рисунок 6 – Зависимость степени разложение капсулированного феррата натрия от продолжительности выдержки их на воздухе
Степень разложения капсулированного феррата натрия возрастает с увеличением продолжительности пребывания капсул на воздухе; при этом, увеличение массы оболочки капсулы снижает степень разложения феррата при прочих равных условиях. Так, капсулированный феррат натрия с трехкратным превышением массы оболочки капсулы над ферратом сохраняет свою стабильность на 40% после 40 дней пребывания на воздухе.
Представляло интерес определить стабильность капсулированного феррата натрия в щелочном растворе, поскольку обработка сточных вод имеет место при рН выше 7.
На рисунке 7 приведены зависимости степени разложения капсулированного феррата натрия от продолжительности контакта его с раствором 9 М NaOH.
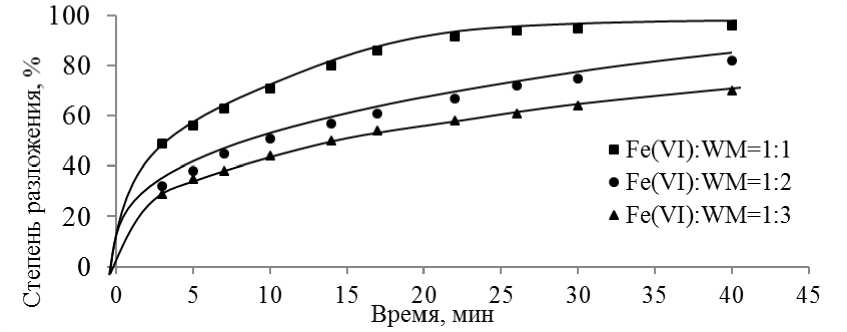
Рисунок 7 – Зависимость степени разложения капсулированного феррата натрия от продолжительности контакта его с раствором 9 М NaOH
Максимальная степень разложения капсулированного феррата натрия достигает 90% за 30 мин контакта капсул с раствором.
Увеличение массы оболочки капсулы, как и ожидалось, приводит к большей устойчивости ферратов натрия, и за те же 30 мин степень разложения феррата составляет уже 50 - 55% при трехкратном превышении массы оболочки капсулы над массой феррата. Для тестирования капсулированного феррата натрия осуществлена обработка им модельных растворов. Исследована его активность в очистке модельного раствора от фенола. Для изучения процесса очистки модельного раствора от фенола капсулированным ферратом натрия и выяснения роли рН в этом процессе был приготовлен раствор с концентрацией фенола 40 мг/л в присутствии гидроксида натрия
(рН раствора варьировался от 4 до 12, продолжительность обработки составляла 80 мин).
По окончании обработки определили содержание фенола в обработанном растворе. Результаты представлены на рисунке 8.
Из рисунка 8 видно, что первые 10-15 мин степень разложения фенола достигла 7080% от максимально возможной в данных условиях, дальнейшее увеличение времени обработки незначительно увеличило степень разложения фенола в воде. С увеличением рН раствора степень разложения фенола снизи- лась, что связано с саморазложением феррат- ионов в щелочной среде. Значение рН=6,5 является наиболее оптимальным для очистки воды от фенола с использованием феррат- ионов; так как феррат-ионы при данном значении рН наиболее устойчивы.
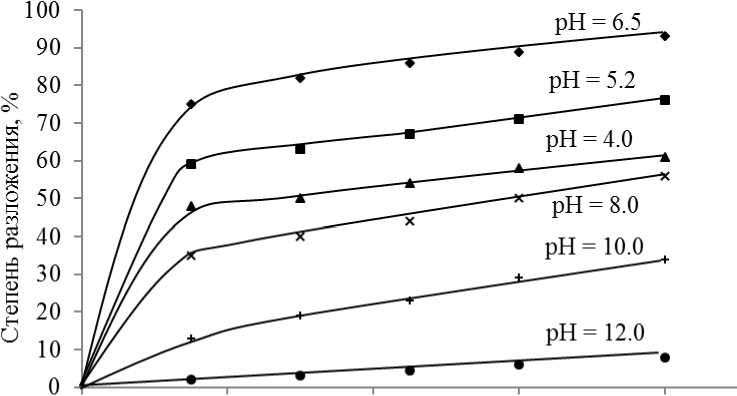
О 20 40 60 80Время, мин
Рисунок 8 – Зависимость степени разложения фенола от времени обработки и рН раствора
Важным фактором в любой химической технологии, в том числе в технологиях водоочистки, являются кинетические параметры процесса [9]. На рисунке 9 приведены конс танты скорости реакции феррат-ионов с фенолом при обработке воды капсулированным ферратом натрия (без перемешивания).
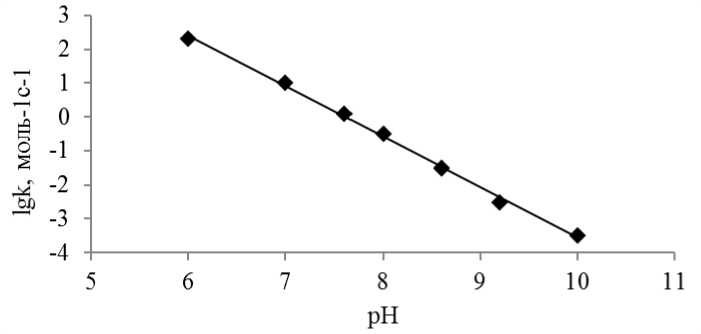
Рисунок 9 - Зависимость константы скорости реакции капсулированного феррата натрия с фенолом в воде от рН раствора
Так как реакция феррат-ионов с фенолом второго порядка, то для расчета константы скорости реакции использовалось следующее уравнение 3:
<4^), (3)
где: т - продолжительность обработки, с;
С и Со - текущая и начальная концентрации фенола в воде, моль/л.
Для ряда значений рН (6; 7; 7,5; 8; 8,5; 9; 10) были определены средние значения констант скоростей по трем измерениям.
Кривая на рисунке показывает, что наблюдается линейная зависимость между логарифмом константы скорости и рН раствора. Повышение щелочности раствора негативно сказывается на значениях константы скорости. Это объясняется тем, что в присутствии свободных гидроксильных групп (т.е. в щелочном растворе) феррат-ионы более устойчивы, чем в нейтральной и кислой средах, и хуже вступают во взаимодействие с фенолом в растворе. Полученные результаты согласуются с данными авторов [10].
Следующим этапом исследований было определение влияния концентрации феррата натрия на степень разложения фенола в водном растворе. Образцы капсулированного феррата натрия вводились в модельный раствор фенола (1 мг/л) в концентрациях 0,5; 1,0 и 1,5 г/л раствора. Затем в определенные промежутки времени определялось текущее содержание фенола в растворе. Результаты представлены на рисунке 10.
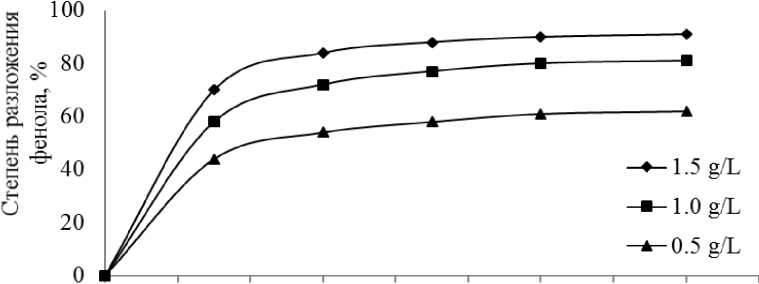
0 10 20 30 40 50 60 70 80 90
Время, мин
Рисунок 10 - Зависимость степени разложения фенола в воде от концентрации капсулированного феррата натрия и времени
Кривые показывают, что уже через 10 мин контакта капсулированного феррата с раствором практически достигается максимальная степень разложения фенола в воде. В дальнейшем разложение протекает с невысокой скоростью, и достигает 90% при концентрации капсулированного феррата натрия в растворе 1,5 г/л.
Выводы
По результатам проведенных исследований сделаны следующие выводы:
-
- показана возможность стабилизации твердого феррата натрия путем его капсули-рования. Найдено, что стабильность капсулированного феррата натрия в воде и в щелочном растворе значительно возрастает в сравнении с некапсулированным ферратом;
-
- найдены константы скорости реакции взаимодействия феррат-ионов с фенолом в водном растворе в диапазоне рН от 6 до 10. Показано, что логарифм константы скорости линейно снижается с увеличением рН раствора.
Доказано, что с увеличением рН раствора степень разложения фенола снижается, это связано с саморазложением феррат-ионов в щелочной среде. Значение рН=6,5 является наиболее оптимальным для очистки воды от фенола с использованием феррат–ионов, это связано с тем, что при данном значении рН феррат – ионы наиболее устойчивы.
Таким образом, использование капсулированного феррата натрия является подходящей и надежной технологией для очистки содержащих красители сточных вод отделочного производства текстильных предприятий. Капсулированный феррат натрия позволит добиться высокой степени обесцвечивания и удаления других загрязнителей, причем очищенная вода может повторно применяться для процессов промывки.
Список литературы Инновационная технология очистки сточных вод в текстильной промышленности
- Кадникова О.Ю., Алтынбаева Г.К., Айдарханов А.М., Шалдыкова Б.А., Успанова С.С. Переработка отходов швейно-трикотажного производства // Известия высших учебных заведений. Технология текстильной промышленности. - 2016. № 5 (365). - С. 141-143
- Kadnikova, O., Altynbayeva, G., Kuzmin, S., Aidarkhanov, A., Shaldykova, B. Recycling of production waste as a way to improve environmental conditions - 2018. // Energy Procedia 147. - P. 402-408.
- Kadnikova, Olga; Altynbayeva, Gulnara; Aidarkhanov, Arman; и др. Improving the technology of processing sewing and knitwear production waste. International scientific conference - environmental and climate technologies // Conect -2016. Energy Procedia: - 2014. - Т. 113: Р. 488-493
- Kadnikova, Olga; Altynbayeva, Gulnara; Aidarkhanov, Arman; и др. Potential analysis of implementation of developed technology for processing of sewing and knitting fabrics / International Scientific Conference on Environmental and Climate Technologies. Riga, LATVIA Energy Procedia. - 2017. - Т. 128.: Р. 411-417.
- Кадникова О.Ю. Рециклинг отходов трикотажного производства / В сборнике: Приоритетные направления развития образования и науки Сборник материалов II Международной научно-практической конференции. В 2-х томах. Редколлегия: О.Н. Широков [и др.]. 2017. - С. 154-156.
- Нурмухамбетова Б.Т., Кадникова О.Ю., Мухлис К.Ж., Джусупова-Парфилькина И.М Вторичное использование отходов производства как фактор сохранения экологической среды // Школа университетской науки: парадигма развития, 2017. - № 1-4 (23-26). - С. 170-172.
- Zhang D. X., Liu Q., Zhang Y. M. Treating Effect of Potassium Ferrate to Aquaculture Recirculating Water //Advanced Materials Research. - 2014. - Т. 1004. - С. 1005-1007.
- Экспрессный метод определения ферратов в щелочной среде с помощью гидроксоком-плексовхрома (III) / В.И. Супрунович, О.В. Павлова, И.Д. Головко, Д.А. Головко. // Вопр. химии и хим. технологии. - 2009 - № 6- С.83-87.
- Bouzek K., Roušar I. Influence of anode material on current yields during ferrate (VI) production by anodic iron dissolution Part I: Current efficiency during anodic dissolution of grey cast iron to ferrate (VI) in concentrated alkali hydroxide solutions //Journal of applied electrochemistry. - 1996. - Т. 26. - №. 9. - Р. 919-923.
- Bouzek K., Roušar I., Taylor M. A. Influence of anode material on current yield during ferrate (VI) production by anodic iron dissolution Part II: Current efficiency during anodic dissolution of white cast iron to ferrate (VI) in concentrated alkali hydroxide solutions //Journal of applied electro-chemistry. - 1996. - Т. 26. - №. 9. - Р. 925-931.


