Интеграция миниинвазивных навигационных технологий в клиническую практику многопрофильного медицинского учреждения
Автор: Карпов О.Э., Ветшев П.С., Бруслик С.В., Левчук А.Л., Свиридова Т.И., Слабожанкина Е.А., Бруслик Д.С.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 2 т.12, 2017 года.
Бесплатный доступ
Обобщен и проанализирован опыт работы за последние семь лет работы в ФГБУ «НМХЦ им. Н.И. Пирогова» Минздрава России. Выполнено 2117 операций под контролем ультразвука и рентгенотелевидения (РТВ), из них при заболеваниях органов гепатопанкреатобилиарной зоны - 1110, при послеоперационных осложнениях- 443, при поражении других органов- 624. Возраст пациентов варьировал от 18 до 93 лет (средний возраст составил 44,6лет); женщины 53%, мужчин было 47%. Все пациенты находились на стационарном лечении. Миниинвазивные операции выполняли в условиях специально оборудованной операционной. Примерно треть от общего количества выполненных операций носили диагностический характер, в остальных случаях лечебный. В послеоперационном периоде проводили оценку эффективности выполнения миниинвазивных вмешательств, на основании контроля количества и качества отделяемого по дренажу, общего состояния пациента, лабораторных показателей, результатов инструментальных и рентгеноконтрастных исследований.
Миниинвазивные вмешательства, мининвазивные технологии, заболевания органов гепатопанкреатобилиарной зоны, чрескожные навигационные технологии, острый деструктивный панкреатит, эхинококкоз органов брюшной полости
Короткий адрес: https://sciup.org/140188665
IDR: 140188665 | УДК: 614.21:
Miniinvasive navigation technologies are in multifield medical establishment: the modern state and prospects
Generalized and analyzed work experience for the last seven years of work in FSBI «NMSC. N.I. Pirogov» of the Ministry of Health of Russia. 2117 operations under the control of ultrasound and X-ray television were performed, of which 1110 for diseases of the hepatopancreatobiliary zone, 443 for postoperative complications, 624 for lesions of other organs. The age of patients varied from 18 to 93 years (mean age was 44.6 years); Women 53%, men were 47%. All patients were on inpatient treatment. Minimally invasive operations were performed under conditions of a specially equipped operating room. About a third of the total number of performed operations were diagnostic in nature, in other cases, medical. In the postoperative period, the effectiveness of minimally invasive interventions was assessed, based on monitoring the amount and quality of the drainage, the general condition of the patient, laboratory parameters, the results of instrumental and radiopaque studies.
Текст научной статьи Интеграция миниинвазивных навигационных технологий в клиническую практику многопрофильного медицинского учреждения
Новой вехой в развитии клинической хирургии стало внедрение миниинвазивных технологий. Мини-инвазивные технологии (МИТ) имеют неоспоримые преимущества, которые теперь хорошо известны клиницистам и пациентам, что подтверждено многочисленными исследованиями и большим опытом, накопленным отечественными и зарубежными специалистами. В настоящее время в крупных отечественных и зарубежных медицинских центрах многие из МИТ неразрывно связаны с повседневной клинической практикой. Первые упоминания о МИТ появились порядка 100 лет назад, и лишь в последние 20 лет они получили прогрессивное развитие и признание специалистов. Отправной точкой внедрения чрескожных мининивазивных вмешательств, принято считать 1952 г., после первого сообщения R.F. Carter и G.V. Saypol о выполнении чрескожной холангиографии [24, 27, 30]. Внедрение УЗИ и ультразвуковой навигации в медицинскую практику существенно изменило диагностические возможности, ускорив развитие МИТ [23, 25, 29]. Примерно с середины 80-х годов прошлого столетия миниинвазивные вмешательства начинают постепенно внедряться в нашей стране, а к рубежу двухтысячных годов в ведущих центрах были сформулированы основные показания к большинству чрескожных вмешательств, при различных заболеваниях органов брюшной полости и забрюшинного пространства [2, 4, 26].
Началом становления и дальнейшего развития чрескожных МИТ в Пироговском Центре во многом связано с реализацией в 2009 году концепции развития ультразвуковых и рентгенохирургических методов диагностики и лечения (О.Э. Карпов, П.С. Ветшев, С.В. Бруслик) и созданием соответствующего отделения. Особенностью отделения является то, что оно выполняет функции как диагностического, так и лечебного подразделения, при этом применяются чрескожные миниинвазивные вмешательства под контролем ультразвука и рентгенотелевидения как в отдельности, так и в сочетании с другими МИТ (эндоскопическими, эноваскулярными и др.), кроме того внедрена неинвазивная технология – ультразвуковая абляция (HIFU).
Следующим этапом развития стало создание в 2014 году, по инициативе Пироговского Центра, секции «Мининвазивные технологии под контролем УЗИ и РТВ» в Ассоциации гепатопанкреатибилиарных хирургов стран СНГ. В работе координационного совета секции принимают участие ведущие специалисты по МИТ из различных регионов России и зарубежные коллеги, что позволяет выработать единую точку зрения на применение миниинвазивных операций в лечении различных заболеваний и отразить ее в резолюциях пленумов, съездов Ассоциации.
В течение короткого периода в клиническую практику Центра удалось внедрить весь спектр миниинвазивных

вмешательств (порядка 40 видов операций), в том числе гибридных и рандеву-технологий, выполняемых только в ведущих отечественных и зарубежных медицинских учреждениях. Важно отметить, что доля осложнений после миниинвазивных вмешательств за все годы их применения не превышает одного процента, что значительно меньше аналогичных показателей мировой статистики.
Материалы и методы
За период с 2009 по 2016г в отделении УЗ и РХМ диагностики и лечения ФГБУ «НМХЦ им. Н.И. Пирогова» Минздрава России выполнено 2117 операций под контролем ультразвука и рентгенотелевидения (РТВ), из них при заболеваниях органов гепатопанкреатобилиар-ной зоны – 1110, при послеоперационных осложнениях – 443, при поражении других органов – 624. Возраст пациентов варьировал от 18 до 93 лет (средний возраст составил 44,6 лет); женщины 53%, мужчин было 47%. Все пациенты находились на стационарном лечении.
МИТ применяли в условиях специально оборудованной операционной, оснащенной УЗ – аппаратом (УЗ аппарат SonoSite M-Turbo, УЗ система GE Logiqе), С-дугой (КМС-950, Philips), аппаратами для наркоза. Независимо от вида оперативных вмешательств, операции выполняли операционные бригады в составе двух врачей, операционной сестры, анестезиологической бригады в специализированной операционной с обязательным соблюдением условий асептики и антисептики.
В послеоперационном периоде проводили оценку эффективности выполнения миниинвазивных вмешательств (общее состояние пациента, количество и качество отделяемого по дренажу, лабораторные показатели, результаты инструментальных и рентгеноконтрастных исследований и т.д.).
Осложнения при миниинвазивных вмешательствах составляли менее 1% от общего числа выполненных операций, в основном это было кровотечение, гемобилия, миграция дренажа, перфорация полого органа, пролежень стенки кишки от прилегающего дренажа.
Спектр применения МИТ в Пироговском Центре достаточно широк и разнообразен – это доброкачественные и злокачественные заболевания печени, желчевыводящих путей, желудка, поджелудочной железы, селезенки, почек, плевральных полостей, перикарда, брюшной полости, а также лечение различных послеоперационных осложнений в абдоминальной, грудной и сердечно-сосудистой хирургии.
Выполняемые нами миниинвазивные операции можно разделить на две основные группы:
-
I. Диагностические – различные варианты биопсий, пункций, которые являются достаточно важным аспектом нашей деятельности, поскольку от них в большинстве случаев зависит выбор тактики лечения пациента и характер операции. Из диагностических процедур, которые составляют примерно одну треть от общего числа операций, чаще всего выполняли чрескожную биопсию
под контролем ультразвука доброкачественных и злокачественных (первичных и вторичных) опухолей печени, а также лечебно-диагностические пункции жидкостных образований (кист, гематом, абсцессов, отграниченных скоплений желчи и др.). Чрескожные МИТ, в данном аспекте, позволяют быстро, с минимальной травматичностью и частотой осложнений провести верификацию заболевания, решить вопрос о необходимости и методике дренирования, получить материал для морфологической исследования и в конечном итоге помочь клиницисту своевременно и правильно поставить диагноз и определить оптимальный план лечения пациента.
-
II. Лечебные – вмешательства, которые могли быть промежуточным этапом при подготовке пациента к традиционной операции, либо являться окончательным видом лечения. По нашему опыту, примерно в 30% от общего числа операций, миниинвазивные вмешательства становятся самостоятельным и окончательным вариантом лечения, что в полной мере соответствует принципам щадящей хирургии и мировой практике.
Основные результаты
Наибольшее распространение и значение имеют лечебные МИТ под УЗ-навигацией и рентгенологическим контролем (РТВ) при следующих клинических ситуациях.
Обтурационная желтуха . Одно из грозных проявлений заболеваний органов гепатопанкреатобилиарной зоны. Этот синдром, зачастую является первым клиническим признаком заболеваний печени, желчевыводящих путей, поджелудочной железы, двенадцатиперстной кишки и др. Как грозное осложнение указанных заболеваний, механическая желтуха (МЖ) значительно утяжеляет состояние пациентов развитием печеночной и почечной недостаточности, кровотечений, гнойных процессов в желчных протоках и печени, а также ряда других осложнений и часто приводит к полиорганной недостаточности [6, 7, 21].
В последнее десятилетие во многих многопрофильных хирургических и онкологических учреждениях, в том числе и Пироговском Центре, в лечебно-диагностическом алгоритме, используемом при синдроме обтурационной желтухи, в качестве общепринятого стандарта, предусмотрено применение МИТ. При этом независимо от антеградного или ретроградного метода декомпрессии билиарного тракта, МИТ являются эффективными методами лечения при механической желтухе доброкачественного или злокачественного генеза заболевания.
В нашей клинической практике используем весь необходимый спектр чрескожных МИТ под УЗ и РТВ навигацией для декомпрессии желчных протоков – различные варианты желчеотведения, начиная от холецистостомии, наружного и наружно-внутреннего дренирования, одномоментного дренирования через две доли печени, в том числе с сочетанием наружного и наружно-внутреннего дренирования у одного пациента (рис. 1) и, заканчивая

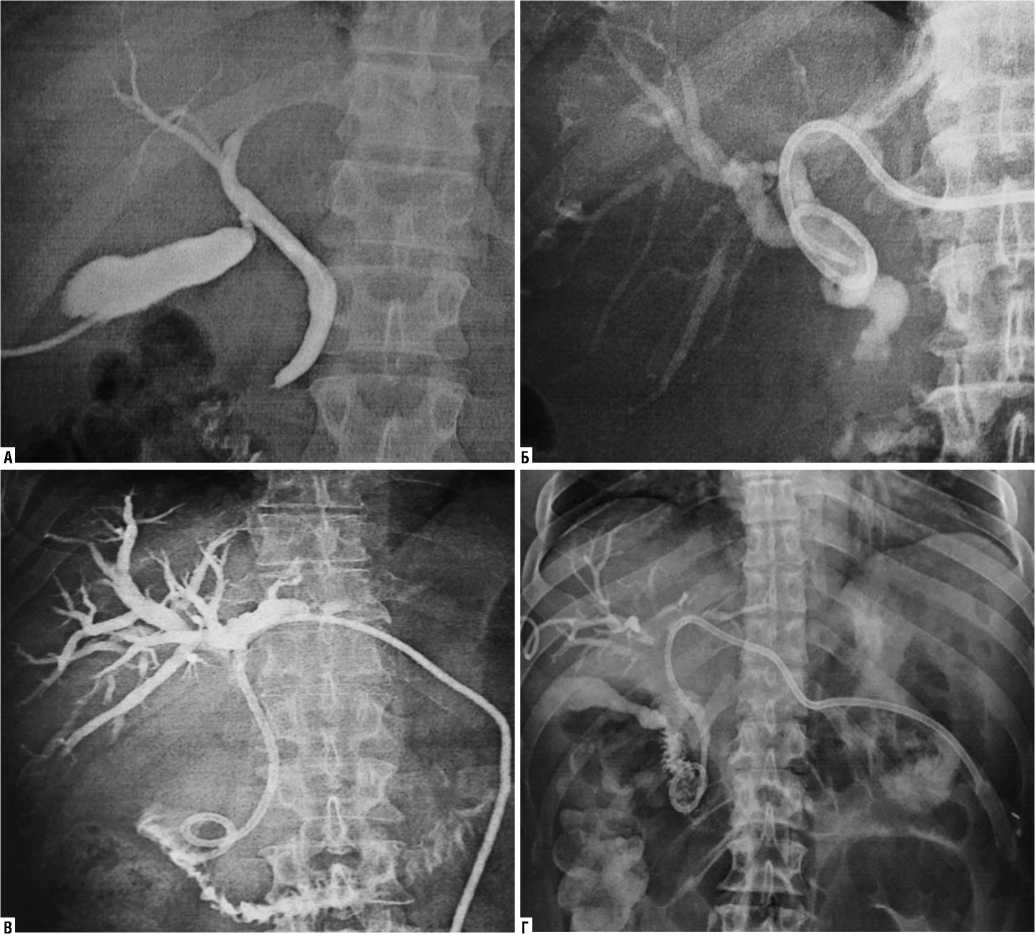
Рис. 1. Чрескожное чреспеченочное желчеотведение: А – холецистостомия; Б – наружная холангиостомия; В – наружно-внутренняя холангиостомия через левую долю; Г – сочетание наружной холангиостомии через правую долю и наружно-внутренняя холангиостомия через левую долю печени
более сложным вмешательством, таким как, билиарное стентирование, требующее соответствующей подготовки больного, расчета необходимого инструментария, расходного материала и высокой профессиональной квалификации специалистов, выполняющих данную операцию.
Полученный опыт свидетельствует о целесообразности применения двухэтапного подхода в лечении пациентов с механической желтухой [8, 11, 31]. Первым этапом выполняем декомпрессию желчных протоков путем использования чрескожных мининвазивных вмешательств (наружное, наружно-внутреннее желче-отведение, холецистостомия и т.д.) или эндоскопических методов (ЭПСТ, назобилиарное дренирование, билиарное стентирование). При этом выбор метода декомпрессии зависел от уровня блока.
Вторым этапом, после стабилизации состояния пациента и снижения интоксикации, обсуждали возможность выполнения радикального оперативного вмешательства (традиционная, лапароскопическая), при невозможности его выполнения, применяли паллиативное стентирование желчных протоков (антеградное или ретроградное по показаниям), с последующим проведением химиотерапии, которые являлись окончательным методом лечения, зачастую улучшая качество жизни пациентов с МЖ опухолевого генеза.
Решающим фактором перехода от первого этапа ко второму являются: общее состояние пациента, коли-

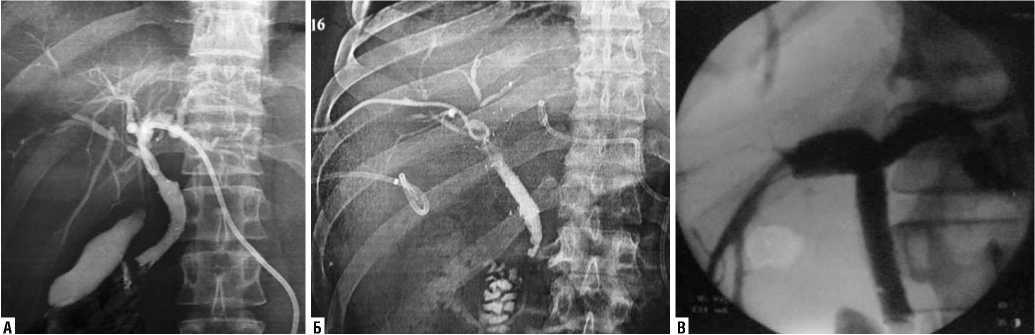
Рис. 2. Варианты антеградного стентирования: А – стандартное; Б – У-образное; В – Т-образное
чество отделяемой желчи и динамика билирубинемии, спектр микробного обсеменения желчи, наличие и выраженность гнойных осложнений, в первую очередь, холангита, холангиогенных абсцессов печени, функциональное состояние печени и другие проявления полиор-ганной недостаточности. Одним из важных критериев являются биохимические показатели: ко второму этапу обычно переходили только после медленного снижения уровня билирубина до уровня и ниже 60 мк моль/л, и, не ранее 5 суток после выполнения декомпрессии желчных протоков, снижения уровня трансаминаз и щелочной фосфатазы до референтных значений, стабильного состояния пациента. Все критерии оценивали комплексно, при этом считаем, что малооправданно и рискованно только на основании динамики одного из них принимать решение о возможности выполнения следующего этапа лечения.
В случаях необходимости установки стента в желчные протоки использовали как стандартные варианты антеградного стентирования, так и варианты, применяемые при высоком блоке желчных протоков – это Т- и У-образное стентирование (рис. 2). По нашему мнению, для стентирования желчных протоков при механической желтухе опухолевого генеза следует применять покрытые саморасширяющиеся нитиноловые стенты. При высоком блоке с частичным поражением сегментарных протоков в некоторых ситуациях допустимо применение непокрытых саморасширяющихся стентов. При низком блоке желчевыводящих путей, обусловленных поражением головки или дистальной части внепеченочных желчных протоков и отсутствии панкреатической гипертензии, целесообразно использование частично непокрытых в дистальной части нитиноловых стентов. Стентирование желчных протоков нитиноловыми стентами у пациентов с механической желтухой доброкачественного генеза, как окончательный этап лечения, не выполняли.
В последние годы, именно при поражении желчных протоков и механической желтухе, в клиническую практику Пироговского Центра были внедренны тандемные
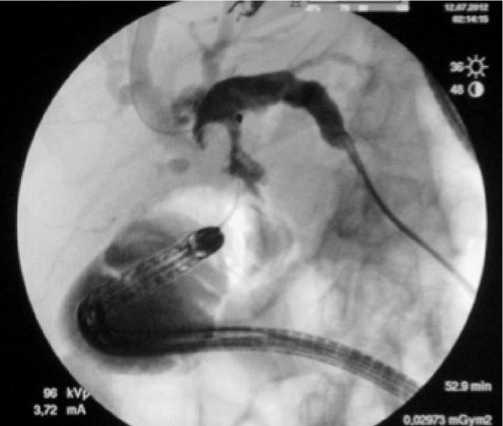
Рис. 3. Интраоперационная рентгенограмма. Рандеву-технология (чрескожная и эндоскопическая) при удалении конкрементов из внутри и внепеченочных желчных протоков после панкреатодуоденальной резекции
(рандеву, гибридные) вмешательства в наиболее сложных, казалось бы, неразрешимых в рамках одной из МИТ, клинических случаях. У пациентов, после оперативного вмешательства, например, при развитии стриктуры билиодигестивного анастомоза, после выполнения панкреатодуоденальной резекции, наличии конкрементов, инородного тела во внутри- и внепеченочных желчных протоках (рис. 3), опухолевой стриктуре желчных протоков с целью контроля установки стента, коррекции его положения при миграции, реканализации окклюзированного стента или рестентирования потребовалось одномоментное применение антеградного чрескожного и ретроградного эндоскопического доступов. Эти вопросы были обсуждены на конференции «Сочетанное применение инновационных миниинвазивных технологий в многопрофильном стационаре», проведенной в Пиро-
говском Центре в ноябре 2012 года. Таких пациентов не много, за 7 лет работы отделения – 15 пациентов, но все они нуждались в оказании квалифицированной медицинской помощи в многопрофильном стационаре с применением рандеву-технологий. Подобные вмешательства позволяют избежать сложных открытых операций.
Острый деструктивный панкреатит . Тяжелое заболевание, в основе которого лежат воспалительные и дегенеративные процессы, вызванные аутолизом ткани железы ее собственными ферментами. Основные причины данного заболевания, патогенетические механизмы, фазы развития процесса, разнообразные методы диагностики и лечения разработаны уже давно, но, к сожалению, на практике результаты лечения острого панкреатита остаются хуже ожидаемых, что в основном связано с нерациональным и несвоевременным использованием современных технологий [10, 22]. Среди причин высокой летальности одно из важных мест, занимает поздняя диагностика деструктивных форм острого панкреатита и разнообразных его осложнений, неадекватный выбор консервативной и хирургической тактики [9, 18].
Принятый у нас алгоритм комплексного лечения острого деструктивного панкреатита во всех случаях при необходимости хирургического вмешательства, первым этапом предусматривает применение именно чрескожных МИТ. Клиническая практика и наш опыт свидетельствует о высокой эффективности использования этих технологий в лечении острого деструктивного панкреатита и его осложнений [1, 19].
По нашему мнению, отношение к острым жидкостным скоплениям при деструктивном панкреатите должно быть дифференцированным. Эти жидкостные скопления не окружены капсулой, содержимое их агрессивно за счет высокой концентрации панкреатических фермен- тов. В большинстве наблюдений острые жидкостные скопления объемом до 100 мл подвергаются резорбции под воздействием адекватной терапии. При острых парапанкреатических скоплениях более 100 мл считаем целесообразным выполнить тонкоигольную пункцию с последующим интраоперационным решением вопроса о необходимости наружного дренирования.
В клиниках, обладающих всем спектром МИТ, оправдано применение чрескожных миниинвазивных вмешательств при распространенных формах панкреоне-кроза – флегмоне парапанкреатической, параколической, парадуоденальной, параренальной клетчатки, секвестрации забрюшинной клетчатки (рис. 4). Известно, что своевременное использование этих вмешательств позволяет снизить летальность при этом тяжелом заболевании в несколько раз. Лечение острого деструктивного панкреатита длительное (иногда до 2,5–3 месяцев), в ряде случаев, с целью адекватного дренирования гнойного процесса в забрюшинной клетчатке, выполнения чрескожной некрсеквестрэктомии требует установки большого числа дренажей (одномоментно до 22 дренажей у одного пациента), для ведения которых необходим внятный комплексный подхода (санаций, замены и своевременная коррекции положения, удаление и т.д.), но наш опыт показывает, что именно такая тактика позволяет получить в большинстве случаев положительный результат – купировать воспалительный процесс в забрюшинной клетчатке и практически полностью излечить больного.
Важное значение МИТ имеют и в лечении осложнений острого деструктивного панкреатита, например, при формировании псевдокисты, имеющей связь с протоковой системой поджелудочной железы. Отсутствие капсулы, стихающий воспалительный процесс поджелудочной железы не позволяют использовать традиционное
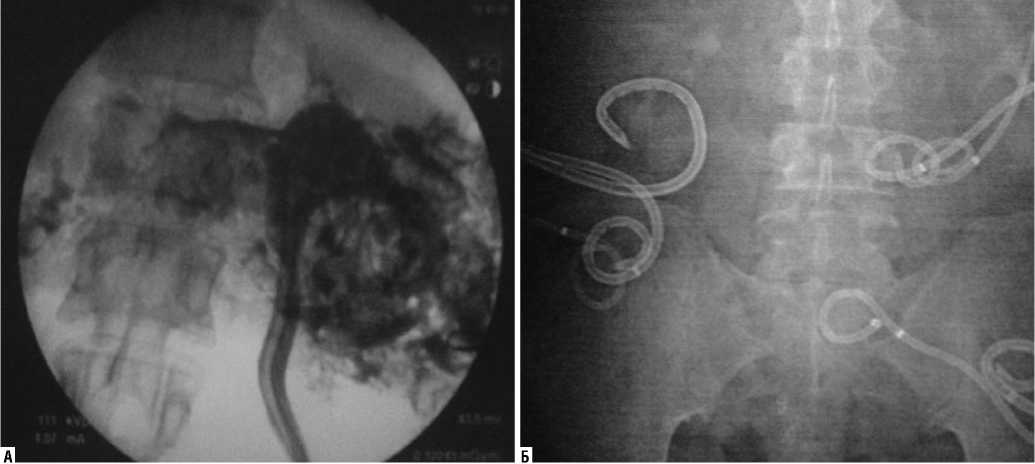
Рис. 4. Дренирование забрюшинной клетчатки при осложненном течении острого деструктивного панкреатита: А – 2 дренажа; Б – 7 дренажей
хирургическое вмешательство (цистоэнтеростомия, цистогастростомия). Именно с помощью МИТ за несколько этапов удается добиться создания внутреннего анастомоза между псевдокистой и просветом 12-ти перст-ной кишки. Выполнение подобной операции возможно в остром периоде, и нет необходимости дожидаться формирования капсулы для создания подобного анастомоза хирургическим путем (рис. 5).
Изолированное применение только навигационных технологий в лечении острого деструктивного панкреатита и его осложнений не всегда приводит к успеху, поэтому, целесообразно лечение таких больных в многопрофильных клиниках, имеющих в арсенале возможности применения операций из минидоступа, лапароскопических и эндоскопических внутрипросветных технологий в последовательном или сочетанном варианте, так называемых, гибридных, «рандеву-технологий» и др. (чрескожных и эндоскопических, чрескожных и лапароскопических, чрескожных и эндоваскулярных и т.п.). Этот мультидис-циплинарный подход требует дальнейшего изучения в специализированных клиниках и набора клинического материала [12].
Опыт лечения острого деструктивного панкреатита и его осложнений показывает необходимость отказа от ранних лапаротомий в пользу использования многокомпонентной консервативной терапии, дополняемой при необходимости МИТ. Показание к лапаротомии возникают редко – при гнойном перитоните или арро-зивном кровотечении. Подобный подход позволил нам добиться положительных результатов у 94,3% больных с деструктивным панкреатитом в стадии гнойно-некротических осложнений. При этом среди всех пациентов, пролеченных с помощью МИТ, летальный исход отмечен только в одном случае.
Следовательно, современное развитие МИТ – чрескожных, видеоэндоскопических, лапароскопических, эндоваскулярных, операций из минидоступа и различных их сочетаний, позволяет решать практически все задачи лечения у этой тяжелой категории больных с минимальной хирургической агрессией.
Паразитарное (эхинококкоз) поражение органов брюшной полости, наиболее тяжелое заболевание, со- провождающееся формированием кистозных структур практически в любом органе и забрюшинной клетчатке. В последние годы кардинально изменились подходы к диагностике и выбору лечения больных эхинококкозом, были выявлены многие морфологические особенности паразита, внедрены новые методы щадящей хирургии [3, 5].
Современная хирургия эхинококкоза включает как традиционные, так и эндовидеохирургические и чрескожные мининвазиивные вмешательства. Традиционные вмешательства в хирургии эхинококкоза сохраняют свою ведущую роль и остаются основным методом лечения. Хотя все большее применение находят лапароскопические методы при определенных локализациях кисты [3, 5, 16]. Накопленный мировой опыт показал, что чрескожные мининвазивные (пункционнодренирующие) методы под контролем УЗИ занимают все большее место при лечении больных эхинококкозом [3, 5, 28]. Применение чрескожных вмешательств дает лучшее результаты при моновезикулярных кистах (I–II тип по Gharbi) без кальциноза фиброзной капсулы, при этом размеры кисты, как правило, не имеют принципиального значения. Однако, при кистах более 10 см целесообразен более сдержанный подход. Кисты малых размеров (до 3–4 см) подлежат чрескожной пункции с противопаразитарной обработкой 87% глицерином. При кистах большего размера показано наружное чрескожное дренирование, противопаразитар-ная обработка глицерином с обязательным удалением всех герминативных элементов кисты (рис. 6).
Чрескожная эхинококкэктомия также применима при отказе больного от традиционного вмешательства, тяжелом состоянии, сложных клинических ситуациях, при резидуальном и рецидивном эхинококкозе. По своей эффективности чрескожные методы не уступают традиционным видам лечения эхинококкоза при соблюдении всех технических приемов вмешательства, применения их по показаниям и могут занять соответствующее место в хирургии эхинококкоза. Противопоказаниями к щадящим операциям при эхинококкозе считаются множественные дочерние и внучатые кисты в просвете материнской (рис. 7), прорыв кисты в брюшную и плевральные полости. Обязательным, считаем, является
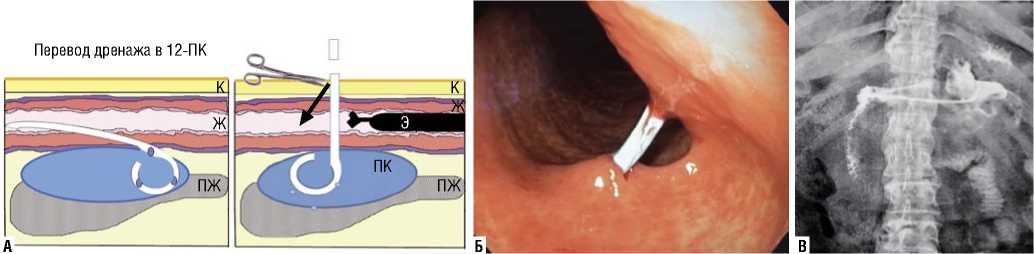
Рис. 5. Этапы цистогастростомии: А – схема цистогастростомии; Б – эндоскопический этап выполнения цистогастростомии; В – интраоперационная рентгенограмма. Цистогастростома функционирует адекватно
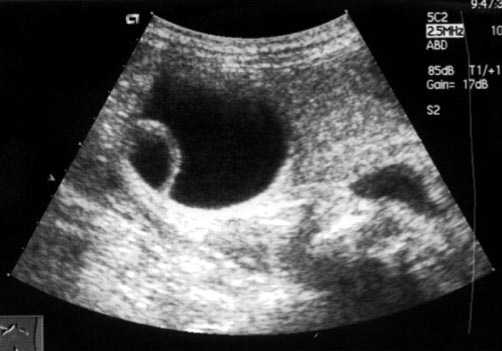
Рис. 7. Ультразвуковая сканограмма. Материнская эхинококковая киста с дочерней кистой в полости
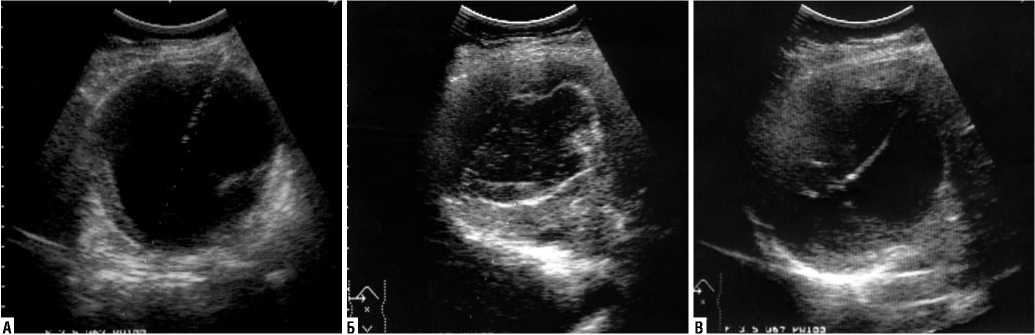
Рис. 6. Интраоперационные ультразвуковыке сканограммы этапов чрескожной эхинококкэктомии: А – пункция кисты и противопаразитарная обработка; Б – спадение хитиновой оболочки под воздействием гермецида; В – дренирование кисты
комплексный подход, включающий применение послеоперационной противогельминтной терапии независимо от использованной хирургической технологии.
Осложнения после хирургических вмешательств . Чрескожные МИТ во многом являются, методом выбора, в лечении пациентов этой группы. Пункция и при необходимости последующее дренирование помогают справиться с такими послеоперационными осложнениями, как гематома, абсцесс, отграниченные скопления жидкости в малом тазу, брюшной полости, плевральных полостях, в ложе удаленного органа, перикарде и т.д. При этом за 3–4 дня удается купировать клинические проявления осложнения у оперированных больных такие как, гипертермия, болевой синдром, явления интоксикации и т.д., в том числе и в условиях отделения реанимации, позволяя избежать повторного оперативного вмешательства.
Обсуждение
Сегодня трудно представить работу многопрофильного стационара без подразделений, использующих в своей работе инновационные МИТ- внутрипросветные эндоскопические, навигационные чрескожные, эндоваскулярные и т.д. [11, 20, 21]. Важное значение МИТ в клинической практике и основные показания к их применению у ведущих специалистов не вызывают разногласий. Эти вопросы регулярно и всесторонне обсуждаются на крупных форумах с участием смежных специалистов, что позволяет выработать взвешенные рекомендации для практикующих врачей в виде резолюций и постановлений Ассоциации гепатопанкреатобилиарных хирургов стран СНГ [14, 15, 17]. Но многие вопросы применения чрескожных МИТ при различных заболеваниях остаются до конца нерешенными, это связано с недостаточностью накопленного опыта или устойчивых предпочтений отдельных клиник, противопоставления МИТ и традиционных хирургических операций. Неоспоримыми преимуществами МИТ является их малая травматичность, низкая частота осложнений и летальности, но намного лучшее качество жизни оперированных больных и т.д. Однако при этом, не все хирургические проблемы можно решить только в рамках МИТ. Принятый в Пироговском Центре мультидисциплинарный (пациент-ориентирован-ный) подход, позволяет правильно определить стратегию и тактику ведения пациента, найти оптимальный путь к применению тех или иных хирургических технологий или путь к разумному и сочетанному (последовательному) их применению [12, 13]. Именно возможности многопрофильного стационара позволяют выбрать из всего спектра вмешательств оптимальный набор и рациональный порядок использования (последовательно, сочетанно) диагностических и лечебных МИТ, традиционных операций. В качестве примера, лечение злокачественных первичных и вторичных поражений печени, когда после резекции печени, возникает необходимость выполнения артериальной или портальной химиоэмболизации с последующей ультразвуковой абляцией (HIFU) и дальнейшим проведением химиотерапии. Причем синергидный эффект последовательного либо сочетанного применения
этих методов, намного превосходит эффект от их раздельного применения.
В перечне нерешенных, спорных вопросов применения МИТ заслуживает внимание лечение цистобилиарных свищей после чрескожной эхинококкэктомии из печени, закрытие внутренних и наружных дигестивных свищей при лечении острого деструктивного панкреатита, чрескожное стентирование доброкачественной стриктуры протока поджелудочной железы, необходимость применения чрескожных вмешательств при распространенных гнойных процессах в брюшной полости и забрюшинной клетчатке. Из перспективных направлений развития МИТ следует отметить применение диагностических и лечебных чрескожных видеоэндоскопических внутрипротоковых вмешательств, дальнейшее – совершенствование материалов для изготовления инструментов и расходных материалов, в том числе и биодеградирующих стентов.
Заключение
В завершении важно подчеркнуть, что современные навигационные, миниинвазивные хирургические технологии, динамично развиваясь и совершенствуясь, занимают все более достойное место в клинической практике. За этими инновационными методами будущее, о чем свидетельствует опыт ведущих отечественных и зарубежных клиник. Их дальнейшее развитие и широкое внедрение в клиническую практику требует мультидисциплинарного подхода, активного обсуждения на научных форумах и на страницах периодических изданий. Необходима дальнейшая интеграция миниинвазивных и цифровых технологий (информационных, телекоммуникационных, электронного документооборота и др.) с целью оптимизации клинических протоколов и рекомендаций, совершенствования персонифицированного (пациент-ориентированного) подхода в лечении.
Список литературы Интеграция миниинвазивных навигационных технологий в клиническую практику многопрофильного медицинского учреждения
- Андреев А.В., Ившин В.Г., Гольцов В.Р. Лечение инфецированного панкреанекроза с помощью мининвазивных вмешательств. Анналы хирургической гепатологии. 2015; 20 (3): 110-116.
- Ветшев П.С., Ипполитов Л.И., Ветшев С.П., Коваленко Е.И. Спорные вопросы и негативные тенденции в диагностике и хирургическом лечении случайно выявленных опухолей надпочечников//Хирургия, 2005, № 6, С. 11-14.
- Ветшев П.С., Мусаев Г.Х. Эхинококкоз: современный взгляд на состояние проблемы. Анналы хирургической гепатологии. 2006; 11 (1): 111-117.
- Ветшев П.С., Мусаев Г.Х., Бруслик С.В. Мининвазивные чрескожные технологии: история, традиции, негативные тенденции и перспективы//Анналы хирургической гепатологии. 2014. Т. 19 -№ 1. -С. 12-16.
- Ветшев П.С., Мусаев Г.Х., Фатьянова А.С. Эхинококкоз: основы диагностики и роль мининвазивных технологий (обзор литературы) Анналы хирургической гепатологии. 2015; 20 (3): 117-123.
- Гальперин Э.И., Ахаладзе Г.Г., Котовский А.Е., Глебов К.Г., Чевокин А.Ю., Момунова О.Н. Патогенез и лечение острого гнойного холан-гита. Анналы хирургической гепатологии. 2009; 14 (4): 13-21.
- Гальперин Э.И., Ветшев П.С. Руководство по хирургии желчных путей (руководство для врачей) 2-е издание. М.: Видар-М, 2009. 568 с.
- Гальперин Э.И., Котовский А.Е., Момунова О.Н. Темп декомпрессии желчных протоков при механической желтухе опухолевой этиологии. Хирургия. 2011; 8: 33-40.
- Гольцов В.Р., Савелло В.Е., Бакунов А.М., Дымников Д.А., Курочкин Д.М., Батиг Е.В. Гнойно-некротический парапанкреатит: эволюция взглядов на тактику лечения. Анналы хирургической гепатологии. 2015; 20 (3): 75-83.
- Дюжева Т.Г., Джус Е.В., Шефер А.В., Ахаладзе Г.Г., Чевокин А.Ю., Котовский А.Е., Платонова Л.В., Гальперин Э.И. Конфигурация некроза поджелудочной железы и дифференцированное лечение острого панкреатита. Анналы хирургической гепатологии. 2013; 18 (1): 92-102.
- Карпов О.Э., Ветшев П.С., Бруслик С.В., Маады А.С. Сочетанное применение ретроградного и антеградного доступов при сложном холедохолитиазе. Анналы хирургической гепатологии. 2013; Т.18. 1; 59-62.
- Карпов О.Э., Ветшев П.С., Левчук А.Л. Интеграция инновационных технологий и мультидисциплинарного подхода в хирургическую практику. Вестник Национального медико-хирургического центра им Н.И. Пирогова. 2016; 11 (3): 3-7.
- Карпов О.Э., Ветшев П.С., Левчук А.Л., Шимкович С.С. Становление пациенториентированной хирургии в многопрофильном Федеральном учреждении.//Вестник НМХЦ им. Н.И. Пирогова. -2017. -№ 2. -С. 7-11.
- Резолюция ХIV Международного конгресса хирургов -гепатологов стран СНГ «Актуальные проблемы хирургической гепатологии» 19-21 сентября. 2007г, Санкт-Петербург, Россия. Анналы хирургической гепатологиию2007; 12: 110-112.
- Резолюция XXI Международного конгресса Ассоциации гепатопанкреато-билиарных хирургов стран СНГ «Актуальные проблемы гепатолбилиарной хирургии» 7-9 сентября. 2015г., Ташкент, Узбекистан. Анналы хирургической гепатологиию. 2015; 4 (20): 128-131.
- Резолюция XXI Международного конгресса ассоциации гепатопанкреатобилиарных хирургов стран СНГ «Актуальные проблемы хирургической гепатологии» 9-12 сентября. 2014г, Пермь, Россия. Анналы хирургической гепатологиию 2015; 3 (20): 139-141.
- Резолюция Пленума правления (Тюмень). Анналы хирургической гепатологии. 2014; 3: 138-140.
- Толстой А.Д., Багненко С.Ф., Красногоров В.Б., Курыгин А.А., Гринев М.В., Лапшин В.Н., Гольцов В.Р. Острый панкреатит (протоколы диагностики и лечения). Хирургия. Журнал им. Н.И. Пирогова. 2005; 7: 19-23.
- Харьков Д.П., Федорук А.М., Савченко А.В., Руммо О.О. Псевдокисты поджелудочной железы: эффективность чрескожной миннивазивной технологии формирования панкреатоцистогастроанастомоза на стенте. Анналы хирургической гепатологии. 2015; 20 (3): 117-123.
- Шевченко Ю.Л. Щадящая хирургия. Геотар-медиа. Москва, 2005.
- Шевченко Ю.Л., Ветшев П.С., Стойко Ю.М., Левчук А.Л., Бардаков В.Г., Степанюк И.В. Хирургическая тактика при синдроме механической желтухи. Вестник Национального медико-хирургического центра им. Н.И. Пирогова. 2009; 4 (1): 10-13.
- Beger H.G. Matsuno S., Cameron J.L. Diseases of the pancreas. Current surgical therapy. Springer -Berlin, Heidelberg, New York.2008. 950 p.
- Burcharth F.A. New endoprostesis for nonoperative intubation of the biliary tract in malignant obstructive jaundice//Surg. Gynec. Obstet. 1978. -Vol. 146. P. 76-78.
- Carter F.,Saypol G. Transabdominal cholangiography. JAMA. 1952; 148 (4): 253255.
- Glenn F., Evans J.A., Mujahed Z., Thorbjarnarson B.//Ann. Surg., 1962. 156, 451.
- Hanke S., Pedersen J.F. Percutaneus puncture of pancreatic cysts guided by ultrasound.//Surg.Gunecol.Obstet. 1976 -Vol. 142 -P. 551-552
- Huard P, Do-Xuan-Hop. La ponction transhepatique des canaux biliares//Bull Soc Med Chir Indochine 1937; 15: 1090.
- Kelly K, Weber S.M. Cystic diseases of the liver and bile ducts. J. gastrointest. Surg.2014; 18 (3): 627-634 DOI: 10.1007/s11605-013-2426-8
- Menghini G. One-second needle biopsy of the liver.//Gastroenterology 1958; 35: 190-199.
- R. Franklin Carter, George M. Saypol. TRANSABDOMINAL CHOLANGIOGRAPHY//JAMA. 1952; 148(4): 253-255.
- Zhang Y.G., Li T.W., Peng W.J/, Li G.D., He X.H., Xu L.C. Clinikal outcomus and prediction of survival following percutaneous biliary drainage for malignant obstructive jaundice. Oncology Letters. 2014; 7 (4): 1185-1190.


