Интегративный анализ взаимодействия электростимуляционной системы и сердца
Автор: Нужный В.П., Киблер Н.А., Цветкова А.С., Шмаков Д.Н., Нужный П.В., Панько С.В.
Журнал: Известия Коми научного центра УрО РАН @izvestia-komisc
Рубрика: Биологические науки
Статья в выпуске: 2 (6), 2011 года.
Бесплатный доступ
Изучены структурно-функциональная организация сердца и качество жизни пациентов с имплантированными электрокардиостимуляционными система- ми. Выявлены ограничение физической зоны комфортности и инверсия век- тора качества жизни в социальное ожидание. Установлено наличие трехлет- них циклов функционирования сердца, в течение которых оно изменяется в направлении упрощения структурной и функциональной организации. Ус- тановлен рост величины энтропии сердца, отражающей физиологические осо- бенности его функционирования. На основании экспериментальных данных на адекватных человеку по типу активации модельных животных (собака) объяснен ряд закономерностей функциональной деятельности сердца челове- ка при электрокардиостимуляции.
Система сердца, электрокардиостимуляция (экс), информационная энтропия сердца, структурно-функциональная организация, качество жизни
Короткий адрес: https://sciup.org/14992453
IDR: 14992453 | УДК: 612.172
The combined analysis of the interaction of electrocardiostimulating system and the heart
The structural and functional organization of the heart with implanted electrocardiostimulation system and quality of life under cardiostimulation were studied. Transformation of the electrophysiological and structural parameters in the heart were shown. Decrease of electrical heterogeneity of myocardium was revealed. The development of informational entropy of the heart system is correlated with dynamics of the structural transformation.
Текст научной статьи Интегративный анализ взаимодействия электростимуляционной системы и сердца
Со времени имплантации первого электрокардиостимулятора (ЭКС) в 1958 г. достигнуты значительные успехи в кардиостимуляционных технологиях [1 – 3]. Остаются малоизученными механизмы функционирования сердца при ЭКС, исследование которых составляет одну из основных задач фундаментальной физиологии и клинической кардиологии. Сложность электрических процессов в миокарде [4, 5], отсутствие единого представления о роли изменений гетерогенности реполяризации [6], особенно при кардиостимуляции, затрудняют анализ этих влияний на структурные и функциональные преобразования в сердце, уровень которых определяется количеством и качеством возможных состояний системы сердца, а их развитие повинуется закону случая или принципу неопределенности [7].
Процессы, происходящие в сердце при кардиостимуляции, являясь по сути физиологическими, приводят к дезорганизации его деятельности, что проявляется в различных его функциональных свойствах [8 – 10], анализ изменений которых не дает достаточной информации для оценки эффективности взаимодействия кардиостимуляционной системы и сердца. До настоящего времени остаются открытыми вопросы, какую же цену заплатит сердце, чтобы сохранить свое физиологическое предназначение? И сохранит ли оно свою функциональную неоднородность [11, 12] при жесткой синхронизации функций с внешним электрическим стимулом?
Интенсивность протекающих процессов зависит от поступающей в систему информации [13, 14], которая является причиной изменения ее состояния путем внесения определенности в реализацию того или иного события, и определяет уровень энтропии, при котором данная система будет существовать [15]. В биологических системах энтропия Шеннона не тождественна понятию физической энтропии [16], в них она связана со значением «ценности» или целесообразности информации для сохранения живой системы [17, 18].
При очевидной целесообразности ЭКС для пациента выявлены и недостатки долговременной кардиостимуляции в виде минимизации ожидаемых клинических и долгосрочных эффектов в улучшении качества жизни [19 – 21].
Таким образом, определение функционального состояния сердца связано с решением классической задачи статистического анализа получаемой медицинской информации. В свою очередь, задача измерения и анализа информации сводится к теории меры, т.е. меры информации, позволяющей делать определенные выводы.
Целью исследования явилось выяснение закономерностей структурно-функциональной организации сердца при предсердно-желудочковой стимуляции и электростимуляции верхушки правого желудочка на основе интегративного анализа взаимодействия ЭКС системы и сердца.
Для объяснения ряда закономерностей функциональной деятельности сердца при ЭКС проведены клинические и экспериментальные исследования. В эксперименте использовали адекватные человеку по типу активации миокарда модельных животных, в частности, собаку [22, 23].
Материал и методы
Экспериментальная часть выполнена в соответствии с международными правилами обращения с экспериментальными животными (Guide for the Care and Use of Laboratory Animals – публикация US National Institutes of Health: NIH Publication № 85-23, ред. 1996) на беспородных взрослых собаках обоих полов (n=13). Животных наркотизировали (тиопентал Na 50мг/кг, золетил 15мг/кг), переводили на искусственную вентиляцию легких. Проводили торакотомию. Температуру тела поддерживали на уровне 37-38° С. Процессы деполяризации и реполяризации в сердце изучали осуществляя предсердно-желудочковую и ЭКС верхушки правого желудочка. Интрамуральные электрограммы регистрировали при последовательном изменении режимов ЭКС с помощью игольчатых электродов, общее количество макроэлектродов составляло 64 в каждом эксперименте. Регистрацию электрических потенциалов производили с помощью 128-канальной системы для синхронной регистрации электрического поля сердца [24]. Пространственно-временные и амплитудные характеристики кардиоэлектрического поля в интрамуральных слоях желудочков исследовали при помощи хронотопографических карт.
Структурную и функциональную организацию сердца изучали у пациентов в возрасте 60.4±6.3 года (n=30) в период с 1998 по 2004 гг., которым были выполнены первичные имплантации ЭКС в предсердно-желудочковом режиме. Показаниями к имплантации ЭКС явились сино-атриаль-ная и полная атриовентрикулярная блокады сердца. Пациенты с тяжелой сопутствующей патологией из эксперимента исключались. Изучали морфологические и функциональные показатели сердца, определяли тип ремоделирования и динамику структурной организации сердца, параметры центральной гемодинамики [25-27]. Качество жизни (КЖ) у 60 пациентов с 1998 по 2007 г. изучали с использованием краткой версии международной ан- кеты – MOS – SF-36 (Medical, Outcomes Study – Short Form) [28]. Возраст пациентов составил 65.6±3.1 года. Конечной точкой исследования являлось изучение влияния ЭКС технологии на связанное со здоровьем качество жизни.
Данные в работе представлены в виде: среднее арифметическое ± стандартное отклонение (M±σ). Для оценки различий временных параметров применяли критерий Стьюдента для попарно связанных вариант. Для определения зависимости времени реполяризации от времени активации и локальных длительностей реполяризации рассчитывали коэффициенты корреляции. Для оценки различий временных параметров применяли критерий Уилкоксона для попарно связанных вариант и критерии Фридмана и Ньюмена-Кейлса для множественных сравнений. Значимым считали результат статистических исследований при вероятности p<0.05. Величину энтропии сердца рассчитывали у пациентов (n=30), которым в период с 1998 по 2004 г. выполнены первичные имплантации предсердно-желудочковых ЭКС и у которых были изучены КЖ, динамика структурной организации сердца и параметры центральной гемодинамики. Использовали методику расчета логарифмической меры информации, позволяющей переделать информационно-энтропийные характеристики сердца, как необходимую сердцу информацию по объему и новизне в условиях замещенной функции [16, 29]. Группы изучаемых показателей объединяли по морфологическим и функциональным показателям. Состояние сердца g оценивали более или менее однородными группами показателей X (морфологические, функциональные и др.), которые отражают морфологические параметры и структурно-функциональные характеристики сердца в процессе долговременной кардиостимуляции. Группы нумеровали с помощью индекса i. Предположим, что каждая из этих групп содержит m(i) конкретных параметров, нумеруемых индексом j. Каждому обследуемому лицу присваивали номер k, каждому периоду снятия показателей (исходный – до имплантации кардиостимулятора, через полгода, через один год, через два-три года и через пять-семь лет после имплантации) – индекс l. Всего обследуемых – r, общее число показателей – t. Вычисляли вначале безразмерные величины Y:
у ( kl ) _ у( kl )
у (kl) _ X 1 X i (min),
Yij = y( kl) _ y( kl)
X i (max) X i (min)
X(kl)
где 1 (min) и i (max) , соответственно, минимальная и максимальная величины по всем показателям i -й группы для выбранных k и l.
В целях перевода статистических измерительных безразмерных величин в информацию, нормировали величины (2) так, чтобы результаты p ( kl ) нормировки n обрели свойства вероятности –
V P< kl ) - 1 p nkl ) ^ [0,1] и ^ =1 n и.
P ( kl ) = n
у( kl l ij
g m ( i )
XX Y jkl 1
i = 1 j = 1
i - 1
n = X m(j 1 + j здесь j=1 - общий индекс измеряемо го показателя безотносительно использованного
ранее деления на группы. Рассчитывали общую
энтропию системы сердца по всем нормированным безразмерным показателям (3):
H ( kl 1 =
—
t
X p'k 1 • in( p ;“ ) )
n=1__________________________ ln( t1
Вычисляли среднюю по всем r обследуемым энтропию для каждого периода измерений l:
H ( 1 1 =
r
X H ( kl 1
k = 1
r
Строили графики H(l) от l, отображающие развитие средней энтропии системы сердца у мужчин и женщин в зависимости от сроков имплантации кардиостимулятора.
Результаты и обсуждение
Реполяризация интрамуральных слоев желудочков сердца собаки при ЭКС верхушки правого желудочка. В отличие от синусного ритма, последовательность реполяризации миокарда желудочков повторяет последовательность активации: верхушка правого желудочка реполяризуется через 158.3±27.2 мс, а основание левого – через 223.1±34.8 мс после электрического стимула . Гетерогенность ARI в левом желудочке при ЭКС верхушки правого желудочка становится значимо меньше (35.5±15.1 мс; p<0.05 (рис.1). В обоих желудочках сердца собаки выявлена инверсия апикобазального градиента реполяризации, которая обусловлена изменением распределения интервалов активация – восстановление в субэндокардиальных и интрамуральных слоях. В отличие от синусного ритма меж-
желудочковый градиент реполяризации при ЭКС верхушки правого желудочка выражен в области верхушки и формируется более длительными ARI на верхушке левого желудочка (255.8±45.1 мс) по сравнению с верхушкой правого желудочка (239.0± 44.0 мс; p<0.05).
Реполяризация интрамуральных слоев желудочков сердца собак при предсердно-желудочковой ЭКС (рис.2). Направление апикобазального градиента реполяризации идентично синусному ритму и представлено более короткими ARI на верхушке правого желудочка по сравнению с его основанием (241.1±39.7 и 261.4±38.8 мс, соответственно; p<0.05). В левом желудочке, наоборот, короткие ARI обнаружены в основании по сравнению с его верхушкой (236.4±45.3 и 249.2±38.6 мс, соответственно; p<0.05). При предсердно-желудочковой ЭКС увеличивается дисперсия локальных длительностей реполяризации (88.2±31.3 мс) по сравнению с синусным ритмом (75.1±12.1 мс), что сохраняет электрическую неоднородность миокарда левого желудочка в большей степени, чем ЭКС верхушки правого желудочка. Данный режим ЭКС характеризуется образованием межжелудочкового градиента реполяризации также в основании желудочков, но который, в отличие от синусного ритма, имеет противоположное направление (рис.3). При предсердно-желудочковой ЭКС образуется несколько областей активации миокарда: ранние – в области стимуляции на верхушке правого желудочка через 11.4±7.9 мс от начала стимула и через 22.4±0.4 мс за счет прорыва волны деполяризации в нижней трети межжелудочковой перегородки. Поздние области активации возникают, соответственно, в основании задней стенки левого желудочка через 52.9 ±14.8 мс и на задней стороне верхушки левого желудочка через 56.8 ±13.1 мс. При этом общее время охвата возбуждением миокарда желудочков увеличивается по сравнению с синусным ритмом до 57.1±19.4 мс (p<0.003). На верхушке правого желудочка в зоне стимуляции через 173.9±28.1 мс образуется одна область ранней реполяризации. В нижней трети межжелудочковой перегородки и в основании левого желудочка выявляются две области поздней реполяризации, которые возникают, соответственно, через 245.6±16.9 мс и 234.4±45.6 мс, и общее
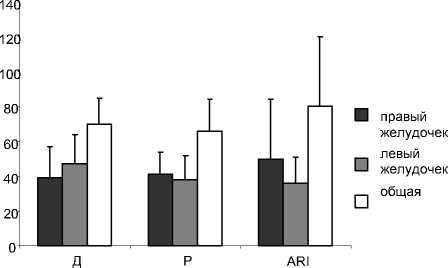
Рис.1. Дисперсии времен деполяризации (Д), реполяризации (Р) и локальных длительностей реполяризации (ARI) миокарда желудочков собак при ЭКС верхушки правого желудочка.
мс
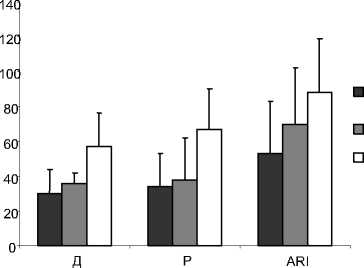
правый желудочек левый желудочек общая
Рис. 2. Дисперсии времен деполяризации (Д), реполяризации (Р) и локальных длительностей реполяризации (ARI) миокарда желудочков собак при предсердно-желудочковой ЭКС .
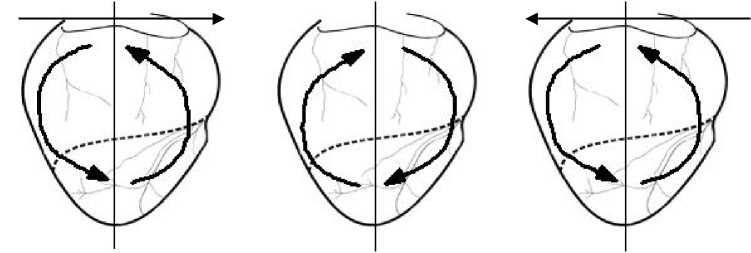
А Б В
Рис.3. Схема изменений направления апикобазального и межжелудочкового градиентов реполяризации сердца собаки при синусном ритме (А), монополярной желудочковой (Б) и предсердно-желудочковой стимуляции (В).
время восстановления возбудимости увеличивается до 64.0±22.9 мс (p<0.01). Детерминированность последовательности реполяризации от активации более значима при предсердно-желудочковой стимуляции, чем при синусном ритме, но меньше, чем при ЭКС верхушки правого желудочка (r= 0.37).
Таким образом, если при синусном ритме миокарду желудочков присущи наличие электрической гетерогенности и независимость пространственно-временных характеристик распределения реполяризации от деполяризации, то ЭКС области верхушки правого желудочка сопровождается возникновением значимой детерминированности последовательности реполяризации от деполяризации, повышением электрической однородности миокарда левого желудочка, повышением трансмурального градиента в основании правого желудочка. Межжелудочковый градиент формируется в области верхушки, а апикобазальный градиент в отличие от синусового ритма инвертируется. При предсердно-желудочковой ЭКС образуются две области ранней активации: в области верхушки правого желудочка и в нижней трети перегородки, вследствие чего электрическая гетерогенность в свободной стенке левого желудочка, в сравнении с ЭКС верхушки правого желудочка, увеличивается, однако не достигает значений синусного ритма. Направление апикобазального градиента реполяризации идентично как при синусном ритме. Межжелудочковый градиент реполяризации формируется в основании сердца, но в отличие от синусного ритма направлен в противоположную сторону (в сторону правого желудочка). Основные изменения в распределении интервалов активация – восстановление при различных режимах ЭКС зарегистрированы в субэндокардиальных и интрамуральных слоях левого желудочка и на верхушке.
Таким образом, ЭКС верхушки правого желудочка и предсердно-желудочковая ЭКС изменяют электрофизиологические характеристики миокарда по сравнению с синусным ритмом. В результате детерминированности процесса реполяризации от деполяризации формируется необходимый уровень электрического ремоделирования в миокарде, вследствие чего происходит локальное и региональное перераспределение механической нагрузки, что является основой последующей быстрой структурной и функциональной перестройки сердца.
Структура и функция сердца пациентов при предсердно-желудочковой ЭКС. Конечный диастолический размер левого желудочка увеличивается с 5.14±0.39 см до 5.38±0.26 (p < 0,05). Продольный систолический размер левого желудочка уменьшается с 6.69±0.45 см до 6.34±0.47 (p < 0,05). Индекс сферичности миокарда левого желудочка в систолу увеличился с 0.52±0.06 до – 0.56±0.05 через два-три года, до – 0.58±0.05 через семь лет (p<0.05). Одновременно с объемными показателями, возрастает индекс массы миокарда с 149.47±31.46 г/м² до 163.86±29.97. В течение первых трех лет ЭКС толщина задней стенки левого желудочка и межжелудочковой перегородки увеличивается соответственно с 1.18±0.18 см до 1.25±0.10, и с 1.32±0.34 см до 1.33±0.31, что отражает, по-видимому, возникновение в миокарде областей, испытывающих большую нагрузку во время ЭКС, которая нивелируется гипертрофией стенок левого желудочка. Выявлена динамическая трансформация геометрических моделей левого желудочка. Исходно в равной степени присутствовали концентрическая и эксцентрическая гипертрофия миокарда левого желудочка. В течение первого года ЭКС увеличивается число концентрической гипертрофии ЛЖ в 1.5 раза, а количество пациентов с эксцентрической гипертрофией миокарда, наоборот, уменьшается. К третьему году ЭКС начинается трансформация типов ремоделирования, увеличивается доля пациентов с эксцентрической гипертрофией миокарда, число которых продолжает нарастать к седьмому году стимуляции (рис.4). Таким образом, в ранний период ЭКС гиперфункция кардиомиоцитов и концентрическая гипертрофия миокарда изменяют эффективную преднагрузку и оптимально переводят напряжение
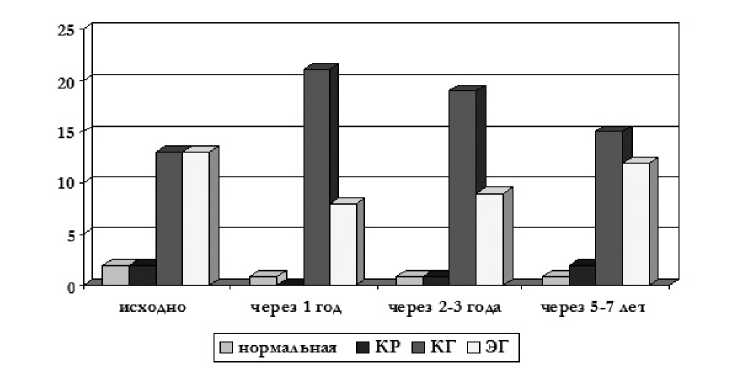
Рис.4. Динамика геометрических моделей левого желудочка (ЛЖ) сердца у пациентов с предсердно-желудочковой ЭКС. Нормальная геометрия миокарда; КР – концентрическое ремоделирование; КГ – концентрическая гипертрофия ЛЖ; ЭГ – эксцентрическая гипертрофия ЛЖ.
казателей качества жизни: показатель социальной активности равен 72.5±4.3%, показатель сравнительной оценки состояния здоровья – 66.7±4.5%, а болевые ощущения сохранялись на уровне 62.3±5.1%. Снижение пациентами оценки физической активности до 27.5±6.2%, а ролевого эмоционального функционирования до 34.4±6.5%. (р<0.05) при сохраненных гемодинамических показателях, указывает на отсут- ствие у пациентов навыков коррекции новых, связанных с ЭКС ощущений, которые воспринимаются, как проявления болезни в стенки левого желудочка во внутрижелудочковое давление на фоне усиливающегося электромеханического асинхронизма. Несмотря на то, что локальные изменения в миокарде могут быть критичными, целое сердце все равно сохраняет функциональную однородность системы, которая реализуется через структурную организацию миокарда и способствует тому, что ранний период ЭКС сопровождается улучшением качества жизни пациентов. В связи с постоянным нарастанием величины миокардиального стресса на третьем году ЭКС формируется тенденция к укорочению продольного систолического размера левого желудочка и увеличивается индекс сферичности миокарда. Подобные изменения в сердце способствуют уменьшению механической нагрузки на миокард левого желудочка вследствие увеличения сферичности миокарда. Именно этот период ЭКС сопровождается ухудшением показателей качества жизни [20], особенно физического статуса, с сохранением исходных параметров центральной гемодинамики и знаменует собой процесс начала долговременной динамической структурно-функциональной организации сердца.
Качество жизни пациентов (таблица). Показатели качества жизни пациентов претерпевают разнонаправленные изменения. Суммарный показатель качества жизни составляет 49.2±4.5%. При этом выявлено снижение всех по-
Показатели качества жизни в зависимости от длительности ЭКС (n=60)
|
Показатели качества жизни, % |
0,5 лет |
1 год |
2 года |
3 года |
4 года |
5 лет |
7лет |
|
Ролевое физическое функционирование |
54±4,1 |
60±2,5 |
54±3,6 |
33±4,5 |
35±6,2 |
75±1,8 |
28±5,6 |
|
Физическое функционирование |
38±12,3 |
39±8,6 |
17±2,4 |
11±5,6* |
25±7,9 |
21±1,5 |
31±0,9 |
|
Боль |
64±5,3 |
73±4,2 |
54±1,3 |
41±3,5 |
31±4,3 |
51±1,9 |
68±5,4 |
|
Оценка здоровья |
47±5,4 |
43±6,8 |
46±5,9 |
59±5,7 |
52±8,6 |
55±4,6 |
52±2,8 |
|
Жизнеспособность |
48±4,3 |
34±2,6 |
52±5,8 |
45±4,9 |
45±2,8 |
50±1,9 |
46±1,4 |
|
Социальная активность |
79±2,1 |
66±4,5 |
60±6,5 |
100±8,1 |
88±0,6 |
75±4,6 |
75±5,6 |
|
Ролевое эмоциональное функционирование |
44±2,4 |
48±2,9 |
17±5,4 |
17±6,8 |
33±3,5 |
33±7,5 |
42±6,8 |
|
Социальное функционирование |
66±5,6 |
40±2,8 |
59±2,9 |
60±5,6 |
80±8,9 |
68±4,6 |
58±5,8 |
|
Сравнительная оценка состояния |
79±2,6 |
75±5,8 |
63±4,6 |
75±8,3 |
50±2,5 |
50±1,9 |
44±5,6 |
*- р<0,05 внутри подгруппы в соответствии с критерием Ньюмена - Кейлса.
условиях отсутствия ожидаемого комфорта. Анализ в подгруппах выявил значимое снижение пациентами оценки физической активности в возрасте от 50 до 59 лет (р<0.05), особенно низким до 11±5.6% (р<0.05) этот показатель оценивался на третьем году ЭКС, в эти сроки отмечается падение и без того низкого уровня ролевого социального функционирования. В то время как в течение первых двух лет после имплантации ЭКС качество жизни пациентов характеризовалось повышением роли физической и социальной составляющей. На третьем году ЭКС выявлена тенденция к ухудшению качества жизни во всех возрастных группах, независимо от режима стимуляции с последующей стабилизацией показателей к шестому году ЭКС, которые, однако, не достигают прежнего уровня.
Информационно-энтропийная характеристика сердца пациентов с предсердно-желудочковой ЭКС. Исходно величина энтропии у мужчин была ниже, чем у женщин, и составила 0.7896 и 0.7905, соответственно. Прирост энтропии у мужчин в течение первых шести месяцев кардиостимуляции был незначительным, и ее величина равна 0.7897. Величина энтропии в последующие шесть месяцев первого года ЭКС у мужчин отмечалась выраженным ростом значения до уровня 0.7914, при этом график кривой роста приобретал вертикальный подъем. В последующие годы ЭКС в сроки до двух с половиной лет у мужчин выявлено продолжающееся значительное увеличение развития энтропии, которая достигала величины 0.7935. В следующий период ЭКС до шести лет также наблюдалось продолжающееся увеличение энтропии Шеннона до величины 0.7950, однако скорость развития энтропии замедлялась (рис.5). Величина энтропии Шеннона у женщин исходно была выше, чем дивидуальной структурной организации сердца и центральной гемодинамики позволяет констатировать, что величина энтропии, отражающая различные и, возможно, разнонаправленные состояния сердца в измеряемых временных интервалах, не выходит за границы определенного физиологического оптимума функционирования сердца и характеризует стремление сердца находиться в пределах физиологического комфорта в течение всего периода кардиостимуляции.
Заключение
Лимитирование электрофизиологических процессов в миокарде, повышение электрической однородности, изменения структурно-функциональной организации сердца и тренд развития величины энтропии сердца позволяют констатировать, что одним
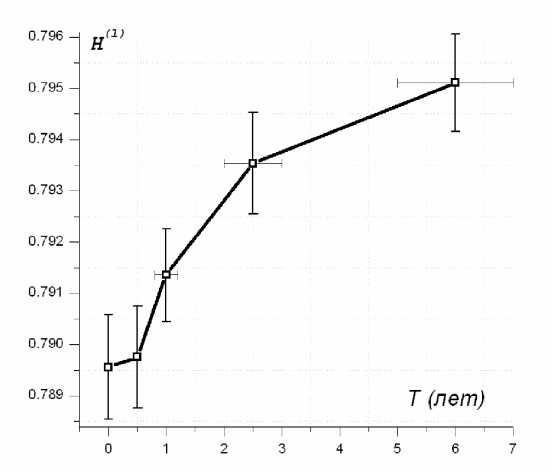
Рис. 5. Динамика развития энтропии сердца у мужчин с предсердно-желудочковой ЭКС в различные сроки кардиостимуляции (объяснение в тексте).
0 1 2 3 4 5 6 7
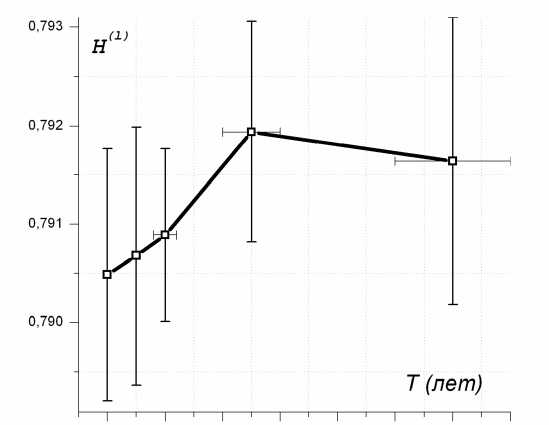
Рис.6. Динамика развития энтропии сердца у женщин с предсердно-желудочковой ЭКС в различные сроки кардиостимуляции (объяснение в тексте).
у мужчин и составляла 0.7905. В течение первых шести месяцев ЭКС величина энтропии увеличилась до 0.7907. При этом скорость нарастания величины энтропии соответствовала скорости роста энтропии мужчин. Второе полугодие ЭКС у женщин в отличие от мужчин не сопровождалось резким ростом значений энтропии. К окончанию первого года ЭКС величина энтропии у женщин была меньше и составляла 0.7909 (у мужчин – 0.7914). В течение первого года ЭКС у женщин установлен равномерный рост энтропии. В сроки стимуляции от одного года до двух с половиной лет выявлено резкое развитие энтропии Шеннона, которая хотя и имела быстрое увеличение до значения 0.7919, но уступала в полтора раза величине энтропии в эти сроки у мужчин (0.7935). Темп развития энтропии у женщин после двух с половиной лет ЭКС замедлялся, и становился меньше (0.7917), чем у мужчин (0.7950) (рис.6). Развитие энтропии сердца у мужчин и женщин свидетельствует о том, что воздействие ЭКС на подсистемы сердца вызывает одинаковые реакции со стороны сердца, но у мужчин влияние ЭКС на сердце более выражено. Динамика ин- из механизмов поддержания функционирования сердца в условиях его системной автономности и изоляции при длительной ЭКС является «упрощение» параметров структурно-функциональной организации миокарда. Для сохранения основной целеполагающей функции сердце платит большую «цену» через динамично образующиеся структуры, которые, в свою очередь, претерпевают развитие « от сложного к простому».
Таким образом, перераспределение локальной и региональной работы сердца на новый энергетический уровень, включение механизмов осуществления оптимальных функциональных связей физиологических систем организма, управляющих переходом от одного способа гомеостаза к другому и определяющих так называемое «функциональное» ремоделирование миокарда, является по сути доминирующей составляющей в структурно-функциональной организации сердца в течение первых трех лет ЭКС и характеризуется улучшением качества жизни пациентов и сопровождается ростом энтропии сердца, поэтому в ранний период ЭКС возможны обратимость структурной организации сердца и уменьшение энтропии.
Переключение процессов управления с энергетического уровня на филогенетический является доминирующим после трех лет ЭКС и узловым моментом в функциональной деятельности сердца, расширяя или сужая для пациентов сферу жизнедеятельности, имеет свою биологическую или структурную «цену», зависит от интенсивности триггерных механизмов, реализующих эволюционную программу инвариативности сердца. В этот период ЭКС происходит уменьшение и даже распад функциональных связей между органами и системами организма ввиду их физиологической нецелесообразности в сохраняющихся условиях протезированной системной функции сердца, поэтому обратимость в структурной организации сердца становится в принципе невозможна. Рост энтропии в этом случае является уже мерой необратимости структурной организации сердца и характеризует протекание процессов в направлении, совпадающем с эволюционным старением системы, а направление вектора времени внутри системы сердца, наоборот, в обратную сторону.
-
1. Продолжительная электрокардиостимуляция при имплантируемых ЭКС кардинально изменяет структурно-функциональную организацию сердца: лимитирует электрофизиологические процессы, создавая тем самым условия для динамической перестройки структур сердца в формы целесообразных моделей функционирования. Электрокардиостимуляция изменяет качество жизни пациентов, ограничивая мотивационный механизм взаимодействия пациента и социума.
-
2. В течение первых двух лет электрокардиостимуляция повышает физическую и социальную составляющие качества жизни. На третьем году происходит их значительное снижение с последующей инверсией физической составляющей зоны комфортности на социальную за счет возрастающих социальных ожиданий.
-
3. Анализ информационной энтропии позволяет количественно осуществлять интегративную оценку функционального состояния сердца. При электрокардиостимуляции развитие информационной энтропии сердца сопровождается постоянным ростом ее величины и претерпевает изменения, отражающие физиологические особенности функционирования сердца во временных интервалах, соотносится с динамикой структурных преобразований в сердце, носит нелинейный фазовый характер и происходит по скачкообразной траектории, предопределяя периоды трехлетних устойчивых циклов функционирования системы сердца.
Исследование поддержано Уральским отделением РАН (Программа Президиума РАН и Программа поддержки совместных проектов, выполняемых с ДВО РАН).
Список литературы Интегративный анализ взаимодействия электростимуляционной системы и сердца
- Мюжика Ж., Егоров Д., Барольд С. Новые перспективы в электрокардиостимуляции. СПб.: Сильван, 1995. С.162-170.
- Хирманов В.Н., Шальдах М., Юзвинкевич С.А. Возможности современной электрокардиостимуляции в лечении сердечной недостаточности//Сердечная недостаточность, 2001. Т.2. №5. С.228-230.
- Бокерия Л.А., Ревишвили А.Ш., Дубровский И.А. Состояние электрокардиостимуляции в России в 2005 году//Вестник аритмологии, 2007. №47. С.5-9.
- Akar F.G., Laurita K.R., Rosenbaum D.S. Cellular basis for dispersion of repolarization underlying reentrant arrhythmias//J. Electrocardiol., 2000. Vol.33. P.23-31.
- IKr contributes to the altered ventricular repolarization that determines long-term cardiac memory/M.N.Obreztchickova, K.W.Patberg, A.Plotnikov, N.Ozgen, I.N.Shlapakova, A.V.Rybin, E.A.Sosunov, P. Jr.Danilo, E.P.Anyukhovsky, R.B.Robinson, M.R.Rosen//Cardiovasc. Res. 2006. Vol.71. P.88-96.
- Prinzen F.W., Peschar M. Relation between the pacing induced sequence of activacion and left ventricular pump function in animals//Pacing Clin. Electrophysiol., 2002. Vol.25. Р.484-498.
- Борн М. Моя жизнь и взгляды. М.: Прогресс, 1973. С.141-158.
- Anyukhovsky E.P., Sosunov E.A., Feinmark S.J., Rosen M.R. Effects of quinidine of repolarization in canine epicardium, midmyocardium, and endocardium: II. In vivo study//Circulation, 1997. Vol.96. Nо. 11. P.4019-4026.
- Asynchronous electrical activation induces asymmetrical hypertrophy of the left ventricular wall/M.F.M.Van Oosterhout, F.W.Princen, T.Arts, J.J.Schreuder, W.Y.R.Vanagt, J.P,M.Cleutjens, R.S.Reneman/Circulation, 1998. Vol.98. P.588-595.
- Andersen H.R., Nielsen J.C. Single-lead ventricular pacing is no longer an option for sick sinus syndrome//J. Am. Coll. Cardiol, 2004. Vol.43. Nо. 11. P.2072-2074.
- Шумаков В.И., Бляхман Ф.А. Связь механической неоднородности миокарда с функциональным резервом сердца//Тез. Рос. нац. конгр. кардиологов. СПб., 2002. С.472.
- Проценко Ю.Л. Влияние неоднородности и нелинейности механических характеристик миокарда на его сократимость: Диссертация в виде научного доклада. Сыктывкар, 2005. С.11-13, 30-32.
- Фролов В.А., Моисеева Т.Ю. Живой организм как информационно-термодинамическая система//Вестник Российского университета дружбы народов: Серия «Медицина», 1999. №1. С.6-14.
- Нестеров В. Теория квантовой энтропийной логики. Международная академия//Межакадемический информационный бюллетень. СПб.: МАИСУ, ИНТАН, 1999. №13-14. С.29-31.
- Кучин Л.Ф., Кулиш С.Н., Черенков А.Д. и др. Информационное поле и его взаимосвязь с окружающим миром//Радiоелектроннi компютернi системи, 2009. №2(36). С.142-147.
- Шеннон К.Э. Работы по теории информации и кибернетике. М., 1963. 827с.
- Мелик-Гайказян И.В. Информационные процессы и реальность. М.: Наука Физматлит., 1998. 192 с.
- Левченко В.Ф., Старобогатов Я.И. Попытка оценки биоразнообразия в палеоэпохи//Теоретические основы биоразнообразия. СПб., 2000. С.35-38
- Нужный В.П., Шмаков Д.Н., Азаров Я.Э., Нужная Т.Г. Качество жизни пациентов с имплантированной кардиостимуляционной системой//Анналы аритмологии, 2008. №1. С.75-87.
- Galtes I., Lamas G.A. Cardiac Pacing for Bradycardia Support: Evidence-based approach to pacemaker selection and reprogramming//Curr. Treat. Options Cardiovasc. Med., 2004. Vol.6 (5). Р.385-395.
- Cost-effectiveness of physiological pacing: results of the Canadian Health Economic Assessment of Physiologic Pacing/B.J.O' Brien, G.Blackhouse, R.Goeree, J.S.Healey, R.S.Roberts, M.Gent, S.J.Connolly. Heart Rhythm. 2005. Vol.2(3). Р.270-275.
- Total Excitation of the Isolated Human Heart/D.Durrer, R.Van Dam, G.Freud, M.Janse, F.Meijler, R. Arzbaecher//Circulation, 1970. Vol.41, Nо.6. P.899-912.
- Scher A.M., Young A.C. The pathwаy of ventricular depolarization in dog//Circ. res., 1956. Vol.4. P.461-469.
- Многоканальная система для синхронной регистрации электрического поля сердца/М.П.Рощевский, Д.Н.Шмаков, И.М.Рощевская, А.В.Плосков, М.Ю.Камбалов, В.А.Витязев, Н.В.Артеева//Тезисы докладов XVIII съезда физиологического общества им.И.П.Павлова. Казань, 2001. С.418
- Шиллер Н., Осипов М.А. Клиническая электрокардиография. М., 1992. С.21-27.
- Виноградова Т.С. Инструментальные методы исследования сердечно-сосудистой системы. М.: Медицина, 1986. С.284-385.
- Ganau A., Devereux R.B., Roman M.J. Patterns of left ventricular hypertrophy and geometric remodeling in essential hypertension//J. Am. Coll. Cardiol., 1992. Vol.19. P.1550-1558.
- Ware JE, Jr, Sherbourne C.D. The MOS 36 -item Short -Form Health Survey (SF-36). (Medical, Outcomes Study -Short Form)//J. Conceptual framework and item selection. Med. Care, 1992. Vol.30. Р.473-83.
- Ратис Е.В., Ратис Ю.Л., Козупица Г.С. Информационно-энтропийный подход к определению здоровья//СПб.: Вестник Балтийской педагогической академии, 1999. №1. Вып.25. С.38-46.


