Искусственный интеллект и нейронные сети в урологии
Автор: Щамхалова К.К., Меринов Д.С., Артемов А.В., Гурбанов Ш.Ш.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Экспериментальная урология
Статья в выпуске: 2 т.16, 2023 года.
Бесплатный доступ
Введение. Обзор посвящен анализу мирового опыта применения искусственного интеллекта в медицине и урологии. Материалы и методы. Обзор проведен на основе данных, опубликованных в базах PubMed, Научной электронной библиотеки eLibrary.ru и сайтах профессиональных медицинских ассоциаций. В статью отобрано 43 научных публикаций. Результаты. В обзоре литературы подробно рассмотрены виды нейросетей и особенности их применения. Особое внимание уделено использованию искусственного интеллекта в медицинской визуализации, в частности в урологии. Представлены последние публикации об эффективности и точности разработки применения метода коннеционизма в искусственной нейронной сети (ИНС). Изложены данные о преимуществе и недостатке искусственного интеллекта для прогностической модели. Также нами рассмотрены основные ошибки, отображенные в публикациях, касающиеся недостоверных или некачественно созданных нейросетей и исследований при применении ИНС для клинической практики. Выводы. Применение нейросетей как инструмента в ежедневной клинической практике специалиста все еще ограничено. Главными проблемами остаются недостоверность созданных моделей и отсутствие удобных в работе алгоритмов.
Искусственная нейронная сеть, искусственный интеллект, машинное обучение, урология
Короткий адрес: https://sciup.org/142239000
IDR: 142239000 | DOI: 10.29188/2222-8543-2023-16-2-32-37
Artificial intelligence and neural networks in urology
Introduction. The review is devoted to the analysis of the world experience in the use of artificial intelligence in medicine and urology. Materials and methods. The review was conducted on the basis of data published in the PubMed, Scientific Electronic Library eLibrary.ru databases and on the professional medical associations websites. The article contains 43 scientific publications. Results. In this literature review, the types of neural networks and the features of their application are considered in detail. Special attention is paid to the use of artificial intelligence in medical imaging, particularly in urology. Effectiveness and accuracy of developing the connectionism method application in artificial neural network (ANN) in recent publications are presented. Advantages and disadvantages of artificial intelligence for a predictive model are outlined. We also considered the main mistakes displayed in publications regarding unreliable or poorly created neural networks and studies in the use of ANNs for clinical practice. Conclusion. The use of neural networks as a tool in the daily clinical practice of a specialist is still limited. The main problems are still the unreliability of the created models and lack of easy-to-use algorithms.
Текст научной статьи Искусственный интеллект и нейронные сети в урологии
Для наиболее успешного выбора тактики лечения пациента необходимо учитывать множество факторов: особенности течения заболевания, сопутствующие заболевания, конституционные, генетические факторы и т.д. Помимо этого специалист должен иметь представление обо всех особенностях применения современных методов лечения, как хирургических, так и консервативных. Обычно, с годами в течение работы, накапливая опыт и знания из своей практики, литературы и опыта других специалистов, врач формирует свой алгоритм лечения пациентов в каждом отдельном клиническом случае. Главным ограничением для специалиста при обработке большого объема данных является время [1].
Вследствие этого возникает ряд последовательных ошибок, приводящих к неблагоприятным последствиям. Так, например, ежегодно в США смертность от неправильно поставленного диагноза и тактики лечения среди госпитализированных пациентов составляет около 80 000 человек [2].
Развитие современных технологий,таких как искусственный интеллект (ИИ), позволяет мимикрировать под когнитивные функции человека, сокращая время для обработки больших объемов данных и позволяя использовать точное прогнозирование для персонализированного лечения пациента [3].
Эти преимущества дали возможность для широкого применения ИИ в медицине и других сферах [4–7]. Термин искусственный интеллект можно отнести к области компьютерных наук, впервые его ввел ученый специалист в области компьютерных технологий John McCarthy в 1956 году [8]. Под термином ИИ подразумевается применение автоматизированного или компьютерного моделирования поведения человека для решения сложных задач [9].
МАТЕРИАЛЫ И МЕТОДЫ
Обзор проведен на основе данных об использовании искусственного интеллекта в медицине, опубликованных в базах PubMed pubmed/), Научной электронной библиотеки и веб-сайтах профессиональных ас-социаций.В данном обзоре особое внимание уделено исследованиям о применении ИИ в урологии. Поиск в базах осуществлялся по следующим ключевым словам: машинное обучение (machine learning), искусственный интеллект (artificial intelligence), нейронные сети (neural networks). Были найдены данные с 1976 по 2022 гг. Из них были исключены короткие сообщения, тезисы и неактуальные данные. После чего, исходя из последовательности изложения материал в рукописи и импакт-факторов,было отобрано 43 источника для цитирования.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Существуют три подхода к ИИ: символизм (основанный на «символическом» (человекочитаемом) методе, такой как IBM Watson на начальном этапе разработки), коннекционизм (на основе таких методов как глубокое обучение или искусственная нейронная сеть) и Байесовский (на основе теоремы Байеса) [6].
Машинное обучение (МО) – это набор методов которые автоматически обнаруживают шаблоны, заданные ранее в представленных данных, а затем используют их для прогнозирования. МО – это класс методов искусственного интеллекта.
В работах A. Newell и H.A. Simon разработана так называемая парадигма символьной обработки информации. Авторы выдвинули гипотезу о физической символьной системе, в соответствии с которой человеческое мышление представляет собой некоторую систему оперирующую с материальными символами, отображающими действительность [10].
Символизм стал одним из самых используемых методов ИИ в медицине, получив широкое распространение в медицинской визуализации [11–16]. В урологии применение методов ИИ позволило добиться высоких результатов диагностики и прогнозирования рака предстательной железы [16]. Первые данные были продемонстрированы в 1994 году P. Snow и соавт. о возможности применения ИИ при прогнозированиирезультатов биопсии у мужчин с аномалиями уровня простатспецифи-ческого антигена (ПСА), атакже для определения исхода лечения после радикальной простатэктомии [17].
В современных исследованиях T.H. Nguyen и соавт. достигли 97% точности при диагностике рака предстательной железы на основе оцифрованных гистологических исследований, а в работах A. Algohary и соавт. алгоритмы машинного обучения позволили увеличить точность диагноза на 33-80% при отрицательных результатах биопсии, выполненной под контролем магнитно-резонансной томографии (МРТ) и на 30–60% – при положительных результатах биопсии [18-19].
С целью оптимизации лечения мочекаменной болезни J. Jendeberg и соавт.применили нейронную сеть, которая дифференцировала камни дистального отдела мочеточника от флеболитов. Данные ИИ и специалистов сравнивались для оценки эффективности разработанного алгоритма. Всего был исследован 341 пациент, которые были поделены на три группы: с камнем в дистальном отделе мочеточника, с флеболитом глубоких вен таза, либо итем и другим. Точностьдиагностики составила 94%,90% и 92% соответственно. Средняя точность диагностики врачом-рентгенологом составляла 86% [20].
-
A. Parakh и соавт. применили в своей работе искусственную нейронную сеть (ИНС) глубокого обучения с каскадным классификатором. На первом этапе изображение вручную сегментировалось на участки тела,
экспериментальная и клиническая урология №2 2 0 2 3 корректировалась ось изображения и оттенки серого кодировались в многооконный формат RGB. Затем ИНС-1 анализируя изображения, определяла участки снимка отображающие мочевые пути. На последнем этапе ИНС-2 выявляла на определенныхучастках изображения конкрементов (рис. 1). Изображения делились не только по наличию или отсутствию конкрементов мочевых путей (почки, мочеточника или мочевого пузыря), но и по объему каменной нагрузки. Выборка пациентов составила 435 пациентов, всем пациентам проводилось компьютерная томография, затем пациенты были поделены на 2 группы с камнями (229 пациентов) и без (206). Точность диагностики составила 95% [21].
Рассматривая альтернативный метод ИИ, такой как коннекционизм, необходимо отметить особенности его применения в медицине и нереализованный потенциал вместе с его недостатками. Коннекционизм состоит в предположении, что когнитивные функции, такие как мышление, могут быть описаны сетями взаимосвязанных элементов, составляющих нейронную сеть. Каждая ИНС содержит три слоя: задача первого «входного» слоя – обработать информацию. Следующий слой «скрытый» (их может быть довольно большое количество). Их задача – та, ради которой строилась нейронная сеть: анализ. И задача «выходного» слоя – представить информацию в конечном виде. Каждый узел – это искусственный нейрон или элементарный процессор (рис. 2) [22].
Построение нейронной сети включает в себя процесс обучения,т.е. применение данныхдля «тренировочного набора». В процессе «тренировки» связи между отдельными узлами изменяются, на последующем этапе с новыми дан-нымипроверяется,насколькоуспешнообучилась ИНС [23].
Ш.Х. Ганцев и соавт. предложили ИИ для прогнозирования результатов лечения рака мочевого пузыря, ис-
Входные данные
Input data
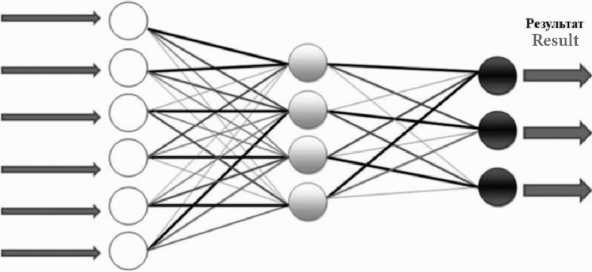
Входной слои Скрытый слой Выходной слон
Input layer Hidden layer Оutput layer
Рис.2. Упрощенная модель нейросети [24]
Fig.2. Simplified neural network model [24]
пользуя клинические и морфологическиеданные, атакже учитываяуже проведенное раннее лечение пациента [25].
В исследовании О.И.Аполихина и соавт. было предложено использование ИИ для расчета индивидуального риска сердечно-сосудистых заболеваний у пациентов с эректильной дисфункцией. Точность прогноза составила 80,3% [26].
Нейронные сети в урологии получили свое распространение не только в области методов визуализации, онкоурологии и андрологии, но и для прогностической модели в лечении мочекаменной болезни (МКБ).
В работе С.А. Голованова и соавт. была разработана модель машинного обучения, позволяющая диагностировать химический состав камня in vivo по результатам метаболических показателей мочи и крови пациентов с МКБ. Точность прогнозирования составила 99,5–100% [27].
Для прогнозирования полного устранения камней (stone free) после перкутанной нефролитотрипсии A. Aminsharifi и соавт. разработали ИИ на основе данных 254 пациентов, позволяющий определять наличие или от-
Обработка
КТ сканCT scan
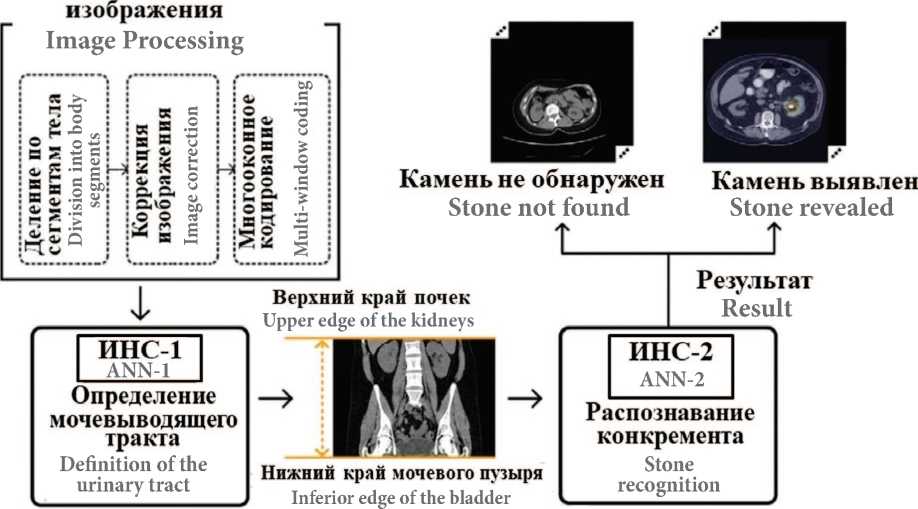
Рис.1. Схематическое изображение этапов предварительной обработки и поэтапного распознавания КТ-скана двумя нейронными сетями [21]
Fig. 1. Schematic representation of the stages of pre-processing and stage-by-stage recognition of a CT-scan by two neural networks [21]

сутствие резидуальных камней с точностью до 82,8%. В работе применялись не только такие данные как размер конкремента или аномалии развития верхних мочевыводящих путей, но и уровень гемоглобина, индекс массы тела (ИМТ), локализация конкрементов (в чашечно-лоханочной системе (ЧЛС)) и т.д. с целью расчетапослеопе-рационных осложнений [24].
M.Y. Yang и соавт применили ИНС для прогностической модели «stone free rate» при использованииретроград-ной интраренальной хирургии, исследовав данные 201 пациента. В работе при построениимодели они учитывали множество факторов, такие как возраст пациента, ИМТ, ко-личество,размер и плотность конкрементов и наличие или отсутствие гидронефроза. Висследовании было создано две прогностические модели, общая точность, специфичность и чувствительность моделей составила 76% [28].
-
I. Seckiner и соавт. разработали нейросеть с учетом совокупности характеристик конкремента, анатомии почек и конституции человека для определения эффективности дистанционной нефролитотрипсии и добились точности в 99% [29].
А.Г. Коцарь и соавт разработали математическую модель прогнозирования рецидива МКБ, которая продемонстрировала специфичность и чувствительность 98 и 89 % соответственно [30]. Также Ф.П. Капсаргиным и соавт. был разработан ИИ, определяющий наиболее оптимальную хирургическую тактику лечения МКБ, при этом ошибка ИИ составила около9% (в работе были использованы методы консервативной терапии, дистанционной литотрипсии (ДЛТ), перкутанной нефролито-трипсии, контактной уретеролитотрипсии, открытых операций) [31].
Одна из наиболее крупных работ с применением ИНС была представлена А.В. Ершовым и соавт. В работе было исследовано 625 пациентов с МКБ. Предметом исследования было определение эффективности нейросетевых алгоритмов с целью прогноза развития послеоперационных осложнений прихирургическом лечении нефролитиаза. Пациенты были поделены на группы по расположению конкрементов в ЧЛС, по наличию или отсутствию обструкции пиелоуретрального сегмента, по структурным изменениям мочевых путей (таких как добавочный нижнеполярный сосуд, нефроптоз, удвоение почки и т.д.), по бактериурии, наличию или отсутствию кист почек, цистита или хронического пиелонефрита в анамнезе и т.д. Также при построении нейронной сети учитывались данные сопутствующих заболеваний, такие как заболевания легких, сахарный диабет или ожирение. При диагностике всем пациентам выполнялось ультразвуковое исследование (УЗИ) мочевыделительной системы, и 500 пациентам потребовалось выполнение мультиспиральной компьютерной томографии (МСКТ). Пациенты, которым выполнили сеансы ДЛТ, составили 297 человек, применение перкутанной нефролитотрип-сии потребовалось для 266 человек, 62 пациентам была выполнена традиционная любмотомия. На основе этих данных была разработана нейронная сеть, в дальнейшем была продемонстрирована целесообразность применения разработанной методики в практике врача-уролога [32].
Важно отметить, что ИНС работает только в том случае, если применяется достаточное количество входных данных. Возможность обучения на основе адекватных размеров выборки и непредвзятые наборы для обучения, были признаны наиболее решающими факторами в разработке рабочей модели ИИ [33–34].
Основываясь на систематическом обзоре 22 работ I. Balki и соавт. делают неутешительные выводы о частом пренебреженииучеными расчета объемавыборки в зависимости от применяемых ими алгоритмов и конечных целей исследований. Данная проблема не имеет на сегодняшний день точной практической рекомендации по решению, но полное пренебрежение планирования объема исследований делает эксперименты не рентабельными и даже опасными для медицинского сообщества [36].
В недавней большой статье Ассоциации радиологов Канады также описывается влияние размера данных на эффективность модели, и подчеркнута важность разработки надежных, клинически проверенных моделей для медицинских учреждений [37].
В обзорной статье А.А. Прановича и соавт. представлены исследования, которые, по заключениям авторов, в большинстве случаев не применимы в практике, поскольку используют упрощенные модели МО и обладают малой выборкой данных для обучения. Модели, использовавшие многослойную искусственную нейронную сеть показали более перспективные результаты [38].
Использование «big data» (большихданных)является ограничением применения технологии для создания МО при разработке ИИ для редких заболеваний. Помимо этого, в отличие от проспективных клинических исследований (в которых испытуемые обычно набираются выборочно, в соответствии с критериями включениями и особенностями клинической ситуации), данные, используемые для разработки алгоритма глубокого обучения часто приходится собирать из разных источников, либо значительно уменьшать размер выборки, создавая ИИ на основе недостаточного количества входных данных [39].
Еще одной значительной проблемой является «преувеличение» преимущества ИИ над диагностикой проведенной специалистами. В статье 2013 года E.A. Rafferty и соавт. продемонстрированы результаты исследования на базе 5 крупных медицинских центров которые показали улучшение точности диагностики рака молочной железы с применением МО, в сравнении с диагностикой, выполненной врачами [40]. Дополнительные методы исследования (такие как томосинтез) заложенные в алгоритм программы и ранее недоступные для специалистов ввиду непокрытия их страховыми компаниями,были сразу введены в практику что позволило включить их в медицинскую страховку при диагностике рака молочной железы в США. Тем не менее, крупномасштабное исследование разработанное E.A. Rafferty и соавт. и сравнивающее точность системы ИИ с эффективностью диагностики 101 рентгенолога, не подтвердило преимущество ИИ над специалистами при наличии одинакового количества методов исследований [41].
Соответственно,при сравнении ИИ с работой врачей, необходимо учитывать «идеальные» условия входных данных для алгоритма,которые часто отличаются от клинической практики и возможностей стационарной работы. В публикациях S.M. McKinney и соавт. был представлен алгоритм, который по точности превзошел всех специалистов, с которыми было выполнено сравнение. Затем были представлены данные, где специалисты работали с применением ИИ,что не только увеличило эффективность, но и снизило затраченное время диагностики для врачей на 88% [42].
ИИ применяется во всех областях медицины, на всех этапах диагностики, лечения и прогнозирования отдаленных последствий. В урологии МО все еще инструмент для исследований,не применяемый в ежедневной клинической практике. Это может быть связано как с отсутствием потенциально применимых алгоритмов в работе, так и с высокой стоимостью использования или сложностями введения методов в практику. Одним из главных направлений будущих исследований ИИ в урологии может стать разработка алгоритмов,помогающих специалистам не только диагностировать и лечить персонализировано паци-ента,но и рассчитать стоимость лечения пациентов (данные которых, могут быть применены в дальнейшем при расчетах страховыми компаниями) [43–45].
ЗАКЛЮЧЕНИЕ
Недостаточный объем данных при создании большинства нейросетей приводит к тому, что при использовании алгоритма в клинической работе точность оказывается ниже оценки специалиста,поэтому применение ИИ в ежедневной практике лечащего врача все еще остается в прогнозах по данным публикуемой литературы.
Необходимо разработать полноценный иудобный в работе инструмент для специалиста, который будет подходить и применяться не только в исследовательской деятельности и «идеальных» условиях при разработке ИИ, но и в стационарах разной степени оснащенности. Это позволит сократить время, затрачиваемое врачом,на создание индивидуального алгоритма лечения.
Важной задачей в оптимизации лечения урологических заболеваний должны стать объединение предыдущего опыта разработки ИИ и создание достоверной применимой на практике модели, помогающей в клинической работе уролога.
Список литературы Искусственный интеллект и нейронные сети в урологии
- Mintz Y, Brodie R. Introduction to artificial intelligence in medicine. Minim Invasive Ther Allied Technol 2019;28(2):73–81. https://doi.org/10.1080/13645706.2019.1575882.
- Leape LL, Berwick DM, Bates DW. What Practices Will most improve safety? Evidence-based medicine meets patient safety. JAMA 2002;288(4):501–7. https://doi.org/10.1001/jama.288.4.501.
- Hameed BMZ, Shah M, Naik N, Rai BP, Karimi H, Rice P., et al. The ascent of artificial intelligence in endourology: a systematic review over the last 2 decades. Curr Urol Rep 2021;22(10):53. https://doi.org/10.1007/s11934-021-01069-3.
- Chen J, Asch S. Machine learning and prediction in medicine: beyond the peak of inflated expectations. N Engl J Med 2017;376(26):2507–09. https://doi.org/10.1056/NEJMp1702071.
- Cabitza F, Rasoini R, Gensini GF. Unintended consequences of machine learning in medicine. JAMA 2017;318(6):517–8. https://doi.org/10.1001/jama.2017.7797.
- Lee JG, Jun S, Cho YW, Lee H, Kim GB, Seo JB, Kim N. Deep learning in medical imaging: general overview. Korean J Radiol 2017;18(4):570–84. https://doi.org/10.3348/kjr.2017.18.4.570.
- Kohli M, Prevedello L, Filice R, Geis JR. Implementing machine learning in radiology practice and research. AJR Am J Roentgenol 2017;208(4):754–60. https://doi.org/10.2214/AJR.16.17224.
- Andresen SL. John McCarthy: father of AI. Intell Syst IEEE 2002;17(5):84–5. https://doi.org/10.1109/MIS.2002.1039837.
- Klot CA, Kuczyk MA. Künstliche intelligenz und neuronale netze in der urologie. [Artificial intelligence and neural networks in urology]. Die Urologie 2019;58(3):291–9. https://doi.org/10.1007/s00120-018-0826-9.
- Newell A, Simon HA. Computer science as empirical inquiry: symbols and search. Commun ACM 1976;19(3):113–126. https://doi.org/10.1145/360018.360022.
- Tran WT, Sadeghi-Naini A, Lu FI, Gandhi S, Meti N, Brackstone M, et al. Computational radiology in breast cancer screening and diagnosis using artificial intelligence. Can Assoc Radiol J 2021;72(1):98–108. https://doi.org/10.1177/0846537120949974.
- Esteva A, Kuprel B, Novoa RA, Ko J, Swetter SM, Blau HM, Thrun S. Dermatologist-level classification of skin cancer with deep neural networks. Nature 2017;542(7639):115–8. https://doi.org/10.1038/nature21056.
- Bar A, Wolf L, Amitai O, Toledano E, Einekave E. Compression fractures detection on CT. J Med Imaging 2017;10134:10134. https://doi.org/10.1117/12.2249635.
- Gulshan V, Peng L, Coram M, Stumpe MC, Wu D, Narayanaswamy A, et al. Development and validation of a deep learning algorithm for detection of diabetic retinopathy in retinal fundus photographs. JAMA 2016; 316(22):2402–10. https://doi.org/10.1001/jama.2016.17216.
- Laukamp KR, Thiele F, Shakirin G, Zopfs D, Faymonville A, Timmer M, et al. Fully automated detection and segmentation of meningiomas using deep learning on routine multiparametric MRI. Eur Radiol 2018;29(1):124–32. https://doi.org/10.1007/s00330-018-5595-8.
- Djavan B, Remzi M, Zlotta A, Seitz C, Snow P, Marberger M. Novel artificial neural network for early detection of prostate cancer. J Clin Oncol 2002;20(4):921–9. https://doi.org/10.1200/ JCO.2002.20.4.921.
- Snow PB, Smith DS, Catalona WJ. Artificial neural networks in the diagnosis and prognosis of prostate cancer: a pilot study. J Urol 1994;152(5 Pt 2):1923–6. https://doi.org/10.1016/ s0022-5347(17)32416-3.
- Nguyen TH, Sridharan S, Macias V, Kajdacsy-Balla A, Melamed J, Do MN, et al. Automatic Gleason grading of prostate cancer using quantitative phase imaging and machine learning. J Biomed Opt 2017;22(3):36015. https://doi.org/10.1117/1.JBO.22.3.036015.
- Algohary A, Viswanath S, Shiradkar R, Ghose S, Pahwa S, Moses D, et al. Radiomic features on MRI enable risk categorization of prostate cancer patients on active surveillance: preliminary findings. J Magn Reson Imaging 2018;(48):818–28. https://doi.org/10.1002/jmri.25983.
- Jendeberg J, Thunberg P, Lidén M. Differentiation of distal ureteral stones and pelvic phleboliths using a convolutional neural network. Urolithiasis 2021;49(1):41–9. https://doi.org/10.1007/ s00240-020-01180-z.
- Parakh A, Lee H, Lee JH, Eisner BH, Sahani DV, Do S. Urinary stone detection on CT images using deep convolutional neural networks: evaluation of model performance and generalization. Radiol Artif Intell 2019;1(4):e180066. https://doi.org/10.1148/ryai.2019180066.
- Степанов П. Искусственные нейронные сети. Молодой ученый 2017;138(4):185–7. [Stepanov P. Artificial neural networks. Molodoy uchenyy = Young scientist 2017;138(4):185–7. (In Russian)].
- Zendehdel R, Masoudi-Nejad A, H Shirazi F. Patterns prediction of chemotherapy sensitivity in cancer cell lines using FTIR spectrum, neural network and principal components analysis. Iran J Pharm Res 2012;11(2):401–10.
- Aminsharifi A, Irani D, Pooyesh S., Parvin H, Dehghani S, Yousofi K, et al. Artificial neural network system to predict the postoperative outcome of percutaneous nephrolithotomy. J Endour 2017; 31(5):461–7. https://doi.org/10.1089/end.2016.0791.
- Ганцев Ш.Х., Зимичев А.А., Хрисанов Н.Н., Клементьева М.С. Применение нейронной сети в прогнозировании рака мочевого пузыря. Медицинский Вестник Башкорто- стана 2010;(3):44–46. [Gantsev Sh.Kh., Zimichev A.A., Khrisanov N.N, Klementyeva M.S. Application of a neural network in predicting bladder cancer. Meditsinskiy vestnik Bashkortostana = Bashkortostan Medical Journal 2010;(3):44–6. (In Russian)].
- Аполихин О.И., Ефремов Е.А., Шадеркин И.А., Золотухин О.В., Мадыкин Ю.Ю., Зеленский М.М. Прогнозирование развития эректильной дисфункции и сердечно-сосудистых заболеваний на основании профиля факторов риска. Экспериментальная и клиническая урология 2017;(4):34–41. [Apolikhin O.I., Efremov E.A., Shaderkin I.A., Zolotuhin O.V., Madykin Yu.Yu., Zelenskiy M.M. Prediction of development of erectile dysfunction and cardiovascular diseases based on the risk factors profile. Eksperimentalnaya i klinicheskaya urologiya= Experimental and Clinical Urology 2017;(4):34–41. (In Russian)].
- Голованов С.А., Сивков А.В., Просянников М.Ю., Дрожжева В.В. Метаболические факторы риска и формирование мочевых камней. Исследование IV: Прогнозирование химического состава камня in vivo по метаболическим показателям. Экспериментальная и клиническая урология 2018;(4):54–63. [Golovanov S.A., Sivkov A.V., Prosyannikov M.Yu., Drozhzheva V.V. Metabolic risk factors and urinary stone formation. Study IV: Prediction of the chemical composition of the stone in vivo according to metabolic parameters. Eksperimentalnaya i klinicheskaya urologiya = Experimental and Clinical Urology 2018;(4):54–63. (In Russian)].
- Zhu XH, Yang MY, Xia HZ, He W, Zhang ZY, Liu YQ, et al. Application of machine learning models in predicting early stonefree rate after flexible ureteroscopic lithotripsy for renal stones. Beijing Da Xue Xue Bao Yi Xue Ban 2019;51(4):653–9. https://doi.org/10.19723/ j.issn.1671-167X.2019.04.010.
- Seckiner I, Seckiner S, Sen H, Bayrak O, Dogan K, Erturhan S. A neural network — based algorithm for predicting stone-free status after ESWL therapy. Intl Braz J Urol 2017;43(6):1110–4. https://doi.org/10.1590/S1677-5538.IBJU.2016.0630.
- Коцарь А.Г., Серегин С.П., Новиков А.В. Автоматизированная система поддержки принятия решений уролога по прогнозированию и профилактике камнеобразования при мочекаменной болезни. Урология 2013;(5):16–20. [Kotsar A.G., Seregin S.P., Novikov A.V. Automated urologist decision support system for the prediction and prevention of stone formation in urolithiasis. Urologiya = Urology 2013;(5):16–20. (In Russian)].
- Капсаргин Ф.П., Ершов А.В., Зуева Л.Ф., Мылтыгашев М.П., Бережной А.Г. Применение нейронных сетей в выборе метода лечения мочекаменной болезни. Омский научный вестник 2015;1(138):68–70. [Kapsargin F.P., Ershov A.V., Zueva L.F., Myltygashev M.P., Berezhnoy A.G. The use of neural networks in the choice of treatment for urolithiasis. Omskiy Nauchnyy Vestnik = Omsk Scientific Bulletin 015;1(138):68–70. (In Russian)].
- Ершов А.В., Неймарк А.И., Капсаргин Ф.П., Бережной А.Г., Винник Ю.Ю. Использование нейронных алгоритмов при выборе метода оперативного лечения мочекаменной болезни. Урология 2021;(4)47–52. [Ershov A.V., Neymark A.I., Kapsargin F.P., Berezhnoy A.G., Vinnik Y.Y. The use of neural algorithms when choosing a method of surgical treatment of urolithiasis. Urologiya = Urology 2021;(4):47–52. (In Russian)]. https://doi.org/10.18565/urology.2021.4.47-52.
- Park SH, Han K. Methodologic guide for evaluating clinical performance and effect of artificial intelligence technology for medical diagnosis and prediction. Radiology 2018;286(3):800-9. https://doi.org/10.1148/radiol.2017171920.
- Pellegrini E, Ballerini L, Hernandez MDCV, Chappell FM, González-Castro V, Anblagan D, et al. Machine learning of neuroimaging for assisted diagnosis of cognitive impairment and dementia: a systematic review. Alzheimers Dement (Amst) 2018;10:519–35. https://doi.org/10.1016/ j.dadm.2018.07.004.
- Schnack HG, Kahn RS. Detecting neuroimaging biomarkers for psychiatric disorders: sample size matters. Front Psychiatry 2016;7:50. https://doi.org/10.3389/fpsyt.2016.00050.
- Balki I, Amirabadi A, Levman J, Martel AL, Emersic Z, Meden B, et al. Sample-size determination methodologies for machine learning in medical imaging research: a systematic. Can Assoc Radiol J 2019;70(4):344–53. https://doi.org/10.1016/j.carj.2019.06.002.
- Tang A, Tam R, Cadrin-Chênevert A, Guest W, Chong J, Barfett J, et al. Canadian Association of Radiologists white paper on artificial intelligence in radiology. Can Assoc Radiol J 2018;69(2):120–135. https://doi.org/10.1016/j.carj.2018.02.002.
- Пранович А.А., Исмаилов А.К., Карельская Н.А., Костин А.А., Кармазановский Г.Г., Грицкевич А.А. Искусственный интеллект в диагностике и лечении мочекаменной болезни. Российский журнал телемедицины и электронного здравоохранения 2022;8(1)42–57. [Pranovich A.A., Ismailov A.K., Karelskaya N.A., Kostin A.A., Karmazanovsky G.G., Gritskevich A.A. Artificial intelligence in the diagnosis and treatment of kidney stone disease. Rossiyskiy zhurnal telemeditsiny i elektronnogo zdravookhraneniya = Russian Journal of Telemedicine and E-Health 2022;8(1)42–57. (In Russian)]. https://doi.org/10.29188/2712-9217-2022-8-1-42-57.
- Lakhani P, Sundaram B. Deep learning at chest radiography: automated classification of pulmonary tuberculosis by using convolutional neural networks. Radiology 2017;284(2):574–82. https://doi.org/10.1148/radiol.2017162326.
- Rafferty EA, Park JM, Philpotts LE, Poplack SP, Sumkin JH, Halpern EF, et al. Assessing radiologist performance using combined digital mammography and breast tomosynthesis compared with digital mammography alone: results of a multicenter, multireader trial. Radiology 2013;266(1):104–13. https://doi.org/10.1148/radiol.12120674.
- Rodriguez-Ruiz A, Lång K, Gubern-Merida A, Broeders M, Gennaro G, Clauser P, et al. Stand-alone artificial intelligence for breast cancer detection in mammography: comparison with 101 radiologists. J Natl Cancer Inst 2019;111(9):916–22. https://doi.org/10.1093/jnci/djy222.
- McKinney SM, Sieniek M, Godbole V, Godwin J, Antropova N, Ashrafian H, et al. International evaluation of an AI system for breast cancer screening. Nature 2020;577(7788):89–94. https://doi.org/10.1038/s41586-019-1799-6.
- New F, Somani BK. A complete world literature review of quality of life in patients with kidney stone disease. Curr Urol Rep 2016;17(12):88. https://doi.org/10.1007/s11934-016-0647-6.
- Geraghty R, Jones P, Herrmann T, Aboumarzouk O, Somani BK. Ureteroscopy seems to be clinically and financially more cost efective than shock wave lithotripsy for stone treatment: systematic review and meta-analysis. World J Urol 2018;36(11):1783–93. https://doi.org/10.1007/ s00345-018-2320-9.
- Constanti M, Calvert RC, Thomas K, Dickinson A, Carlisle S. Cost analysis of ureteroscopy (URS) vs extracorporeal shockwave lithotripsy (ESWL) in the management of ureteric stones <10 mm in adults: a UK perspective. BJU Int 2020;125(3):457–66. https://doi.org/10.1111/bju.14938.


