Использование искусственного интеллекта для диагностики пневмонии при COVID-19 и туберкулеза легких в Кыргызской Республике
Автор: Б.Э. Эмилов, А.А. Сорокин, М.А. Жакыпов, А.Б. Кересбекова, О.А. Салибаев, Т.Ч. Чубаков
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Клиническая медицина
Статья в выпуске: 4, 2024 года.
Бесплатный доступ
В настоящее время не вызывает сомнений необходимость контроля таких легочных заболеваний, как COVID-19, вызываемый вирусом SARS-CoV-2, и туберкулез. Одним из важнейших направлений данной работы является быстрая и точная диагностика, в т.ч. с использованием методов визуализации легких, основанных на искусственном интеллекте (ИИ). Цель. Проверка возможности применения ИИ в целях обнаружения пневмонии при COVID-19 и туберкулеза легких на основе цифровых рентгенограмм. Материалы и методы. Исследование включало в себя несколько этапов: разработку модели ИИ для обучения обнаружению пневмонии при COVID-19 и туберкулеза легких; создание базы тестирующих рентгенданных; интерпретацию данных врачами-рентгенологами; использование ИИ в диагностике пневмонии при COVID-19 и туберкулеза легких. Результаты. ИИ продемонстрировал хорошую прогностическую способность (чувствительность – 88,31 % и 83,33 %, специфичность – 96,67 % и 97,78 % для пневмонии и туберкулеза легких соответственно). Он эффективно обрабатывает и анализирует большие объемы данных, что способствует экономии времени врачей. Однако в целях обеспечения большей безопасности ответственность за окончательное заключение должен нести медицинский персонал. Оптимальным представляется сотрудничество врачей-рентгенологов и ИИ, в котором последний вы-полняет роль вспомогательного инструмента в условиях высокой нагрузки или нехватки специ-алистов, что может повысить точность рентгенологических заключений и обеспечить их своевременность.
COVID-19, туберкулез легких, искусственный интеллект, пневмония, рентген-диагностика, машинное обучение
Короткий адрес: https://sciup.org/14132322
IDR: 14132322 | DOI: 10.34014/2227-1848-2024-4-82-98
Artificial intelligence in diagnosing COVID-19 pneumonia and pulmonary tuberculosis in the Kyrgyz Republic
Nowadays, the necessity to control lung diseases such as COVID-19 caused by the SARS-CoV-2 virus and tuberculosis is obvious. One of the most important areas of this work is rapid and accurate diagnostics, including lung imaging based on artificial intelligence (AI). Objective. The aim of the paper is to test AI for detecting COVID-19 pneumonia and pulmonary tuberculosis based on digital X-ray patterns. Materials and Methods. The study included several stages. 1. Development of an AI model for detecting COVID-19 pneumonia and pulmonary tuberculosis. 2. Creation of a test X-ray data base. 3. Interpretation of data by radiologists. 4. Use of AI for diagnosing COVID-19 pneumonia and pulmonary tuberculosis. Results. AI demonstrated good prognostic ability (sensitivity – 88.31 % and 83.33 %, specificity – 96.67 % and 97.78 % for pneumonia and pulmonary tuberculosis, respectively). AI effectively processes and analyzes big data, which saves doctors’ time. However, in order to ensure greater safety, healthcare professionals should bear responsibility for the final diagnosis. The collaboration between radiologists and AI seems to be desirable. AI can be an auxiliary tool in conditions of high workload or shortage of specialists, as it can improve the accuracy of radiological reports and ensure their timeliness.
Текст научной статьи Использование искусственного интеллекта для диагностики пневмонии при COVID-19 и туберкулеза легких в Кыргызской Республике
Введение. COVID-19, вызываемый вирусом SARS-CoV-2, повлиял на здоровье населения во всем мире [1]. Для контроля пандемии COVID-19 необходима быстрая и точная диагностика заболевания [2]. Важно отметить, что SARS-CoV-2 может привести к пневмонии при COVID-19, в связи с чем большое значение приобретает дифференциальная диагностика вирусной, бактериальной и других респираторных инфекций, таких как туберкулезная болезнь (ТБ), с использованием методов визуализации легких [3].
ТБ является основной причиной смерти от одного инфекционного агента, хотя он в значительной степени излечим и предотвратим. Так, в 2019 г. у 2,9 млн чел. из 10 млн заболевших туберкулез не был диагностирован или зарегистрирован во Всемирной организации здравоохранения [4].
Для достижения глобальной цели по искоренению туберкулеза к 2030 г. требуется научно обоснованное использование инновационных инструментов скрининга [5]. Продукты искусственного интеллекта (ИИ) были рекомендованы ВОЗ для интерпретации рентгеновских снимков органов грудной клетки с целью сортировки и скрининга на туберкулез больных от 15 лет и старше [4]. Однако эта рекомендация не предусматривает конкретных продуктов и требует дополнительных исследований. Между тем рынок решений компьютерного обнаружения продолжает расти. Так, например, по состоянию на май 2024 г. в данной сфере насчитывалось 16 продуктов, не говоря уже о тех, которые находятся в стадии разработки [6–8].
Пневмония при COVID-19 [9, 10] и ТБ легких [11–15] на рентген-снимках проявляются по-разному, но могут иметь схожие симптомы, такие как затрудненное дыхание, кашель и лихорадка [16]. В связи с этим для назначения правильного курса лечения необходима надежная система ИИ, которая может обнаруживать и классифицировать различные респираторные заболевания, имеющие перекрывающиеся проявления.
В последнее десятилетие использование ИИ в лучевой диагностике получило широкое распространение: нейронные сети глубокого обучения все чаще используются для анализа результатов рентгенографии органов грудной клетки (РОГК) [17, 18]. Кроме того, возможные будущие периоды пандемии могут привести к росту рабочей нагрузки врачей-рентгенологов, что обусловит острую нуждаемость в новых автоматизированных инструментах анализа изображений, которые будут классифицировать или сегментировать участки рентгенограммы для поддержки диагностического рабочего процесса.
Таким образом, системы поддержки принятия решений на основе ИИ зарекомендовали себя как новая исследовательская тенденция и в сфере здравоохранения [19]. В последние месяцы пандемии автоматизированное обнаружение пневмонии или других заболеваний легких привлекло значительное внимание как клинических исследователей, так и исследователей ИИ. Разработка медицинских систем на основе ИИ, а также их внедрение в медицинскую практику играют все более заметную роль в модернизации лечения [20, 21].
Стандартные методы визуализации, применяемые в диагностике заболеваний легких, включают в себя РОГК и компьютерную томографию (КТ). Безусловно, КТ является золотым стандартом, однако имеет более высокую стоимость, оказывает радиационное воздействие и не всегда легко доступна во всем мире [22]. В то же время РОГК доступна по цене и является одним из наиболее распространенных методов визуализации, используемых в диагностике кардиоторакальных и легочных заболеваний [23–25].
Цель исследования. Проверка возможности применения ИИ в целях обнаружения пневмонии при COVID-19 и туберкулеза легких на основе цифровых рентгенограмм.
Материалы и методы. Исследование включало в себя несколько этапов.
Обучение ИИ состоит в том, что он учится распознавать признаки пневмонии и туберкулеза при любой конфигурации этих заболеваний на рентгенограмме. Именно поэтому данные для машинного обучения были ретроспективными и общее число использованных рентген-снимков составило около 700 тыс. [26].
В целях обработки медицинских изображений в последнее время активно используются методы глубокого машинного обучения [27]. Одним из наиболее эффективных направлений является использование сверхточных нейронных сетей (Convolutional Neural Networks, CNN). CNN включают в себя обширный класс архитектур искусственных нейронных сетей, продемонстрировавших высокие результаты в области компьютерного зрения [28].
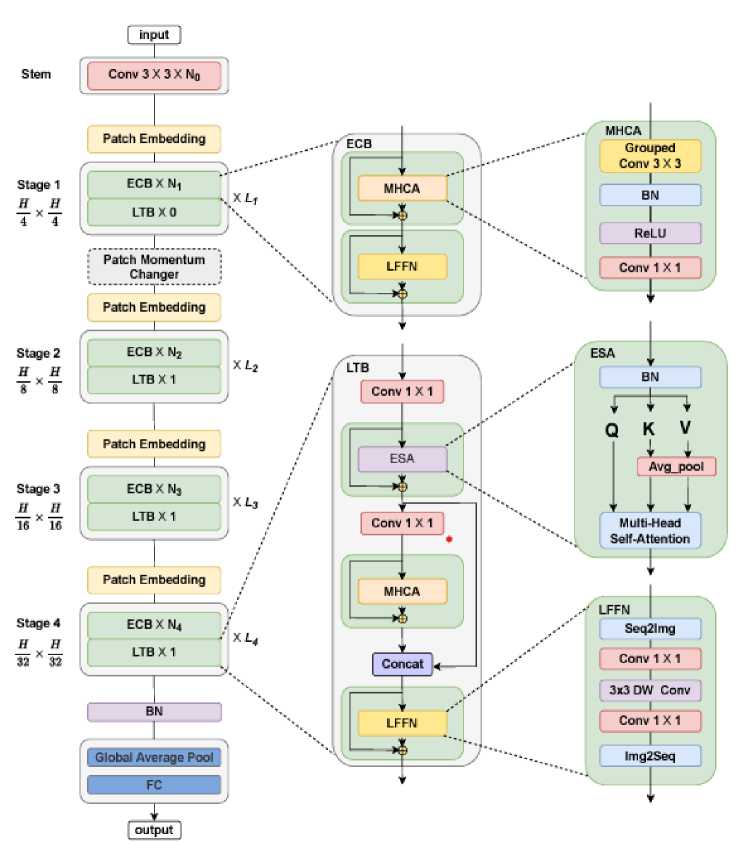
Нами в качестве модели машинного обучения была использована нейронная сеть на базе архитектуры MedVit (рис. 1). В исследовании [29] приведены результаты сравнения качества работы нейронной сети на базе архитектуры MedVit и других систем. Базой для проверки являлись 12 наборов различных по нозологии медицинских данных.
LFFN
Stem
Stage 1 H H
T ' T
Stage 2 H H T^T
Stage 3 и a is x и
Stage 4
H H
32 X $2
LFFN
Patch Embedding
ECBX N1
LTB X 0
Patch Momentum Changer
Patch Embedding
Patch Embedding I
Global Average Pool output
ESA
Conv 3 X 3 X No
ECB X N2
LTB XI
Xi-2
ECB X N4
LJB XI
Q К V
Avg_pool
ESA
Conv1X1
LI B |
Conv1X1
.-•/ECB
MHCA
MHCA | Grouped
Conv 3X3
ReLU
Conv1X1
MHCA
Seq2lmg
| Con cat
LFFN lmg2Seq
Conv 1X1
3x3 DW Conv I Conv1X1
ECB X N)
Xi-3
LJB X 1
Patch Embedding
Multi-Head Self-Attention
Рис. 1. Архитектура нейронной сети MedVit
Fig. 1. Architecture of the MedVit neural network
Нейронные сети семейства архитектур vision transformer эффективны в решении задач классификации медицинских снимков [26]. Во всех экспериментах использовался вариант модели MedViT_large, обученный на ряде крупных открытых наборов данных рентген-снимков грудной клетки: ChestX-ray8 (National Institute of Health, США) [30], CheXpert (Стэнфордский университет) [31], RSNA Pneumonia Challenge [32], MIMIC-CXR (Массачусетский институт технологий) [33].
В данное исследование были включены цифровые рентген-снимки пациентов с подтвержденными в период 2021–2022 гг. пневмонией при COVID-19 и ТБ легких, а также снимки легких без патологических изменений. Рентгенограммы в формате DICOM (Digital Imaging and Communications in Medicine) [34], полученные из нескольких государственных медицинских центров Бишкека, были использованы в качестве базы тестирующих ИИ данных.
На следующем этапе тремя врачами-рентгенологами, работающими в различных клиниках, оценивались характер, полнота, содержание и сущность описаний всех рентген-снимков [9–15]. Исследовательской командой был адаптирован шаблон описания рентгенограмм органов дыхания 1FAIpQLScwy2fdAAbkNX22H634ojnz-quoqL0cq
ZWx5-51KkTvfFsEew/viewform), основанный на рекомендациях И.П. Королюка [35] и
Средний стаж рентгенологов составил 26,6 года.
Всем цифровым рентген-снимкам были присвоены индивидуальные идентификационные номера, которые в целях соблюдения чистоты исследования были разными у каждого врача-рентгенолога. Все рентгенограммы, качество которых исследователи сочли неподходящим или плохим, были исключены, чтобы избежать непредвиденных ошибок в интерпретации.
Для обеспечения возможности использования модели было разработано веб-приложение, которое было размещено на сервере, установленном в центре обработки данных.
Для работы с веб-приложением пользователям предоставлен персональный компьютер с установленным веб-браузером Google Chrome и доступом к Интернету на скорости не менее 512 Kbps. Веб-приложение было протестировано на версиях Chrome 120 и выше. Для стабильной работы браузера рекомендуется не менее 4GB ОЗУ. Доступ к веб-приложению был настроен в рентген-кабинете одной из клиник первичного уровня здравоохранения Кыргызской Республики.
Статистический анализ проводился с использованием программного обеспечения MedCalc 22.021 [36]. В целях определения наиболее эффективного классификатора для диагностики были построены кривые рабочих характеристик приемника (ROC) и проанализирована площадь под кривой (AUC) и 95-процентные доверительные интервалы.
Значение AUC с доверительным интервалом, который не включал значение 0,5, считалось доказательством того, что тест обладал некоторой способностью проводить различие между двумя группами. Оптимальное значение отсечения положительных результатов от отрицательных было оценено с использованием индекса Юдена, который максимизирует разницу между частотой истинно положительных и ложноположительных результатов по всем возможным значениям отсечения. Различия в эффективности распознавания между моделями были проверены на статистическую значимость путем применения теста Делонга [37] к соответствующим значениям AUC.
ROC-кривые являются широко используемым методом оценки диагностических характеристик теста. Путем сопоставления частоты истинно положительных результатов (чувствительность) с частотой ложноположительных результатов (специфичность) для диапазона пороговых значений кривая позволяет оценить общую точность теста при различении положительных и отрицательных случаев. AUC представляет собой сводную статистику кривой ROC, значения которой варьируются от 0,5 (что указывает на случайное предположение) до 1,0 (что указывает на совершенную дискриминацию). Чем выше значение AUC, тем лучше диагностические характеристики теста.
Результаты. Были отобраны 276 и 77 рентгенограмм пациентов с ТБ легких и пневмонией при COVID-19 соответственно, а также 90 рентген-снимков здоровых лиц. Результаты работы ИИ мы сравнили с заключениями 3 врачей-рентгенологов (рис. 2).
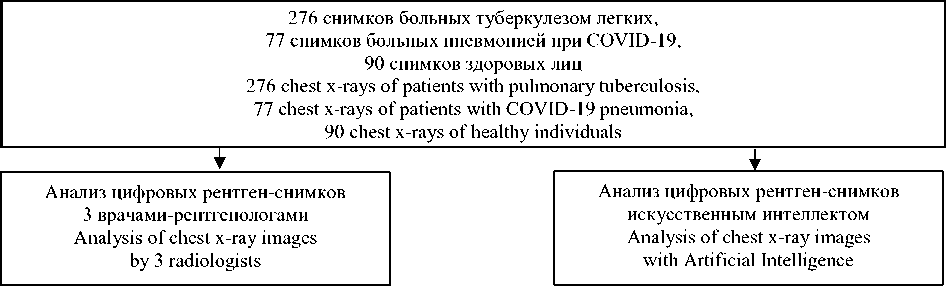
Рис. 2. Схема исследования
Fig. 2 . Study design
Эффективность работы ИИ по выявлению туберкулеза легких практически не отличалась от эффективности работы врачей-рентгенологов, что доказывает хорошую прогности- ческую способность машинного анализа (рис. 3). Аналогичная картина наблюдалась и при диагностике пневмонии как осложнения COVID-19 (рис. 4).
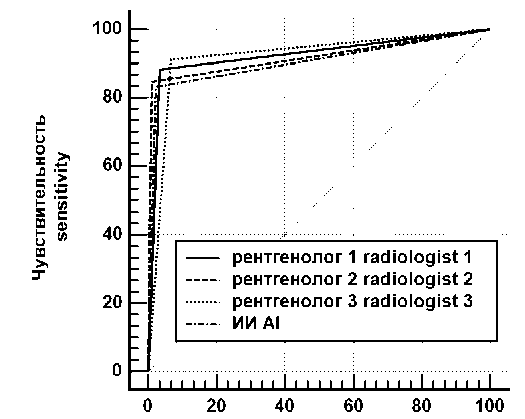
100-специфичность 10О-specificity
Рис. 3. Сравнение ROC-кривых, характеризующих работу рентгенологов и ИИ при диагностике туберкулеза легких
-
Fig. 3. Comparison of ROC curves characterizing the work of radiologists and AI in diagnosing pulmonary tuberculosis
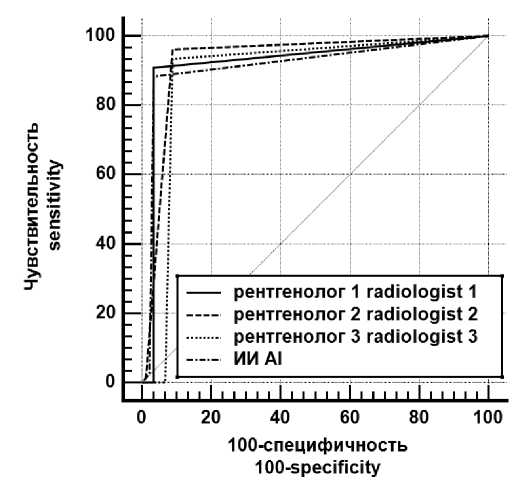
Рис. 4. Сравнение ROC-кривых, характеризующих работу рентгенологов и ИИ при диагностике пневмонии как осложнения COVID-19
-
Fig. 4. Comparison of ROC curves characterizing the work of radiologists and AI in diagnosing COVID-19 complicated with pneumonia
Данные, представленные на рис. 3 и 4, демонстрируют, что площади под кривыми, характеризующими работу врачей-рентгенологов и ИИ, имеют очень близкие значения. Также во всех случаях имеют место очень высокая специфичность и не менее высокая чувствительность.
В целях определения эффективности классификаторов для диагностики были рассчитаны численные характеристики ROC-кривых для больных туберкулезом легких (табл. 1) и COVID-19, осложненным пневмонией (табл. 2).
Таблица 1
Table 1
Численные характеристики ROC-кривых при диагностике туберкулеза легких
Numerical characteristics of ROC curves in patients with pulmonary tuberculosis
|
Переменная Variable |
AUC |
SEa |
95 % CI |
|
Рентгенолог_1 Radiologist_1 |
0,925 |
0,014 |
0,893–0,950 |
|
Рентгенолог_2 Radiologist_2 |
0,918 |
0,012 |
0,885–0,944 |
|
Рентгенолог_3 Radiologist_3 |
0,923 |
0,016 |
0,891–0,948 |
|
ИИ AI |
0,906 |
0,014 |
0,871–0,933 |
Примечание. SE – стандартная ошибка (standard error); a – E.R. DeLong et al. [37]; CI – доверительный интервал (confidence interval). Далее обозначения те же.
Note. SE – standard error; a – E.R. DeLong et al. [37]; CI – confidence interval. Hereafter, designations are the same.
Таблица 2
Table 2
Численные характеристики ROC-кривых при диагностике пневмонии как осложнения COVID-19
Numerical characteristics of ROC curves in patients with COVID-19 complicated with pneumonia
Максимальные значения AUC при выявлении туберкулеза имеют место у врача 1 и врача 3, несколько меньшие – у врача 2 и
ИИ (табл. 1). Однако при диагностике пневмонии как осложнения COVID-19 наибольшие значения AUC характерны для врача 1 и вра-
являются статистически значимыми. Это подтверждается сравнением AUC друг с другом (табл. 3, 4).
Таблица 3
Table 3
Парное сравнение AUC ROC-кривых при диагностике туберкулеза легких Pairwise comparison of AUC-ROC curves in patients with pulmonary tuberculosis
|
Рентгенолог_1 ~ Рентгенолог_2 Radiologist _1 ~ Radiologist _2 |
Рентгенолог_1 ~ Рентгенолог_3 Radiologist _1 ~ Radiologist _3 |
||
|
Z statistic |
0,414 |
Z statistic |
0,139 |
|
Significance level |
p=0,679 |
Significance level |
p=0,889 |
|
Рентгенолог_1 ~ ИИ Radiologist _1 ~ AI |
Рентгенолог_2 ~ Рентгенолог_3 Radiologist _2 ~ Radiologist _3 |
||
|
Z statistic |
1,020 |
Z statistic |
0,258 |
|
Significance level |
p=0,308 |
Significance level |
p=0,796 |
|
Рентгенолог_2 ~ ИИ Radiologist _2 ~ AI |
Рентгенолог_3 ~ ИИ Radiologist _3 ~ AI |
||
|
Z statistic |
0,691 |
Z statistic |
0,912 |
|
Significance level |
p=0,490 |
Significance level |
p=0,362 |
Таблица 4
Table 4
Парное сравнение AUC ROC-кривых при диагностике пневмонии как осложнения COVID-19
Pairwise comparison of AUC-ROC curves in patients with COVID-19 complicated with pneumonia
Данные табл. 3, 4 свидетельствуют о том, что во всех случаях р>0,05, т.е. статистически значимых различий не зарегистрировано.
Аналогичное заключение можно сделать на основании результатов анализа чувствительности и специфичности предикторов (табл. 5, 6).
|
Рентгенолог_1 ~ Рентгенолог_2 Radiologist _1 ~ Radiologist _2 |
Рентгенолог_2 ~ Рентгенолог_3 Radiologist _2 ~ Radiologist _3 |
||
|
Z statistic |
0,292 |
Z statistic |
1,148 |
|
Significance level |
p=0,770 |
Significance level |
p=0,251 |
|
Рентгенолог_1 ~ Рентгенолог_3 Radiologist _1 ~ Radiologist _3 |
Рентгенолог_2 ~ ИИ Radiologist _2 ~ AI |
||
|
Z statistic |
1,137 |
Z statistic |
0,469 |
|
Significance level |
p=0,256 |
Significance level |
p=0,639 |
|
Рентгенолог_1 ~ ИИ Radiologist _1 ~ AI |
Рентгенолог_3 ~ ИИ Radiologist _3 ~ AI |
||
|
Z statistic |
0,206 |
Z statistic |
0,653 |
|
Significance level |
p=0,837 |
Significance level |
p=0,513 |
Таблица 5
Table 5
Оценка чувствительности и специфичности предикторов при диагностике туберкулеза легких
Estimations of sensitivity and specificity of predictors in patients with pulmonary tuberculosis
|
Чувствительность, % Sensitivity in % |
95 % CI |
Специфичность, % Specificity in % |
95 % CI |
|
|
Рентгенолог 1 Radiologist 1 |
88,41 |
84,0–91,9 |
96,67 |
90,6–99,3 |
|
Рентгенолог 2 Radiologist 2 |
84,78 |
80,0–88,8 |
98,89 |
94,0–100,0 |
|
Рентгенолог 3 Radiologist 3 |
91,30 |
87,3–94,3 |
93,33 |
86,1–97,5 |
|
ИИ AI |
83,33 |
78,4–87,5 |
97,78 |
92,2–99,7 |
Таблица 6
Table 6
Оценки чувствительности и специфичности предикторов при диагностике пневмонии как осложнения COVID-19
Estimation of sensitivity and specificity of predictors in patients with COVID-19 complicated with pneumonia
Как видно из табл. 5, 6, значения специфичности всех четырех предикторов довольно близки, тогда как чувствительность ИИ несколько ниже остальных. Это различие статистически не значимо, поскольку доверительный интервал ИИ сильно пересекается с доверительными интервалами других предикторов [36].
Обсуждение. Согласно сложившимся представлениям [38, 39] одной цифровой рентгенограммы легких недостаточно для постановки таких клинических диагнозов, как COVID-19, осложненный пневмонией, или туберкулез
легких. Необходимо использовать дополнительные источники информации. В качестве одного из них может выступать ИИ.
В этом исследовании оценивалась эффективность работы ИИ, который был обучен обнаруживать признаки пневмонии при COVID-19 и ТБ легких на рентгенограмме.
ИИ может использоваться для замены или дополнения экспертной интерпретации простой рентгенограммы врачом при скрининге на туберкулез и способен сократить задержки описания снимков при нехватке квалифицированного
В других работах [42–46], в которых применялись модели ИИ для обнаружения пневмонии на рентгенограмме, использовался подход декомпозиции классов с использованием глубокой архитектуры CNN – convolutional neural network (Detrac ResNet). Чувствительность метода составила 97,9 %, хотя эксперимент проводился на меньшем наборе данных [44]. Исследование, в котором использовалась предварительно обученная CNN (ResNet 50), включало только аномальные рентгеновские снимки и показало общую точность 89,2 %. Методы, представленные в этих работах, требуют знаний в области машинного обучения, и их трудно внедрить в клиническую практику [45].
Мы провели независимый анализ интерпретаций трех врачей-рентгенологов и сравнили их рабочие характеристики с характеристиками модели. ИИ продемонстрировал хорошую прогностическую способность (чувствительность – 88,31 % и 83,33 %, специфичность – 96,67 % и 97,78 % для диагностики пневмонии при COVID-19 и туберкулеза легких соответственно). Такие показатели делают модель потенциальным инструментом скрининга для выявления и сортировки пациентов с COVID-19, осложненным пневмонией, и туберкулезом легких. Врачи-рентгенологи могут легко получить доступ к модели и загрузить рентгенограммы, что облегчает ее внедрение в клиническую практику.
Заключение. Одним из главных преимуществ ИИ является способность быстро обрабатывать и анализировать большие объемы данных, что позволяет врачам экономить время и сосредоточиться на более сложных случаях. Это особенно актуально в условиях пандемии, когда нагрузка на медицинские учреждения значительно возрастает. Автоматизация процессов, таких как распознавание паттернов на рентгеновских снимках, может ускорить диагностику и, как следствие, начало лечения.
Однако важно подчеркнуть, что ИИ не может полностью заменить человека. Роль врача в интерпретации результатов остается критически значимой. Несмотря на высокую точность алгоритмов врачи и пациенты часто испытывают недоверие к полностью автоматизированным системам. Ответственность за окончательное заключение должна оставаться за медицинским персоналом, что обеспечивает более высокий уровень безопасности и доверия со стороны пациентов.
Таким образом, идеальным вариантом является сотрудничество врачей и ИИ. Врач может использовать ИИ как дополнительный инструмент, который помогает в принятии решений, особенно в условиях высокой нагрузки или нехватки специалистов. Такое взаимодействие может привести к более точным и своевременным рентгенологическим заключениям, что особенно важно для пациентов с пневмонией и туберкулезом легких.
Итак, интеграция ИИ в лучевую диагностику представляет собой многообещающий шаг вперед, который при правильном подходе может значительно повысить качество медицинской помощи.
Список литературы Использование искусственного интеллекта для диагностики пневмонии при COVID-19 и туберкулеза легких в Кыргызской Республике
- Gorbalenya A.E., Baker S.C., Baric R.S., de Groot R.J., Drosten C., Gulyaeva A.A. The species severe acute respiratory syndrome-related coronavirus: classifying 2019-nCoV and naming it SARS-CoV-2. Nat. Microbiol. 2020; 5: 536-544. DOI: 10.1038/s41564-020-0695-z.
- Chen J., Wu L., Zhang J., Zhang L., Gong D., Zhao Y., Chen Q., Huang S., Yang M., Yang X., Hu S., Wang Y., Hu X., Zheng B., Zhang K., Wu H., Dong Z., Xu Y., Zhu Y., Chen X., Zhang M., Yu L., Cheng F., Yu H. Deep learning-based model for detecting 2019 novel coronavirus pneumonia on high-resolution computed tomography. Sci. Rep. 2020; 10 (1): 19196. DOI: 10.1038/s41598-020-76282-0.
- Zhi Zhen Qin, Melissa S. Sander, Bishwa Rai, Collins N Titahong, Santat Sudrungrot, Sylvain N. Laah, LalMani Adhikari, E. Jane Carter, Lekha Puri, Andrew J. Codlin, Jacob Creswell. Using artificial intelligence to read chest radiographs for tuberculosis detection: a multi-site evaluation of the diagnostic accuracy of three deep learning systems. Sci Rep. 2019. 9: 15000. DOI: 10.1038/s41598-019-51503-3.
- Saskia den Boon, Cecily Miller. WHO operational handbook on tuberculosis. Module 2: screening - systematic screening for tuberculosis disease. Geneva: World Health Organization; 2021. URL: https://iris.who.int/bitstream/handle/10665/340256/9789240022614-eng.pdf?sequence=1 (дата обращения: 25.04.2024).
- Paula I. Fujiwara, Katherine Floyd, Blessina Kumar. A paradigm shift in the fight against tb. Stop TB Partnership. Global Plan to End TB: 2018-2022. Geneva: Stop TB Partnership; 2019. URL: https://stoptb.org/assets/documents/global/plan/GPR_2018-2022_Digital.pdf (дата обращения: 25.04.2024).
- Qin Z.Z., Naheyan T., RuhwaldM., Denkinger C.M., Gelaw S., Nash M., Creswell J., Kik S.V. A new resource on artificial intelligence powered computer automated detection software products for tuberculosis programmes and implementers. Tuberculosis (Edinb). 2021; 127: 102049.
- Qin Z.Z., Barrett R., Del Mar Castro M., Zaidi S., Codlin A.J., Creswell J., Denkinger C.M. Early user experience and lessons learned using ultra-portable digital X-ray with computer-aided detection (DXR-CAD) products: A qualitative study from the perspective of healthcare providers. PLOS ONE. 2023; 18 (2): e0277843. DOI: https://doi.org/10.1371/journal.pone.0277843.
- Liang S., Xu X., Yang Z., Du Q., Zhou L., Shao J., Guo J., Ying B., Li W., Wang C. Deep learning for precise diagnosis and subtype triage of drug-resistant tuberculosis on chest computed tomography. Med Comm. 2024; 5: e487. DOI: https://doi.org/10.1002/mco2.487
- Martinez Chamorro E., Díez Tascon A., Ibanez Sanz L., Ossaba Velez S., Borruel Nacenta S. Radiologic diagnosis of patients with COVID-19. Radiologia (Engl Ed). 2021; 63 (1): 56-73. DOI: 10.1016/ j.rx.2020.11.001.
- Abougazia A., Alnuaimi A., Mahran A., Ali T., Khedr A., Qadourah B., Shareef A., Zitouni S., Kahveci S., Alqudah B., Al Yassin Y., Eldesoky M., Abdelmoneim A., Youssef R. Chest X-Ray Findings in COVID-19 Patients Presenting to Primary Care during the Peak of the First Wave of the Pandemic in Qatar: Their Association with Clinical and Laboratory Findings. Hindawi. Pulmonary Medicine. 2021; 2021: 4496488. DOI: https://doi.org/10.1155/2021/4496488.
- Meyer M., Clarke P., O'Regan A.W. Utility of the lateral chest radiograph in the evaluation of patients with a positive tuberculin skin test result. Chest. 2003; 124: 1824.
- Geng E., Kreiswirth B., Burzynski J., Schluger N.W. Clinical and radiographic correlates of primary and reactivation tuberculosis: a molecular epidemiology study. JAMA. 2005; 293: 2740.
- Khan M.A., Kovnat D.M., Bachus B. Clinical and roentgenographic spectrum of pulmonary tuberculosis in the adult. Am J Med. 1977; 62: 31. DOI: 10.1016/0002-9343(77)90346-1.
- Restrepo C.S., Katre R., Mumbower A. Imaging Manifestations of Thoracic Tuberculosis. Radiol Clin North Am. 2016; 54: 453. DOI: 10.1016/j.rcl.2015.12.007.
- Curry International Tuberculosis Center. Radiographic Manifestations of Tuberculosis: A Primer for Clinicians. Second Edition. URL: https://www.currytbcenter.ucsf.edu/products/view/radiographic-manifes-tations-tuberculosis-primer-clinicians-second-edition-cd-rom (дата обращения: 25.04.2024).
- Ramona Cioboata, Viorel Biciusca, Mihai Olteanu, Corina Maria Vasile. COVID-19 and Tuberculosis: Unveiling the Dual Threat and Shared Solutions Perspective. J Clin Med. 2023; 12 (14): 4784. DOI: 10.3390/jcm12144784.
- Chartrand G., Cheng P.M., Vorontsov E. Deep learning: a primer for radiologists. Radiographics. 2017; 37: 2113-2131.
- Krizhevsky A., SutskeverI., Hinton G.E. Imagenet classification with deep convolutional neural networks. Adv Neural Inf Process Syst. 2012; 2012: 1097.
- Stacey D., Légaré F., Lewis K., Barry M.J., Bennett C.L., Eden K.B., Holmes-Rovner M., Llewellyn-Thomas H., Lyddiatt A., Thomson R., Trevena L. Decision aids for people facing health treatment or screening decisions. Cochrane Database Syst. Rev. 2017; 4 (4): CD001431. DOI: 10.1002/ 14651858.CD001431.pub5.
- Greenspan H., San José Estépar R., Niessen W.J., Siegel E., Nielsen M. Position paper on COVID-19 imaging and AI: From the clinical needs and technological challenges to initial AI solutions at the lab and national level towards a new era for AI in healthcare. Med. Image Anal. 2020: 66: 101800. DOI: 10.1016/j.media.2020.101800.
- Corinne Merle, Vanessa Veronese, Debora Pedrazzoli. Determining the local calibration of computerassisted detection (CAD) thresholds and other parameters: a toolkit to support the effective use of CAD for TB screening. Geneva: World Health Organization; 2021. URL: https://iris.who.int/bitstream/han-dle/10665/345925/9789240028616-eng.pdf (дата обращения: 25.04.2024).
- Andrew A.S. Soltan, Samaneh Kouchaki, TingtingZhu, Dani Kiyasseh, Thomas Taylor, Zaamin B. Hussain, Tim Peto, Andrew J. Brent, David W. Eyre, David Clifton. Artificial intelligence driven assessment of routinely collected healthcare data is an effective screening test for COVID-19 in patients presenting to hospital. medRxiv; 2020. URL: https://www.medrxiv.org/content/10.1101/2020.07.07.20148361v1.full.pdf+html (дата обращения: 25.04.2024). DOI: 10.1101/2020.07.07.20148361.
- Visca D., Ong C.W.M., Tiberi S., Centis R., D'Ambrosio L., Chen B., Mueller J., Mueller P., Duarte R., Dalcolmo M., Sotgiu G., Migliori G.B., Goletti D. Tuberculosis and COVID-19 interaction: A review of biological, clinical and public health effects. Pulmonology. 2021; 27 (2): 151-165. DOI: 10.1016/j.pul-moe.2020.12.012.
- Islam S.R., Maity S.P., Ray A.K., Mandal M. Deep learning on compressed sensing measurements in pneumonia detection. Int. J. Imaging Syst. Technol. 2022; 32 (1): 41-54. DOI: 10.1002/ima.22651.
- Williams G.J., Macaskill P., KerrM., Fitzgerald D.A., Isaacs D., Codarini M., McCaskillM., Prelog K., Craig J.C. Variability and accuracy in interpretation of consolidation on chest radiography for diagnosing pneumonia in children under 5 years of age. Pediatr. Pulmonol. 2013; 48: 1195-1200. DOI: 10.1002/ ppul.22806.
- Shamshad F., Khan S., Zamir S.W., Khan M.H., Hayat M., Khan F.S., Fu H. Transformers in medical imaging: A survey. Med Image Anal. 2023; 88: 102802. DOI: 10.1016/j.media.2023.102802.
- Zhou S.K., Greenspan H., Davatzikos C., Duncan J.S., van Ginneken B., Madabhushi A., Prince J.L., Rueckert D., Summers R.M. A review of deep learning in medical imaging: Imaging traits, technology trends, case studies with progress highlights, and future promises. Proc IEEE Inst Electr Electron Eng. 2021; 109 (5): 820-838. DOI: 10.1109/JPROC.2021.3054390.
- Lecun Y., Bottou L., Bengio Y., Haffner P. Gradient-based learning applied to document recognition, Proceedings of the IEEE. 1998; 86 (11): 2278-2324.
- Manzari O.N., AhmadabadiH., KashianiH., Shokouhi S.B., Ayatollahi A. MedViT: A robust vision transformer for generalized medical image classification. Comput Biol Med. 2023; 157: 106791. DOI: 10.1016/j. compbiomed.2023.106791.
- Xiaosong Wang, Yifan Peng, Le Lu, Zhiyong Lu, Mohammadhadi B., Ronald M.S. ChestX-ray8: Hospital-scale Chest X-ray Database and Benchmarks on Weakly-Supervised Classification and Localization of Common Thorax Diseases. IEEE Conference on Computer Vision and Pattern Recognition (CVPR); 2017: 3462-3471. URL: https://www.researchgate.net/publication/316736470_ChestX-ray8_Hospital-scale_Chest_X-ray_Database_and_Benchmarks_on_Weakly-Supervised_Classification_and_Localiza-tion_of_Common_Thorax_Diseases (дата обращения: 25.04.2024). DOI: 10.1109/CVPR.2017.369.
- Jeremy Irvin, Pranav Rajpurkar, Michael Ko,Yifan Yu, Silviana Ciurea-Ilcus, Chris Chute, Henrik Marklund, Behzad Haghgoo, Robyn Ball, Katie Shpanskaya,Jayne Seekins, David A. Mong, Safwan S. Halabi, Jesse K. Sandberg, Ricky Jones, David B. Larson, Curtis P. Langlotz, Bhavik N. Patel, Matthew P. Lungren, Andrew Y. Ng. CheXpert: A Large Chest Radiograph Dataset with Uncertainty Labels and Expert Comparison. In AAAI Conference on Artificial Intelligence; 2019. URL: http://arxiv.org/ abs/1901.07031 (дата обращения: 25.04.2024).
- Shih G., Wu C.C., Halabi S.S., Kohli M.D., Prevedello L.M., Cook T.S., Sharma A., Amorosa J.K., Arteaga V., Galperin-Aizenberg M., Gill R.R, Godoy M.C.B., Hobbs S., Jeudy J., Laroia A., Shah P.N.,
- Vummidi D., Yaddanapudi K., Stein A. Augmenting the National Institutes of Health Chest Radiograph Dataset with Expert Annotations of Possible Pneumonia. Radiol Artif Intell. 2019; 1 (1): e180041. DOI: 10.1148/ryai.2019180041.
- Johnson A.E.W., Pollard T.J., Berkowitz S.J., Greenbaum N.R., Lungren M.P., Deng C.Y., Mark R.G., Horng S. MIMIC-CXR, a de-identified publicly available database of chest radiographs with free-text reports. Sci Data. 2019; 6 (1): 317. DOI: 10.1038/s41597-019-0322-0.
- Kahn C.E.Jr., Carrino J.A., Flynn M.J., Peck D.J., Horii S.C. DICOM and radiology: past, present, and future. J Am Coll Radiol. 2007; 4 (9): 652-657. DOI: 10.1016/j.jacr.2007.06.004.
- Королюк И.П. Лучевая диагностика: учебник для вузов. 2020; 217.
- MedCalc® Statistical Software version 22.021 (MedCalc Software Ltd, Ostend, Belgium). URL: https://www.medcalc.org (дата обращения: 25.04.2024).
- DeLong E.R., DeLong D.M., Clarke-Pearson D.L. Comparing the areas under two or more correlated receiver operating characteristic curves: a nonparametric approach. Biometrics. 1988; 44: 837-845.
- SayeedaRahman, Maria Teresa VillagomezMontero, KherieRowe. Epidemiology, pathogenesis, clinical presentations, diagnosis and treatment of COVID-19: a review of current evidence. Expert Rev Clin Pharmacol. 2021; 14 (5): 601-621. DOI: 10.1080/17512433.2021.1902303.
- Goletti D., Delogu G., Matteelli A., Migliori G.B. The role of IGRA in the diagnosis of tuberculosis infection, differentiating from active tuberculosis, and decision making for initiating treatment or preventive therapy of tuberculosis infection. Int J Infect Dis. 2022; 124 (1): 12-19. DOI: 10.1016/ j.ijid.2022.02.047.
- Corinne Merle, Vanessa Veronese, Debora Pedrazzoli. Determining the local calibration of computerassisted detection (CAD) thresholds and other parameters: a toolkit to support the effective use of CAD for TB screening. Geneva: World Health Organization; 2021. Licence: CC BY-NC-SA 3.0 IGO.
- Cecily Miller, Annabel Baddeley, Dennis Falzon. WHO consolidated guidelines on tuberculosis. Module 2: screening - systematic screening for tuberculosis disease. Geneva: World Health Organization; 2021. URL: https://www.who.int/publications/i/item/9789240022676 (дата обращения: 25.04.2024).
- Rajaraman S., Antani S. Weakly labeled data augmentation for deep learning: A study on COVID-19 detection in chest X-rays. Diagnostics. 2020; 10: 358. DOI: 10.3390/diagnostics10060358.
- Abbas A., Abdelsamea M.M., Gaber M.M. Classification of COVID-19 in chest X-ray images using DeTraC deep convolutional neural network. Applied Intelligence. 2021; 51: 854-864. DOI: https://doi.org/ 10.1007/s 10489-020-01829-7.
- Hall L.O, Paul R., Goldgof D.B., Rahul P., Gregory M. Finding covid-19 from chest x-rays using deep learning on a small dataset. arXiv preprintarXiv. 2020: 1-8. DOI: https://doi.org/10.48550/arXiv.2004.02060 (дата обращения: 25.04.2024).
- Murphy K., SmitsH., Knoops A.J.G., KorstM.B.J.M., Samson T., ScholtenE.T., Schalekamp S., Schaefer-Prokop C.M., Philipsen R.H.H.M., Meijers A., Melendez J., van Ginneken B., Rutten M. COVID-19 on Chest Radiographs: A Multireader Evaluation of an Artificial Intelligence System. Radiology. 2020; 96 (3): 166-172. DOI: 10.1148/radiol.2020201874.
- Holzinger A., Biemann C., Pattichis C.S., Douglas B.K. What do we need to build explainable AI systems for the medical domain? arXiv. 2017. DOI: https://doi.org/10.48550/arXiv.1712.09923.


