Использование лабораторных показателей свертывающей системы крови у пациентов с фибрилляцией предсердий, принимающих дабигатрана этексилат, для оценки возможного кровотечения при радиочастотной аблации
Автор: Усенков Станислав Юрьевич, Баталов Роман Ефимович, Борисова Елена Вячеславовна, Хлынин Михаил Сергеевич, Арчаков Евгений Александрович, Попов Сергей Валентинович
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 4 т.32, 2017 года.
Бесплатный доступ
В статье приведены результаты, полученные при сравнении показателей гемостаза у пациентов с фибрилляцией предсердий, получавших дабигатрана этексилат в периоперационный и постоперационный периоды на фоне проведения катетерного лечения аритмии, с данными, когда антикоагулянтная терапия не проводилась. Изучалась возможность использования общепринятых показателей свертывающей системы крови у пациентов с фибрилляцией предсердий, принимавших дабигатрана этексилат, для оценки возможного риска кровотечения в периоперационный период при проведении радиочастотной аблации.
Дабигатрана этексилат, фибрилляция предсердий, антикоагулянтная терапия
Короткий адрес: https://sciup.org/149125180
IDR: 149125180 | УДК: 616.125 | DOI: 10.29001/2073-8552-2017-32-4-17-22
The use of blood coagulation laboratory parameters for assessment of bleeding risk during radiofrequency ablation procedure in atrial fibrillation patients receiving dabigatran etexilate
The article presents the results of the analysis of hemostasis parameters in atrial fibrillation patients with and without anticoagulation therapy with dabigatran etexilate in the perioperative period of the arrhythmia ablation. We evaluated the capabilities of using the conventional indicators of the blood coagulation in atrial fibrillation patients receiving dabigatran etexilate to assess the possible risk of bleeding in the perioperative period of radiofrequency ablation.
Текст научной статьи Использование лабораторных показателей свертывающей системы крови у пациентов с фибрилляцией предсердий, принимающих дабигатрана этексилат, для оценки возможного кровотечения при радиочастотной аблации
Общая распространенность фибрилляции предсердий (ФП) в популяции составляет около 2% [1, 2]. При этом распространенность ФП увеличивается с возрастом: от 0,5% у лиц 40–50 лет до 5–15% — у лиц 80 лет [3–6]. ФП не является жизнеугрожающей аритмией, однако ее наличие увеличивает смертность у кардиологических пациентов в 2 раза, риск внезапной сердечной смерти — в 1,3 раза, развития сердечной недостаточности — в 3,4 раза, возникновения ишемического инсульта — в 5 раз [7–10].
Повышение риска развития инсульта и прогрессирование сердечной недостаточности — основное клиническое значение ФП. Острое нарушение мозгового кровообращения с одинаковой частотой регистрируется у пациентов с бессимптомным и симптомным течением ФП. В связи с этим в настоящее время антикоагулянтная терапия является обязательным компонентом лечения ФП вне зависимости от формы аритмии и основывается на оценке риска тромбоэмболических осложнений по шкале CHA2DS2-VASc [1, 10]. Доказано, что антикоагулянтная терапия заметно превосходит по эффективности антитромбоцитарную терапию [2, 11].
Одними из основных препаратов для профилактики инсульта и системных тромбоэмболий являются антагонисты витамина К. Как показал метаанализ плацебокон-тролируемых исследований, прием данных препаратов снижает относительный риск развития ишемического инсульта на 67%, а общей смертности — на 26% [12]. Препарат обладает непредсказуемой фармакокинетикой и фармакодинамикой вследствие как генетических особенностей пациентов, так и специфики его лекарственного метаболизма, требует постоянного лабораторного контроля и имеет длительное время до развития клинического эффекта. В период прерывания приема варфа-рина или на фоне нетерапевтических значений международного нормализованного отношения (МНО) во многих случаях развивается ишемический инсульт [12]. В исследованиях, посвященных новым пероральным антикоагулянтам (НОАК): RE-LY — дабигатрана этексилат, ROCKET-AF — ривароксабан и ARISTOTLE — апиксабан, доказано, что препарат имеет не меньшую, чем варфа-рин, эффективность, а частота крупных кровотечений, как и при приеме варфарина, составляла от 2,13 до 3,6%. Так, исследование RE-LY показало, что частота возникновения ишемического инсульта на фоне приема дабига-трана этексилата в дозе 300 и 220 мг/сут составила 1,11 и 1,53% в год соответственно, а на фоне приема варфари-на — 1,69% [8, 13, 14]. Проведенные метаанализы международных исследований также показывают, что НОАК могут быть безопасной альтернативой варфарину при проведении антикоагулянтной терапии пациентам, подвергающимся катетерной аблации или электрической кардиоверсии при ФП [11, 13].
При приеме дабигатрана этексилата отмечается удлинение активированного частичного тромбопластинового времени (АЧТВ) и тромбинового времени (ТВ). У больных, получающих постоянную терапию дабигатраном в дозе 150 мг 2 раза в сутки, АЧТВ примерно в 2 раза превышает нормальные показатели. В то же время увеличение дозы и, соответственно, концентрации лекарственного вещества в плазме не ведет к пропорциональному удлинению АЧТВ. Иначе говоря, АЧТВ не является специализированным тестом для выявления передозировки препарата. При этом превышение АЧТВ в 2–3 раза выше границы нормы перед приемом очередной дозы препарата было ассоциировано с повышенным риском кровотечения.
Особенно чувствительным тестом для определения действия дабигатрана является ТВ. Оно прямо пропорционально концентрации препарата в плазме. Но и этот тест имеет свои ограничения, так как неинформативен при передозировке препарата. Кроме того, не следует забывать и о том, что тест плохо стандартизован.
Для проведения таких коагуляционных тестов, как АЧТВ и ТВ, необходимо наличие специализированной лаборатории.
Метод определения активированного времени свертывания (ABC) позволяет контролировать и регулировать уровень гепаринизации пациента и оценивать полноту нейтрализации гепарина при проведении катетерного лечения ФП. Большими достоинствами метода являются доступность, простота в выполнении и отсутствие специализированных лабораторных реактивов.
Однако работ, посвященных изучению изменений показателей свертывающей системы крови при приеме НОАК, в настоящее время немного. Цель данного исследования — определение возможности использования общепринятых показателей свертывающей системы крови у пациентов с ФП, принимавших дабигатрана этексилат, для оценки возможного риска кровотечения в перио-перационный период при проведении радиочастотной аблации (РЧА).
Материал и методы
В исследование включено 30 пациентов с персистирующей и пароксизмальной формами ФП, которые на момент поступления в клинику не использовали антикоагулянты, из них было 13 (43%) мужчин. Возраст пациентов составлял от 44 до 71 года, средний возраст — 59,4±7,4 года. Диагноз ишемической болезни сердца верифицирован у 9 пациентов (с пароксизмальной формой ФП — 5 человек), ишемическая болезнь сердца в сочетании с гипертонической болезнью — 10 пациентов (из них 3 — с пароксизмальной формой ФП), хронический миокардит, активность 0 — 3 пациента (у 1 из них пароксизмальная форма ФП), гипертоническая болезнь — 7 пациентов (у 4 из них пароксизмальная форма ФП) и 1 пациент — с гипертрофической кардиомиопатией и персистирующей формой ФП. При поступлении в стационар проводилось стандартное исследование гемостаза. Определяли МНО, АЧТВ, АВС, ТВ до назначения дабига-трана этексилата (далее дабигатран). После этого всем пациентам назначался дабигатран в дозе 150 мг 2 раза в день, и прием препарата продолжался от 3 до 5 дней.
За сутки до операции производили забор крови утром, за 1 ч до приема очередной дозы дабигатрана, для определения показателей гемостаза. Проводили чреспищеводное ультразвуковое исследование (ЧПУЗИ) на предмет обнаружения тромбов в полости левого предсердия и ушке левого предсердия. В день проведения РЧА утром определяли показатели гемостаза, при этом в день операции дабигатран отменяли. Во время операции после пункции межпредсердной перегородки начиналась инфузия гепарина, одномоментно болюсное введение 3000 Ед., затем постоянная инфузия со скоростью 1000 Ед./ч. Каждые 15 мин производилось измерение АВС (значения поддерживались в пределах 300–350 с), по результатам титровали скорость инфузии гепарина. В течение 24 ч после операции продолжалась непрерывная инфузия гепарина. При этом очередной забор крови производили через 16–18 ч после операции на фоне гепаринотерапии. Через 4 ч после отмены гепарина возобновляли прием дабигатрана в дозе 150 мг 2 раза в день. На следующий день утром, через 11 ч после приема препарата, проводили очередной забор крови.
Таким образом, получили следующие контрольные точки: 1-я — при поступлении, когда пациенты не использовали антикоагулянты; 2-я — за сутки перед процедурой РЧА; 3-я — в день вмешательства, 4-я — через 24 ч после процедуры, во время продолжающейся инфузии гепарина; 5-я точка — после отмены гепарина и начала приема дабигатрана.
Всем пациентам проводили оценку гемостаза с использованием прибора ACL TOP Family и реактивов Instrumentation Laboratory Company-Bedford, MA 01730-
Таблица
Показатели гемостаза в контрольных точках
2143 (США). Венозную кровь с цитратом натрия забирали в пробирку Vacutainer, после чего доставляли в клинико-диагностическую лабораторию.
Для оценки АВС нами использовалась система определения коагуляции цельной крови Hemochron® Response производства ITC (США).
Полученные данные подвергались статистической обработке при помощи программы STATISTICA 6.0 for Windows. Данные представлены в виде M±m, где M — среднее значение; m — стандартное отклонение. Количественные показатели, закон распределения которых отличался от нормального, представляли в виде Me (Q25–Q75), где Me — медианное значение показателя, а (Q25–Q75) — интерквартильный разброс. Проверку статистической значимости различий производили с использованием непараметрических критериев. Статистическую значимость различий количественных признаков проверяли при помощи U-критерия Манна– Уитни(сравненияпопарно независимыхгруппданных) и W-критерия Вилкоксона (сравнения попарно связанных групп данных при исследовании динамики показателя внутри группы). Для выяснения значимости различий качественных и ранговых признаков использовали точный тест Фишера (сравнение частотных характеристик качественных признаков). Различия считали статистически значимыми при p<0,05.
Результаты и обсуждение
Полученные результаты представлены в таблице.
|
Показатели |
1-я контрольная точка |
2-я контрольная точка |
3-я контрольная точка |
4-я контрольная точка |
5-я контрольная точка |
|
АЧТВ, с (Me (Q25–Q75)) |
28,4 (26,4–30,2) |
37 (34,1–40,2)* |
35,4 (32,8–40,6)* |
119,3 (93,9–236,6)* |
33,1 (29,3–39,2)* |
|
АВС, с (M±m) |
125,8±17,3 |
157,1±23,2* |
166,6±13,1* |
289,8±18,1* |
155,6±32,4* |
|
ТВ, с (M±m) |
15,5±1,5 |
109,3±40,8* |
122,1±42,6* |
105,3±31,7* |
75,2±52,1** |
|
МНО, отн. ед. (M±m) |
0,95±0,05 |
1,01±0,07** |
1,03±0,08* |
1,07±0,1* |
1,11±0,16* |
Примечание: * — уровень статистической значимости, где р<0,01 в сравнении с 1-й контрольной точкой; ** — уровень статистической значимости, где р<0,05 в сравнении с 1-й контрольной точкой.
При оценке результатов АЧТВ были выявлены статистически значимые изменения (р<0,01), которые характеризовались увеличением значений после начала приема дабигатрана, а также дальнейшим их увеличением при начале использования гепарина, что соответствует действию гепарина (4-я контрольная точка), рис. 1.
Значения АЧТВ после отмены гепарина уменьшились до уровня данных при приеме дабигатрана в сравнении с исходными значениями (р<0,01).
При сравнении показателя АВС на всех контрольных точках при приеме дабигатрана и инфузии гепарина с показателем АВС в исходной точке, когда антикоагулянтная терапия не проводилась, выявлено увеличение АВС до 157,13±23,24 с (р<0,01) во 2-й точке; в точке, когда пациент получал гепарин, показатель АВС достиг в среднем 289,8±18,1 (р<0,01). Прирост показателя АВС у пациентов, принимающих дабигатран, составил порядка 25% от исходного значения. При этом на фоне инфузии гепарина прирост АВС составил более 100% от исходного показателя. Следует отметить, что после отмены гепарина и назначения дабигатрана показатель АВС возвращался к уровню, зарегистрированному до
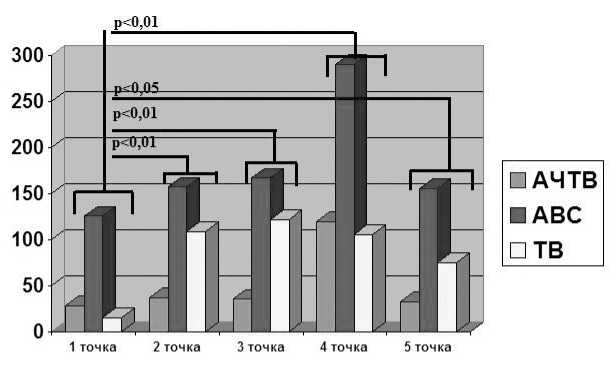
Рис. 1. Динамика изменений показателей гемостаза
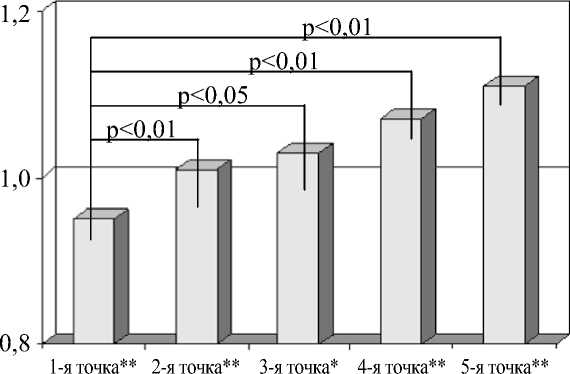
Рис. 2. Динамика изменения МНО Примечание: * — p<0,05; ** — p<0,01.
операции (см. рис. 1). В процессе исследования показателей после операции уровень значений АВС поддерживался в пределах 250–300 мс, что было продиктовано исходной гипокоагуляцией в начале выполнения РЧА и увеличением показателей АЧТВ более 100 с после процедуры.
Изменения ТВ при использовании дабигатрана были наиболее информативны и показательны. При оценке показателей ТВ выявлено его увеличение до 109,3±40,75 с (р<0,01) во 2-й точке, при этом в следующей точке отмечается прирост показателя до 122,1±42,61 с (р<0,01). В точке, когда пациент получал гепарин, показатель ТВ достиг в среднем 105,33±31,67 с (р<0,01), в 5-й точке отмечалось снижение показателя ТВ до 75,18±52,1 с (р<0,05), см. рис. 1.
Снижение ТВ в 5-й точке можно объяснить тем фактом, что пациент к этому моменту не принимал даби-гатран двое суток, и накануне забора крови в 5-й контрольной точке он получил только 1 капсулу дабигатрана в дозе 150 мг.
Интересные результаты получены при определении МНО. Известно, что дабига-тран мало влияет на величину протромбинового времени и, соответственно, на уровень МНО. При статистической обработке данных выявлено статистически значимое увеличение показателя МНО у пациентов, принимающих дабигатран (р<0,05), рис. 2.
Так, после начала приема дабигатрана выявлено увеличение МНО с 0,95±0,05 до 1,01±0,07 Ед. (р<0,05), затем МНО еще больше увеличилось в 3-й точке до 1,03±0,08 Ед. (р<0,01), в 4-й — до 1,07±0,08 Ед. (р<0,01), в 5-й — до 1,11±0,09 Ед. (р<0,01). Плавный прирост МНО к 5-й контрольной точке имеет статистически значимое увеличение, оставаясь в пределах допустимых нормальных значений показателя МНО, и таким образом, данный показатель не является клинически значимым.
За весь период наблюдения у пациентов, принимавших дабигатран, не было зарегистрировано крупных кровотечений, в том числе и в местах пункции бедренной вены. В одном случае перед оперативным лечением у пациентки по данным ЧПУЗИ выявлен тромбоз ушка левого предсердия, образование которого связано с длительностью ФП и отсутствием антикоагулянтной терапии.
Дабигатран является препаратом, не требующим лабораторного контроля. Тем не менее существуют риски кровотечения при проведении катетерного лечения ФП и при инфузии гепарина, когда требуется быстрое определение показателей гемостаза на фоне приема дабигатрана.
Пациенты, принимавшие дабигатрана этексилат, требуют пристального внимания при проведении инфузии гепарина во время РЧА устьев легочных вен во избежание избыточной гипокоагуляции.
Выводы
Нами выявлены изменения, которые при необходимости можно использовать для оценки гемостаза у пациентов, принимавших дабигатран, а именно изменения показателей АЧТВ (в среднем с 28,4 до 37 с) и ТВ (в среднем с 15,5 до 109,3 с), но для их применения требуется наличие реактивов, специализированное оборудование и запас времени.
Показатель АВС (в среднем изменение с 125,8 до 157,1 с) является соизмеримым и легкодоступным методом оценки гемостаза. Увеличение АВС у пациентов, принимающих дабигатран перед РЧА, более чем на 25% требует пристального внимания и возможной коррекции вводимой дозы гепарина в начале катетерного лечения.
Дабигатран в качестве антикоагулянтной терапии у пациентов с неклапанной ФП является удобным и безопасным препаратом. При необходимости оценки риска кровотечений в экстренных ситуациях у пациентов, принимающих дабигатран, возможно применение измерения АВС.
Список литературы Использование лабораторных показателей свертывающей системы крови у пациентов с фибрилляцией предсердий, принимающих дабигатрана этексилат, для оценки возможного кровотечения при радиочастотной аблации
- Баталов Р.Е., Антонченко И.В., Попов С.В. Антикоагулянтная терапия для фибрилляции предсердий / Российский медицинский журнал. 2017; 19(14): 905-909.
- Баталов Р.Е., Попов С.В., Егай Ю.В. Лечение фибрилляции предсердий (обзор литературы) / Сибирский медицинский журнал. 2011; 26(4): 8-14.
- Моисеев С.В. Когда и как применять дабигатран при фибрилляции предсердий / Рациональная фармакотерапия в кардиологии. 2012; 6(8): 819-824.
- Хорев Н.Г., Момот А.П., Залозный Д.А. Новые оральные антикоагулянты (обзор литературы) / Фарматека. 2010; 18/19: 20-26.
- Шубик Ю.В. Антитромботическая терапия при фибрилляции предсердий /Вестн. аритмологии. 2014; 75: 50-75.
- Heeringa J., van der Kuip D., Hofman А. Prevalence, incidence and lifetime risk of atrial fibrillation: the Rotterdam study / Eur. Heart J. 2006; 27: 949-953.
- Prystowsky E., Katz A. Atrial fibrillation in textbook of cardiovascular medicine. Philadelphia: Lippincott-Raven, 1998: 1661.
- Patel M.R., Mahaffey K.W., Garg J. For the ROCKET-AF Investigators. Rivaroxaban versus warfarin in nonvalvular atrial fibrillation / N. Engl. J. Med. 2011; 365: 883-891.
- Wann L.S., Curtis A.B., Januaru C.T. 2011 ACCF/AHA/HRS focused update on the management of patients with atrial fibrillation (updating the 2006 Guideline) / Heart Rhythm. 2011; 8: 158- 176.
- Wyse D. The Euro Heart Survey on atrial fibrillation / Eur. Heart J. 2005; 26(22): 2356-2357.
- Hart R.G., Pearce L.A., Aguilar M.I. Meta-analysis: antithrombotic therapy to prevent stroke in patient who have nonvalvular atrial fibrillation / Ann. Intern. Med. 2007; 146: 857-867.
- Connolly S.J., Eikelboom J., Joyner C. et al. For the AVERROES Steering Committee and Investigators. Apixaban in patients with Atrial Fibrillation / N. Engl. J. Med. 2011; 364: 806-817.
- Connolly S.J., Ezekowitz M.D. et al. For the RE-LY Steering Committee and Investigators. Dabigatran versus warfarin in patients with atrial fibrillation / N. Engl. J. Med. 2009; 361: 1139-1351.
- Гиляров М.Ю., Магомадова М.У., Сулимов В.А. Алгоритм подборы дозы варфарина с учетом носительства полиморфизмов генов цитохрома CYP2C9 и субъединицы 1 витамин К эпоксиредуктазы / Вестник аритмологии. 2011; 63: 28-30.


