Использование метода капиллярного электрофореза в оценке пищевых продуктов и напитков
Автор: Зипаев Д.В., Тулина А.А., Кожухов А.Н.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Пищевая биотехнология
Статья в выпуске: 1 (83), 2020 года.
Бесплатный доступ
Метод капиллярного электрофореза может использоваться при оценке качества, безопасности, фальсификации и идентификации пищевых продуктов и напитков. Он отличается высокой точностью (до 97 %) и эффективностью. С помощью него можно определять содержание различных катионов и анионов, органических кислот, углеводов, витаминов, аминокислот, консервантов, антиоксидантов, флавоноидов, синтетических красителей, имеющих большое значение для технохимического контроля производства продукции на предприятии. Метод капиллярного электрофореза позволяет определить натуральность и качество безалкогольных и алкогольных напитков путем выявления наличия или отсутствия органических кислот в пробе, а также анализа их количественного содержания и соотношения, даёт возможность контролировать ферментативные процессы и проводить корреляцию со вкусом конечного продукта. Кроме того, данный метод можно использовать при оценке качества воды, используемой в качестве основного сырья для производства напитков...
Капиллярный, электрофорез, детектирование, идентификация, фальсификация, пищевые, продукты, напитки
Короткий адрес: https://sciup.org/140248339
IDR: 140248339 | УДК: 543.6 | DOI: 10.20914/2310-1202-2020-1-82-87
The use of capillary electrophoresis in the evaluation of food and beverages
The method of capillary electrophoresis can be used to assess the quality, safety, falsification and identification of food and beverages. It is characterized by high accuracy (up to 97%) and efficiency. Using it, you can determine the content of various cations and anions, organic acids, carbohydrates, vitamins, amino acids, preservatives, antioxidants, flavonoids, synthetic dyes, which are of great importance for the technological control of production at the enterprise. The method of capillary electrophoresis allows you to determine the naturalness and quality of soft drinks and alcoholic drinks by detecting the presence or absence of organic acids in the sample, as well as analyzing their quantitative content and ratio, makes it possible to control enzymatic processes and correlate with the taste of the final product. In addition, this method can be used to assess the quality of water used as the main raw material for the production of beverages. It allows you to determine the content of pesticides and fungicides in the raw materials used for the production of food and beverages...
Текст научной статьи Использование метода капиллярного электрофореза в оценке пищевых продуктов и напитков
Оценка качества и безопасности, а также оценка различных питательных и функциональных свойств пищевых продуктов и напитков подразумевают использование надежных, действенных, чувствительных и экономически эффективных аналитических методов.
В последние годы одним из наиболее активно развивающихся аналитических методов является метод капиллярного электрофореза (КЭ). Данный метод весьма интересен для анализа большого количества соединений за счет своей высокой эффективности разделения, малых требований к образцам и реагентами скорости
This is an open access article distributed under the terms of the Creative Commons Attribution 4.0 International License
Зипаев Д.В. и др. Вестник ВГУИТ, 2020, Т. 82, №. 1, С. 82-87 анализа. Капиллярный электрофорез зарекомендовал себя как очень полезный и дополняющий аналитический инструмент, особенно когда анализируются высокополярные и заряженные метаболиты и объем выборки ограничен. Целевой анализ осуществляется для оценки качества и безопасности, включая комбинацию процедур подготовки образца и последующего анализа методом капиллярного электрофореза заданного количества соединений из сложной смеси.
В качестве альтернативной стратегии целевого анализа существуют разработки профильных технологий, создающих потенциал для улучшения аналитов, которые можно определить одновременно в одном анализе [1].
Цель работы – определить возможность использования метода КЭ для оценки пищевых продуктов и напитков.
Обсуждение
Предпосылки появления электрофореза связаны с открытием электроосмоса в начале XIX в. и законом Кольрауша о независимом движении ионов (1897). Интенсивное использование метода капиллярного электрофореза в аналитической практике началось с достижения Д.У. Йоргенсона (1983), предложившего использовать наряду с электрофорезом электроосмотический поток, обеспечивающий движение компонентов пробы в одну сторону и позволяющий реализовать электрофорез в приборе с одним детектором [2].
Применение кварцевых капилляров, положительно зарекомендовавших себя, начиная с 1973 г., в многочисленных методиках с использованием капиллярной газовой хроматографии, в методе электрофореза, в начале 90-x гг. XX в. позволило создать аналитическое оборудование, способное конкурировать с признанными методами газовой и жидкостной хроматографии.
Метод капиллярного электрофореза позволяет анализировать ионные и нейтральные компоненты различной природы с высокой экспрессностью и уникальной эффективностью. В основе капиллярного электрофореза лежат электрокинетические явления – электромиграция ионов и других заряженных частиц и электроосмос. Эти явления возникают в растворах при помещении их в электрическое поле преимущественно высокого напряжения. Если раствор находится в тонком капилляре, например, в кварцевом, то электрическое поле, наложенное вдоль капилляра, вызывает в нем движение заряженных частиц и пассивный поток жидкости, в результате чего проба разделяется на индивидуальные компоненты, так как параметры
Традиционно капиллярный электрофорез сравнивают с высокоэффективной жидкостной хроматографией (ВЭЖХ), поскольку в обоих методах разделение происходит в ограниченном пространстве (капилляре или колонке) с участием движущейся жидкой фазы (буферного раствора или подвижной фазы (элюента), и для регистрации сигналов используют схожие принципы детектирования и программы обработки данных.
Тем не менее у методов есть отличия, которые, безусловно, относятся к достоинствам капиллярного электрофореза: высокая эффективность разделения (сотни тысяч теоретических тарелок), недоступная ВЭЖХ и связанная с плоским профилем ЭОП; малый объем анализируемой пробы и буферов (не более 1–2 мл в день), при этом практически не требуется применение высокочистых, дорогостоящих органических растворителей; отсутствие колонки, сорбента, проблем с его старением и, значит, заменой колонки; простая и недорогая аппаратура; экспрессность и низкая себестоимость единичного анализа [3].
Метод капиллярного электрофореза основан на разделении компонентов сложной смеси в кварцевом капилляре под действием приложенного электрического поля. Микрообъем анализируемого раствора (около 2 нл) вводят в капилляр, предварительно заполненный подходящим буфером – электролитом. После подачи к концам капилляра высокого напряжения (до 30 кВ) компоненты смеси начинают двигаться по капилляру с разной скоростью, зависящей, в первую очередь, от заряда и массы (точнее – величины ионного радиуса), и в разное время достигают зоны детектирования. Детектирование – это диапазон между пределами, выраженными заявленными значениями нижнего и верхнего пределов. Полученная последовательность пиков называется электрофореграммой, при этом качественной характеристикой вещества является параметр удерживания (время миграции), а количественной – высота или площадь пика, пропорциональная концентрации вещества. На рисунке 1 представлена принципиальная схема капиллярного электрофореза.
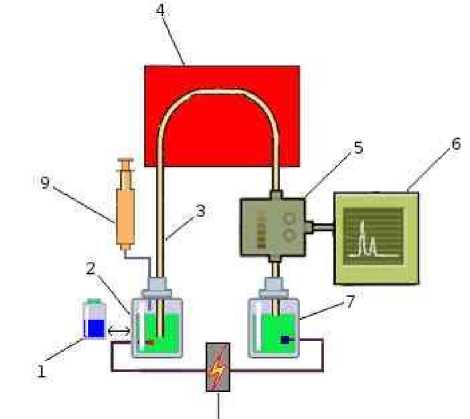
Рисунок 1. Принципиальная схема капиллярного электрофореза: 1 – виала с образцом, которая меняется местами с буферным раствором при заборе пробы; 2 – буферный раствор с анодом; 3 – капиллярная колонка; 4 – термостат; 5 – детектор; 6 – система сбора данных; 7 – буферный раствор с катодом; 8 – источник высокого напряжения; 9 – система контроля давления
Figure 1. Schematic diagram of capillary electrophoresis: 1 – vial with a sample, which changes places with a buffer solution when sampling; 2 – buffer solution with an anode; 3 – capillary column; 4 – thermostat; 5 – detector; 6 – data acquisition system; 7 – buffer solution with a cathode; 8 – source of high voltage; 9 – pressure control system
В последнее время метод капиллярного электрофореза получает все большее распространение в анализе различных пищевых продуктов и напитков. Цель метода заключается в определении органических кислот (в том числе индивидуальные формы D- и L-изомеров), сахара, неорганических катионов и анионов, консервантов, антиоксидантов, синтетических красителей, подсластителей, витаминов, аминокислот, ароматических альдегидов, аминов, флавоноидов, антоцианинов, пестицидов, фунгицидов и микотоксинов в пищевых продуктах и напитках, избыточное количество которых может привести к существенному отрицательному воздействию на здоровье человека.
Одним из наиболее широко известных примеров использования метода КЭ в анализе пищевых продуктов является его применение в определении гидроксикарбоновых кислот. На сегодняшний день такие гидроксикислоты как яблочная, молочная, лимонная, винная, очень широко применяются в пищевой промышленности в качестве консервантов, стабилизаторов и вкусовых добавок. По этой причине контроль их содержания в продуктах питания необходим.
В области определения гидроксикислот представлены практически все аналитические методы, начиная от классических и заканчивая современными высокоэффективными методами хроматографии и капиллярного электрофореза.
В настоящее время разработана новая методика капиллярно-электрофоретического определения гидроксикарбоновых кислот в продуктах питания. Для косвенного фотометрического детектирования этих веществ в качестве светопоглощающего компонента ведущего электролита предложено использовать 3-нитро-бензойную кислоту. Это существенно увеличивает чувствительность определения (вплоть до n ×10 мкг/л) по сравнению с имеющимися аналогами. Оптимизирован состав ведущего электролита: 3-нитробензойная кислота 10 мМ, цетилтриметиламмоний бромид 0,5 мМ, ЭДТА 0,1 мМ, моноэтаноламин до рН = 5,3 ед. Методика протестирована на образцах пищевых продуктов: фруктах, соках, нектарах, винах, пиве и т. п. Правильность полученных при анализе результатов подтверждена методом «введено–найдено».
Однако ввиду новизны метода КЭ и небольшого количества публикаций по вопросу его использования для определения гидроксикислот оптимальные условия определения этих аналитов и, прежде всего, состава используемых в анализе буферных растворов требуют уточнения [4].
Метод КЭ хорошо зарекомендовал себя не только в оценке пищевых продуктов, но и в анализе напитков. Например, метод капиллярного электрофореза активно используется для определения содержания кофеина, витаминов С, РР и В 6 в энергетических напитках. Определение кофеина, сахарината натрия, ацесульфама К, бензойной, аскорбиновой и сорбиновой кислот в алкогольных и безалкогольных напитках методом КЭ регламентировано впервые введенным ГОСТ Р 53193–2008 [5]. Предполагается, что главными источниками ошибок в методе КЭ являются непостоянство электроосмотического потока и дозирование образца [6].
Крайне важно использование метода капиллярного электрофореза в определении ионов железа и меди в коньяках, ведь коньяк является одним из самых фальсифицируемых алкогольных напитков. Один из показателей качества коньяка – содержание в нем ионов железа (III) и меди (II), которое нормируется ГОСТ Р 51618–2009 и составляет не более 1,0–1,5 и 5 мг/л соответственно [7]. Избыток этих ионов приводит к ухудшению вкусовых качеств напитка, а также оказывает негативное воздействие на организм человека при его употреблении.
Капиллярный электрофорез является перспективным методом, позволяющим избежать длительной пробоподготовки. Разработана методика определения железа (III) и меди (II) в коньяках данным методом с детектированием с помощью диодной матрицы с пределами обнаружения 0,06 и 0,60 мг/л соответственно. Посторонние вещества, присутствующие в коньяке, не мешают определению. Правильность результатов анализа подтверждена методом «введено–найдено». Данные, полученные методом КЭ, хорошо согласуются с результатами масс-спектрометрии с индуктивно связанной плазмой [8].
Применение метода капиллярного электрофореза распространяется и на анализ консервантов в гранатовом соке. Это особенно актуально в связи с острой проблемой недекла-рируемого производителями использования консервантов в соках, в том числе предназначенных для детского питания. При использовании метода КЭ возможно определение консервантов и антиоксидантов в напитках без предварительной отгонки или экстракции. Простота пробоподго-товки делает анализ экспрессным и снижает его себестоимость.
Известный факт, что при контроле качества и безопасности напитков важен анализ пищевых синтетических красителей. При использовании метода капиллярного электрофореза подготовка пробы заключается в селективном выделении красителей на оксиде алюминия с последующей их десорбцией водным раствором аммиака.
Метод КЭ может успешно применяться и в алкогольной отрасли для контроля качества сырья и готовой продукции. Состав воды для производства ликеро-водочных изделий во многом определяет технологические и органолептические параметры последних. Особенностью водоподготовки в ликеро-водочной отрасли является использование водоумягчающих установок, действующих по принципу ионного обмена. Водка, произведенная с использованием воды, очищенной таким образом, имеет характерный катионный профиль.
Стоит обратить внимание на то, что определение содержания неорганических катионов и сравнение электрофореграммы образца с электрофореграммой эталонных образцов вин, виноматериалов, коньяков и коньячных спиртов позволяет установить подлинность анализируемых образцов.
При превышении верхней границы диапазона концентраций по любому из катионов виноматериал или вино следует считать натуральным, но подверженным помутнениям в течение гарантийного срока хранения. При обнаружении массовой концентрации калия менее 400 мг/л виноматериал или вино следует признать разбавленным водно-спиртовой смесью. Пониженные концентрации остальных катионов отражают технологические особенности производства. Отсутствие или наличие массовых концентраций всех катионов менее 10 мг/л свидетельствуют о полной фальсификации напитка. Отсутствие катионов в коньяках и коньячных спиртах также свидетельствует о фальсификации напитка.
Для анализа консервантов (сорбиновой и бензойной кислот) в безалкогольных напитках и соках с помощью метода капиллярного электрофореза используют зонный вариант с простым буфером на основе буры. Подготовка пробы – стандартная: фильтрование образца и при необходимости разбавление. В случае сильногазированных напитков необходимо провести дегазирование образца.
Метод КЭ позволяет определить натуральность и качество безалкогольных и алкогольных напитков путем выявления наличия или отсутствия органических кислот в пробе, а также анализа их количественного содержания и соотношения, даёт возможность контролировать ферментативные процессы и проводить корреляцию со вкусом конечного продукта. Подготовка пробы представляет собой разбавление и центрифугирование. Явным преимуществом использования данного метода является отсутствие мешающего влияния неорганических анионов, бензойной, аскорбиновой и сорбиновой кислот. Фосфат-ион может количественно определяться в рамках приведенных условий анализа [9–12].
Измерение хмелевых α - и β -кислот (гуму-лонов и лупулонов) и горьких пивных кислот (изогумулонов) актуально на всех этапах производства пива. Хмелевые кислоты являются биохимическими маркерами сорта хмеля. Горькие пивные кислоты стабилизируют пивную пену, подавляют развитие нежелательных микроорганизмов и придают горький вкус напитку.
Метод их измерения с помощью капиллярного электрофореза основан на дегазировании образца, экстракции кислот из подкисленной пробы в изооктан, последующем удалении избытка растворителя и растворении сухого остатка в смеси вода / метанол; разделении, идентификации и определении относительного содержания компонентов в варианте мицеллярной электрокинетической хроматографии с использованием в качестве ведущего электролита боратного буфера с добавками додецилсульфата натрия. Детектирование компонентов проводят по их собственному поглощению при длине волны 215 нм [3].
Заключение
В целом можно заключить, что вышеперечисленные принципы и примеры, лежащие в основе метода КЭ, делают его одним из наиболее перспективных методов анализа. Сейчас он динамично развивается и получает всё более широкое применение в различных областях аналитической химии. Несмотря на то что теоретические основы капиллярного электрофореза достаточно сложны, сам метод довольно прост и доступен, он дает неоспоримые преимущества перед другими методиками при выполнении различных измерений.
Список литературы Использование метода капиллярного электрофореза в оценке пищевых продуктов и напитков
- Ib??ez C., Acunha T., Vald?s A., Garc?a-Ca?as V. et al. Capillary Electrophoresis in Food and Foodomics // Methodsin Molecular Biology. 2016. P. 471-507.
- Беленький Б.Г. Высокоэффективный капиллярный электрофорез. СПб.: Наука, 2009. 320 с.
- Комарова Н.В., Каменцев Я.С. Практическое руководство по использованию систем капиллярного электрофореза "Капель". СПб.: Веда, 2006. 212 с.
- Голубенко А.М., Никоноров В.В., Никитина Т.Г. Определение гидроксикарбоновых кислот в продуктах питания методом капиллярного электрофореза // Журнал аналитической химии. 2012. Т 67. № 9. С. 866-870.
- ГОСТ Р 53193-2008. Напитки алкогольные и безалкогольные. Определение кофеина, аскорбиновой кислоты и ее солей, консервантов и подсластителей методом капиллярного электрофореза. М.: Стандартинформ, 2010. 15 с.
- Хасанов В.В., Слижов Ю.Г., Хасанов В.В. Анализ энергетических напитков методом капиллярного электрофореза // Журнал аналитической химии. 2013. Т 68. № 4. С. 385.
- ГОСТ Р 51618-2009 Коньяки российские. Общие технические условия. М.: Стандартинформ, 2000. 10 с.
- Попова О.В., Сурсякова В.В., Бурмакина Г.В., Рубайло А.И. Определение ионов железа и меди в коньяках методом капиллярного электрофореза // Журнал аналитической химии. 2015. Т. 70. № 2. С. 174.
- Rokhas M.K., R?nn J.L., Wiklund C., Emmer ?. Analysis of butterfly reproductive proteins using capillary electrophoresis and mass spectrometry // Analytical biochemistry. 2019. V. 566. P. 23-26.
- Ghosal S. Band Broadening Theories in Capillary Electrophoresis // Microfluidic Electrophoresis. New York: Humana Press, 2019. P. 143-166.
- Junger A. S., de Jesus F.F.S., Fracassi da Silva J.A., Daniel D. et al. A simple and fast method for determination of benzocaine and lidocaine in pharmaceutical formulations by capillary electrophoresis with spectrophotometric detection // Separation Science Plus. 2019. V. 2. № 11. P. 422-427.
- Ghosal S. Band Broadening Theories in Capillary Electrophoresis // Microfluidic Electrophoresis. New York, Humana Press, 2019. P. 143-166.


