Использование различных имплантационных материалов в реконструктивной хирургии. Экспериментальное исследование
Автор: Епифанов С.А., Апостолиди К.Г., Балин В.Н., Перова Н.В., Бекша И.С.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.8, 2013 года.
Бесплатный доступ
Проведена сравнительная оценка интеграции различных имплантационных материалов биологического и синтетического происхождения в эксперименте на животных. Разработанный способ комбинированного использования богатой тромбоцитами плазмы крови в комбинации с имплантационным материалом позволяет снизить местную воспалительную реакцию, исключить смещение имплантата, уменьшить количество послеоперационных осложнений, сократить период реабилитации.
Пористый полиэтилен, силикон, кость, хрящ, богатая тромбоцитами плазма
Короткий адрес: https://sciup.org/140188165
IDR: 140188165 | УДК: 615.462:
The use of different implant materials in reconstructive surgery. Experimental study
A comparative evaluation of the integration of different biological and synthetic implant materials in animal experiments. The developed method of combined use of platelet-rich plasma in combination with implant materials can reduce the local inflammatory reaction, prevent displacement of the implant, reduce the number of postoperative complications, and shorten the period of rehabilitation.
Текст научной статьи Использование различных имплантационных материалов в реконструктивной хирургии. Экспериментальное исследование
Актуальность
В настоящее время проводятся активные исследования, посвященные изучению способов повышения интеграции различных имплантатов и трансплантатов в реконструктивной хирургии. Перспективным методом считается применение факторов роста непосредственно в области хирургического вмешательства, которые играют ведущую роль в стимуляции и регуляции процессов заживления ран в организме (A. Garg, D. Gargenese, I. Peace, 2000).
К факторам, которые первыми запускают каскад процессов регенерации, относятся полученные из тромбоцитов факторы роста и трансформирующие факторы роста (R. Marx, 2001). Богатая тромбоцитами плазма (PRP, БоТП) представляет собой «выжимку» из аутокрови, содержащую тромбоциты в количестве, превышающем исходное. БоТП стимулирует ангиогенез и митоз клеток, которые участвуют в процессе регенерации. В силу этого, БоТП не может значительно улучшить характеристики неклеточных костных материалов (R. Marx, E. Carlson 1998). Однако, поскольку сокращение сроков роста и созревания кости было продемонстрировано при применении аутогенной кости и БоТП, то можно предположить, что применение комбинации различных имплантационных материалов и БоТП тоже приведет к увеличению скорости интеграции и заживления послеоперационной раны. В исследованиях Y. Foukaya с соавт. (2012) достоверно доказано уменьшение апоптоза клеток адипоцитов в культуре in vitro при добавлении к ним богатой тромбоцитами плазмы.
Вышеуказанные данные свидетельствуют о большом потенциале обогащенной тромбоцитами плазмы при хирургических операциях и являются стимулом для использования ее в клинической практике.
Для обоснования возможности использования различных имплантационных материалов в комбинации с богатой тромбоцитами плазмой в реконструктивной хирургии нами был проведен эксперимент.
Целью экспериментального исследования стало изучение свойств и взаимодействия богатой тромбоцитами плазмы с различными имплантационными материалами, наиболее часто применяемыми в практике, в эксперименте на животных.
Основные задачи экспериментального исследования:
– на основе морфогистологических исследований определить реакцию окружающих тканей на костный, хрящевой трансплантат (взят у крыс, не участвующих в эксперименте), силикон, пористый биосовместимый полиэтилен («Medpor», производитель «Stryker®», США), а также комбинации указанных материалов с богатой тромбоцитами плазмой;
– определить выраженность воспалительной реакции, степень миграции, резорбции и замещения соединительной тканью имплантируемого материала.
Материалы и методы
Эксперимент провели на 36 половозрелых самцах крыс линии Вистар весом от 170 до 250 г.
Данное исследование выполняли в соответствии с ГОСТ 10993.6 – 2009 и с требованиями Правил лабораторной практики в Российской Федерации (Приказ Министерства здравоохранения и социального развития Российской Федерации № 708н от 23.08.2010).

Все манипуляции с животными были проведены согласно принципам гуманного отношения к животным в соответствии с Международными рекомендациями, а также с соблюдением биоэтических норм и требований Международного комитета по науке.
Животных содержали в стандартных условиях, соответствующих Санитарным правилам по устройству, оборудованию и содержанию экспериментально-биологических клиник (вивариев), группами по 9 особей в поликарбонатных клетках. В качестве подстила использовали древесные опилки лиственных пород.
Животные получали стандартный гранулированный корм для лабораторных грызунов ПК 120-899. Микробиологический статус кормов соответствует ГОСТ Р 51849-2001 «Ветеринарно-санитарные нормы и требования к качеству кормов для непродуктивных животных» и не оказывает негативного влияния на результаты проводимого теста. Фильтрованную водопроводную воду давали в стандартных питьевых бутылочках. Микробиологический статус воды соответствует СанПиН 2.1.4.1074-01 «Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения» и не оказывает негативного влияния на результаты проводимого теста.
Животные были адаптированы в лаборатории в течение 14 дней до начала эксперимента. Во время этого периода осуществлялся ежедневный осмотр внешнего состояния животных. Во время карантина все крысы оставались здоровыми.
Животных распределяли по группам рандомизи-рованно.
Каждому животному присваивали индивидуальный номер, помечаемый индивидуальным окрашиванием, и фиксируемый на карточке клетки.
Дизайн исследования:
Образцы, использованные в эксперименте
-
1. Силикон;
-
2. «Medpor», производитель «Stryker®», США;
-
3. Кость (аутокость), взятая из кончика хвоста крыс;
-
4. Хрящ, взятый из уха крыс, не участвующих в эксперименте.
Подготовка богатой тромбоцитами плазмы крови
У крыс, не участвующих в дальнейшем эксперименте, производили забор крови в пластиковую пробирку с антикоагулянтом (3,8% раствор цитрата натрия) в соотношении 1 : 9, центрифугировали при 1200 об/мин. (около 300g) в течение 5 минут и собирали супернатант.
Подготовка образцов
Силикон и «Medpor» были представлены на исследования в готовом виде. Кость извлекали из кончика хвоста имплантируемой крысы (аутокость). Хрящ извлекали из уха интактной крысы.
Для обработки тестируемых материалов богатой тромбоцитами плазмой крови образцы помещали в плазму и добавляли 10% раствор хлористого кальция (из расчета 1мл плазмы – 4 капли раствора) до образования гелеобразной массы, после чего образцы имплантировали в теменно-затылочную область крыс под надкостницу (рис. 1).
Формирование групп
Крысы были разделены на 4 группы методом случайной выборки. Имплантацию производили с двух сторон (стороны L и R): в левую сторону (L) имплантировали чистый материал, в правую (R) – тот же материал, но выдержанный в плазме (рис. 2).
Группы распределились следующим образом:
-
a. Группа №1 – L- силикон; R- силикон с богатой тромбоцитами плазмой;
-
b. Группа №2– L- «Medpor»; R- «Medpor» с богатой тромбоцитами плазмой;
-
c. Группа №3 – L-кость; R- кость с богатой тромбоцитами плазмой;
-
d. Группа №4 – L-хрящ; R- хрящ с богатой тромбоцитами плазмой.
Подготовка к имплантации
За 24 часа до начала проведения исследования животных не кормили. Перед имплантацией крысам проводили общую анестезию.
В области имплантации выбривали шерсть.
Проведение имплантации
Место имплантации обрабатывали раствором спирта (70%). В асептических условиях с помощью одноразовых скальпелей производили 2 разреза в теменнозатылочной области. С левой стороны под надкостницу помещали нативный материал, справа – обработанный
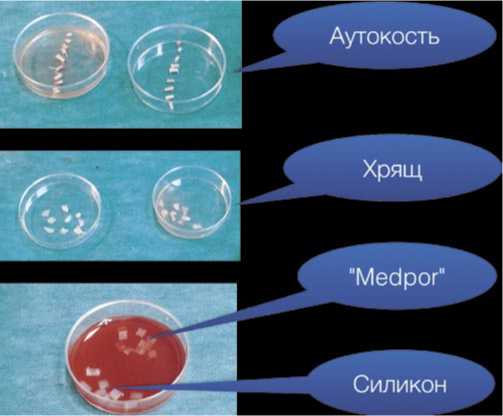
Рис. 1. Имплантируемые образцы
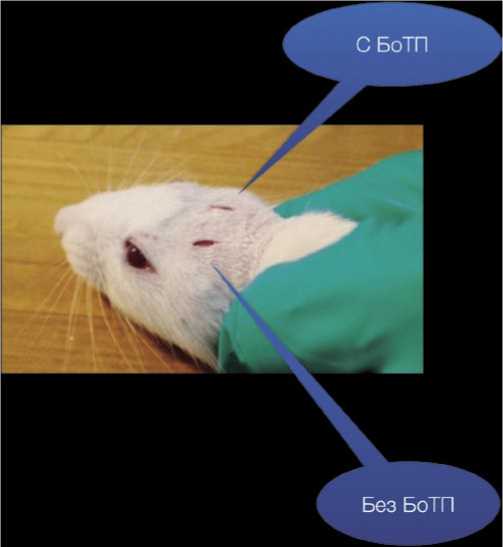
Рис. 2. Зона имплантации
богатой тромбоцитами плазмой. Раны ушивали рассасывающимся шовным материалом «MONOCRYL*Plus» фирмы «Eticon».
Наблюдение за животными
На протяжении исследования вели наблюдение за каждым животным. Объектом ежедневного контроля были:
– общий вид (шерстный покров, глаза, уши, конечности, зубы);
– состояние и поведение (активность, походка, темперамент, питание); физиологические функции (дыхание, слюноотделение, мочеиспускание, экскрет);
– заживление ран (сроки заживления, наличие инфекции, гематом, некротических тканей, тип заживления).
Этапы исследования
Животных из эксперимента выводили в 3 этапа: 2 недели, 1 месяц, 3 месяца после имплантации.
Сразу после гибели производили забор материала из зоны имплантации вместе с образцами для гистологических
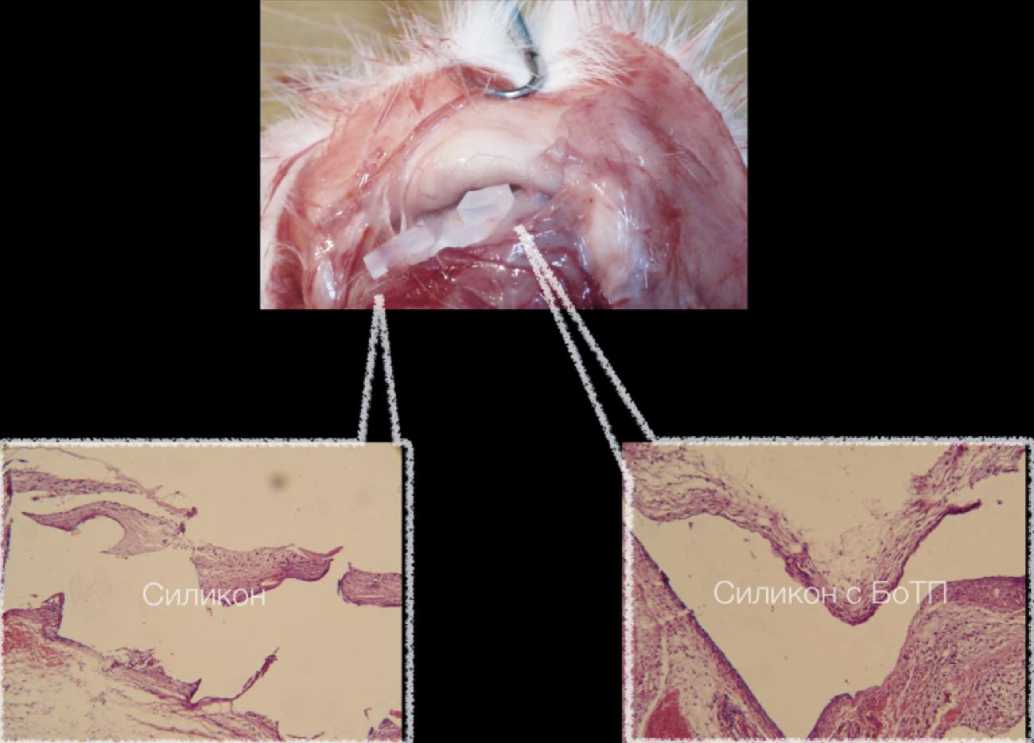
Рис. 3. Фото и гистограмма зоны имплантации у животных 1 группы на 14 сутки

исследований. Ткани с образцами, извлеченные после эвтаназии, подвергали обработке: фиксировали в 10% растворе нейтрального формалина, заливали в парафин по общепринятой методике, изготовляли серийные срезы толщиной 5 мкм, окрашивали гематоксилин-эозином и по методу Маллори. Образцы с костной тканью предварительно подвергали декальцинированию с помощью раствора Трилона Б.
Результаты исследования
Группа 1 (имплантируемый материал – силикон), 14-сутки после имплантации.
Признаков воспалительной реакции мы не наблюдали, однако определялось значительное смещение имплантата слева (3 балла), тогда как комбинация синтетического материала и плазмы ограничивала миграцию имплантата (2 балла).
При гистологическом исследовании препаратов – микроскопческая картина стадии формирования многослойной соединительнотканной капсулы. В воспалительный процесс вовлечены окружающие ткани, в которых присутствуют форменные элементы крови, гигантские клетки воспалительного ряда, нейтрофилы. Исследование биоптата с силиконом в нативном виде показывает более выраженный отек рыхлой неупорядоченной клетчатки (рис. 3).
Группа 1 (имплантируемый материал силикон), 30-сутки после имплантации.
При макроскопическом исследовании наблюдали картину, аналогичную таковой на 14 сутки после имплантации – более выраженную миграцию имплантата в нативном виде без признаков воспаления.
Гистологическая картина в подгруппе L-силикон характеризовалась отсутствием процесса капсулообразо-вания. Вокруг имплантата рыхлая неоформленная ткань. Форменные элементы крови отсутствуют (рис. 4).
В подгруппе R-силикон с богатой тромбоцитами плазмой клетки воспалительного ряда в минимальном количестве. Капсула образуется из коллагеноподобных волокон, за капсулой образовалась рыхлая неупорядоченная соединительная ткань (рис. 5).
Группа 1 (имплантируемый материал силикон), 90-сутки после имплантации.
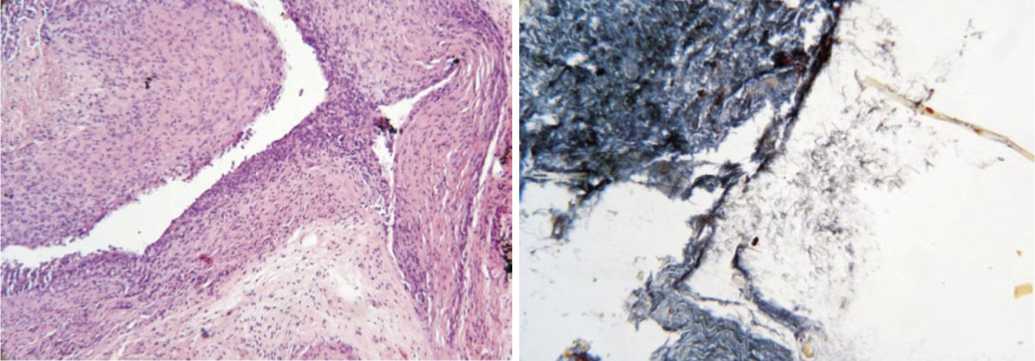
Рис. 4. Гистологическая картина в подгруппе L-силикон на 30 сутки
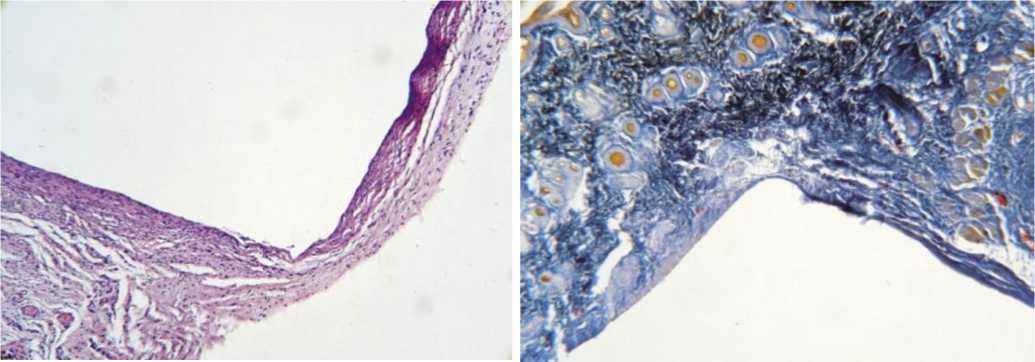
Рис. 5. Гистологическая картина в подгруппе R-силикон с богатой тромбоцитами плазмой на 30 сутки
Макроскопический анализ аналогичен предыдущим исследованиям – в обеих подгруппах выраженное смещение имплантата, без признаков воспаления вокруг него.
Гистологическая картина в подгруппе L-силикон – характеризовалась завершением процесса капсулообра-зования. Сформирована плотная многослойная капсула. Окружающие ткани без признаков воспаления (рис. 6).
Во второй подгруппе сформирована тонкая со-единительно-тканная капсула вокруг имплантата. Прилегающие ткани имеют рыхлую структуру с большим количеством сосудов (рис. 7).
Группа 2 (имплантируемый материал «Medpor»), 14-сутки после имплантации.
При макроскопическом исследовании пределяется выраженная воспалительная реакция в подгруппе L-«Por-ex» (3 балла). При комбинации синтетического материала и плазмы отмечена менее выраженная воспалительная реакция (2 балла). Признаков миграции имплантата не отмечено в обеих группах.
При гистологическом исследовании в подгруппе L-«Medpor» наблюдается воспалительный процесс с за- полнением пор материала клетками воспалительного ряда. Вокруг плотной структуры имплантата формируется плотная соединительная ткань.
В подгруппе R-«Medpor» с богатой тромбоцитами плазмой отмечается менее выраженная воспалительная реакция (рис. 8).
Группа 2 (имплантируемый материал «Medpor»), 30-сутки после имплантации.
Признаков воспалительной реакции и смещения имплантата мы не наблюдали в обеих подгруппах.
При микроскопическом исследовании в подгруппе L-«Medpor» процесс капсулообразования как таковой отсутствует. Вокруг имплантата рыхлая неоформленная соединительная ткань (рис. 9).
В подгруппе R-«Medpor» с богатой тромбоцитами плазмой вокруг имплантата сформирована плотная капсула без признаков воспаления. Поры заполнены рыхлыми фибробластами (рис. 10).
Группа 2 Имплантируемый материал «Medpor», 90-сутки после имплантации.
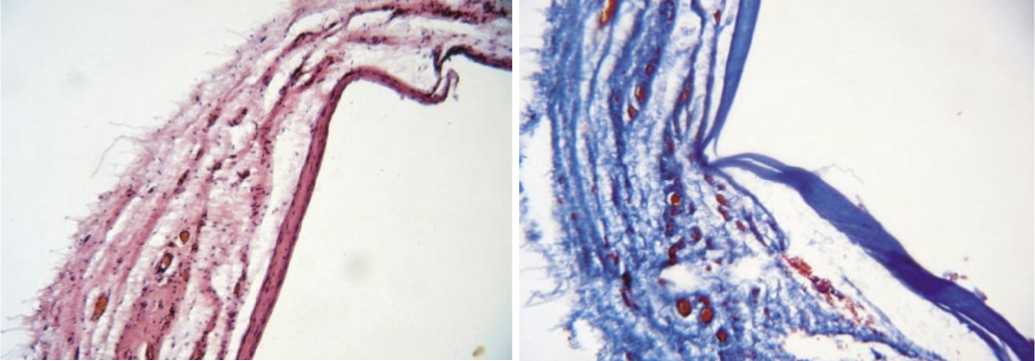
Рис. 6. Гистологическая картина в подгруппе L-силикон на 90 сутки
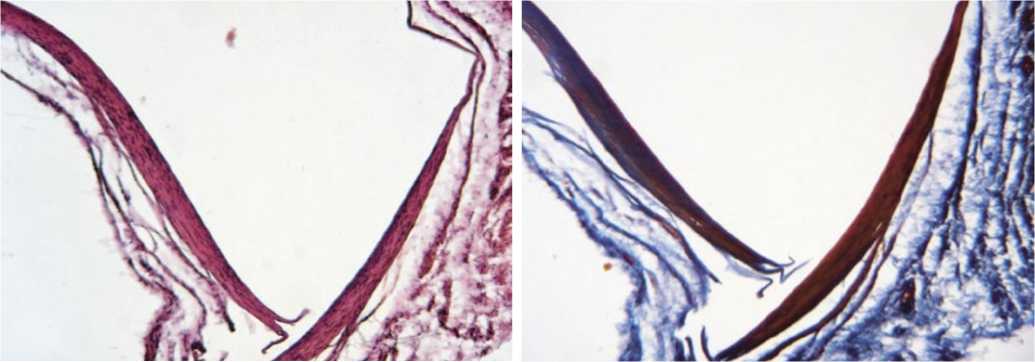
Рис. 7. Гистологическая картина в подгруппе R-силикон с богатой тромбоцитами плазмой на 90 сутки
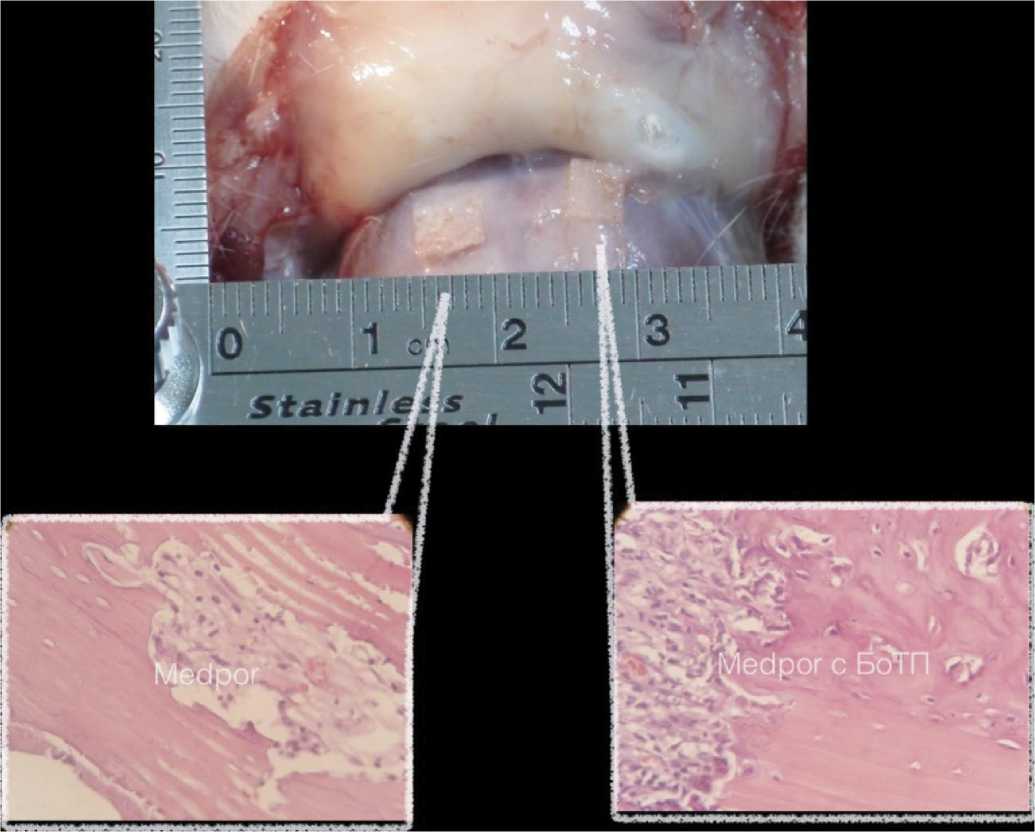
Рис. 8. Фото и микроскопическая картина зоны имплантации у животных 2 группы на 14 сутки
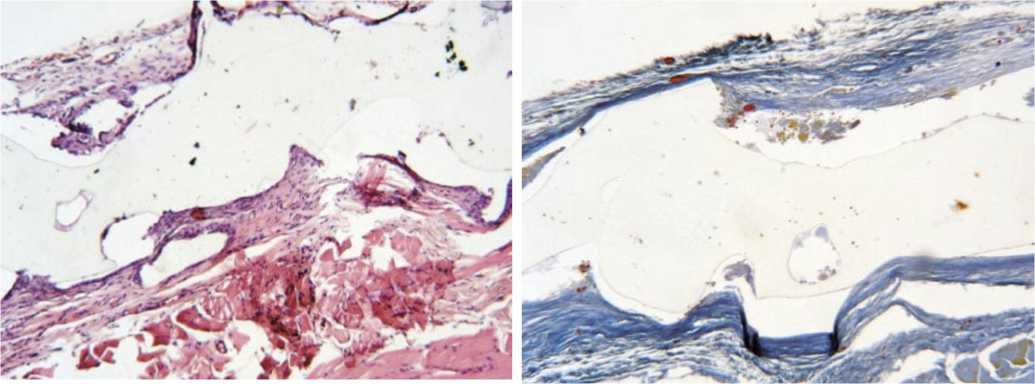
Рис. 9. Гистологическая картина зоны имплантации у животных в подгруппе L-«Medpor» на 30 сутки
Макроскопическая картина аналогична предыдущему исследованию.
Микроскопически в подгруппе L-«Medpor» видны четкие границы материала с образовавшейся тонкой соединительно-тканной оболочкой. Форменные клетки крови еще присутствуют в ткани (рис. 11).
Во второй подгруппе ткани плотно интегрированы с имплантируемым материалом, поры заполнены рыхлой соединительной тканью. Признаков воспаления не наблюдается (рис. 12).
Группа 3 (имплантируемый материал кость), 14-сутки после имплантации.
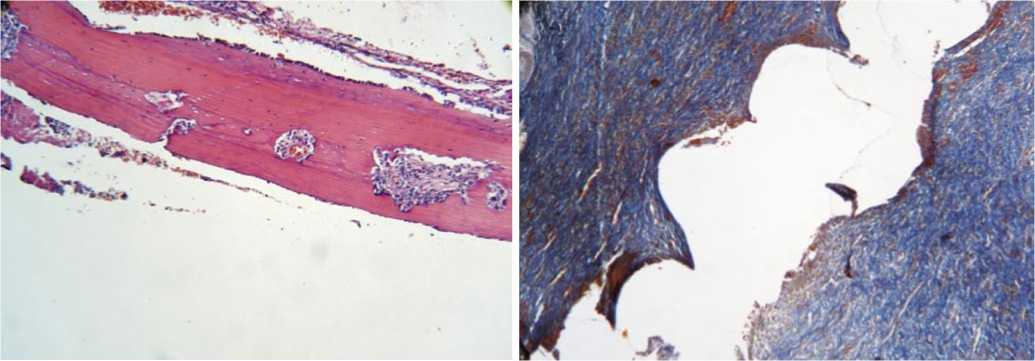
Рис. 10. Гистограмма зоны имплантации у животных в подгруппе R-«Medpor» с богатой тромбоцитами плазмой на 30 сутки
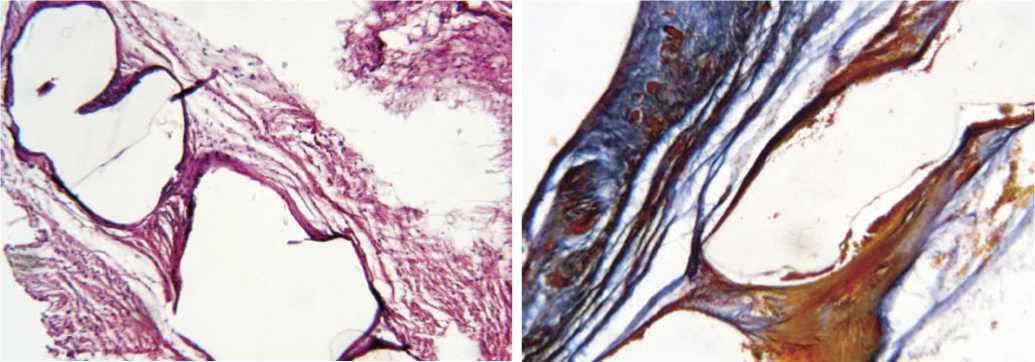
Рис. 11. Гистологическая картина зоны имплантации у животных в подгруппе L-«Medpor» на 90 сутки
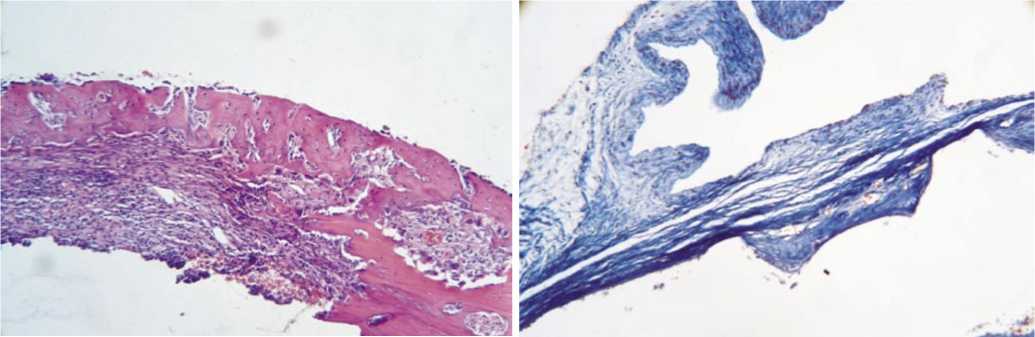
Рис. 12. Гистограмма зоны имплантации у животных в подгруппе R-«Medpor» с богатой тромбоцитами плазмой на 90 сутки
При макроскопическом исследовании отмечена умеренная миграция имплантата в подгруппе L-кость (2 балла), в подгруппе R-кость с богатой тромбоцитами плазмой (1 балл). Признаков воспаления не наблюдалось в обеих подгруппах.
Микроскопически в подгруппе L-кость границ между материалом и тканью нет. В зоне имплантации большое количество гигантских клеток. В подгруппе R-кость с богатой тромбоцитами плазмой зона костного имплантата инфильтрирована форменными элементами крови. Воспалительный процесс умеренной степени. Выраженная нейтрофильная реакция (рис. 13).
Группа 3 (имплантируемый материал кость), 30-сутки после имплантации .
Макроскопическая картина свидетельствует о частичной резорбции имплантатов в обеих подгруппах без признаков воспаления. Миграции имплантатов не определяется.
При гистологическом исследовании в зоне имплантации подгруппы
L-кость наблюдается незавершенный воспалительный процесс, с большим количеством фибробластоподобных клеток, рыхлая ткань чередуется с плотно «упакованными» слоями соединительной ткани (рис. 14).
Во второй подгруппе определяется зона соединения имплантата с окружающей тканью в виде пластов выраженной капсулоподобной ткани. Воспалительный процесс на стадии угасания (рис. 15).
Группа 3 (имплантируемый материал кость), 90-сутки после имплантации.
Макроскопическая картина аналогична предыдущему исследованию.
Гистологическая картина в первой подгруппе характеризуется образованием вокруг костного трансплантата многослойной плотной капсулы инфильтрированной фибробластами без признаков организации соединительной ткани (рис. 16).
Микроскопически в подгруппе R-кость с богатой тромбоцитами плазмой, ткани интегрированы с им-
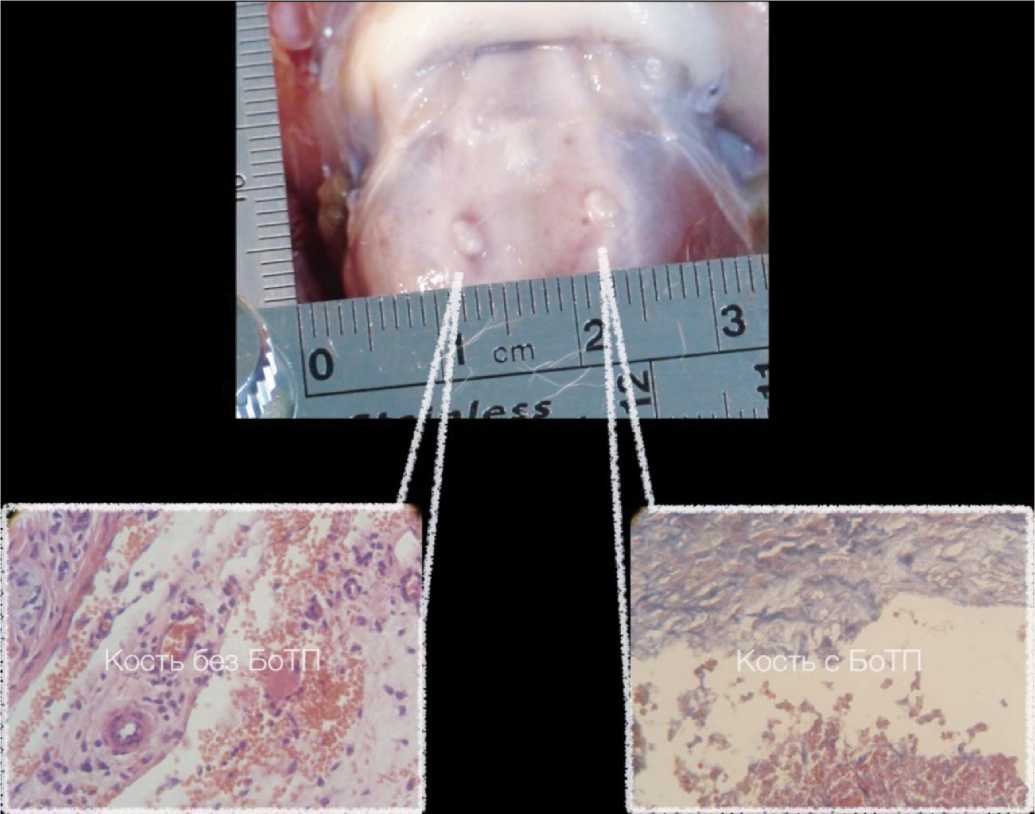
Рис. 13. Макро и микроскопическая картина зоны имплантации у животных 3 группы на 14 сутки
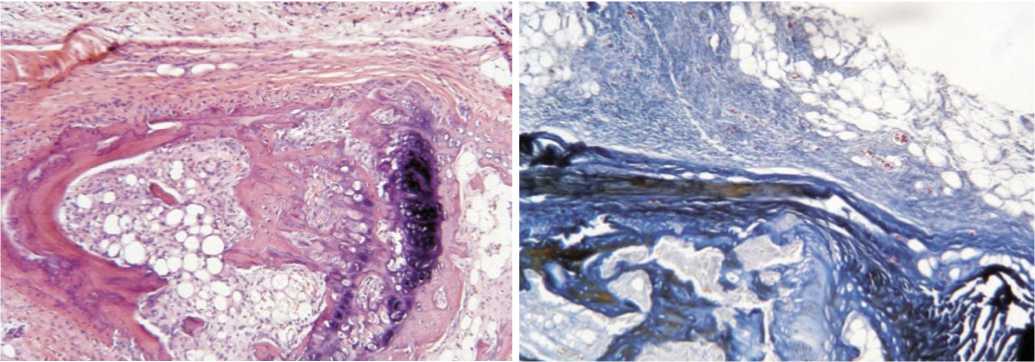
Рис. 14. Гистологическая картина зоны имплантации у животных в подгруппе L-кость на 30 сутки
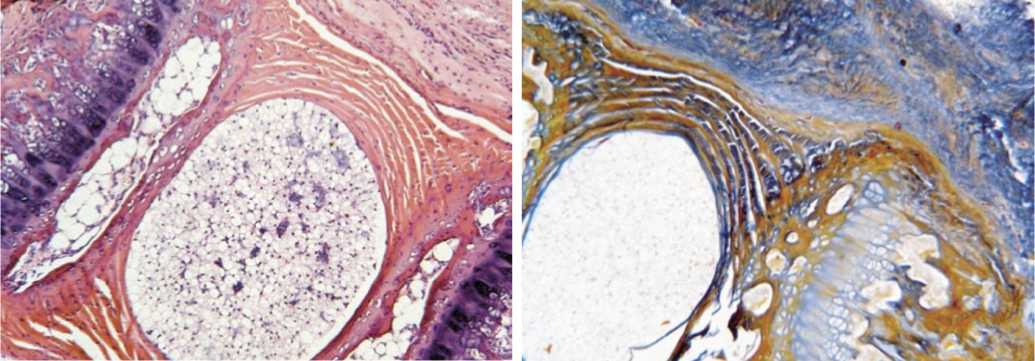
Рис. 15. Гистограмма зоны имплантации у животных в подгруппе R-кость с богатой тромбоцитами плазмой на 30 сутки
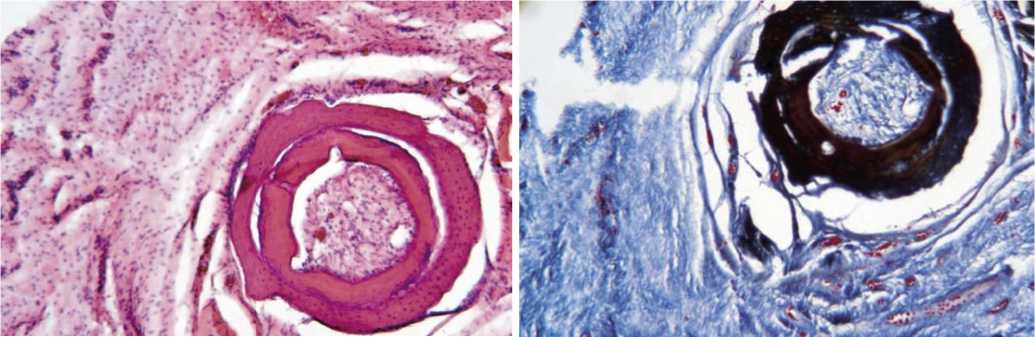
Рис. 16. Гистологическая картина зоны имплантации у животных в подгруппе L-кость через 90 дней
плантируемым материалом, поры заполнены рыхлой соединительной тканью.
Признаков воспаления не наблюдается. В зоне заживления просветы сосудов, заполненные форменными элементами крови, что может свидетельствовать об анн-гиогенезе (рис. 17).
Группа 4 (имплантируемый материал хрящ), 14-сутки после имплантации.
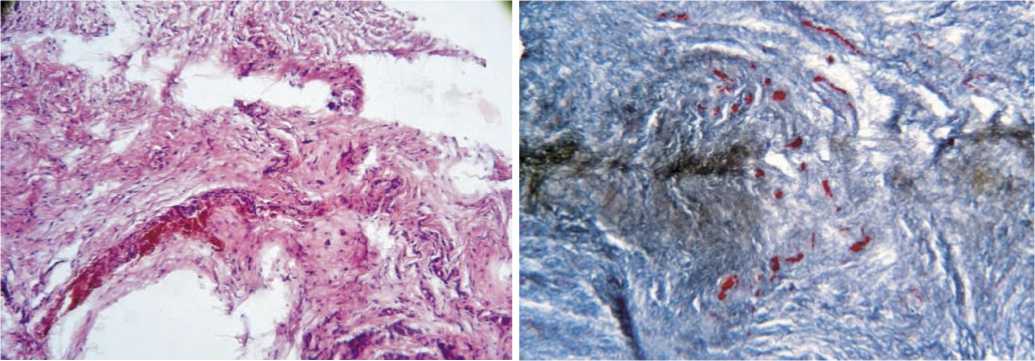
Рис. 17. Гистологическая картина зоны имплантации у животных в подгруппе R-кость с богатой тромбоцитами плазмой через 90 дней
Признаков воспалительной реакции мы не наблюдали, однако определялось незначительное смещение имплантата слева (2 балла), тогда как комбинация хряща и плазмы ограничивала миграцию имплантата (1 балл).
Микроскопическая картина характеризовалась наличием воспалительной реакции умеренной степени в подгруппе L-хрящ, ткани вдоль имплантата «укладываются» в фибробластоподобные слои.
В подгруппе R-хрящ с богатой тромбоцитами плазмой зона имплантата инфильтрирована форменными элементами крови, определяются признаки воспалительного процесса в умеренной степени, выражена нейтрофильная реакция (рис. 18).
Группа 4 (имплантируемый материал хрящ), 30-сутки после имплантации.
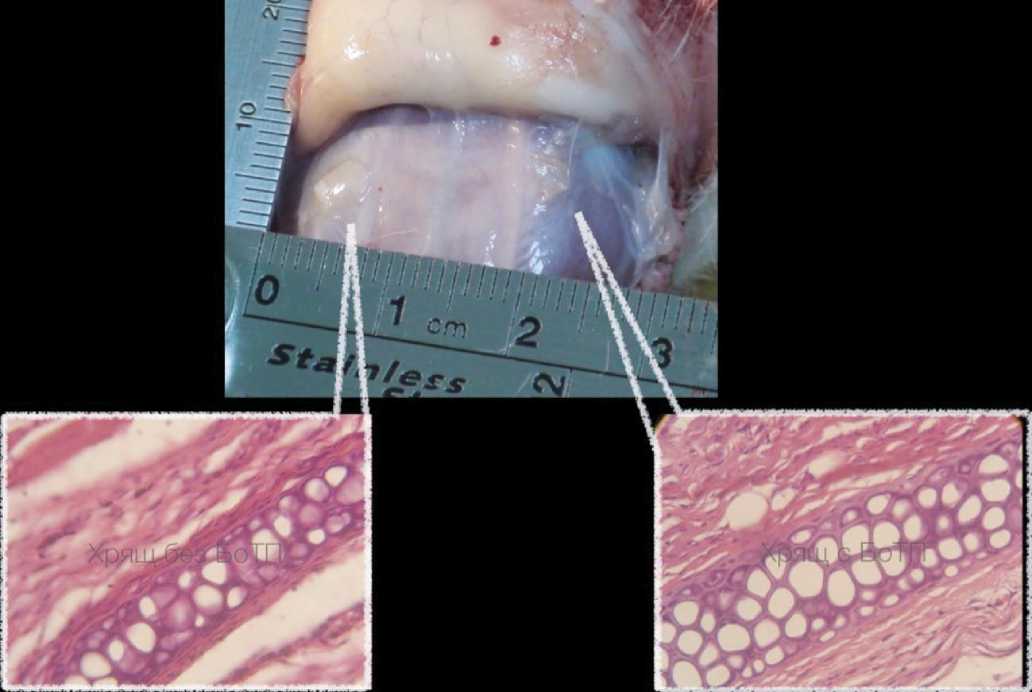
Рис. 18. Макро и микроскопическая картина зоны имплантации у животных 4 группы на 14 сутки
Макроскопическая картина не отличалась от предыдущего исследования.
В подгруппе L-хрящ вдоль имплантата формируется соединительно-тканая капсула с вкраплением гигантских клеток. Ткань вокруг капсулы рыхлая, не дифференцированная (рис. 19).
В подгруппе R-хрящ с богатой тромбоцитами плазмой в зоне соединения имплантата с окружающей тканью визуализируются пласты выраженной капсулоподобной ткани. Воспалительный процесс на стадии угасания (рис. 20).
Группа 4 (имплантируемый материал хрящ), 90-сутки после имплантации.
Макроскопически признаков воспаления нет в обеих подгруппах. Отмечено незначительное смещение имплантатов (1 балл).
Сформирована многослойная рыхлая капсула, имеющая более плотные слои к имплантату в подгруппе L-хрящ (рис. 21).
На 90-е сутки в подгруппе R-хрящ с богатой тромбоцитами плазмой клетки занимали все углубления и дефекты в имплантате (рис. 22).
Таким образом, при оценке макроскопической картины во всех группах животных нами отмечено более стабильное положение имплантируемого материала в комбинации с богатой тромбоцитами плазмой. Резорбцию мы наблюдали только в группе с имплантацией костного материала в обеих подгруппах.
При гистологической оценке состояния имплантатов и реакции окружающих тканей были выявлены:
– низкая степень интеграции к окружающим тканям силикона в обеих подгруппах при минимальной воспалительной реакции окружающих тканей;
– умеренная воспалительная реакция окружающих тканей при имплантации пористого полиэтилена, менее выраженная в комбинации с богатой тромбоцитами плазмой;
– высокая степень интеграции к окружающим тканям пористого полиэтилена;
– потеря структурности обоих вариантов костного имплантата на ранних сроках, что связано с частичной резорбцией костного материала;
– сохранение структурности и отсутствие миграции хрящевого имплантата более выражено в комбинации с богатой тромбоцитами плазмой.
Таким образом, в результате проведенного экспериментального исследования на основании макроскопического анализа и гистологического исследования мы убедились в преимуществах комбинированного использования богатой тромбоцитами плазмы как с синтетическими, так и с биологическими материалами. В этих случаях достигается большая ранняя структурная стабильность комплекса «ткань-имплантат» на фоне менее выраженной воспалительной реакции окружающих тканей.
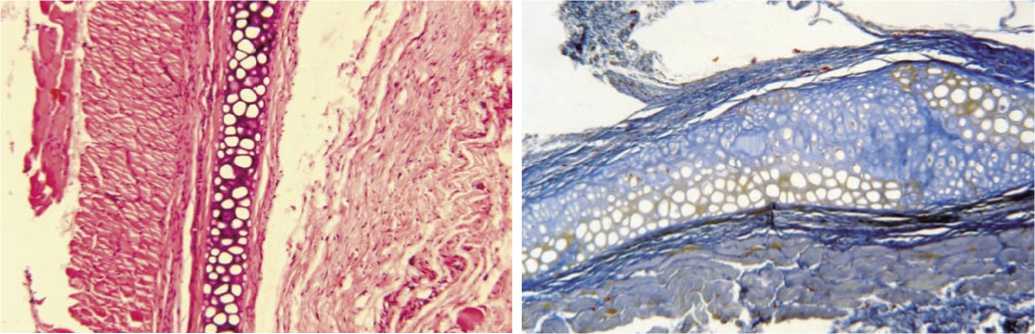
Рис. 19. Гистологическая картина зоны имплантации у животных в подгруппе L-хрящ через 30 дней
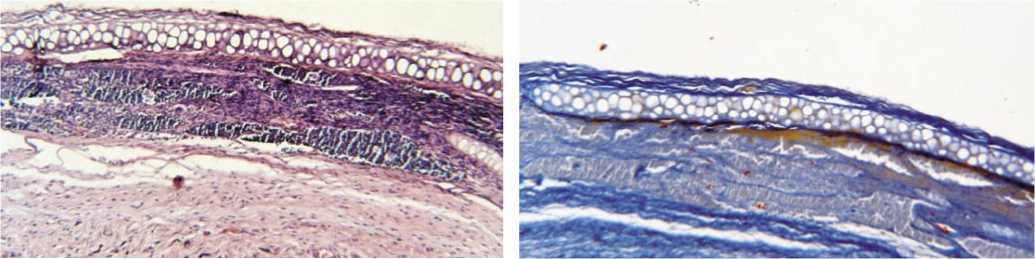
Рис. 20. Гистологическая картина зоны имплантации у животных в подгруппе R-хрящ с богатой тромбоцитами плазмой через 30 дней
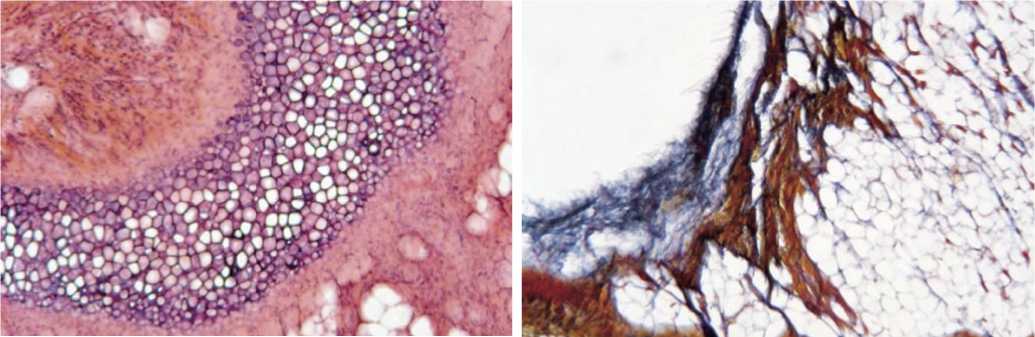
Рис. 21. Гистологическая картина зоны имплантации у животных в подгруппе L-хрящ на 90 сутки
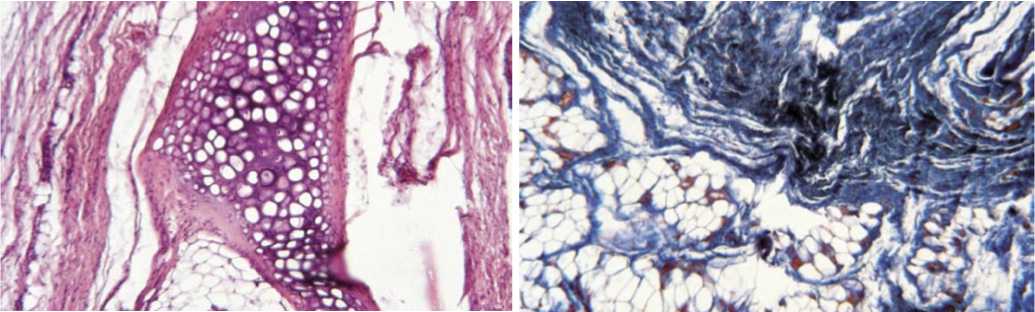
Рис. 22. Гистограмма зоны имплантации у животных в подгруппе R-хрящ с богатой тромбоцитами плазмой через 90 дней
Список литературы Использование различных имплантационных материалов в реконструктивной хирургии. Экспериментальное исследование
- Choi BH, Zhu SJ, Kim BY, Huh JY, Lee SH, Jung JH. Effect of platelet-rich plasma (PRP) concentration on the viability and proliferation of alveolar bone cells: an in vitro study.//Int J Oral Maxillofac Surg. 2005 Jun; 34(4): 420-4
- Choukroun J, Adda F, Schoeffler C, Vervelle A. Une opportunite en paro-impla-ntologie. Le PRF (platelet richfibrin).Implantodont 2001; 41: 55-62.
- Fennis JP, Stoelinga PJ, Jansen JA. Mandibular reconstruction: a histological andhistomorphometricstudyontheuseofautogenous scaffolds, particulate cortico-can-cellous bone grafts and platelet rich plasma in goats. Int J Oral Maxillofac Surg. 2004 Jan; 33(l): 48-55.
- Hanna R, Trejo PM, Weltman RL. Treatment of intrabony defects with bovine-derived xenograft alone and in combination with platelet-rich plasma: a randomized clinical trial. J Periodontal. 2004 Dec; 75(12): 1668-77.
- Jain S., Jin L.J. and Corbet E.F., Preparation and assessment of Platelet Rich Plasma for periodontal surgery, Journal of Dental Research. 2004, 83 (Spec IssA): 1133.
- Kilian O, Alt V, Heiss C, Jonuleit T, Dingeldein E, Flesch I, Fidorra U, Wenis-ch S, Schnettler R. New blood vessel formation and expression of VEGF receptors after implantation of platelet growth factor-enriched biodegradable nanocrystalline hydroxyapatite.//Growth Factors. 2005 Jun; 23(2): 125-33.
- Lekovic V, Camargo PM, Weinlaender M, Vasilic N, Aleksic Z, Kenney EB. Effectiveness of a combination of platelet-rich plasma, bovine porous bone mineral and guided tissue regeneration in the treatment of mandibular grade II molar furcations in humans. J Clin Periodontal. 2003 Aug;30(8):746-51.
- Man D, Plosker H, Winland-Brown JE. The use of autologous platelet-rich plasma (platelet gel) and autologous platelet-poor plasma (fibrin glue) in cosmetic surgery. Plast Reconstr Surg. 2001 Jan;107(l):229-37; discussion 238-9.
- Marx R.E., Garg A.K., Dental and craniofacial applications of platelet-rich plasma. Quintessence books 2005: 3-49; 103-133.
- Marx R.E., Platelet-Rich Plasma: Evidence to Support Its Use J Oral Maxillofac Surg 62: 489-496, 2004.
- Marx RE, Carlson ER, Eichstaedt RM, Schimmele SR, Strauss JE, Georg-eff KR. Platelet-rich plasma: Growth factor enhancement for bone grafts. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 1998 Jun;85(6): 638-46.
- Mendonca-Caridad JJ, Juiz-Lopez P, Rubio-Rodriguez JP. Frontal sinus obliteration and craniofacial reconstruction with platelet rich plasma in a patient with fibrous dysplasia. Int J Oral Maxillofac Surg. 2006 Jan;35(l):88-91.
- Okuda K, Tai H, Tanabe K, Suzuki H, Sato T, Kawase T, Saito Y, Wolff LF, Yoshiex H. Platelet-rich plasma combined with a porous hydroxyapatite graft for the treatment of intrabony periodontal defects in humans: a comparative controlled clinical study. J Periodontol. 2005 Jun; 76(6): 890-8.
- Oyama T, Nishimoto S, Tsugawa T, Shimizu F. Efficacy of platelet-rich plasma in alveolar bone grafting. J Oral Maxillofac Surg. 2004 May; 62(5): 555-8.
- Sammartino G, Tia M, Marenzi G, di Lauro AE, D’Agostino E, Claudio PP. Use of autologous platelet-rich plasma (PRP) in periodontal defect treatment after extraction of impacted mandibular third molars. J Oral Maxillofac Surg. 2005 Jun; 63(6): 766-70.
- Sanchez AR, Eckert SE, Sheridan PJ, Weaver AL. Influence of platelet-rich plasma added to xenogeneic bone grafts on bone mineral density associated with dental implants. Int J Oral Maxillofac Implants. 2005 Jul-Aug; 20(4): 526-32.
- Wojtowicz A, Chaberek S, Kryst L, Urbanowska E, Ciechowicz K, Ostrowski K. Fourier and fractal analysis of maxillary alveolar ridge repair using platelet rich plasma (PRP) and inorganic bovine bone. Int J Oral Maxillofac Surg. 2003 Feb; 32(l): 84-6.
- Zhang CQ, Yuan T, Zeng BF. Experimental study of the effect of platelet-rich plasma on osteogenesis in rabbit.//Chin Med J (Engl). 2004 Dec; 17(12): 1853-5.


