Исследование антимюллерова гормона у собак
Автор: Хуснетдинова Н.Ф., Ипполитова Т.В.
Статья в выпуске: 2 т.242, 2020 года.
Бесплатный доступ
По количеству антимюллерова гормона можно определить отсутствие или наличие яичников у самок. Показаны достоверные различия содержания АМГ у самок интактных и стерилизованных. Содержание АМГ у самок в разные периоды полового цикла не одинаковы. У собак с овариореминантным синдромом уровень АМГ не всегда различается от уровня АМГ у стерилизованных.
Гормон, амг, собаки, эндокринология
Короткий адрес: https://sciup.org/142224228
IDR: 142224228 | УДК: 636.7:612.08 | DOI: 10.31588/2413-4201-1883-242-2-198-202
Research of antimuleller hormone in dogs
The presence or absence of ovaries in females may be told by the quantity of anti-Mullerian hormone. The evidential differences between the quantities of AMH in untreated and neutered females have been demonstrated. The quantity of AMH in females in different periods of genesial cycle is not the same. The level of AMH in dogs with Ovarian remnant syndrome is not always different from the level of AMH in neutered ones.
Текст научной статьи Исследование антимюллерова гормона у собак
Эндокринные исследования для оценки функционального состояния животных имеют огромное значение. Достижения, отметившие развитие эндокринологии за последние годы, заставили переосмыслить и существенно дополнить наши преставления о механизмах репродуктивных процессов. Гормонов, отвечающих за исправное функционирование репродуктивной системы животных много. Одним из наименее изученных среди них является антимюллеров гормон (АМГ).
В 19 веке немецким анатомом и физиологом Иоганном Мюллером был описан проток, названный мюллеровым. Первоначально мюллеров проток есть у зародышей как женского, так и мужского пола. У будущих особей мужского рода Мюллеров проток редуцируется под действием антимюллерова гормона. Об этом свидетельствуют исследования, проведенные [4, 8] на мышах и овцах. А у зародышей жен- ского пола недостаток АМГ позволяет Мюллерову протоку формироваться дальше и из него образуется матка и верхняя часть влагалища.
Секреция АМГ у особей мужского рода начинается в период эмбриогенеза и продолжается на протяжении всей жизни. Секретируется АМГ у самцов клетками Сертоли. АМГ у самок синтезируется клетками гранулезы первичных, преан-тральных и антральных фолликулов [6]. В работах на мышах показано, что наиболее высокая концентрация АМГ определялась в преантральных и малых антральных фолликулах [9], а в более крупных антральных фолликулах количество АМГ постепенно снижается. В этом случае АМГ, секретируемый пулом растущих фолликулов, выступает в качестве сигнала обратной связи, подавляя первоначальный выбор первичных фолликулов [2].
Выявлено, что в естественных усло- виях и в условиях эксперимента in vitro на мышах усиливается переход примордиальных фолликулов в первичные при отсутствии АМГ, что приводит к раннему истощению яичников. Основная функция АМГ это торможение роста фолликулов яичника при выборе доминантных фолликулов. Достигается это путем ингибирования перехода примордиальных фолликулов в первичные, растущие фолликулы и путем ингибирования чувствительности к фолликулостимулирующему гормону преантраль-ных и малых антральных фолликулов.
В связи с тем, что АМГ синтезируется исключительно в половых железах [3], он может быть использован в качестве теста, подтверждающего наличие или отсутствия ткани гонад. Ряд авторов [1] исследуя АМГ у собак на различных тест системах сообщают о различной чувствительности теста. Разногласия связаны очевидно с тем, что АМГ является видоспецифичным гормоном (по химической структуре является гликопротеином, относится к семейству В-трасформирующих факторов роста [6]) и не каждая тест система может быть пригодна для его выявления.
В этой связи целью нашей работы было определить концентрацию АМГ в сыворотке крови у стерилизованных самок, интактных и у самок с реминантным яичником на тест системе АМГ GEN 2.
Причиной появления реминантного яичника является неполное удаление тканей яичника во время овариоэктомии или реваскуляризация тканей яичников, по неосторожности уроненных в брюшную полость. Синдром реминантного яичника у собак впервые описали Le Roux и Van Der Walt d в 1977 году. Подозрение на оварио-реминантный синдром возникает тогда, кода у ранее стерилизованного животного появляются признаки течки. Остатки тканей яичников приводят к продолжению выработки гормонов, которые вызывают половое поведение.
Материал и методы исследований. Данное исследование проведено на клинически здоровых собаках разных пород в возрасте от 2 до 14 лет. Перед взятием крови собирали анамнез, проводили клинический осмотр, производили цитологию мазков, УЗИ яичников и матки. Самки были разделены на три группы: интактные самки (n=15) в возрасте 2-6 лет, самки с реминантным яичником (n=7) в возрасте (4-8 лет) и стерилизованные самки без ре-минанта (n=10) в возрасте от 3 до 12 лет. Диагноз овариореминантный синдром был подтвержден диагностической лапарато-мией. Для исследования кровь брали из подкожной вены предплечья в количестве 2-3 мл, затем ее отстаивали в течение 30 мин и центрифугировали при 3300 об\мин в течение 10 мин. Сыворотку отделяли, замораживали и хранили при t -20 °C до использования в исследованиях. Размораживание и повторное замораживание не допускалось. У всех сук были взяты образцы крови для определения АМГ и прогестерона в сыворотки крови.
Определение содержания АМГ проводили иммуноферментным методом с помощью наборов фирмы Beckman Coulter на анализаторе Sunrise Touch. Набор для определения АМГ – AMG GEN 2. Уровень прогестерона в сыворотке крови измеряли с использованием серийно выпускаемых наборов фирмы Хема. Результаты вагинальной цитологии, концентрацию прогестерона оценивали для определения стадии полового цикла. Мазки окрашивали набором для быстрого дифференциального окрашивания Диахим-Дифф-Квик. Цифровые данные, полученные в эксперименте, обработаны биометрически на персональном компьютере с использованием прикладной программы GraphPad Prism v.8. Выборки проходили проверку на нормальность распределения по тесту Шапиро-Вилк. Проверка гипотез проводилась с помощью двухфакторного дисперсионного анализа и t-тест в случае необходимости. Значение p<0,05 считалось статистически значимым.
Результаты исследований. Проведенное исследование на самках собак показало, что у интактных собак АМГ в зависимости от стадии полового цикла составил в период анэструса 2,14±0,36 нг/мл (0,63-4,8) и в период диэструса 1,58±0,1 нг/мл (1,4-1,76). У четырех самок с подтвержденным по узи реминантным яични- ком АМГ в фазу анэструса составил 1,42±0,13 нг/мл, (1,2-1,8). Однако у трех самок с подтвержденным по узи реми- нантным яичником АМГ в фазу диэструса был менее 0,19 нг/мл. Данные приведены на рисунке 1.
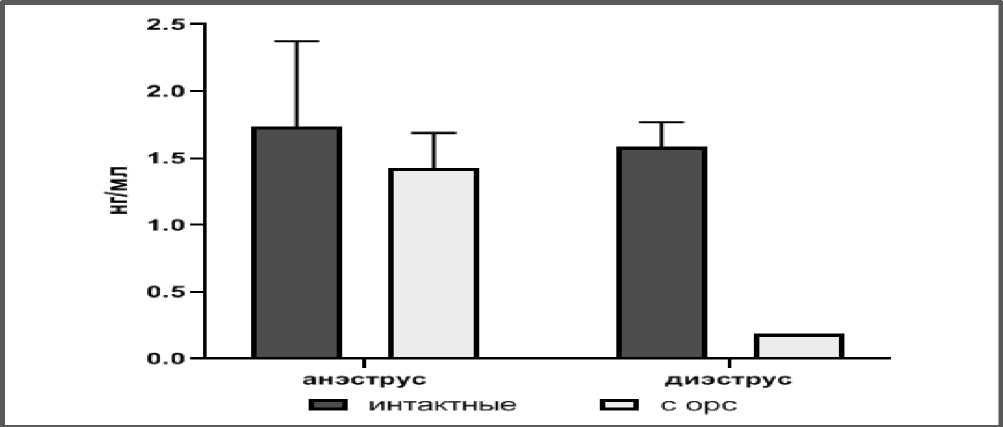
Рисунок 1 – Содержание АМГ в анэструс и диэструс у интактных самок и самок с овариоре-минантным синдромом
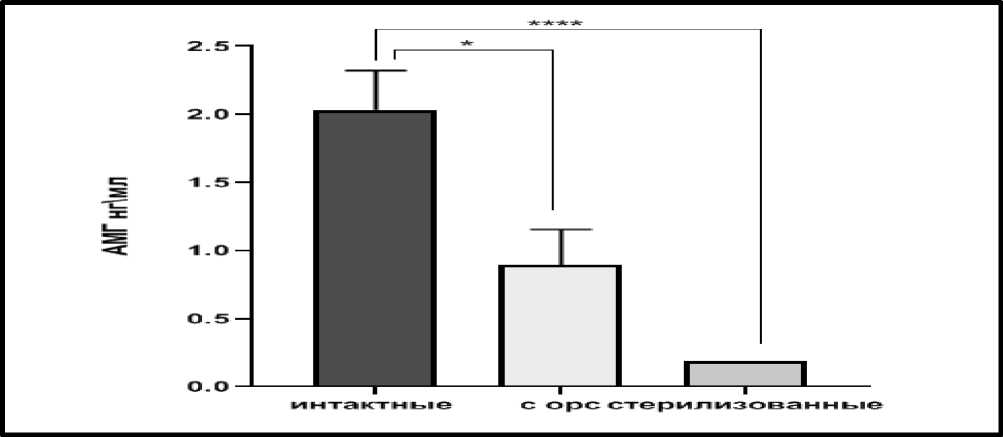
Рисунок 2 – Содержание АМГ у интактных, стерилизованных и с ОРС самок. *p= 0,0129,
****p <0,0001.
Все стерилизованные самки имели уровни АМГ ниже предела обнаружения анализа (<0,19 нг/мл). Таким образом, специфичность правильной идентификации по АМГ самок без яичников составила 100 %. То есть у стерилизованных самок АМГ не выявлен.
Разница между стерилизованными самками и нестерилизованными достоверно различалась (p<0,0001). У 7 собак с овариореминантным синдромом была проведена лапаратомия для подтверждения наличия ткани яичника. Гистологическое исследование подтвердило, что все образцы представляли собой ткань яичника. Концентрация АМГ в сыворотке крови у самок с овариореминантным синдромом была достоверно ниже, чем у группы не-стерилизованных сук (p<0,01). Данные приведены на рисунке 2.
Цитологическое исследование мазков влагалища, клинические данные и уровень прогестерона в сыворотке крови позволили определить стадию полового цикла у каждой самки. В период анэструса у интактных самок прогестерон составил 2,6±0,25 нмоль/л, у собак с овариореми-нантным синдромом – 3,6±0,5 нмоль/л, у стерилизованных – 2,0±0,2 нмоль/л.
В период диэструса у интактных прогестерон составил 28,7±1,02 нмоль/л, у собак с овариореминантным синдромом – 24,1±3,04 нмоль/л. Данные приведены в таблице 1.
Таблица 1 – Содержание антимюллерова гормона и прогестерона у собак разных групп
|
Наименование групп |
Уровень АМГ, нг/мл |
Уровень прогестерона, нмоль\л |
|
Интактные самки в фазе анэструса(n=12) |
2,14±0,36 |
2,6±0,25 |
|
Интактные самки в фазе диэструса (n=3) |
1,58±0,1 |
28,7±1,02 |
|
Стерилизованные самки с реминантным яичником в фазе диэструса (n=3) |
<0,19 |
24,1±3,04 |
|
Стерилизованные самки с реминантным яичником в фазе анэструса (n=4) |
1,42±0,13 |
3,6±0,5 |
|
Cтерилизованные самки (n=10) |
<0,19 |
2,0±0,2 |
Заключение. Настоящее исследование показало, что уровень АМГ в сыворотке крови у стерилизованных самок значительно ниже, чем у интактных. Это заключение указывает на то, что измерение АМГ в сыворотке крови является полезным инструментом для диагностики того, была ли проведена овариоэктомия и это может быть использовано в приютах как наиболее простой тест для диагностики.
Резюме
По количеству антимюллерова гормона можно определить отсутствие или наличие яичников у самок. Показаны достоверные различия содержания АМГ у самок интактных и стерилизованных. Содержание АМГ у самок в разные периоды полового цикла не одинаковы. У собак с овариореминантным синдромом уровень АМГ не всегда различается от уровня АМГ у стерилизованных.
Список литературы Исследование антимюллерова гормона у собак
- Broekmans, F.J. Anti-mllerian hormone and ovarian dysfunction / F.J. Broekmans, J.A. Visser, J.S. Laven [et al.] // Trends Endocrinol Metab. - 2008. - V. 19. - P. 340-347.
- Durlinger, A.L. Control of primordial follicle recruitment by anti-Mullerian hormone in the mouse ovary/ A.L. Durlinger, P. Kramer [et al.] // Endocrinology. - 1999. - V.140 - P. 589-5796.
- La Marca, A. The Anti-Mullerian Hormone and Ovarian Cancer / A. La Marca, A. Volpe // Human Reproduction Update. - 2005. - V. 13. - P. 265-273.
- Munsterberg, A. Expression of the mouse anti-Mullerian hormone gene suggests a role in both male and female sexual differentiation / A. Munsterberg, R. Lovell // Development. - 1991. -V.113. - P. 613-624.
- Nagashima, J.B. Anti-mullerian hormone in the domestic dog during the anestrus to oestrous transition / J.B. Nagashima, B.S. Hansen, M.M. Matzuk [et al.] // Reprod. Domest. Anim. - 2016. - V. 51. - P. 158-164.
- Picard J.Y. Purification of testicular anti-mullerian hormone allowing direct visualization of the pure glycoprotein and determination of yield and purification factor / J.Y. Picard, N. Josso // Mol. Cell. Endocrinol. - 1984. - V. 34. - P. 23-29.
- Pir, Y.I. Does serum anti-mullerian hormone levels always discriminate presence of the ovaries in adult bitches? / Y.I. Pir [et al.] // Comparison of two ELISA kits. Reprod. Domest. Anim. - 2016. - P. 910-915.
- Sweeney, T. Ontogeny of anti-Mullerian hormone, 3-B-hydroxysteroid dehydrogenase and androgen receptor expression during / T. Sweeney, P.K. Saunders, M.R. Millar [et al.]. -1997. - V. 153. - P. 27-32.
- Weenen, C. Anti-Mullerian Hormone expression pattern in the human ovary: potential implications for intial and cyclic follicle retuitment / C. Weenen, J.S. Laven // Mol. Hum. Reprod. - 2004. - V. 10. - P. 77-83.


