Исследование микроциркуляции у больных с аортальным пороком до и после коррекции
Автор: Окунева Г.Н., Булатецкая Л.М., Семенов И.И., Железнев С.И., Клинкова А.С., Аминов В.В., Кузнецова Е.Г.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Приобретенные пороки сердца
Статья в выпуске: 2 т.10, 2006 года.
Бесплатный доступ
Микроциркуляторный кровоток (МЦК) с помощью метода лазер-допплеровской флоуметрии (ЛДФ) определялся на эпикарде каждой камеры сердца, а также на стенках магистральных сосудов. Измерения производились до и после хирургической коррекции у 58 пациентов с аортальным пороком (АП): 41 пациент с аортальным стенозом (АС) и 17 - с аортальной недостаточностью (АН). По данным эхокардиографии определялся тип гипертрофии ЛЖ (концентрический или эксцентрический). Установлено, что гипертрофия ЛЖ развивается в прямой зависимости от возраста пациентов (r = 0,50) и градиента давления между ЛЖ и Ао (r = 0,71). У пациентов с АП после хирургической коррекции порока наблюдалось достоверное снижение МЦК правых отделов сердца и тенденция к снижению левых отделов. У пациентов с АС до операции повышенному (в 4 раза) по сравнению с АН градиенту между ЛЖ и Ао соответствует достоверно увеличенная гипертрофия ЛЖ и сниженный МЦК по ЛЖ и Ао. После операции у пациентов с АС и АН выявляется снижение МЦК на всех участках и выравнивание градиентов между аналогичными участками. Снижение МЦК по ПЖ и по ЛЖ и выравнивание градиента между ними после хирургической коррекции АП не зависит от типа имплантируемого клапана (механического или биологического).
Короткий адрес: https://sciup.org/142233329
IDR: 142233329
Текст научной статьи Исследование микроциркуляции у больных с аортальным пороком до и после коррекции
Микроциркуляторный кровоток (МЦК) с помощью метода лазер-допплеровской флоу-метрии (ЛДФ) определялся на эпикарде каждой камеры сердца, а также на стенках магистральных сосудов. Измерения производились до и после хирургической коррекции у 58 пациентов с аортальным пороком (АП): 41 пациент с аортальным стенозом (АС) и 17 - с аортальной недостаточностью (АН). По данным эхокардиографии определялся тип гипертрофии ЛЖ (концентрический или эксцентрический). Установлено, что гипертрофия ЛЖ развивается в прямой зависимости от возраста пациентов (r=0,50) и градиента давления между ЛЖ и Ао (r=0,71). У пациентов с АП после хирургической коррекции порока наблюдалось достоверное снижение МЦК правых отделов сердца и тенденция к снижению левых отделов. У пациентов с АС до операции повышенному (в 4 раза) по сравнению с АН градиенту между ЛЖ и Ао соответствует достоверно увеличенная гипертрофия ЛЖ и сниженный МЦК по ЛЖ и Ао. После операции у пациентов с АС и АН выявляется снижение МЦК на всех участках и выравнивание градиентов между аналогичными участками. Снижение МЦК по ПЖ и по ЛЖ и выравнивание градиента между ними после хирургической коррекции АП не зависит от типа имплантируемого клапана (механического или биологического).
В настоящее время в литературе широко обсуждаются результаты клинического использования двустворчатого протеза «МедИнж» [3, 11] и доказывается его высокая надежность и эффективность. Проводится сравнительная оценка различных типов двустворчатых клапанов: «Карбоникс», «МедИнж», «S. Iude», «Carbomedics» и др. на их прочность, долговечность и гемодинамические характеристики [8]. В то же время отмечается минерализация клапанного аппарата при операциях протезирования у больных с митральным и аортальным пороками [7]. Также выявлены особенности интраоперационной дисфункции ПЖ при протезировании аортального клапана (АоК) [5].
Исследование расположения мышечных волокон в гребне межжелудочковой перегородки в норме позволило авторам прийти к заключению о существовании зон морфологического субстрата для формирования патологической гипертрофии выходного отдела ЛЖ [6].
Изучение этиологической диагностики аортальных пороков сердца показало, что причиной АС в 45% была кальцинация двустворчатого клапана и в 45% - дегенеративно-дистрофический кальциноз; АН в 84% случаев обусловлена мезенхимальной дисплазией и в 12% - инфекционным эндокардитом [9].
Приводя сравнительные данные непосредственных результатов операции Росса и протезирования АоК бескаркасными эпоксиобра-ботанными ксенобиопротезами у пациентов с ППС, авторы пришли к выводу о возможности широкого применения обеих хирургических методик при операциях на АоК [4]. Однако многие вопросы, связанные с изучением гемодинамики в системе микроциркуляции, особенно в капиллярном звене, где осуществляются транспортные и метаболические функции кровообращения, остаются до настоящего времени не изученными. Особый интерес представляет изучение микроциркуляции в капиллярах, когда функциональная нагрузка на ЛЖ резко возрастает в условиях аортального порока. В связи с этим возникает несколько вопросов: 1) Как изменяется МЦК в разных отделах сердца после хирургической коррекции порока? 2) Каковы особенности МЦК в левом желудочке при АС и АН? 3) Зависит ли МЦК отделов сердца от типа имплантированного клапана (механического или биологического)?
Цель настоящего исследования - анализ результатов интраоперационного определения МЦК в разных участках сердца и на стенках магистральных сосудов у пациентов с АП до и после коррекции порока.
МАТЕРИАЛ И МЕТОДЫ
МЦК определялся с помощью метода ЛДФ на BLF-21 «Transonic System Inc» (США) в комплексе с персональным компьютером. Записи МЦК производились во время операции поверхностным датчиком типа «R» (rite angle) диаметром 15 мм в течение 20 с на каждом исследуемом участке с последующим расчетом средней величины МЦК. Фиксировались исходные показатели МЦК перед хирургической коррекцией порока с эпикарда каждой камеры сердца (ЛП, ПП, ЛЖ, ПЖ), а также на стенках магистральных сосудов (ЛА, Ао) до и после устранения порока и восстановления гемодинамики (ЛП 1 , ПП 1 , ЛЖ 1 , ПЖ 1 , ЛА 1 , Ао 1 ). Одновременно с измерением МЦК регистрировались основные показатели гемодинамики АДС, АДД, АДср и ЧСС, рассчитывалось двойное произведение (ДП): ЧСС х АДср. Для оценки степени гипертрофии левого желудочка (ГЛЖ) у всех пациентов по данным эхографии анализировались размеры и объемы ЛЖ: КДР, КДО, КСО, а также толщина межжелудочковой перегородки (ТМЖП) и задней стенки ЛЖ (ТЗСЛЖ). Для определения величины ГЛЖ рассчитывалась масса миокарда ЛЖ (ММЛЖ) по формуле N. Reicheck и R. Devereux [19] и затем ее отношение к площади поверхности тела - величина индекса ММЛЖ (ИММЛЖ). При наличии ГЛЖ, по данным приведенных авторов, величины ИММЛЖ превышают 118 г/м2 у мужчин и 104 г/м2 у женщин. Относительная толщина миокарда определялась по формуле: ОТМ=2ТЗСЛЖ/КДР [1].
В соответствии с принципом Ganau оценивали тип гипертрофии: концентрический при показателях ОТМ>0,45, ИММЛЖ>118 г/м2 - у мужчин и >104 г/м2 - у женщин либо эксцентрический - ОТМ<0,45, ИММЛЖ>118 и >104 г/м2 соответственно. Геометрию ЛЖ расценивали как нормальную геометрию (НГ) при ОТМ<0,45, ИММЛЖ<118 и <104 г/м2.
Обследовано 58 пациентов с АП, средний возраст которых составил 47,5±1,54 года (79% лиц мужского пола и 21% - женского). Из них 41 пациент с АС (средний возраст - 49,3±1,70 года) и 17 пациентов с АН (средний возраст 43,2±3,17 года), причем у 79% обследованных были ППС. У всех пациентов были прямые показания к протезированию АоК; 73% пациентов имели хроническую сердечную недостаточность (ХСн) НА, III ФК по NYHA.
У 40 пациентов проанализированы результаты изменений МЦК до и после имплантации механических клапанов: «Карбоникс», «Мед-
Индж», «МИКС» и у 10 пациентов с имплантацией биологических клапанов: «Кемкор», «Кемерово АБ-композит», включая операцию Росса.
РЕЗУЛЬТАТЫ
Как видно из рис. 1, после операции МЦК снижается по всем отделам сердца, при этом достоверно снизился МЦК на четырех участках: по ПП на 13,6±3,22 мл/(100г • мин) (р<0,001) и составил после операции 81% от фона, а также по ПЖ на 7,2±2,73 мл/(100 г • мин) (р<0,01) и составил 91% от фона, по ЛА на 17,7±4,5 мл/ (100 г • мин) (р<0,001) и составил 78% и по Ао на 13,9±5,7 мл/(100 г • мин) (р<0,05) - 80%. По левым отделам сердца отмечена только тенденция к снижению МЦК: на ЛП - 1,0±4,0 (р>0,05), на ЛЖ - 5,1±2,7 мл/(100 г • мин) (р>0,05). В то же время следует отметить, что со стороны центральной гемодинамики наблюдалось незначительное увеличение исследованных параметров: АДД, АДср., ЧСС, ДП (р>0,05). Таким образом, у пациентов с АоП после хирургической коррекции наблюдалось снижение МЦК всех отделов сердца на фоне несущественного по-
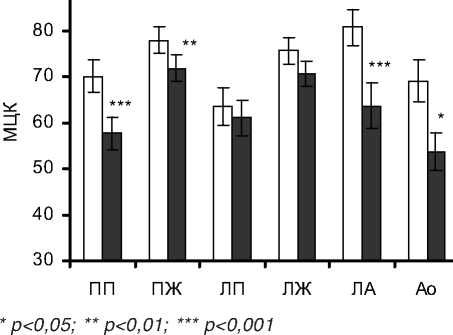
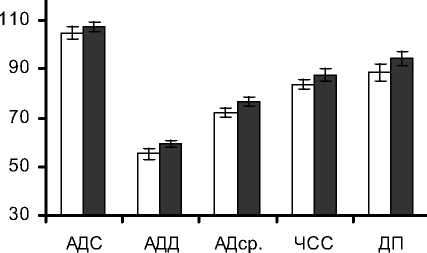
□ до операции □ после операции
Рис. 1. Микроциркуляторный кровоток у больных с аортальным пороком до и после коррекции.
вышения интегральных показателей центральной гемодинамики.
Корреляционный анализ исследуемых показателей выявил следующие значимые корреляции (р<0,01): прямая корреляционная связь возраста пациентов и показателей, характеризующих гипертрофию миокарда ЛЖ: ТМЖП (r=0,48) и ТзСлЖ (r=0,52), т. е. если у пациентов молодого возраста ТЗСЛЖ составляла 1,01,25 см, то в возрасте старше 50 лет она колебалась от 1,5 до 2,2 см и выше (рис. 2). Оба показателя находились в прямой корреляционной зависимости от градиента ЛЖ/Ао: для ТЗСЛЖ r=0,71 (рис. 3); для ТМЖП r=0,47, т. е. гипертрофия ЗСЛЖ в большей степени зависит от градиента ЛЖ/Ао, о чем свидетельствует более высокий коэффициент корреляции. В то же
ТЗСЛЖ =0,96705+ 0,01155 х А г = 0,51644
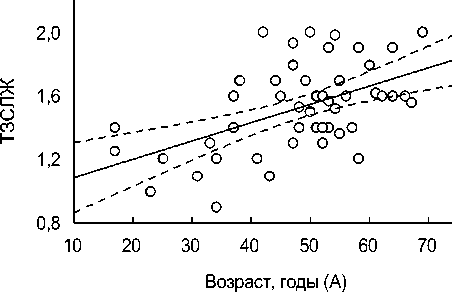
Рис. 2. Регрессионная зависимость ТЗСЛЖ от возраста.
ТЗСЛЖ = 1,2339 + 0,00533 х Градиент Ао/ЛЖ г = 0,71451
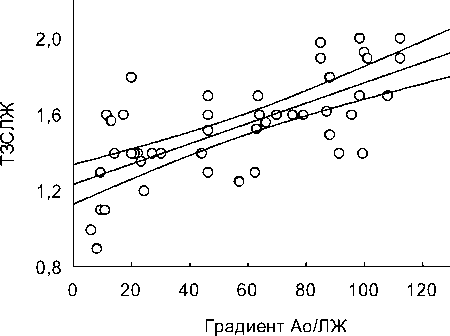
Рис. 3. Регрессионная зависимость ТЗСЛЖ от градиента Ао/ЛЖ.
время ТМЖП находилась в обратной зависимости от КДР (r= -0,34) и МЦК по Ао (r= -0,45), т. е. чем больше была выражена гипертрофия, тем меньше был КДР и тем ниже был МЦК по Ао. Необходимо отметить, что МЦК по Ао находился также в обратной корреляционной зависимости от возраста. Таким образом, гипертрофия МЖП, с одной стороны, развивается в прямой зависимости от возраста пациентов, а значит и длительности существования порока, с другой стороны, она сопряжена со снижением КДР и МЦК по аорте.
Поскольку АП включал в себя две диагностические группы: АС (n=41) и АН (n=17), был проведен анализ всех исследуемых показателей по этим группам (табл. 1). Сопоставление эхокардиографических данных показало, что до операции градиент ЛЖ/Ао у пациентов с АС достоверно увеличен по сравнению с АН: 79±5,1 и 19,7±2,8 мм рт. ст. соответственно (р<0,0001) и, как следствие, повышены показатели, характеризующие гипертрофию: ТЗСЛЖ 1,63±0,04 и 1,31±0,05 см (р<0,0001), ТМЖП - 1,63±0,06 и 1,37±0,08 см (р<0,05). В то же время размеры и КДО ЛЖ у пациентов с АС по сравнению с АН были достоверно снижены: КДР - 5,34±0,13 и 6,37±0,20 см (р<0,0005), КСР - 3,37±0,16 и 4,19±0,21 см (р<0,0001), и КДО - 143,7±10,75 и 210,3±17,28 мл (р<0,005). При этом диастолическое давление у пациентов с АН было в среднем на 21% ниже (р<0,01), чем у пациентов с АС. Интраоперационные показатели МЦК у пациентов с АН по отношению к АС до операции были ниже по ЛП, ЛЖ, Ао, ЛА, однако достоверное снижение отмечено только по Ао (р<0,05). Таким образом, нагрузка повышенным объемом на левые отделы сердца у пациентов с АН, в отличие от пациентов с АС, у которых нагрузка обусловлена повышенным давлением, при водит к снижению МЦК этих отделов. Необходимо отметить, что МЦК по правым отделам существенно не отличался по группам ни до, ни после операции.
После коррекции порока у пациентов с АН наблюдалось достоверное повышение АДД на 45% (р<0,001), при этом отмечено достоверное снижение МЦК по Ао (р<0,01), а также по ЛА (р<0,05), по ЛЖ - тенденция к снижению. У пациентов с АС после операции достоверно снижал ся МЦК только по ПП (р<0,01). На других участках отмечена тенденция к снижению за исключением ЛП и ЛЖ, на которых МЦК практически не менялся. Также не менялись и показатели гемодинамики, АД и ЧСС. Полученные результаты свидетельствуют о том, что у
Таблица 1
Характеристика больных с аортальным стенозом и недостаточностью аортального клапана
|
Показатели - |
Аортальный стеноз |
Аортальная недостаточность |
- Р |
||||
|
п |
М 1 |
±т 1 |
п |
М 2 |
±т 2 |
||
|
До хирургической коррекции |
|||||||
|
ФВ, % |
39 |
0,59 |
0,02 |
18 |
0,62 |
0,02 |
0,513 |
|
ТЗСЛЖ, см |
29 |
1,63 |
0,04 |
18 |
1,31 |
0,05 |
0,000 |
|
ТМЖП, см |
39 |
1,63 |
0,06 |
17 |
1,37 |
0,08 |
0,012 |
|
ОТМ, отн. ед. |
27 |
0,64 |
0,03 |
16 |
0,43 |
0,02 |
0,000 |
|
ММЛЖ, г |
27 |
499,0 |
29,91 |
15 |
509,6 |
45,68 |
0,841 |
|
ИММЛЖ, г/м2 |
26 |
268,1 |
16,83 |
15 |
274,9 |
25,71 |
0,821 |
|
КДР, см |
38 |
5,34 |
0,13 |
16 |
6,37 |
0,20 |
0,000 |
|
КСР, см |
35 |
3,37 |
0,16 |
17 |
4,19 |
0,21 |
0,004 |
|
КДО, мл |
28 |
143,7 |
10,75 |
15 |
210,3 |
17,28 |
0,001 |
|
КСО, мл |
27 |
61,7 |
8,50 |
13 |
85,7 |
12,65 |
0,119 |
|
Градиент ЛЖ/Ао, мм рт. ст. |
31 |
79,0 |
5,06 |
17 |
19,7 |
2,78 |
0,000 |
|
ПП, мл/(мин ■ 100 г) |
30 |
69,8 |
4,66 |
17 |
70,5 |
5,43 |
0,924 |
|
ПЖ, мл/(мин ■ 100 г) |
40 |
79,1 |
3,56 |
18 |
75,3 |
3,56 |
0,541 |
|
ЛП, мл/(мин ■ 100 г) |
27 |
62,3 |
5,06 |
14 |
66,4 |
7,17 |
0,645 |
|
ЛЖ, мл/(мин ■ 100 г) |
38 |
73,0 |
3,71 |
18 |
81,2 |
4,11 |
0,185 |
|
ЛА, мл/(мин ■ 100 г) |
21 |
78,2 |
4,90 |
9 |
86,6 |
5,59 |
0,322 |
|
Ао, мл/(мин ■ 100 г) |
24 |
62,6 |
5,69 |
11 |
83,5 |
4,72 |
0,027 |
|
АДС, мм рт. ст. |
38 |
101,3 |
3,11 |
17 |
113,2 |
3,77 |
0,029 |
|
АДД, мм рт. ст. |
36 |
59,6 |
2,46 |
17 |
46,9 |
3,92 |
0,007 |
|
АДср., мм рт. ст. |
36 |
73,8 |
2,52 |
17 |
69,0 |
3,36 |
0,278 |
|
ЧСС, уд/мин |
38 |
83,6 |
2,42 |
17 |
83,9 |
3,79 |
0,941 |
|
ДП, отн. ед. |
37 |
85,5 |
4,09 |
17 |
95,6 |
5,98 |
0,170 |
|
После хирургической коррекции |
|||||||
|
ПП 1 , мл/(мин ■ 100 г) |
29 |
55,4* |
4,73 |
16 |
61,8 |
4,73 |
0,389 |
|
ПЖ 1 , мл/(мин ■ 100 г) |
37 |
71,0 |
3,35 |
16 |
73,6 |
5,34 |
0,682 |
|
ЛП 1 , мл/(мин ■ 100 г) |
24 |
61,2 |
5,22 |
14 |
61,1 |
5,81 |
0,983 |
|
ЛЖ 1 , мл/(мин ■ 100 г) |
37 |
71,6 |
3,18 |
16 |
68,6 |
5,07 |
0,610 |
|
ЛА 1 , мл/(мин ■ 100 г) |
17 |
64,3 |
6,73 |
7 |
61,9* |
5,35 |
0,830 |
|
Ао 1 , мл/(мин ■ 100 г) |
24 |
54,0 |
5,29 |
12 |
53,4** |
6,57 |
0,946 |
|
АДС 1 , мм рт. ст. |
38 |
105,5 |
2,25 |
17 |
112,6 |
3,76 |
0,097 |
|
АДД 1 , мм рт. ст. |
37 |
57,5 |
1,62 |
17 |
64,2*** |
1,62 |
0,028 |
|
АДср. 1 , мм рт. ст. |
37 |
75,1 |
2,27 |
17 |
80,3* |
2,81 |
0,185 |
|
ЧСС 1 , уд/мин |
37 |
86,4 |
3,21 |
17 |
90,4 |
2,77 |
0,430 |
|
ДП 1 , отн. ед. |
36 |
91,1 |
3,90 |
17 |
101,6 |
4,22 |
0,106 |
Таблица 2
|
Показатели |
Гипертрофия |
Р |
|||||
|
концентрическая |
эксцентрическая |
||||||
|
п |
М 1 |
±т |
п |
М 2 |
±т |
||
|
До хирургической коррекции |
|||||||
|
ФВ, % |
31 |
0,62 |
0,021 |
10 |
0,61 |
0,036 |
0,7516 |
|
ТЗСЛЖ, см |
31 |
1,63 |
0,042 |
10 |
1,22 |
0,050 |
0,0000 |
|
ТМЖП, см |
31 |
1,69 |
0,066 |
10 |
1,26 |
0,055 |
0,0009 |
|
ОТМ, отн. ед. |
31 |
0,63 |
0,026 |
10 |
0,37 |
0,019 |
0,0000 |
|
ММЛЖ, г |
31 |
509 |
31,8 |
10 |
480 |
36,6 |
0,6237 |
|
ИММЛЖ, г/м2 |
31 |
274 |
17,4 |
10 |
262 |
21,5 |
0,7174 |
|
КДР, см |
31 |
5,28 |
0,138 |
10 |
6,67 |
0,218 |
0,0000 |
|
КСР, см |
29 |
3,23 |
0,165 |
10 |
4,45 |
0,272 |
0,0006 |
|
КДО, мл |
27 |
140 |
10,2 |
9 |
235 |
22,5 |
0,0001 |
|
КСО, мл |
25 |
54,1 |
7,54 |
8 |
99,2 |
18,53 |
0,0117 |
|
Градиент ЛЖ/Ао, мм рт. ст. |
30 |
67,2 |
6,39 |
9 |
23,2 |
4,61 |
0,0008 |
|
ПП, мл/(мин ■ 100 г) |
26 |
72,6 |
4,14 |
10 |
69,7 |
8,29 |
0,7385 |
|
ПЖ, мл/(мин ■ 100 г) |
31 |
80,9 |
3,85 |
10 |
79,3 |
7,95 |
0,8403 |
|
ЛП, мл/(мин ■ 100 г) |
23 |
64,7 |
4,88 |
10 |
68,6 |
8,84 |
0,6823 |
|
ЛЖ, мл/(мин ■ 100 г) |
31 |
74,8 |
3,89 |
10 |
77,0 |
5,66 |
0,7718 |
|
ЛА, мл/(мин ■ 100 г) |
18 |
82,3 |
4,56 |
6 |
85,5 |
7,73 |
0,7236 |
|
Ао, мл/(мин ■ 100 г) |
18 |
66,6 |
6,81 |
7 |
83,3 |
6,38 |
0,1678 |
|
АДС, мм рт. ст. |
29 |
100,2 |
4,01 |
10 |
113,1 |
3,22 |
0,0785 |
|
АДД, мм рт. ст. |
27 |
56,9 |
3,57 |
10 |
45,4 |
3,32 |
0,0751 |
|
АДср., мм рт. ст. |
27 |
71,7 |
3,48 |
10 |
68,0 |
2,62 |
0,5380 |
|
ЧСС, уд/мин |
30 |
81,0 |
2,37 |
10 |
82,7 |
3,41 |
0,7062 |
|
ДП, отн. ед. |
29 |
82,4 |
5,05 |
10 |
93,7 |
5,09 |
0,2258 |
|
После хирургической коррекции |
|||||||
|
ПП 1 , мл/(мин ■ 100 г) |
24 |
55,7** |
5,12 |
10 |
57,6 |
6,36 |
0,8330 |
|
ПЖ 1 , мл/(мин ■ 100 г) |
24 |
70,6 |
3,71 |
10 |
75,4 |
7,73 |
0,5324 |
|
ЛП 1 , мл/(мин ■ 100 г) |
22 |
62,8 |
5,20 |
10 |
63,9 |
7,57 |
0,9108 |
|
ЛЖ 1 , мл/(мин ■ 100 г) |
27 |
72,5 |
3,52 |
10 |
67,4 |
6,89 |
0,4777 |
|
ЛА 1 , мл/(мин ■ 100 г) |
15 |
64,5 * |
6,93 |
5 |
64,4 |
7,21 |
0,9980 |
|
Ао 1 , мл/(мин ■ 100 г) |
18 |
49,5 * |
5,08 |
8 |
42,1*** |
6,48 |
0,4101 |
|
АДС 1 , мм рт. ст. |
29 |
108,4 |
3,26 |
10 |
110,4 |
4,37 |
0,7519 |
|
АДД 1 , мм рт. ст. |
28 |
59,8 |
2,34 |
10 |
63,0** |
2,74 |
0,4506 |
|
АДср. 1 , мм рт. ст. |
28 |
75,9 |
2,57 |
10 |
78,8 |
3,00 |
0,5430 |
|
ЧСС 1 , уд/мин |
30 |
85,3 |
3,20 |
10 |
94,0 |
3,77 |
0,1554 |
|
ДП 1 , отн. ед. |
29 |
92,4 |
4,28 |
10 |
103,8 |
5,75 |
0,1661 |
Характеристика больных аортальным пороком с концентрической и эксцентрической гипертрофией ЛЖ
Таблица 3
Сравнительные данные пациентов с имплантированным механическим и биологическим протезом
Анализ полученных результатов в зависимости от вида гипертрофии показал, что из 58 пациентов с АП 76% имели концентрическую гипертрофию левого желудочка (КГЛЖ) - все больные с АС, а 24% - эксцентрическую гипертрофию левого желудочка (ЭГЛЖ), преимущественно больные с АН (табл. 2). У пациентов с КГЛЖ средняя величина ТЗСЛЖ составляла 1,63±0,042 см (p<0,00001), а у больных с ЭГЛЖ - 1,22±0,050 см. По данным эхографии, все размеры ЛЖ были достоверно выше при ЭГЛЖ (p<0,0001). Градиент ЛЖ/Ао составлял при КГЛЖ 67,2±6,39 мм рт. ст., а при ЭГЛЖ 23,2±4,61 мм рт. ст. (p<0,001). Отмечено, что МЦК до операции по ЛЖ составил при КГЛЖ 74,8±3,89 мл/(100 г • мин), при ЭГЛЖ - 77,0±5,6 мл/(100 г• мин), т. е. достоверно не отличался. После коррекции порока МЦК по ЛЖ при КГЛЖ почти не изменился - 72,5±3,5 мл/(100 г • мин), а при ЭГЛЖ этот показатель снизился до 67,4±6,9 мл/(100 г • мин). Отмечено достоверное снижение МЦК по стенке Ао после коррекции порока у пациентов с КГЛЖ с 66,6±6,81 до 49,5±5,08 мл/(100 г• мин) (p<0,005) и с 83,3±6,4 до 42,1±6,5 мл/(100 г • мин) (p<0,001) при наличии ЭГЛЖ. Одновременно у пациентов с ЭГЛЖ повышалось АДД с 45,4±3,3 до 63±2,7 мм рт. ст. (p<0,001). Эти результаты достоверно свидетельствуют о том, что после успешно выполненной кардиохирургической операции происходит выравнивание МЦК в аналогичных отделах сердца пациентов как с КГЛЖ, так и с ЭГЛЖ.
Проведен сравнительный анализ МЦК после имплантации механических и биологических протезов аортального клапана (табл. 3). Исходно МЦК отделов сердца исследуемых групп достоверных отличий не имели. После устранения порока происходит снижение МЦК по всем отделам сердца независимо от типа протеза (табл. 3). Можно отметить только более заметное снижение МЦК по ЛП при протезировании биологическим протезом. Таким образом, после коррекции порока независимо от типа протеза МЦК по ПЖ и ЛЖ снижается и исчезает градиент между ними.
ОБСУЖДЕНИЕ
В результате проведенных исследований было установлено, что выраженность гипертрофии ТЗСЛЖ и ТМЖП у пациентов с АП зависит от возраста пациентов. Согласно уравнению регрессии, нормальные значения ТМЖП у пациентов с АП сохраняются в среднем до 30летнего возраста, а у пациентов старше 40 лет ТМЖП превышает 1,4 см. Следовательно, хирургическую коррекцию порока необходимо производить в более раннем возрасте, когда еще не возникла выраженная гипертрофия миокарда ЛЖ.
При изучении пациентов с ГЛЖ A.B. Nichols et а1. установили, что кровоток и ПО2 на единицу миокардиальной массы зависит от систолического напряжения стенки [18]. J. Barldi, J. Scomazzoni среди больных с ГЛЖ выделили 2 группы: 1) с миокардиальным кровотоком и потреблением О2миокардом, превышающим норму; 2) с избыточной гипертрофией, сопровождающейся сниженным кислородным напряжением и низким кровотоком на 100 г миокарда [12]. По результатам наших ранее опубликованных исследований МЦК отделов сердца у пациентов с АП, исходные показатели до операции также были распределены на две группы: 1) с исходным низким МЦК по ЛП, ЛЖ, Ао; 2) с исходным высоким МЦК по ЛП, ЛЖ, Ао, что очевидно обусловлено разной степенью гипертрофии. Измерение МЦК после коррекции порока свидетельствовало о нормализации МЦК по ЛЖ: при исходном низком уровне МЦК по ЛЖ он повышался, а при высоком - снижался, так как снижалось систолическое напряжение стенки ЛЖ [10].
Это отчасти объясняется тем, что у больных с АС выявляются зоны миокарда с нормальным, увеличенным либо сниженным кровотоком. При перегрузке давлением ГЛЖ, обусловленная увеличением диаметра кардиомиоцитов, приводит к повышению внутрикапил-лярной дистанции в миокарде [15, 16]. Плотность капилляров больше всего снижается в субэндокарде и среднем слое миокарда [14]. Однако близкий к норме миокардиальный кровоток в состоянии покоя не исключает возможности перфузионных нарушений в периоды кардиальной нагрузки. Исследуя резервный кровоток у больных с массой ЛЖ>200 г, авторы пришли к выводу о снижении коронарного вазодилятационного резерва [17]. Увеличение сосудистого сопротивления коронарного русла в гипертрофированном миокарде при перегрузке давлением может быть результатом: 1) неадекватного роста коронарной сосудистой сети во время гипертрофии и снижением капиллярного кровотока на единицу массы, 2) увеличением экстрасосудистых сил, затрудняющих кровоток по интрамуральным коронарным сосудам гипертрофированного ЛЖ, 3) комбинации того и другого [12].
Высокое систолическое давление, вызванное АП, приводит к гипертензионным изменениям внутри коронарной сети, ухудшению ва-зодилятаторной резервной возможности и развитию типичной стенокардии.
Как известно, развитие гипертрофии миокарда проходит 3 стадии:1) компенсаторная; 2) стабильная; 3) миокардиальное истощение с сердечной недостаточностью. Результаты наших исследований МЦК по ЛЖ и левым отделам сердца также свидетельствуют о разной степени развития гипертрофии у больных с АС и АН. В условиях гипертрофии у больных с ППС выявлена значительная коллатерализация коронарных сосудов. Так, индекс межкоронарных коллатеральных сосудов, по данным аутопсии, в норме составлял 4,7, а в гипертрофированных сердцах до 7,4 [13].
Однако наши данные показали, что перераспределение МЦК происходит очень быстро после коррекции порока, т. е. МЦК нормализуется. Сравнение АС и АН выявило существенные различия МЦК по ЛЖ. У больных с АН, по данным ЭхоКГ, увеличены размеры и объемы ЛЖ: КДР, КСР, КСО, КДО и преобладает эксцентрическая гипертрофия, а также снижено АДД. У больных с АС, напротив, все эхокардиографические показатели ниже и чаще выявляется концентрический тип гипертрофии ЛЖ. Кроме того, у больных с АС снижен МЦК по левым отделам сердца: ЛП и ЛЖ, а также по Ао.
После коррекции порока у пациентов с АН снижается МЦК на всех участках миокарда, включая ЛЖ, АДД достоверно повышается. У больных с АС МЦК снижается на ЛП, ПП, легочной артерии, Ао, но не меняется на ЛЖ, где имеет место выраженная КГЖ. Имеются литературные данные о том, что гипертрофия миокарда после коррекции АП исчезает только через 0,6-1,0 год [2]. Характерно, что МЦК по ПЖ не меняется после коррекции порока ни у больных с АС, ни у больных с АН.
Проведенный сравнительный анализ данных о МЦК отделов сердца после имплантации механических и биологических протезов показал отсутствие различий между ними. Полученные результаты еще раз подтвердили, что независимо от типа искусственного клапана сердца после коррекции АП функциональная нагрузка на ЛЖ уменьшается, в результате чего снижается МЦК по всем отделам сердца.
ВЫВОДЫ
-
1. По данным корреляционного анализа, ГЛЖ у пациентов с АП развивается в прямой зависимости от возраста пациентов и градиента давления между ЛЖ и Ао.
-
2. У пациентов с АП после хирургической коррекции порока наблюдалось достоверное снижение МЦК правых отделов сердца и тенденция к снижению МЦК левых отделов.
-
3. У пациентов с АС до операции повышенному (в 4 раза) по сравнению с АН градиенту ЛЖ/Ао соответствует достоверно более выраженная ГЛЖ и сниженный МЦК по ЛЖ и Ао.
-
4. После операции у пациентов как с АС, так и с АН выявляется снижение МЦК на всех уча
-
5. Гемодинамические изменения в системе микроциркуляции миокарда (снижение МЦК по ПЖ и по ЛЖ и выравнивание градиента между ними) после хирургической коррекции АП не зависят от типа имплантируемого клапана.
стках и выравнивание градиентов между аналогичными участками.
Список литературы Исследование микроциркуляции у больных с аортальным пороком до и после коррекции
- Баллюзек М.Ф., Шпилькина Н.А. // Регионарное кровообращение и микроциркуляция. 2003. Т. 2, № 10. С. 50-53.
- EDN: LACWLX
- Бокерия Л.А., Муратов Р.М., Беридзе И.З. и др. // Бюл. НЦССХ им. А.Н. Бакулева. 2005. Т. 6, № 5. С. 24.
- EDN: RWPEGF
- Добротин С.С., Земекова Е.Н., Гамзаев А.Б. и др. // Бюл. НЦССХ им. А.Н. Бакулева. 2003. Т. 4, № 11. С. 32.
- EDN: SNBNXV
- Караськов А.М., Железнев С.И., Назаров В.М. // Бюл. НЦССХ им. А.Н. Бакулева. 2005. Т. 6, № 5. С. 43.
- Кричевский Л.А., Хандюков С.Б., Козлов И.А. // Бюл. НЦССХ им. А.Н. Бакулева. 2001. Т. 2, № 6. С. 25.


