Исследование микросателлитных локусов генома сахарной свеклы (Betavulgaris L. ssp. vulgaris) для создания технологии генетического анализа линий и гибридов
Автор: Шалаева Т.В., Анискина Ю.В., Колобова О.С., Велишаева Н.С., Логвинов А.В., Мищенко В.Н., Шилов И.А.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Молекулярные маркеры
Статья в выпуске: 3 т.58, 2023 года.
Бесплатный доступ
При промышленном семеноводстве сахарной свеклы ( Beta vulgaris L . ssp. vulgaris ) необходимо строго следить за поддержанием качества и размножением линий - компонентов гибридов. Одним из инструментов сопровождения этого процесса может быть метод микросателлитного анализа. Имеется множество сообщений о микросателлитных локусах в геноме сахарной свеклы. Однако для их использования в селекционной практике нужна высокопроизводительная и удобная в применении технология анализа. Для создания такой технологии, позволяющей получать стабильные ДНК-профили, требуется более детальное изучение геномных микросателлитных профилей на большой выборке верифицированного селекционного материала сахарной свеклы. В представленном исследовании впервые проведен детальный анализ первичной структуры ряда микросателлитных локусов генома сахарной свеклы с целью определения природы полиморфизма этих участков генома и их пригодности для получения устойчивых ДНК-профилей. Совместно с селекционерами (ФГБНУ Первомайская селекционно-опытная станция сахарной свеклы, г. Гулькевичи, Краснодарский край) нами была отобрана коллекция из 146 образцов сахарной свеклы ( B. vulgaris ), включающая 28 МС-линий, 28 линий О-типа, 82 линии-опылителя, 6 гибридов отечественной селекции (Азимут, Корвет, Первомайский, Рубин, Фрегат, Успех), гибриды Добрава и Доротея. Этот растительный материал был проанализирован по 12 микросателлитным локусам - FDSB 502, FBSB 1001, FDSB 1033, Unigene 27833, Unigene 26753, Unigene 16898, Unigene 17623B, Unigene 15915, Unigene 17923, SB 04, SB 09, SB 15. Аллельные варианты каждого локуса были амплифицированы, клонированы в плазмидный вектор pAL2-T и секвенированы. Результаты секвенирования аллелельных вариантов микросателлитных локусов FDSB 1001, FDSB 1033, Unigene 16898, Unigene 17623B, Unigene 26753, Unigene 17923, Unigene 27833, SB 04 подтвердили, что полиморфизм длин этих локусов обусловлен исключительно числом тандемных повторов в амплифицируемом фрагменте ДНК. Локус Unigene 15915 был исключен из дальнейшей работы, поскольку в нуклеотидных последовательностях его аллельных вариантов, помимо микросателлитных повторов (CА)n, были выявлены дополнительные инсерции и делеции. Полиморфизм аллельных вариантов микросателлитных локусов SB 09, SB 15 и FDSB 502 обусловлен сложными (составными) повторами. При этом локусы SB 09 и SB 15 были выбраны для дальнейшей работы, поскольку обеспечивали получение стабильных ДНК-профилей. По аллельным вариантам локуса FDSB 502 был выявлен полиморфизм (TC)n(GAT)n(AAG)n, что в ряде случаев может осложнять получение достоверных результатов генотипирования. Поэтому для использования локуса FDSB 502 при создании технологии генетического анализа линий и гибридов сахарной свеклы мы предлагаем использовать разработанные нами праймеры, фланкирующие только его вариабельные микросателлитные повторы (GAT)n и (AAG)n. Полученные в представленном исследовании результаты предполагается в дальнейшем использовать для создания технологии генетического анализа линий и гибридов сахарной свеклы. Такая технология может стать надежным лабораторным инструментом для сопровождения селекционного процесса и промышленного семеноводства сахарной свеклы.
Beta vulgaris, сахарная свекла, генотипирование, микросателлитный анализ, днк-профиль
Короткий адрес: https://sciup.org/142238891
IDR: 142238891 | УДК: 635.112:631.522./524:577.2 | DOI: 10.15389/agrobiology.2023.3.483rus
Investigation of the sugar beet (Betavulgaris l. ssp. vulgaris) microsatellite loci structure to develop a technology for genetic analysis of sugar beet lines and hybrids
The quality control in the course of maintenance and reproduction of sugar beet ( Beta vulgaris L . ssp. vulgaris ) hybrid parent lines upon seed production is highly important. The method of microsatellite analysis seems to be very perspective tool to provide genotyping during breeding and seed production. Different research groups reported about microsatellite loci in the sugar beet genome. However, the implementation of this technique into the breeding process requires the development of robust and high-throughput technology of analysis. To develop a technology for obtaining stable DNA profiles, a more detailed study of the sugar beet genome microsatellite loci is required using a large set of verified breeding material. The sequencing a number of sugar beet genome regions containing microsatellite loci to clarify the nature of polymorphism as well as ability for providing the stable DNA profiles has been made in this study. Together with breeders (Pervomayskaya Selection and Experimental Station, Krasnodar Krai), a collection of 146 sugar beet plant samples was selected, including 28 male-sterile (MS) lines, 28 O-type lines, 82 pollinator lines, 6 hybrids of Russian selection (Azimut, Corvette, Pervomaisky, Rubin, Fregate, Uspekh) as well as Dobrava and Dorothea hybrids. Five plants of each sample were analyzed for 12 microsatellite loci, FDSB 502, FBSB 1001, FDSB 1033, Unigene 27833, Unigene 26753, Unigene 16898, Unigene 17623B, Unigene 15915, Unigene 17923, SB 04, SB 09, and SB 15. Allelic variants of each locus were amplified, cloned into the pAL2-T plasmid vector and sequenced. The results of sequencing the microsatellite loci FDSB 1001, FDSB 1033, Unigene 16898, Unigene 17623B, Unigene 26753, Unigene 17923, Unigene 27833, and SB 04 revealed that their length polymorphism is solely due to the different number of tandem repeats in the amplified DNA fragment. The locus Unigene 15915 was excluded from further work because of insertions and deletions in the flanking regions of microsatellite repeats (AC)n in its allelic variants. The polymorphism of allelic variants of the microsatellite loci SB 09, SB 15, and FDSB 502 is due to the complex (composite) repeats. Nevertheless, the SB 09 and SB 15 loci were approved for further study, since they produced stable DNA profiles. The allelic variants of the locus FDSB 502 contained the (TC)n(GAT)n(AAG)n sequence, which in some cases may complicate the analysis. To use this locus for the genetic analysis of sugar beet lines and hybrids, we propose the primers flanking only variable microsatellite repeatsб the (GAT)n and (AAG)n separately. The results we report here are prospective to develop a technology for the genetic analysis of sugar beet lines and hybrids as a reliable tool for both breeding and seed production.
Текст научной статьи Исследование микросателлитных локусов генома сахарной свеклы (Betavulgaris L. ssp. vulgaris) для создания технологии генетического анализа линий и гибридов
Сахарная свекла ( Beta vulgaris L . ssp. vulgaris ) — важная техническая культура, на долю которой приходится примерно 40 % мирового производства сахара. Также она используется в качестве высокоэнергетического питания для животных (свекловичная патока и свекловичный жом) и выращивается для производства биотоплива (1, 2).
В недалеком прошлом основными показателями результативности селекционного процесса были нецветушность и выход сахара с единицы количества сырья и площади посева. В настоящее время к числу важнейших хозяйственно ценных требований также относят повышение технологиче-
∗ Исследование выполнено в рамках государственного задания «Разработка технологий генотипирования сельскохозяйственных культур для ускорения и сопровождения селекционного процесса» (431-2022-0002).
ской пригодности сырья, получение семян с высокими посевными и физическими свойствами, толерантность к гербицидам, устойчивость к болезням, вредителям, факторам внешней среды, а главное — рентабельность семеноводства и возделывания коммерческих посевов (3-5).
В связи с этим современные гибриды сахарной свеклы создаются на основе раздельноплодных форм с цитоплазматической мужской стерильностью (ЦМС) и так называемых закрепителей признака ЦМС (линии О-типа) и являются многокомпонентными (6). Поэтому процесс промышленного семеноводства сахарной свеклы весьма сложен и требует соблюдения ряда условий. Прежде всего, необходимо строго следить за качественным поддержанием и размножением всех компонентов, к которым, как минимум, относятся компоненты материнской формы — МС-линия (линия с цитоплазматической мужской стерильностью) и линия-закрепитель О-типа, а также компонент отцовской формы — линия-опылитель.
Создание промышленного гибрида сахарной свеклы представляет собой многостадийный процесс, включающий скрещивания определенных родительских линий с получением простых промежуточных гибридов. Подбор каждого компонента гибрида в процессе селекционной работы осуществляется с учетом специфической комбинационной способности, значение которой определяют опытным путем (тест-скрещивания). Таким образом, для стабильного получения коммерческого гибрида необходимо контролировать все компоненты, использованные при получении финального гибрида, а также промежуточных гибридов.
Одним из инструментов лабораторного сопровождения селекции и семеноводства служит генетический анализ, с помощью которого можно оценивать качество селекционного материла на разных этапах создания гибрида сахарной свеклы. Такой анализ необходим для генетической идентификации линий — компонентов гибрида, а также для оценки их однородности.
Для анализа растительных геномов может быть применен ряд молекулярно-генетических методов — RFLP (restriction fragment length polymorphism) (7), AFLP (amplified fragment length polymorphism) (8), RAPD (random amplified polymorphic DNA) (9), SCAR (sequence characterized amplified region) (10), SNP (single nucleotide polymorphism) (11), DArT (diversity array technology) (12), SSR (simple sequence repeat) или микросателлитный анализ (13). Среди них для идентификации генотипов растений самыми часто используемыми являются методы SNP и SSR. Следует отметить, что метод исследования однонуклеотидных полиморфизмов (SNP) применялся для анализа генома как сахарной свеклы (14-16), так и целого ряда других культур — какао (17), огурца (18), цветной капусты (19), жимолости (20). Тем не менее использование этого метода анализа для надежной идентификации генотипов требует разработки и последующего учета большого числа маркеров (от сотен до нескольких тысяч), а также дорогостоящего оборудования для получения и обработки результатов.
Для перечисленных нами целей наиболее перспективным представляется анализ полиморфизма микросателлитных локусов в геноме сахарной свеклы, поскольку микросателлитные маркеры позволяют получать стабильно воспроизводимый ДНК-профиль (праймеры комплементарны консервативным участкам генома) и кодоминантны, что дает возможность использовать их для отслеживания наследования геномов родительских линий в промежуточных и финальных гибридах.
Несмотря на то, что опубликован целый ряд работ по применению метода микросателлитного анализа в селекционных программах по сахарной свекле как за рубежом (21-26), так и в России (27-29), на сегодняшний день отсутствует удобная технология его использования. Для создания такой технологии, позволяющей получать уникальные и стабильные ДНК-профили, требуется более подробное изучение геномных микросателлитных профилей на большой выборке верифицированного селекционного материала сахарной свеклы.
В представленном исследовании нами впервые проведен детальный анализ первичной структуры ряда микросателлитных локусов в геноме сахарной свеклы для определения природы полиморфизма этих участков и их пригодности для получения устойчивых ДНК-профилей.
Целью нашей работы было изучение структуры микросателлитных локусов генома сахарной свеклы для последующего использования в создании технологии генетического анализа линий и гибридов.
Методика . Исследование проводили на 146 образцах сахарной свеклы ( Beta vulgaris L . ), включающих 28 МС-линий, 28 линий О-типа, 82 линии-опылителя, 6 гибридов отечественной селекции (Азимут, Корвет, Первомайский, Рубин, Фрегат, Успех), гибриды Добрава и Доротея (предоставлены ФГБНУ Первомайская селекционно-опытная станция сахарной свеклы, г. Гулькевичи, Краснодарский край). Для получения достоверных результатов использовали растительный материал пяти разных растений каждого образца.
Геномную ДНК выделяли из зеленых листьев методом экстракции с использованием буфера CTAB с дополнительной очисткой хлороформом (30). ДНК в полученных препаратах выявляли методом электрофореза в 1 % агарозном геле с последующим окрашиванием бромистым этидием. Определяли качество и измеряли количество выделенной ДНК на планшетном спектрофотометре SPECTROstar Nano («BMG LABTECH GmbH», Германия).
Амплификацию целевых фрагментов ДНК проводили с локус-спе-цифичными праймерами FDSB 502 (21), FDSB 1001, FDSB 1033, 521.6 (24), SB 04, SB 09, SB 15 (25), Unigene 15915, Unigene 16898, Unigene 17623B, Unigene 17923, Unigene 26753, Unigene 27833 (23), меченными флуоресцентными красителями FAM, R6G, TAMRA и ROX. Полимеразную цепную реакцию (ПЦР) проводили в реакционной смеси объемом 25 мкл следующего состава: 67 мМ трис-HCl, pH 8,8; 16,6 мM (NH 4 ) 2 SO 4 («AppliChem», США); 2,5 мМ MgCl 2 («AppliChem», США); 5 ед/мкл Тaq-ДНК-полимеразы (ООО «ДНК-Технология», Россия), 25 мМ dNTP (ООО «Медиген», Россия), 10 пмоль каждого праймера (НПК «Синтол», Россия) и 2 мкл раствора ДНК. Амплификацию осуществляли в термоциклере CFX-96 («Bio-Rad», США) по программе: 95 ° С — 5 мин; 30 циклов: 94 ° С — 30 с, 53 ° С — 30 с, 72 ° С — 30 с; 72 ° С — 5 мин.
ПЦР-продукты детектировали методом высокоразрешающего капиллярного электрофореза в денатурирующих условиях на генетическом анализаторе ABI PRISM 3130XL («Applied Biosystems», США). Для анализа длины фрагментов 1 мкл ПЦР-продукта смешивали с 0,5 мкл маркера молекулярной массы GeneScan™ 600 LIZ («Applied Biosystems», США) и 8 мкл формамида Super DI («MCLab», CША) и проводили денатурацию фрагментов в течение 5 мин при 95 ° С. Размер ПЦР-фрагментов устанавливали с помощью программного обеспечения «ДНК Фрагментный анализ» (ИАП РАН, Россия).
Подготовка проб для секвенирования включала амплификацию каждого аллельного варианта с немечеными праймерами и последующую очистку полученного амплифицированного фрагмента ДНК с помощью набора Cleanup Mini (ЗАО «Евроген», Россия). Очищенные ПЦР-продукты лигировали в плазмидный вектор pAL2-T (ЗАО «Евроген», Россия), который вводили в клетки штамма Escherichia coli XL1-Blue методом электропорации. Клоны отбирали методом бело-голубой селекции с последующей проверкой на наличие вставки с помощью ПЦР. Плазмидную ДНК выделяли стандартным методом (31). Плазмидные вставки секвенировали методом Сэнгера с использованием стандартной пары праймеров: M13F — 5´-GTTGTAAAACGACGGCСAGTG-3´, M13R — 5´-AGCGGATAACAATT-TCACACAGGA-3´ (НПК «Синтол», Россия). Для достоверности результатов секвенирования по каждому аллельному варианту брали две пробы ДНК неродственных образцов и отбирали по два клона с чашки Петри.
Анализ нуклеотидных последовательностей выполняли с помощью программ Chromas 2.6.6 («Technelysium Pty, Ltd.», Австралия) и Clustal Omega (EMBL’s European Bioinformatics Institute — EMBL-EBI, Великобритания).
Конструирование новых праймеров для микросателлитного локуса FDSB502, фланкирующих только области тандемных повторов, проводили с помощью программного обеспечения Primer3Plus, EMBL , отсутствие вторичных структур в последовательности проверяли с помощью программного обеспечения Oligo Calc: Oligonucleotide Properties Calculator .
Результаты . Полиморфизм микросателлитных локусов в геноме сахарной свеклы изучали на растительном материале коллекции ФГБНУ Первомайская селекционно-опытная станция сахарной свеклы (Краснодарский край, г. Гулькевичи), используемом в селекционной работе в 2018-2022 годах.
Для надежного различения и идентификации растений определяющее значение имеет подбор наиболее информативных микросателлитных локусов. С этой целью на основании анализа данных литературы первоначально выбрали 40 микросателлитных локусов (27). Отбор проводили по следующим критериям: число аллелей в локусе не менее трех; расположение локусов на разных хромосомах, что должно обеспечивать независимое наследование ДНК-маркеров; размер фрагмента ДНК от 100 п.н. до 400 п.н. для надежного определения длин ПЦР-фрагментов.
Полиморфизм отобранных локусов был исследован экспериментально на выборке из 129 образцов сахарной свеклы. Мономорфные, трудно амплифицируемые или дающие неоднозначные и нестабильные результаты локусы были исключены из исследования. В результате осталось 13 микросателлитных локусов — 521.6, FDSB 502, FBSB 1001, FDSB 1033, Unigene 27833, Unigene 26753, Unigene 16898, Unigene 17623B, Unigene 15915, Unigene 17923, SB 04, SB 09, SB 15, которые характеризовались высоким полиморфизмом (число выявляемых аллелей на каждый локус от 3 до 11). С их использованием были получены уникальные ДНК-профили для каждого образца сахарной свеклы (27).
Исследование более обширной выборки из 146 образцов сахарной свеклы подтвердило пригодность указанных локусов для генетического анализа. Исключением оказался локус 521.6 (24), при амплификации которого в ряде случаев, помимо целевого продукта, получали дополнительные неспецифические фрагменты ДНК (рис. 1). Поэтому в дальнейшем локус 521.6 не использовали.
296 299

Рис. 1. Электрофореграмма ПЦР-продуктов микросателлитного локуса 521.6, меченного флуоресцентным красителем TAMRA, у линии сахарной свеклы Оп 66279 7/10 из рабочей коллекции ФГБНУ Первомайская селекционно-опытная станция сахарной свеклы (г. Гулькевичи, Краснодарский край, 2018-2022 годы). При амплификации помимо целевого ПЦР-продукта размера 284 п.н. получены дополнительные неспецифические фрагменты ДНК (272 п.н., 296 п.н., 299 п.н., 347 п.н.).
В результате генетического анализа 146 линий сахарной свеклы отобрали 35 линий с высокой степенью однородности. Однородные линии сахарной свеклы (все растения имели идентичный ДНК-профиль по микро-сателлитным локусам) в дальнейшем были вовлечены в селекционный процесс в качестве компонентов для создания новых гибридов. Линии с неполной однородностью (менее 80 %) подвергались дальнейшему самоопылению с последующим ежегодным контролем однородности с помощью мик-росателлитного анализа.
Все выявленные нами аллельные варианты исследуемых микроса-теллитных локусов приведены в таблице 1.
1. Полиморфизм микросателлитных локусов сахарной свеклы ( Beta vulgaris L . ssp. vulgaris ), выявленный при анализе выборки из 146 образцов рабочей коллекции ФГБНУ Первомайская селекционно-опытная станция сахарной свеклы (г. Гулькевичи, Краснодарский край, 2018-2022 годы)
|
Локус |
Выявленные аллели, п.н. |
Источник литературы |
|
FDSB 502 |
265, 271, 273, 276, 279, 283, 286, 293, 314 |
(21) |
|
FDSB 1001 |
315, 323, 325, 333, 347, 351 |
(24) |
|
FDSB 1033 |
167,177, 193, 195, 197, 199, 221, 229 |
(24) |
|
SB 04 |
180, 186, 189, 192, 195, 198, 201 |
(25) |
|
SB 09 |
130, 133, 136 |
(25) |
|
SB 15 |
146, 150, 154, 160, 166, 170, 174 |
(25) |
|
Unigene 15915 |
299, 305, 314, 321, 339, 342, 345, 349, 383 |
(23) |
|
Unigene 16898 |
276, 279, 285, 291 |
(23) |
|
Unigene 17623B |
147, 153, 156, 159, 162, 165, 168, 171, 174, 177, 180 |
(23) |
|
Unigene 17923 |
193, 195, 197, 199, 201, 203, 205, 209, 215, 219, 225 |
(23) |
|
Unigene 26753 |
282, 285, 288, 291, 294, 297, 303 |
(23) |
|
Unigene 27833 |
190, 199, 205, 208, 211, 214, 217 |
(23) |
Примечание. Размер ПЦР-продуктов определен методом высокоразрешающего капиллярного электрофореза в денатурирующих условиях на генетическом анализаторе ABI PRISM 3130XL («Applied Biosystems», США). В качестве размерного стандарта использовали маркер молекулярной массы GeneScan™ 600 LIZ («Applied Biosystems», США).
Для получения достоверных результатов генетического анализа необходимо, чтобы полиморфизм длин микросателлитных локусов был обусловлен только наличием микросателлитных повторов, и вне области повторов в амплифицируемом фрагменте отсутствовали дополнительные ин-серции или делеции. Поэтому на следующем этапе работы было проведено изучение первичной структуры использующихся в анализе 12 микросател-литных локусов.
Аллельные варианты каждого из этих 12 локусов были индивидуально амплифицированы и клонированы в плазмидный вектор pAL2-T (ЗАО «Евроген», Россия). Полученные трансформанты E. coli, несущие вставки целевых фрагментов ДНК в векторе (рис. 2, колонии белого цвета), отобрали, и их плазмидную ДНК секвенировали, в результате чего были определены нуклеотидные последовательности каждого аллельного варианта соответствующего локуса.
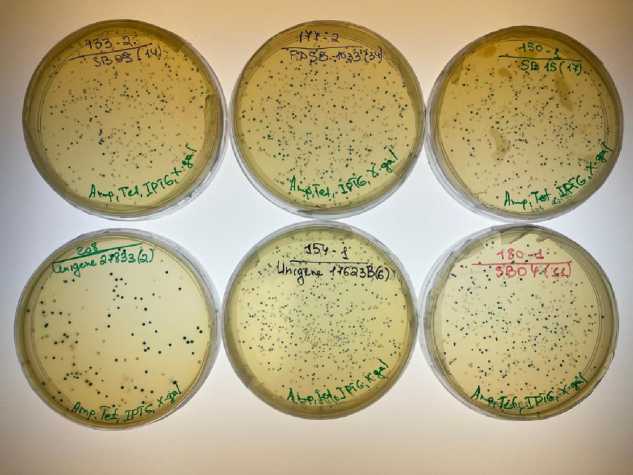
Рис. 2. Чашки Петри с трансформантами Escherichia coli XL1-Blue, несущими плазмидный вектор pAL2-T со вставками целевых фрагментов микросателлитных локусов SB 09, FDSB 1033, SB 15, Unigene 27833, Unigene 17623B и SB 04 (клоны белого цвета) . Фрагменты ДНК микросател-литных локусов получены при анализе рабочей коллекции сахарной свеклы ( Beta vulgaris L . ssp. vulgaris ) ФГБНУ Первомайская селекционно-опытная станция сахарной свеклы (г. Гульке-вичи, Краснодарский край, 2018-2022 годы).
Результаты анализа нуклеотидных последовательностей всех исследуемых в нашей работе микросателлитных локусов схематично представлены на рисунке 3.
FDSB 502
FDSB 1001
FDSB 103.3
SB 04
SB 09
SB 15
Unigene 15915
Unigene 16898
Unigene 17623B
Unigene 17923
Unigene 26753
Unigene 27833
|
GCAAAAACCCAAAACCCTTT |
| (TC)n(GAT)n(AAG)n |
TTTCTCTCTCCTCCTCTTCCTC |
|
|
ATCTTATGCTGCCATGACCA |
(AG)n |
ACTTCAACCACTATCACAAAGTGAG |
|
|
TTCAAATCGCCATCTCCCAG |
|_________
|
GCTGAGATGATCTTTGTTAGGCC |
|
|
ACCGATCACCAATTCACCAT |
GTTTTGTTTTGGGCOAAATG |
||
|
tgcataaaacOcccaacaat |
| (CAA)n(CATln |
AGGGCAACTTTGTTTTGTGG |
|
|
CACCCAGCCTATCTCTCGAC |
(CT)n(GAC>n |
GTGGTGGGCAGTTTTAGGAA |
|
|
TTAGGTCTCTACAACTGATCCC |
(CA>n |
| Имсвуцкя/делецкя | |
TAGGGTCATAGGCAGTAAGATT |
|
AGAACTTAGATTGTOACCTOCT |
(CAA)n |
GATGGGAAGAGAGAGATTAGTG |
|
|
ATTAGACCTCAATCTTCCAGC |
| (CAA)n |
AATAATGGCAATCTACCAGC |
|
|
AACCTTACTCCCTCTGATTTCT |
(CTT)n |
GGAGATACAACTTACAAGAGCC |
|
|
GAGAAACAAATTCACCCATC |
(CAA)n |
GTAGTGGAAGTAAAAGCACCA |
|
|
GAGTCATCAACACCAAAСТАСА |
(ATA)n |
ATTAGCCAAGAAAATCACCC |
Рис. 3. Структура микросателлитных локусов генома образцов сахарной свеклы ( Beta vulgaris L . ssp. vulgaris ) из рабочей коллекции ФГБНУ Первомайская селекционно-опытная станция сахарной свеклы (г. Гулькевичи, Краснодарский край, 2018-2022 годы) . Последовательности, отмеченные светло-зеленым и темно-зеленым цветами, — области праймеров, желтым цветом — область тандемных повторов, розовым — инсерции/делеции.
На рисунке 4 в качестве примера анализа типичного микросателлит-ного локуса, полиморфизм длин амплифицированных фрагментов которого обусловлен только разным числом повторов (в указанном случае САА), приведено выравнивание нуклеотидных последовательностей наиболее часто встречающихся аллелей микросателлитного локуса Unigene 26753.
Unigene 26753_28B-1 Unigene 26753_288-2 Unigene 26753 294-3 Unigene 26753_294-4 Unigene 26753_303~5
Unigene 26753_303-6
Unigene 26753_288~1 Unigene 26753 288-2 Unigene 26753_294-3 Unigene 26753_294-4 Unigene 26753_303-5
Unigene 26753 303-6
Unigene 26753_28B-1 Unigene 26753_288-2 Unigene 26753 294-3 Unigene 26753_294-4 Unigene 26753_303~5
Unigene 26753_303-6
Unigene 26753_288-l Unigene 26753_288~2 Unigene 26753 294-3 Unigene 26753_294-4 Unigene 26753_303-5 Unigene 26753_303-6
Unigene 26753_288-l
Unigene 26753_28B-2
Unigene 26753_294-3
Unigene 26753 294-4
Unigene 26753_303-5
Unigene 26753_303~6
Unigene 26753 288-1
Unigene 26753_28B-2 Unigene 26753_294~3 Unigene 26753 294-4 Unigene 26753_303-5 Unigene 26753_303-6
GAGAAACAAATT CACCCATCAAC АТС T ТСAACAACAACAACAACAACAAC GACAACAACC GAGAAACAAATT CACCCATCAACATCT TCAACAACAACAACAACAACAACAACAACAACC GAGAAACAAATT CACCCATCAACATCT TCAACAACAACAAC CACAACAACAACAACAACA GAGAAACAAATT CACCCATCAACATCT TCAACAACAACAAC CACAACAACAACAACAACA GAGAAACAAATT CACCCATCAACATCT TCAACAACAACAACAACAACAACAAC CACAACG GAGAAACAAATT САСССАТСААС АТС T TC AAC AAC AAC AACAACAACGACAACCACAACA
ACAACAA---------------AGGAGCAAGTTCTTACCAATGCTATGCTCCTCATCAAG
ACAACAA---------------AGGAGCAAGTTCTTACCAATGCTATGCTCCTCATCAAG
ACAACAACAACAA---------AAGAGCAAGTCCTTACCAAAGCTATGCTCCTCATCAMC
AC AAC AAC AACAA---------AAGAGCAAGTTCTTACCAATGCTATGCTCCTCATCAAC
ACAACAACAACAACAACAACAAAAGAGCAAGTT CTTACCAAT GCTATGCTCCTCATCAAC ACAACAACAACAACAACAACAAAAGAGCAAGT T CTT ACCAAT GCTATGCTCCTCATCAAC
CAAAGAAGTGACCAAGCTTTCGCTTTCGCATCGGCGTAGCTCCTCCGCCTGCTCCACCAC CAAAGAAGTGATCAAGCTTTCGCTTTCGCATCGGCGTAGCTCCTCCGCCTGCTCCACCAC CAAGGAAGTGATCAAGCTTTCGCTTTCGCATCAGCGTAGCTCCTCCACATGTTCCACCAC CAAAGAAGTGATCAAGCTTTCGCTTTCGCATCGGCGTAGCTCCTCCACATGTTCCACCAC CAAAGAAGTGATCAAGCTTTCGCTTTCGCATCGGCGTAGCTCCTCCACCTGTTCCACCAC CAAAGAAGTGATCAAGCTTTCGCTTTCGCATCGGCGTAGCTCCTCCACCTGTTCCACCAG
CTCCTCCACCGTCTCCGAGGACCCTTTATCACCAAAAGTTGGGTGTATGGGCCAAGTTAA CTCCTCCACCGTCTCCGAGGACCCTTTATCACCAAAAGTTGGGTGTATGGGCCAAGTTAA CTCCTCCACCGTCTCCGAGGACCCTTTATCACCAAAAGTTGGGTGTATGGGCCAAGTTAA CTCCTCCACCGTCTCCGAGGACCCTTTATCACCAAAAGTTGCGTGTATGGGCCAAGTTAA CTCCTCCACCGTCTCCGAGGACCCTTTACCACCAAAAGTTGGGTGTATGGGCCAAGTTAA CTCCTCCACCGTCCCCGAGGACCCTTTATCACCAAAAGTTGGGTGTATGGGCCAAGTTAA
GAGAAACAACAAAGTTGTTGGTTTTCCAAGTAAGAGTTTTGTTGGTGСTTTTACTTСCAC GAGAAACAACAAAGTTGTTGGTTTTCCAAGTAAGAGTTTTGTTGGTGCTTTTACTTCCAC GAGAAACAACAAAGTTGTTGGTTTTCCCAGTAAGAGTTTCGTTGGTGCTTTTACTTCCAC GAGAAACAACAAAGTTGTTGGTTTTCCAAGTAAGAGTTTTGTTGGTGCTTTTACTTCCAC GAGAAACAACAAAGTTGTTGGTTTTCCAAGTAAGAGTTITG T TGGTGCTTTTACTTCCAC gagaaacaacaaagttgatggttttccaagtaagagttttgtHstgctt t tacttccac

Рис. 4. Сравнение нуклеотидных последовательностей аллельных вариантов микросателлитного локуса Unigene 26753, выявленных в геноме образцов сахарной свеклы ( Beta vulgaris L . ssp. vulgaris ) из рабочей коллекции ФГБНУ Первомайская селекционно-опытная станция сахарной свеклы (г. Гулькевичи, Краснодарский край, 2018-2022 годы) . Светло-зеленым и темно-зеленым цветами выделены области праймеров, желтым цветом — область тандемных повторов. Образец 1 (аллель 288 п.н.) — линия От 7994, образец 2 (аллель 288 п.н.) — линия Оп 19962, образец 3 (аллель 294 п.н.) — линия От 12122, образец 4 (аллель 294 п.н.) — линия МС 11348, образец 5 (аллель 303 п.н.) — линия Оп 10632, образец 6 (аллель 303 п.н.) — линия Оп СП-1П2.
Результаты секвенирования аллелельных вариантов микросателлит-ных локусов FDSB 1001, FDSB 1033, Unigene 16898, Unigene 17623B, Unigene 17923, Unigene 27833, SB 04 также подтвердили, что полиморфизм локусов обусловлен исключительно числом микросателлитных повторов в ам-плифицируемом фрагменте ДНК.
Анализ нуклеотидных последовательностей аллельных вариантов микросателлитного локуса Unigene 15915 показал, что полиморфизм длин амплифицированных фрагментов обусловлен не только разным числом тандемных повторов (CА) n , но и дополнительными инсерциями и делециями в участках ДНК, фланкирующих области повторов (см. рис. 3). Это осложняет интерпретацию результатов микросателлитного анализа, в результате указанный локус Unigene 15915 был исключен из дальнейшей работы.
Результаты секвенирования аллельных вариантов микросателлитных локусов SB 09, SB 15 и FDSB 502 показали, что эти локусы содержат сложные (составные) повторы (см. рис. 3). Тем не менее при амплификации микросателлитных локусов SB 09 и SB 15 были получены стабильные и воспроизводимые ДНК-профили, поэтому два указанных локуса использовали в дальнейшей работе.
Полиморфизм локуса FDSB 502 обусловлен количественными изме- нениями сложного (составного) тандемного повтора (TC)n(GAT)n(AAG)n (см. рис. 3). Следует отметить, что анализ полиморфизма локуса, амплифициро-ванный фрагмент ДНК которого содержит три типа тандемных повторов, может быть в ряде случаев осложнен. Нами ранее показано, что для получения стабильных ДНК-профилей целесообразно одновременно амплифи-цировать не более двух полиморфных участков в одном локусе (32-34).
Для применения в технологии генетического анализа линий и гибридов сахарной свеклы этот локус можно использовать, амплифицируя каждую область тандемных повторов раздельно. В этом случае вероятность получения надежно интерпретируемого ДНК-профиля гораздо выше. С этой целью мы подобрали праймеры, фланкирующие разные группы тандемных повторов в локусе FDSB 502.
Изучение полиморфизма, обусловленного разным числом тандемных повторов каждого вида, на выборке из 146 образцов сахарной свеклы показало, что участок ДНК, содержащий микросателлитный повтор (TC) n , консервативен (число повторов TC во всех образцах одинаково и равно 10), в то время как области микросателлитных повторов (GAT) n и (AAG) n вариабельны. Поэтому для создания технологии генетического анализа линий и гибридов сахарной свеклы представляется перспективным использование только тех праймеров, которые фланкируют микросателлитные повторы (GAT) n и (AAG) n в локусе FDSB 502 (табл. 2).
2. Новые праймеры для амплификации вариабельных участков локуса FDSB 502 в геноме сахарной свеклы ( Beta vulgaris L . ssp. vulgaris )
|
Локус 1 |
Микросателлитный повтор |
^ Пара праймеров |
|
FDSB 502-2 |
(GAT) n |
502-2F: 5´-ACAATGGCGAATCGCTTTTGGGG-3´ 502-2R: 5´-CGTACTCATCTTCATCGTCTTCTTC-3´ |
|
FDSB 502-3 |
(AAG) n |
502-3F: 5´-GAAGAAGACGATGAAGATGAGTACG-3´ 502-3R: 5´-GAATCAACCTTGCCGACATATCC-3´ |
Таким образом, для генотипирования линий и гибридов сахарной свеклы представляются перспективными 12 микросателлитных локусов (табл. 3), которые обеспечивают получение стабильных и однозначно интерпретируемых ДНК-профилей.
3. Микросателлитные локусы, перспективные для создания технологии генотипирования линий и гибридов сахарной свеклы ( Beta vulgaris L . ssp. vulgaris )
|
Локус |
Микросателлитные повторы |
Выявляемые аллели |
|
|
диапазон длин, п.н. |
число |
||
|
Unigene 16898 |
(CAA) n |
276-291 |
4 |
|
Unigene 17623B |
(CAA) n |
147-179 |
11 |
|
Unigene 17923 |
(CTT) n |
193-225 |
11 |
|
Unigene 26753 |
(CAA) n |
282-303 |
7 |
|
Unigene 27833 |
(АТА) n |
190-217 |
7 |
|
FDSB 1033 |
(AG) n |
165-229 |
8 |
|
FDSB 1001 |
(AG) n |
315-351 |
6 |
|
SB 04 |
(ААС) n |
180-201 |
7 |
|
SB 09 |
(CAA) n (CAT) n |
130-136 |
3 |
|
SB 15 |
(CТ) n (GAC) n |
146-174 |
7 |
|
FDSB 502-2 |
(GAT) n |
112-154 |
5 |
|
FDSB 502-3 |
(AAG) n |
223-241 |
4 |
Пр и м еч ани е. Получение стабильных и однозначно интерпретируемых ДНК-профилей при использовании в настоящем исследовании микросателлитных локусов показано на 146 фенотипически охарактеризованных образцах из рабочей коллекции ФГБНУ Первомайская селекционно-опытная станция сахарной свеклы (г. Гулькевичи, Краснодарский край, 2018-2022 годы).
Итак, 146 образцов из рабочей коллекции ФГБНУ Первомайская селекционно-опытная станция сахарной свеклы, включая 28 МС-линий, 28 линий О-типа, 82 линии-опылителя, 6 гибридов отечественной селекции (Азимут, Корвет, Первомайский, Рубин, Фрегат, Успех), гибриды Добрава и Доротея, были проанализированы по 12 микросателлитным локусам — FDSB 502-2, FDSB 502-3, FBSB 1001, FDSB 1033, Unigene 27833, Unigene 26753, Unigene 16898, Unigene 17623B, Unigene 17923, SB 04, SB 09 и SB 15.
При этом наблюдаемый полиморфизм длин аллелей микросателлитных локусов составил для FDSB 502 — 265-314 п.н., FDSB 1001 — 315-351 п.н., FDSB 1033 — 167-229 п.н., SB 04 — 180-201 п.н., SB 09 — 130-136 п.н., SB 15 — 146174 п.н., Unigene 15915 — 299-383 п.н., Unigene 16898 — 276-291 п.н., Unigene 17623B — 147-180 п.н., Unigene 17923 — 193-225 п.н., Unigene
26753 — 282-303 п.н., Unigene 27833 — 190-217 п.н Результаты секвенирования аллелельных вариантов микросателлитных локусов FDSB 1001, FDSB 1033, Unigene 16898, Unigene 17623B, Unigene 26753, Unigene 17923, Unigene 27833, SB 04 подтвердили, что их полиморфизм обусловлен числом тандемных повторов в амплифицируемом фрагменте ДНК. В нуклеотидных последовательностях аллельных вариантов локуса Unigene 15915, помимо мик-росателлитных повторов (СА) n , имеются инсерции и делеции, поэтому мы не рекомендуем использовать этот локус при генотипировании. Полиморфизм локусов SB 09, SB 15 и FDSB 502 обусловлен сложными (составными) повторами. Тем не менее локусы SB 09 и SB 15 обеспечивают получение стабильных ДНК-профилей. В локусе FDSB 502 выявлен полиморфизм (TC) n (GAT) n (AAG) n , что может искажать результаты генотипирования. Для использования этого локуса в технологии генетического анализа линий и гибридов сахарной свеклы мы предлагаем праймеры, фланкирующие только вариабельные микросателлитные повторы (GAT) n и (AAG) n . Полученные в представленном исследовании результаты предполагается в дальнейшем использовать для создания технологии генетического анализа линий и гибридов сахарной свеклы. Такая технология может стать надежным лабораторным инструментом для сопровождения селекционного процесса и промышленного семеноводства этой культуры.
Список литературы Исследование микросателлитных локусов генома сахарной свеклы (Betavulgaris L. ssp. vulgaris) для создания технологии генетического анализа линий и гибридов
- Panella L. Sugar beet as an energy crop. Sugar Techno, 2010, 12: 288-293 (doi: 10.1007/s12355-010-0041-5).
- Tayyab M., Wakeel A., Mubarak M.U., Artyszak A., Ali S., Hakki E.E., Mahmood K., Song B., Ishfaq M. Sugar Beet Cultivation in the Tropics and Subtropics: Challenges and Opportunities. Agronomy, 2023, 13(5): 1213 (doi: 10.3390/agronomy13051213).
- Балков И.Я. Селекция сахарной свеклы на гетерозис. М.,1978.
- Логвинов В.А. Изучение реакции сортов сахарной свёклы на воздействие концентрированных растворов минеральных веществ. В сб.: Селекция и агротехника сахарной свёклы на Северном Кавказе. Киев, 1982: 41-46.
- Суслов В.И., Логвинов В.А., Мищенко В.Н., Суслов А.В., Логвинов А.В. Теоретические и практические аспекты свекловодства в Краснодарском крае. Труды Кубанского государственного университета, 2010, 5: 62-67.
- Балков И.Я., Каракотов С.Д., Логвинов А.В., Логвинов В.А, Мищенко В.Н. Эволюция сахарной свёклы: от огородных форм – до современных рентабельных гибридов. М., 2017.
- Lukow T., Dunfield P.F., Liesack W. Use of the T-RFLP technique to assess spatial and temporal changes in the bacterial community structure within an agricultural soil planted with transgenic and non-transgenic potato plants. FEMS Microbiology Ecology, 2000, 32(3): 241-247 (doi: 10.1111/j.1574-6941.2000.tb00717.x).
- Снигирь Е.А., Пышная О.Н., Кочиева Е.З., Рыжова Н.Н. AFLP-анализ сортового полиморфизма Capsicum annuum L. Сельскохозяйственная биология, 2013, 1: 53-60 (doi: 10.15389/agrobiology.2013.1.53rus).
- Федулова Т.П., Федорин Д.Н., Налбандян А.А., Богомолов М.А. Использование ДНК-маркеров в современных программах селекции сахарной свёклы. Сахар, 2019, 5: 50-53 (doi: 10.24411/2413-5518-2019-00037).
- Feng S., Zhu Y., Yu C., Jiao K., Jiang M., Lu J., Shen C., Ying Q., Wang H. Development of species-specific SCAR Markers Based on a SCoT analysis to authenticate Physalis (Solanaceae) species. Frontiers in Genetics, 2018, 9: 192 (doi: 10.3389/fgene.2018.0019).
- Kishor D. S., Alavilli H., Lee S.-C., Kim J.-G., Song K. Development of SNP markers for white immature fruit skin color in cucumber (Cucumis sativus L.) using QTL-seq and marker analyses. Plants, 2021, 10(11), 2341 (doi: 10.3390/plants10112341).
- Gawroński P., Pawełkowicz M., Tofil K., Uszyński G., Sharifova S., Ahluwalia S., Tyrka M., Wędzony M., Kilian A., Bolibok-Brągoszewska H. DArT markers effectively target gene space in the rye genome. Frontiers in Plant Science, 2016, 7: 1600 (doi: 10.3389/fpls.2016.01600).
- Колобова О.С., Малюченко О.П., Шалаева Т.В., Шанина Е.П., Шилов И.А., Алексеев Я.И., Велишаева Н.С. Генетическая паспортизация картофеля на основе мультиплексного анализа 10 микросателлитных маркеров. Вавиловский журнал генетики и селекции, 2017, 21(1): 124-127 (doi: 10.18699/VJ17.230).
- Möhring S., Salamini F., Schneider K. Multiplexed, linkage group-specific SNP marker sets for rapid genetic mapping and fingerprinting of sugar beet (Beta vulgaris L.). Molecular Breeding, 2004, 14: 475–488 (doi: 10.1007/s11032-004-0900-4).
- Stevanato P., Broccanello C., Biscarini F., Del Corvo M., Sablok G., Panella L., Concheri, G. High-throughput RAD-SNP genotyping for characterization of sugar beet genotypes. Plant Molecular Biology Reporter, 2013 (doi: 10.1007/s11105-013-0685-x).
- Tehseen M.M., Zheng Y., Wyatt N.A., Bolton M.D., Yang S., Xu S.S., Li X., Chu C. Development of STARP marker platform for flexible SNP genotyping in sugar beet. Agronomy, 2023, 13: 1359 (doi: 10.3390/agronomy13051359).
- Padi F.K., Ofori A., Takrama J., Djan E., Opoku S.Y., Dadzie A.M., Zhang D. The impact of SNP fingerprinting and parentage analysis on the effectiveness of variety recommendations in cacao. Tree Genetics & Genomes, 2015, 11(3) (doi:10.1007/s11295-015-0875-9).
- Zhang J., Yang J., Fu S., Ren J., Zhang X., Xia C., Zhao H., Yang K., Wen C. Comparison of DUS testing and SNP fingerprinting for variety identification in cucumber Horticultural Plant Journal, 2022, 8(5): 575-582 (doi: 10.1016/j.hpj.2022.07.002).
- Yang Y., Lyu M., Liu J. et al. Construction of an SNP fingerprinting database and population genetic analysis of 329 cauliflower cultivars. BMC Plant Biol, 2022, 22: 522 (doi: 10.1186/s12870-022-03920-2).
- Li J., Chang X., Huang Q., Liu P., Zhao X., Li F., Wang Y., Chang C. Construction of SNP fingerprint and population genetic analysis of honeysuckle germplasm resources in China. Frontiers in Plant Science, 2023, 14:1080691 (doi: 10.3389/fpls.2023.1080691).
- Laurent V., Devaux P., Thiel T., Viard F., Mielordt S., Touzet P., Quillet M.C. Comparative effectiveness of sugar beet microsatellite markers isolated from genomic libraries and GenBank ESTs to map the sugar beet genome. Theoretical and Applied Genetics, 2007, 115(6): 793-805 (doi: 10.1007/s00122-007-0609-y).
- Smulders M., Esselink D., Everaert I., De Riek J., Vosman B. Characterisation of sugar beet (Beta vulgaris L. ssp. vulgaris) varieties using microsatellite markers. BMC Genetics, 2010, 11: 41 (doi: 10.1186/1471-2156-11-41).
- Fugate K.K., Fajardo D., Schlautman B., Ferrareze J.P., Bolton M.D., Campbell L.G., Wiesman E., Zalapa J. Generation and characterization of a sugarbeet transcriptome and transcriptbased SSR markers. The Plant Genome, 2014, 7(2) (doi: 10.3835/plantgenome2013.11.0038).
- McGrath J.M., Trebbi D., Fenwick A., Panella L., Schulz B., Laurent V., Barnes S., Murray S.C. An open-source first-generation molecular genetic map from a sugar beet ½ table beet cross and its extension to physical mapping. The Plant Genome, 2007, 1: 27-44 (doi: 10.2135/cropsci2006-05-0339tpg).
- Richards C.M., Brownson M., Mitchell S.E., Kresovich S., Panella L. Polymorphic microsatellite markers for inferring diversity in wild and domesticated sugar beet (Beta vulgaris). Molecular Ecology Notes, 2004, 4(5): 243-245 (doi: 10.1111/j.1471-8286.2004.00630.x).
- Srivastava S., Pathak A. D., Kumar R., Joshi B.B. Genetic diversity of sugar beet genotypes evaluated by microsatellite DNA markers. Journal of Environmental Biology, 2017, 38: 777-783 (doi: 10.22438/jeb/38/5/MS-141).
- Шилов И.А., Анискина Ю.В., Шалаева Т.В., Колобова О.С., Велишаева Н.С., Мищенко В.Н., Логвинов А.В. Создание современных гибридов сахарной свёклы с применением микросателлитного анализа. Сахар, 2020, 8: 27-31 (doi: 10.24411/2413-5518-2020-10804).
- Налбандян А.А., Хуссейн А.С. Создание ДНК-профилей растений на основе аллельного разнообразия SSR-маркеров. В сб.: Закономерности и тенденции развития науки в современном обществе. Уфа, 2016: 30-32.
- Налбандян А.А., Хуссейн А.С., Федулова Т.П., Черепухина И.В., Крюкова Т.И., Рденко Т.С. Перспективы использования SSR-маркеров для генотипирования сахарной свеклы. Сахар, 2019, 11: 36-39.
- Doyle J.J., Doyle J.L. A rapid DNA isolation procedure for small quantities of fresh leaf tissue. Phytochemical Bulletin, 1987, 19: 11-15.
- Маниатис Т., Фрич Э., Сэмбрук Дж. Методы генетической инженерии. Молекулярное клонирование. М., 1984.
- Анискина Ю.В., Малиновская Е.В., Шалаева Т.В., Мицурова В.С., Родионова Д.А., Харченко П.Н., Шилов И.А. Технология генетической идентификации сортов и гибридов сорго на основе мультилокусного микросателлитного анализа. Биотехнология, 2018, 34(2): 54-69 (doi: 10.21519/0234-2758-2018-34-2-54-69).
- Секридова А.В., Шилов И.А., Кислин Е.Н., Малюченко О.П., Харченко П.Н. Технология генетической идентификации сортов и диких форм винограда на основе мультилокусного микросателлитного анализа. Биотехнология, 2021, 37(3): 85-95 (doi: 10.21519/0234-2758-2021-37-3-85-95).
- Шилов И.А., Велишаева Н.С., Анискина Ю.В., Колобова О.С., Шалаева Т.В., Борисенко О.М., Демурин Я.Н., Фролов С.С. Генетическая идентификация линий и гибридов подсолнечника Helianthus annuus L. на основе мультиплексного микросателлитного анализа. Достижения науки и техники АПК, 2023, 37(1): 10-15 (doi: 10.53859/02352451_2023_37_1_10).


