Исследование сесквитерпеновых лактонов Artemisia kobstanica
Автор: Алескерова Аделя Новруз, Джахангирова Илхама Рафик, Керимли Эльвин Гаджи, Серкеров Сираджеддин Вели
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Биологические науки
Статья в выпуске: 10 т.8, 2022 года.
Бесплатный доступ
Впервые исследованы сесквитерпеновые лактоны полыни Artemisia kobstanica Rzazade из флоры Азербайджана. Путем колоночной хроматографии из надземной части выделены 3 сесквитерпеновых лактона C15H18O3, т. пл. 171-172 °C (1), C15H20O4, т. пл. 124-126 °C (2), C15H18O4, т. пл. 202-203 °C (3). Лактоны 1 и 3 на основании физико-химических и спектральных (ИК-, и 1H ЯМР-спектры) данных идентифицированы с α-сантонином и артемизином, соответственно. Вещество 2 оказалось новым, впервые выделенным из исследуемого вида полыни мерезолидом. На основании данных, полученных при интерпретации ИК- и 1H ЯМР-спектров ему предложено строение 3-кето-4,5-эпокси-8β, 7α, 11βН-гермакр-10,15-ен-8,12-олида.
Полынь, лактоны, артемизин
Короткий адрес: https://sciup.org/14126119
IDR: 14126119 | УДК: 582.998.1:547.913.2 | DOI: 10.33619/2414-2948/83/05
Study of Artemisia kobstanica sesquiterpene lactones
Sesquiterpene lactones of wormwood Artemisia kobstanica Rzazade from the flora of Azerbaijan were studied for the first time. Three sesquiterpene lactones, C15H18O3, m. p. 171-172 °C (1), C15H20O4, m. p. 124-126 °C (2), C15H18O4, m. p. 202-203 °C (3). Based on physicochemical and spectral (IR and 1H NMR spectra) data, lactones 1 and 3 were identified with α-santonin and artemisinin, respectively. Substance 2 turned out to be new, for the first time isolated from the studied species of wormwood by merezolid. Based on the data obtained from the interpretation of IR and 1H NMR spectra, the structure of 3-keto-4,5-epoxy-8β, 7α, 11βH-germacr-10,15-ene-8,12-olide was proposed to it.
Текст научной статьи Исследование сесквитерпеновых лактонов Artemisia kobstanica
Бюллетень науки и практики / Bulletin of Science and Practice Т. 8. №10. 2022
УДК 582.998.1:547.913.2
Многие экстракты, полученные из видов полыни, используются для лечения эпилепсии, депрессии, бессонницы, раздражительности, психоневрозов и стресса [4]. Эти виды обладают широким спектром биологической активности, такой как противомалярийная, антисептическая, антибактериальная, противоопухолевая, гепатопротекторная, спазмолитическая и противоревматическая активность [4–6].
Известно, что род Artemisia содержит много биологически активных соединений, таких как артемизин, который обладает противомалярийным и цитотоксической активностью в отношении опухолевых клеток [7], арглабин — другая биологически активная молекула, используемая для лечения некоторых видов рака в бывшем СССР [8].
Целью исследования явилось изучение сесквитерпеновых лактонов надземной части Artemisia kobstanica Rzazade.
Материалы и методы исследования
Получение суммы экстрактивных веществ . 250 г мелкоизмельченная воздушно-сухая надземная часть Artemisia kobstanica Rzazade, собранная в период бутонизации в окрестностях с. Нариманабад Шемахинского района Азербайджанской Республики, трехкратно (каждый раз в течение 3 дней) экстрагировали ацетоном. Экстракт отфильтровывали, ацетон отгоняли на роторном испарителе. Полученный остаток 11,63 г темно-зеленая смола. Выход составлял 4,65%.
Хроматографирование суммы экстрактивных веществ. 11,60 г смолы растворяли в 50 мл хлороформа и хроматографировали на колонке, заполненной окисью алюминия (нейтральная, III–IV ст. акт. h=45, d=2,50 см). Объем каждой фракции 100 мл.
Элюирование проводили смесью гексана и бензола (в соотношении 2:1; 1:1; 1:2; 1:3; 1:5; 1:7), бензолом, смесью бензола и хлороформа (в соотношении 2:1; 1:1; 1:2; 1:3; 1:5) и хлороформом.
Из фракции 25–27 элюируемой смесью гексана и бензола в соотношении 1:7 выделили кристаллическое вещество (1) состава C 15 H 18 O 3 , т. пл. 171-172°С (из водного этанола). Из фракций 32–34, элюируемой бензолом получили кристаллы (2), которые после перекристаллизации из водного спирта имели состав C 15 H 20 O 4 , т. пл. 124-126°C. Фракция 41– 44, элюируемые хлороформом содержали кристаллическое вещество (3) состава С 15 H 18 O 4 , т. пл. 202–203 °C (из водного спирта).
ИК-спектры снимали на спектрометре UR-20, спектры 1H ЯМР и 13C на спектрометре Bruker 300 с резонансной частотой 300 МГц для 1H, для 13С 75 МГц. Растворитель СdCl 3 . Химические сдвиги даны по δ шкале. Внутренний стандарт ТМС. Индивидуальность выделенных соединений определяли на пластинках Silufol UV 254, температуру плавления — на столике Boetiusa. Вещества 1 и 3 анализируя физико-химические свойства, в основном, путем непосредственного сравнения ИК-спектров с таковыми достоверных образцов α-сантонина и артемизина, соответственно, идентифицировали с α-сантонином и артемизином. Смешанные пробы 1 и 3 с достоверными образцами упомянутых лактонов депрессии температуры плавления не дают.
Результаты и их обсуждение
Впервые исследованы сесквитерпеновые лактоны вида полыни, описанного Р. Я. Рзазаде из флоры Азербайджана [9].
Хроматографированием суммы экстрактивных веществ (11,60 г) на колонке заполненной нейтральной окисью алюминия (III–IV степени активности) и элюированием гексаном, смесью гексана и бензола в различных соотношениях, бензолом, хлороформом выделены 3 сесквитерпеновых лактона С 15 H 18 O 3 , т. пл. 171–172°С (1), С 15 H 18 O 4 , т. пл. 124–126 °С (2), С 15 H 18 O 4 , т. пл. 202–203 °С (3). Лактоны 1 и 3 на основании данных ИК-, и 1Н ЯМР-спектров, а также с непосредственным сравнением ИК-спектров со спектрами достоверных образцов идентифицировали соответственно с α-сантонином и артемизином. Вещество 2, выделенный из фракций 32–34 элюированием хроматографической колонки бензолом оказалось новым С 15 H 20 O 4 , т. пл. 124-126°С (из водного этанола) и названо мерезолидом. В области характеристических частот ИК-спектра соединения обнаружены полосы поглощения карбонильной группы В-лактонного цикла (1795 см-1), карбонила кетона (1705 см-1) и двойной связи (1652 см-1). Интенсивная полоса при 915 см-1, имеющая в ИК-спектре вещества дает возможность характеризовать двойную связь как метиленовую, находящаяся вне конъюгации с карбонильной группой лактонного цикла [10].
В 13С ЯМР-спектре мерезолида, снятой с полным подавлением спин-спинового взаимодействия с протенами проявляются 15 синглетных сигналов (12; 50; 26,00; 29,50; 39,00; 40,00; 48,00; 51,50; 53,00; 55,00; 55,50; 82,00; 110,00; 143,00; 180,00; 206,0 м. д.), которые соответствуют 15 атомам углерода в его элементном составе.
1Н ЯМР-спектр исследуемого соединения имеет сигнал вторичной метильной группы (1,10 м. д., J=7,00 Гц, 3Н, СН 3 -СН<) винилметильной группы (СН 3 -С=) или при окисном цикле метильной (3Н, С, 2,20 м. д.) и экзоциклической метиленовой группы (с 4,82 и 4,95 м. д., 1Н каждый, СН 2 =С<). Другие сигналы, которые могли бы принадлежать к олефиновым протонам, в спектре отсутствуют. В основе мерезолида лежит гермакрановый углеродный скелет и содержит четыре кислородного атома. Из них два атома образует γ-лактонный цикл, один атом находился в виде кетонной группы, четвертый, по-видимому образует окисное кольцо. Высказанное предложение поддерживают данные 1H, 13C и 13C Dept ЯМР-спектров. Так 13C Dept 135 ЯМР-спектр лактона обнаруживает 11 сигналов, принадлежащих к 11 протонированным атомам углерода молекулы мерезолида: 12,50; 26,00; 29,50; 39,00; 40,00; 48,00; 53,00; 55,00; 55,50; 82,00; 110,00, характеризующиеся 2СН 3 , 4СН 2 , 4СН и 1СН 2 = групп структуры мерезолида. Из четырех однопротонных сигналов, обнаруживаемых 1Н ЯМР-спектром в области 2,40–4,00 м. д. сигнал при 2,90 м. д. (1Н, J 1 =3,0; J 2 =12,0 Гц) по значению химического сдвига характерен таковому для протона при окисном цикле [11].
Согласно литературным данным сигнал метильной группы при окисном цикле в ЯМР-спектре проявляется: эстафиатине при 1,53 [10–12], арглабине — 1,34 м. д. [13], арборесцине — 1,33 м. д. [14, 15].
В 1Н ЯМР-спектре мерезолида сигнал метильной группы при окисном цикле обнаруживается при 2,20 м. д. Парамагнитный сдвиг сигнала СН 3 -группы при окисном цикле, по-видимому, вызван электроноакцепторным влиянием карбонилакетонной группы, находящейся в вицинальном положении. Подобный парамагнитный сдвиг обнаружен в ЯМР-спектре бадхызинина. В спектре последнего сигналы метиленовой связи, обычно проявляемые в виде однопротонных синглетов при 4,80–5,00 м. д., из-за вицинального положения к эпокси группе проявляются в интервале 5,40–5,88 м. д., соответсвенно. Аналогичным образом метильная группа при оксином цикле из-за вицинального положения к кетонной группе при С-3, обнаруживается на 0,40 м. д. в слабом магнитном поле спектра [15 , 16] (Таблица).
Бюллетень науки и практики / Bulletin of Science and Practice Т. 8. №10. 2022
Таблица
Данные 1Н ЯМР-спектра мерезолида 300 МГц (CdCl 3 -d6)
|
С атом |
δ н м. д., J/Hz |
С атом |
δ |
|
1 |
1,89 (2Н, t., J 1 =J 2 =11,40 |
9 |
— |
|
2 |
2,29 (2H, t., J 1 =J 2 =11,40 |
10 |
— |
|
— |
11 |
2,48 (1H, m) |
|
|
— |
12 |
— |
|
|
5 (9) |
2,90 (1H, k, J 1 =3,90; J 2 =12,00 |
13 |
1,10 (3H, d. J=7,0) |
|
7 |
2,76 (1H, m) |
14 |
2,22 (3H, s) |
|
8 (6) |
3,83 (1H, sk, J 1 =3,90; J 2 =11,00; J 3 =15,30 |
15 |
4,82 (1H,s); 4,95 (1H,s) |
Обсуждая вопрос о положении экзометиленовой двойной связи, кетонной группы, окисного и лактонного цикла в гермакрановом углеродном скелете следует отметить, что экзометиленовая группа находится при С-10. Это заключение сделано на том основании, что наряду с 1Н ЯМР-спектральным данным в структуре гермакронолидов, выделенных из представителей рода Artemisia L. экзометиленовая группа находится при С-10. Например, в структуре гермакранолидов искендеролида, шоначалина А и С [15] и др. что касается местонахождения кетонной группы и окисного цикла то заметим, что как было отмечено, синглет метильной группы окисного цикла из-за вицинального положения к кетонной группе претерпевает парамагнитный сдвиг на 0,4 м. д. Следует отметить, что у лактонов группы α-сантонина, выделенных из видов Artemisia кетонная группа находится при С-3, а у группы тауремизина кетонная группа (или ОН-группа), в основном, находится при С-1 [16 , 17].
Исходя из данных, полученных при интерпретации 1Н, 13С, 13С Dept 135 ЯМР-спектров исследуемого лактона (мультиплетность, значения констант спин-спинового взаимодействия лактонного протона и эпокси группы, значения химического сдвига метильной группы при окисном цикле (парамагнитный сдвиг на 0,4 м. д.) мерезолиду можно предложить две альтернативные структуры 1 или 2 (Рисунок).
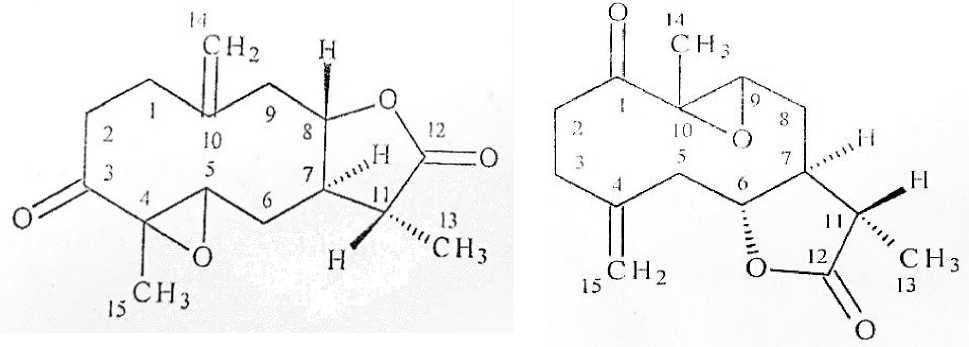
а) б)
Рисунок. Структуры мерезолида (а, б)
Известно, что в процессе биосинтеза происходящие в организме растений образуются вещества с идентичным положением функциональных групп в углеродном скелете и идентичный в отношении стереохимии [18, 19]. Поэтому, из биогенетической точки зрения можно полагать, что, вероятно, мерезолид имеет строение 3-кето-4,5-эпокси-7α,8β,11βН-гермакр-10,15-ен-8,12-олида (Рисунок а).
Список литературы Исследование сесквитерпеновых лактонов Artemisia kobstanica
- Oberprieler C. et al. Tribe Anthemideae Cass. 2009.
- McArthur E. D. Artemisia systematics and phylogeny: cytogenetic and molecular insights // Proceedings RMRS. 1998. №21. P. 67.
- Martin J., Torrell M., Korobkov A. A., Vallès J. Palynological features as a systematic marker in Artemisia L. and related genera (Asteraceae, Anthemideae)-II: implications for Subtribe Artemisiinae delimitation // Plant Biology. 2003. V. 5. №1. P. 85-93. https://doi.org/10.1055/s-2003-37979
- Walter H. L., Memory P. F., Elvin L. Medicinal botany, 2nd. 2003.
- Terra D. A., Amorim L. D. F., Catanho M. T. J. D. A., Fonseca A. D. S. D., Santos-Filho S. D., Brandâo-Neto J., Bernardo-Filho M. Effect of an extract of Artemisia vulgaris L. (Mugwort) on the in vitro labeling of red blood cells and plasma proteins with technetium-99m // Brazilian Archives of Biology and Technology. 2007. V. 50. P. 123-128. https://doi.org/10.1590/S1516-89132007000600015
- Hussain A., Hayat M. Q., Sahreen S., ul Ain Q., Bokhari S. A. Pharmacological Promises of Genus Artemisia (Asteraceae): a Review: Pharmacological Promises of Genus Artemisia // Proceedings of the Pakistan Academy of Sciences: B. Life and Environmental Sciences. 2017. V. 54. №4. P. 265-287-265-287.
- Bilia A. R., de Malgalhaes P. M., Bergonzi M. C., Vincieri F. F. Simultaneous analysis of artemisinin and flavonoids of several extracts of Artemisia annua L. obtained from a commercial sample and a selected cultivar // Phytomedicine. 2006. V. 13. №7. P. 487-493. https://doi.org/10.1016/j.phymed.2006.01.008
- Naqvi S. A. H., Khan M. S. Y., Vohora S. B. Antibacterial, antifungal and anthelmintic studies on Ochrocarpus longifolius // Planta Medica. 1976. V. 29. №1. P. 98-100. https://doi.org/10.1055/s-0028-1097636
- Рзазаде Р. Я. Новые виды, ряды и подроды кавказских полыней // Известия АН Азербайджанской ССР. 1955. С. 17-35.
- Беллами Л. Д. Инфракрасные спектры сложных молекул. М.: Изд-во иностр. лит., 1963. 590 с.
- Кагарлицкий А. Д., Адекенов С. М., Куприянов А. Н. Сесквитерпеновые лактоны растений Центрального Казахстана. Алма-Ата: Наука КазССР, 1987. 237 с.
- Snchez-Viesca F., Romo J. Estafiatin, a new sesquiterpene lactone isolated from Artemisia mexicana (Willd) // Tetrahedron. 1963. V. 19. №8. P. 1285-1291.
- Адекенов С. М., Мухаметжанов К. М., Кагарлицкий А. Д., Куприянов А. Н. Арглабин-новый сесквитерпеновый лактон из Artemisia glabella // Химия природных соединений. 1982. №5. С. 655-656.
- Bates R. B., Cekan Z., Prochazka V., Herout V. The structure of arborescin // Tetrahedron Letters. 1963. V. 4. №17. P. 1127-1130. https://doi.org/10.1016/S0040-4039(01)90788-9
- Серкеров С. В., Мехтиева Н. П. Новый компонент Eupatorium cannabinum L. // Химия природных соединений. 2009. Т. 3. С. 318-320.
- Серкеров С. В. Терпеноиды и фенольные соединения растений семейств Asteraceae и Apiaceae: автореф. дисс. ... д-ра хим. наук. Ташкент, 1991. 52 с.
- Рыбалко К. С. (1978) Природные секвитерпеновые лактоны. М., 320 с.
- Serkerov S. V. Stereochemistry of the eudesmanolides ofFerula oopoda // Chemistry of Natural Compounds. 1980. V. 16. №4. P. 366-367. https://doi.org/10.1007/BF00568369
- Serkerov S. V. Stereochemistry of guaianolides ofFerula oopoda // Chemistry of Natural Compounds. 1980. V 16. №5. P. 448-451. https://doi.org/10.1007/BF00571035


