Исследование строения дикарбоксилатов трис(4-фторфенил) (4-FC6H4)3Sb[OC(O)R]2(R=C6H3F2-2,3, C6H3(NO2)2-3,5, C6H4OMe-2,CF2Br, CH=CHPh,CH3, C?CH)
Автор: Белов Василий Васильевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 4 т.13, 2021 года.
Бесплатный доступ
Взаимодействием трис(4-фторфенил)сурьмы с 2,3-дифторбензойной, 3,5-динитробензойной, 2-метоксибензойной, бромдифторуксусной, фенилакриловой, муравьиной и пропиоловой кислотами в присутствии трет-бутилгидропероксида (1:2:1 мольн.) в диэтиловом эфире при комнатной температуре синтезированы дикарбоксилаты трис(4-фторфенил)сурьмы (4-FC6H4)3Sb[OC(O)R]2, где R = C6H3F2-2,3 (1), C6H3(NO2)2-3,5 (2), C6H4OMe-2 (3), CF2Br (4), CH=CHPh (5), CH3 (6), и C≡CH (7). В ИК-спектрах соединений 1-7, снятых на ИК-Фурье спектрометре Shimadzu IRAffinity-1S в таблетке KBr в области 4000-400 см-1, имеются полосы поглощения карбонильных групп, которые смещены в область низкочастотных колебаний по сравнению с ИК-спектрами исходных кислот. Согласно данным РСА, проведенного на дифрактометре D8 QUEST фирмы Bruker, кристаллографические параметры элементарной ячейки соединения 1: пространственная группа Р-1, а = 9,034(4), b = 11,351(8), c = 14,814(9) Å, α = 70,11(3)°, β = 88,60(2)°, γ = 87,03(2)°, V = 1426(15) Å3, ρвыч = 1,679 г/см3, Z = 2. Атом Sb в комплексе 1 имеет координацию тригональной бипирамиды с карбоксилатными лигандами в аксиальных положениях. Аксиальный угол OSbO составляет 176,95(6)º. Длины связей Sb-O и Sb-С равны 2,135(2), 2,121(2) и 2,113(3)-2,116(3) Å. Расстояния Sb···O=С составляют 3,040(2), 2,861(3) Å, что меньше суммы ван-дер-ваальсовых радиусов сурьмы и кислорода (3,70 Å). Атом сурьмы выходит из экваториальной плоскости [C3] на 0,038 Å. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2051716; deposit@ccdc.cam.ac.uk или http://www.ccdc.cam.ac.uk/data_request/cif).
Триc(4-фторфенил)сурьма, дикарбоксилат, реакция окислительного присоединения, ик-спектр, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147236609
IDR: 147236609 | УДК: 549.242+547.53.024+548.312.2+548.312.5 | DOI: 10.14529/chem210408
The structure study of tris(4-fluorophenyl)antimony dicarboxylates (4-FC6H4)3Sb[OC(O)R]2(R=C6H3F2-2,3, C6H3(NO2)2-3,5, C6H4OMe-2,CF2Br, CH=CHPh,CH3, C?CH)
The interaction of tris(4-fluorophenyl)antimony with 2,3-difluorobenzoic acid, as well as with 3,5-dinitrobenzoic, 2-methoxybenzoic, bromodifluoroacetic, cinnamic, formic, and propionic acids in the presence of tert-butyl hydroperoxide (1:2:1 mol.) in ether at ambient temperature has given tris(4-fluorophenyl)antimony dicarboxylates (4-FC6H4)3Sb[OC(O)R]2, where R = C6H3F2-2,3 (1), C6H3(NO2)2-3,5 (2), C6H4OMe-2 (3), CF2Br (4), CH=CHPh (5), CH3 (6), и C≡CH (7). The IR spectra of compounds 1-7, recorded on a Shimadzu IRAffinity-1S Fourier transform IR spectrometer, in a KBr pellet within the 4000-400 cm-1 interval, contain absorption bands of carbonyl groups, which are shifted to the low-frequency vibration region in comparison with the IR spectra of the initial acids. According to the X-ray diffraction data obtained on a Bruker D8 QUEST diffractometer, compound 1 has the following crystallographic parameters of the unit cell: space group P-1, a = 9.034(4), b = 11.351(8), c = 14.814(9) Å, α = 70.11(3)°, β = 88.60(2)°, γ = 87.03(2)°, V = 1426(15) Å3, ρcalc = 1.679 g/cm3, Z = 2. The antimony atom in 1 has a distorted trigonal-bipyramidal coordination with carboxylate ligands in axial positions. The OSbO axial angle is 176.95 (6)°. The lengths of the Sb-O and Sb-C bonds are equal to 2.135(2), 2.121(2) and 2.113(3)-2.116 (3) Å. The Sb···O=C distances are 3.040(2), 2.861 (3) Å, that is, less than the sum of the van der Waals radii of antimony and oxygen (3.70 Å). The antimony atom departs from the equatorial plane [C3] by 0.038 Å. Complete tables of atom coordinates, bond lengths and valence angles are deposited at the Cambridge Crystallographic Data Center (№ 2051716; deposit@ccdc.cam.ac.uk or http://www.ccdc.cam.ac.uk/data_request/cif).
Текст научной статьи Исследование строения дикарбоксилатов трис(4-фторфенил) (4-FC6H4)3Sb[OC(O)R]2(R=C6H3F2-2,3, C6H3(NO2)2-3,5, C6H4OMe-2,CF2Br, CH=CHPh,CH3, C?CH)
Дикарбоксилаты трис (4-фторфенил)сурьмы, трис (3-фторфенил)сурьмы и три- пара- толилсурьмы, полученные по реакции окислительного присоединения из триарилсурьмы и карбоновых кислот HX в присутствии пероксида активно изучаются в работах [1–22]. В продолжение исследования особенностей синтеза и строения дикарбоксилатов триарилсурьмы синтезирован ряд дикарбоксилатов трис (4-фторфенил)сурьмы (4-FC 6 H 4 ) 3 Sb[OC(O)R] 2 из трифенилсурьмы и трет -бутилгидропероксида в присутствии 2,3-дифторбензойной, 3,5-динитробензойной, 2-метоксибензойной, бромдифторуксусной, фенилакриловой, муравьиной и пропиоловой кислотами . Данный метод синтеза выделяется одностадийностью, мягкими условиями протекания реакции, высоким выходом и чистотой целевого продукта.
Экспериментальная часть
Синтез бис (2,3 - дифторбензоато)[ трис (4 - фторфенил)сурьмы] (4-FC 6 H 4 ) 3 Sb[OC(O)C 6 H 3 F 2 -2,3] 2 (1)
Смесь 150 мг (0,368 ммоль) трис (4-фторфенил)сурьмы, 115 мг (0,737 ммоль) 2,3-дифторидбензойной кислоты и 48 мг (0,368 ммоль) 70%-ного раствора гидропероксида третичного бутила в 30 мл диэтилового эфира выдерживали при 20 °С в течении 24 ч. После медленного удаления растворителя получили 135 мг (78 %) бесцветных кристаллов, которые после перекристаллизации из смеси бензол–гептан (2:1) имели t пл = 128 °C. ИК-спектр, ν , см - 1: 3167, 3099, 3068,
3045, 2991, 2958, 2927, 2856, 1643, 1631, 1577, 1485, 1423, 1394, 1350, 1307, 1294, 1273, 1226, 1165, 1151, 1064, 1012, 954, 831, 786, 758, 721, 702, 677, 632, 584, 511, 470, 459, 418. Найдено, %: С 53,09; Н 2,57. C 32 H 18 F 7 O 4 Sb. Вычислено, %: С 53,14; Н 2,51.
Соединения 2 – 6 синтезировали по аналогичной методике.
Бис (3,5 - динитробензоато)[ трис (4 - фторфенил)сурьма] (4-FC 6 H 4 ) 3 Sb[OC(O)C 6 H 3 (NO 2 ) 2 -3,5] 2 (2) , бесцветные прозрачные кристаллы, выход 95 %, t пл = 199,0 °С. ИК-спектр, ν , см - 1: 3095, 2976, 2881, 1676, 1627, 1583, 1544, 1492, 1460, 1396, 1346, 1309, 1276, 1232, 1180, 1074, 1010, 921, 833, 785,723, 698, 586, 553, 511, 459, 418. Найдено, %: С 46,29; Н 2,25. C 32 H 18 F 3 N 4 O 12 Sb. Вычислено, %: С 46,34; Н 2,19.
Бис (2 - метоксибензоато)[ трис (4 - фторфенил)сурьма] (4-FC 6 H 4 ) 3 Sb[OC(O)C 6 H 4 OMe-2] 2 (3) , бесцветные прозрачные кристаллы, выход 82 %,t пл = 120,0 °С. ИК-спектр, ν , см - 1: 3099, 3068, 2960, 2933, 2839, 2378, 1606, 1593, 1579, 1560, 1521, 1490, 1465, 1440, 1392, 1367, 1301, 1292, 1276, 1255, 1220, 1182, 1165, 1097, 1051, 1026, 1018, 1012, 875, 837, 829, 806, 754, 704, 669, 582, 555, 513, 459, 443, 418. Найдено, %: С 57,52; Н 3,78. C 34 H 26 F 3 O 6 Sb. Вычислено, %: С 57,57; Н 3,70.
Бис (бромдифторацето)[ трис (4 - фторфенил)сурьма] (4-FC 6 H 4 ) 3 Sb[OC(O)CF 2 Br] 2 (4) , бесцветные прозрачные кристаллы, выход 67 %, t пл = 100,0 °С. ИК-спектр, ν , см - 1: 3074, 3057, 2964, 2929, 2860, 2794, 2657, 1716, 1583, 1494, 1398, 1332, 1309, 1234, 1153, 1130, 1072, 1008, 941, 815, 709, 605, 590, 561, 509, 435, 418. Найдено, %: С 34,81; Н 2,05. C 22 H 12 F 7 O 4 Br 2 Sb. Вычислено, %: С 34,86; Н 1,59.
Дициннамат трис (4 - фторфенил)сурьмы (4-FC 6 H 4 ) 3 Sb[OC(O)CH=CHPh] 2 (5) , бесцветные прозрачные кристаллы, выход 53 %, t пл = 113,7 °С. ИК-спектр, ν , см - 1: 3057, 3024, 2837, 2721, 2611, 2538, 2312, 1687, 1680, 1631, 1579, 1492, 1450, 1423, 1342, 1315, 1442, 1288, 1205, 1176, 1163, 1091, 1066, 985, 972, 937, 871, 825, 765, 705, 675, 592, 584, 542, 507, 480, 457, 441, 418. Найдено, %: С 61,60; Н 3,79. C 36 H 26 F 3 O 4 Sb. Вычислено, %: С 61,65; Н 3,74.
Бис (ацето)[ трис (4 - фторфенил)сурьма] (4-FC 6 H 4 ) 3 Sb[OC(O)CH 3 ] 2 (6) , бесцветные прозрачные кристаллы, выход 93 %, t пл = 193,0 °С. ИК-спектр, ν , см - 1: 3097, 3062, 2968, 2924, 2864, 1585, 1492, 1398, 1311, 1300, 1234, 1161, 1095, 1066, 1010, 947, 906, 871, 823, 702, 682, 617, 590, 563, 513, 509, 459, 416. Найдено, %: С 50,26; Н 3,51. C 22 H 18 F 3 O 4 Sb. Вычислено, %: С 50,31; Н 3,46.
Бис (пропиолато)[ трис (4 - фторфенил)сурьма] (4-FC 6 H 4 ) 3 Sb[OC(O)C≡CH] 2 (7) , бесцветные прозрачные кристаллы, выход 65 %, t пл = 115,0 °С. ИК-спектр, ν , см - 1: 3286, 3209, 3086, 2929, 2856, 2559, 2200, 2115, 2100, 1894, 1637, 1620, 1581, 1490, 1396, 1319, 1294, 1276, 1232, 1165, 1068, 1010, 941, 902, 840, 827, 821, 773, 715, 671. 663, 638, 613, 586, 509, 418. Найдено, %: С 52,82; Н 2,64. C 24 H 14 F 3 O 4 Sb. Вычислено, %: С 52,87; Н 2,59.
ИК-спектры соединений 1 – 7 записывали на ИК-спектрометре Shimadzu IR Affinity-1S в таблетках KBr в области 4000–400 см–1.
Элементный анализ проведен на приборе Carlo-Erba 1106.
Рентгеноструктурный анализ (РСА) кристалла соединения 1 проводили на дифрактометре D8 QUEST фирмы Bruker (MoKα-излучение, λ = 0,71073 Å, графитовый монохроматор) при 296(2) К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [23]. Все расчеты по определению и уточнению структуры выполнены по программам SHELXL/PC [24], OLEX2 [25]. Структура определена прямым методом и уточнена методом наименьших квадратов в анизотропном приближении для неводородных атомов. Кристаллографические данные и результаты уточнения структуры приведены в табл. 1. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (для 1 № 2051716; или . Кристаллографические данные и результаты уточнения структуры приведены в табл. 1, основные длины связей и валентные углы – в табл. 2.
Таблица 1
|
Параметр |
1 |
|
Формула |
C 32 H 18 F 7 O 4 Sb |
|
М |
721,21 |
|
Сингония |
Триклинная |
|
Пр. группа |
P -1 |
|
a , Å |
9,034(4) |
|
b , Å |
11,351(8) |
|
c , Å |
14,814(9) |
|
α, град. |
70,11(3) |
|
β, град. |
88,60(2) |
|
γ, град. |
87,03(2) |
|
V , Å3 |
1426,7(15) |
|
Z |
2 |
|
ρ (выч.), г/см3 |
1,679 |
|
µ, мм–1 |
1,050 |
|
F (000) |
712,0 |
|
Размер кристалла, мм |
0,18 × 0,14 × 0,1 |
|
Область сбора данных по 2θ, град. |
7,05–54,28 |
|
Интервалы индексов отражений |
–11 ≤ h ≤ 11, –14 ≤ k ≤ 14, –18 ≤ l ≤ 18 |
|
Измерено отражений |
34707 |
|
Независимых отражений |
6288 ( R int = 0,0329) |
|
Переменных уточнения |
405 |
|
GOOF |
1,077 |
|
R -факторы по I>2σ (I) |
R 1 = 0,0269, wR 2 = 0,0625 |
|
R -факторы по все отражениям |
R 1 = 0,0337, wR 2 = 0,0658 |
|
Остаточная электронная плотность (max/min), e/Å3 |
0,55/–0,46 |
Таблица 2
|
Связь |
d, Å |
Угол |
ω , град |
|
Sb(1)–O(3) |
2,135(2) |
O(1)Sb(1)O(3) |
176,95(6) |
|
Sb(1)–O(1) |
2,121(2) |
C(21)Sb(1)O(3) |
88,67(9) |
|
Sb(1)–C(21) |
2,113(3) |
C(21)Sb(1)O(1) |
91,45(9) |
|
Sb(1)–C(1) |
2,120(2) |
C(21)Sb(1)C(1) |
110,33(10) |
|
Sb(1)–C(11) |
2,116(3) |
C(21)Sb(1)C(11) |
143,98(9) |
|
O(3)–C(47) |
1,305(3) |
C(1)Sb(1)O(3) |
89,00(8) |
|
O(4)–C(47) |
1,223(3) |
C(1)Sb(1)O(1) |
88,10(8) |
|
F(5)–C(4) |
1,361(3) |
C(11)Sb(1)O(3) |
89,29(9) |
|
O(1)–C(37) |
1,276(3) |
C(11)Sb(1)O(1) |
92,41(9) |
|
O(2)–C(37) |
1,224(3) |
C(11)Sb(1)C(1) |
105,58(10) |
|
F(1)–C(32) |
1,331(4) |
C(47)O(3)Sb(1) |
109,96(14) |
|
F(6)–C(14) |
1,358(3) |
C(37)O(1)Sb(1) |
116,44(16) |
Кристаллографические данные, параметры эксперимента и уточнения структуры 1
Основные длины связей ( d ) и валентные углы ( ω ) в структуре 1
Обсуждение результатов
Установлено, что реакции трис (4-фторфенил)сурьмы с такими карбоновыми кислотами, как 2,3-дифторбензойная, 3,5-динитробензойная, 2-метоксибензойная, бромдифторуксусная, фени-лакриловая, муравьиная и пропиоловая в присутствии трет -бутилгидропероксида (мольное соотношение 1:2:1) протекают в эфире с образованием дикарбоксилатов трис (4-фторфенил)сурьмы, выделяемых с выходом 40–90 %.
(4-FC 6 H 4 ) 3 Sb + 2 HOC(O)R + t -BuOOH → (4-FC 6 H 4 ) 3 Sb[OC(O) R ] 2 +H 2 O + t -BuOH,
R = C 6 H 3 F 2 -2,3 ( 1 ), C 6 H 3 (NO 2 ) 2 -3,5 ( 2 ), C 6 H 4 OMe-2 ( 3 ),
CF 2 Br ( 4 ), CH=CHPh ( 5 ), CH 3 ( 6 ), C≡CH ( 7 )
Соединения 1 – 7 представляют собой бесцветные прозрачные кристаллы с четкой температурой плавления, хорошо растворимые в ароматических углеводородах и полярных растворителях. Строение комплексов подтверждено методами ИК-спектроскопии и рентгеноструктурного анализа.
Инфракрасная спектроскопия
В ИК-спектрах дикарбоксилатов триарилсурьмы 1 - 7 , снятых на ИК-Фурье спектрометре Shimadzu IRAffinity-1S в таблетке KBr присутствуют полосы поглощения при 441–459 см–1, которые можно отнести к валентным колебаниям Sb - O. Кроме этих полос ИК-спектры содержат сильные полосы поглощения при 509–513 см–1, относящиеся к валентным колебаниям Sb - С. В ИК-спектрах дикарбоксилатов триарилсурьмы присутствуют также две полосы поглощения в области 1460 - 1490 см–1, характеризующие фенильные группы. Рассмотрение ИК-спектров дикарбоксилатов триарилсурьмы, снятых в интервале 400–4000 см–1, существенно помогает в ответе на вопрос -есть ли координация карбонильного атома кислорода на центральный атом сурьмы. В ИК-спектрах указанных соединений полосы валентных колебаний С=О (1606–1620 см–1) значительно смещены в низковолновую область по сравнению с ИК-спектрами карбоновых кислот (1662– 1702 см–1) [26] (табл. 3), что указывает на координацию атома сурьмы с атомом карбонильного кислорода.
Таблица 3
ИК-спектры дикарбоксилатов трис (4-фторфенил)сурьмы и карбоновых кислот в области валентных колебаний C=O, см–1
|
R |
|||||||
|
C 6 H 3 F 2 -2,3 |
C 6 H 3 (NO 2 ) 2 -3,5 |
C 6 H 4 OMe-2 |
CF 2 Br |
CH=CHPh |
CH 3 |
C≡CH |
|
|
Ar 3 Sb[OC(O)R) 2 |
1643 |
1627 |
1606 |
1716 |
1631 |
1585 |
1637 |
|
HOC(O)R |
1695 |
1707 |
1688 |
1770 |
1680 |
1727 |
1710 |
В ИК-спектре соединения 7 присутствует полоса, характеризующая тройную связь С ≡ С (2100 см–1). В спектрах соединений 1 , 2 , 3 и 5 , содержатся соответствующие двойной связи C=C колебания, характерные для кислот типа RCH=CHCOOH (1643–1676 см–1). Кроме того, в ИК-спектрах исследуемых соединений наблюдаются интенсивные полосы поглощения валентных колебаний фрагмента SbC 3 в интервале 509–511 см–1 соответственно и полосы валентных колебаний С - Н арильных фрагментов при 2800–3100 см–1, а также целый ряд колебаний разного типа, характерных для функциональных групп и заместителей в арильных кольцах и органическом радикале R карбоновой кислоты [27, 28]. В ИК-спектре соединения 2 , например, присутствуют полосы поглощения нитрогрупп, характеризующие валентные колебания NO 2 -групп (1309 и 1154 см–1 соответственно). Для сравнения, в ИК-спектре кислоты соответствующие полосы находятся при 1291 и 1547 см–1.
По данным РСА, в соединении 1 атомы Sb находятся в экваториальной плоскости и имеют искаженную тригонально-бипирамидальную координацию с атомами кислорода карбоксилатных лигандов в аксиальных положениях (рис. 1).
В соединении 1 аксиальный угол OSbO составляет 176,95(6)º. Длины связей Sb-O и Sb-С равны 2,135(2), 2,121(2) и 2,113(3)-2,116(3) Å. Сумма экваториальных углов CSbC имеет значение 359,90(9)º. Атом сурьмы выходит из экваториальной плоскости [C 3 ] на 0,038 Å. Расстояния Sb···O=С составляют 3,040(2), 2,861(3) Å, что меньше суммы ван-дер-ваальсовых радиусов сурьмы и кислорода (3,70 Å) [29].
Формирование кристаллической структуры соединения 1 обусловлено наличием межмолекулярных водородных связей H∙∙∙O(=C) 2,574 Å и H∙∙∙F 2,622 и 2,560 Å. Данные взаимодействия структурируют молекулы кристалла в слои, расположенные перпендикулярно кристаллографической оси b (рис. 2).
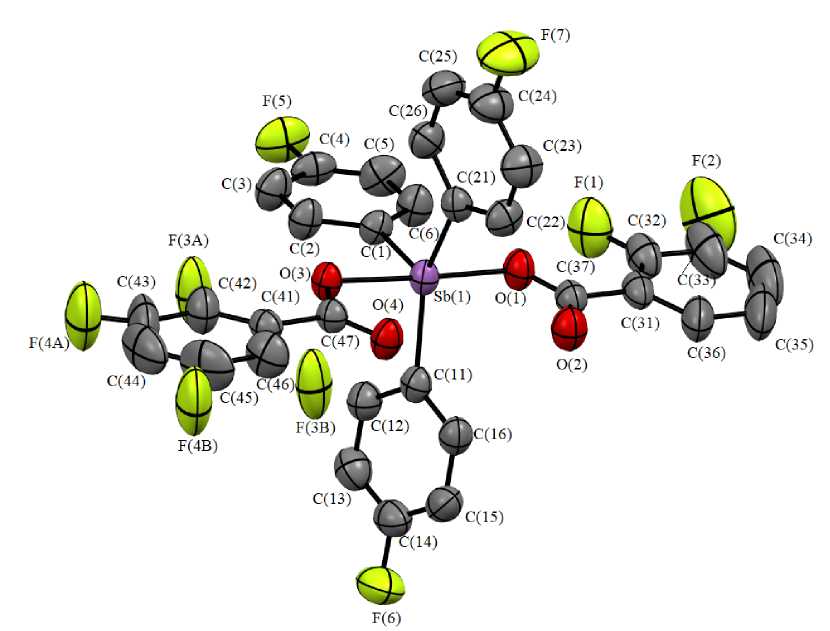
Рис. 1. Общий вид молекулы 1 (атомы водорода не показаны)
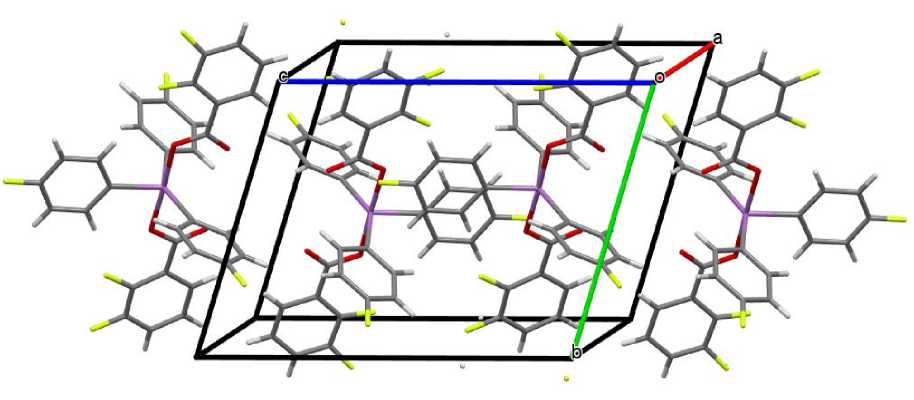
Рис. 2. Упаковка ионов комплекса 1 в кристалле (показан только один слой)
Выводы
Таким образом, в настоящей работе по реакции окислительного присоединения трис(4-фторфенил)сурьмы с 2,3-дифторбензойной, 3,5-динитробензойной, 2-метоксибензойной, бромдифторуксусной, фенилакриловой, муравьиной и пропиоловой кислотами в присутствии трет -бутилгидропероксида (1:2:1 мольн.) в диэтиловом эфире получены семь дикарбоксилатов триа-рилсурьмы типа (Ar)3Sb[OC(O)R]2. В ИК-спектрах полученных соединений наблюдаются полосы поглощения карбонильных групп, которые смещены в область низкочастотных колебаний по сравнению с ИК-спектрами исходных кислот, что указывает на координацию атома сурьмы с атомом карбонильного кислорода. Данные ИК-спектров соединений 1-7 подтверждают данные рентгеноструктурного анализа соединения 1, в котором атомы Sb имеют искаженную тригональ-но-бипирамидальную координацию с атомами кислорода карбоксилатных лигандов в аксиальных положениях, причем расстояния Sb···O=С меньше суммы ван-дер-ваальсовых радиусов сурьмы и кислорода (3,70 Å) и составляют 3,040(2), 2,861(3) Å.
Выражаю благодарность профессору В.В. Шарутину за проведенные рентгеноструктурные исследования.
Список литературы Исследование строения дикарбоксилатов трис(4-фторфенил) (4-FC6H4)3Sb[OC(O)R]2(R=C6H3F2-2,3, C6H3(NO2)2-3,5, C6H4OMe-2,CF2Br, CH=CHPh,CH3, C?CH)
- Improved Methods for the Synthesis of Antimony Triacetate, Triphenylantimonyl Diacetate and Pentaphenylantimoy / T.C. Thepe, R.J. Garascia, M.A. Selvoski et al. // Ohio J. Sci. - 1977. - V. 77, no.3. - P. 134-135.
- Шарутин, В.В. Синтез, реакции и строение арильных соединений пятивалентной сурьмы / B.В. Шарутин, А.И. Поддельский, О.К. Шарутина // Коорд. химия. - 2020. - Т. 46, № 10. - C. 579-648. DOI: 10.31857/S0132344X20100011
- Шарутин, В.В. Синтез и строение фенилпропиолатов тетра- и трифенилсурьмы /
- B.В. Шарутин, О.К. Шарутина, А.Р. Котляров // Журнал неорганической химии. - 2015. - Т. 60, № 4. - С. 525. DOI: 10.7868/S0044457X15040236
- Шарутин, В.В. Синтез и строение фенилацетатов тетра- и трифенилсурьмы / В.В. Шарутин, О.К. Шарутина, В.С. Сенчурин // Журнал неорганической химии. - 2015. - Т. 60, № 9. - C. 1200. DOI: 10.7868/S0044457X15060148
- Шарутин, В.В. Синтез и строение дикарбоксилатов трис(4-фторфенилсурьмы): (4-FC6H4)3Sb[OC(O)R]2, R = CH2I, C6F5 / В.В. Шарутин, О.К. Шарутина // Известия Академии наук. Серия химическая. - 2017. - № 4. - С. 707-710.
- Шарутин, В.В. Синтез и строение дикарбоксилатов трис(4-фторфенил)сурьмы / В.В. Шарутин, О.К. Шарутина // Журнал общей химии. - 2016. - Т. 86, № 8. - С. 1366-1370.
- Synthesis and in vitro Antitumor of Some Triarylantimony Di(N-phenylglycinates) / Yu L., Ma Y-Q., Wang G-C., Li J-S. // Heteroat. Chem. - 2004. - V. 15. - P. 32-36. DÛI:10.1002/hc.10208
- Особенности строения дикарбоксилатов триорганилсурьмы R3Sb[OC(O)R')]2 / В.В. Шарутин, О.К. Шарутина, А.П. Пакусина и др. // Координационная химия. - 2003. - Т. 29, № 11. -С. 843-851.
- Шарутин, В.В. Синтез и строение 4-оксибензоатов тетра- и трифенилсурьмы / В.В. Шару-тин, О.К. Шарутина, В.С. Сенчурин // Журнал неорганической химии. - 2014. - Т. 59, № 9. -С. 1182-1186. DOI: 10.7868/S0044457X14090189
- Шарутин, В.В. Синтез и строение пропиолатов три- и тетрафенилсурьмы / В.В. Шарутин, О.К. Шарутина, В.С. Сенчурин // Коорд. химия. - 2014. - Т. 40, № 2. - С. 108-112. DOI: 10.7868/S0132344X14020108
- Синтез и строение диакрилата трифенилсурьмы / А.В. Гущин, Л.К. Прыткова, Д.В. Шашкин и др. // Вестник Нижегородского университета им. Н.И. Лобачевского. - 2010. -№ 1. - С. 95-99.
- Expperimental and Theoretical Distributijn of Electron Density and Thermopolimerization in Crystals of Ph3Sb(O2CCH=CH2)2 Complex / G.K. Fukin, M.A. Samsonov, A.V. Arapova et al. // J. Solid State Chem. - 2017. - V. 254. - P. 32-39. DOI: 10.1016/j.jssc.2017.06.030
- Шарутин, В.В. Дикарбоксилаты трис(4-фторфенил)сурьмы (4-FC6H4)3Sb[OC(O)R]2, R = Q0H15, Q^-цикло) / В.В. Шарутин, О.К. Шарутина, А.Н. Ефремов // Журн. неорган. химии. -2016. - Т. 61, № 1. - С. 46-50. DOI: 10.7868/S0044457X16010232
- Синтез и строение дикарбоксилатов трис(3-фторфенил)сурьмы: (3-FC6H4)3Sb[OC(O)R]2, R = C6H3(NO2)2-3,5, CH2Br, CH2Cl, CH=CHPh) / В.В. Шарутин, О.К. Шарутина, А Н. Ефремов и др. // Коорд. химия. - 2018. - Т. 44, № 5. С. 333-339. DOI: 10.1134/S0132344X18050109
- Синтез и строение дикарбоксилатов трис(3-фторфенил)сурьмы: (3-FC6H4)3Sb[OC(O)R]2 (R = Œ2Cl, Ph, CH2C6H4NO2-4, С10Н5) / В.В. Шарутин, О.К. Шарутина, Р.В. Решетникова и др. // Журн. неорган. химии. - 2017. - Т. 62, № 11. - С. 1457-1463. DOI: 10.7868/S0044457X17110058
- Calorimetric Study of Organic Compounds of Antimony and Bismuth Ph3Sb(O2CCH=CHCH3)2 and Ph3Bi(O2CCH=CHCH3)2 / I.A. Letyanina, A.V. Markin, N N. Smirnova et al. // J. Therm. Anal. Calorim. - 2016. - V. 125, no. 1. - P. 339-349.
- Особенности строения дикарбоксилатов триорганилсурьмы R3Sb[OC(O)R')]2 / В.В. Ша-рутин, О.К. Шарутина, А.П. Пакусина и др. // Координационная химия. - 2003. - Т. 29, № 11. -С. 843-851.
- Синтез и строение бис[(2Е)-3-(2-фурил)проп-2-еноата] трифенилсурьмы Ph3Sb[O2CCH=CH(C4H3O)]2 / О. С. Калистратова, П. В. Андреев, А. В. Гущин и др. // Кристаллография. - 2016. - Т. 61, № 3. - С. 396-399. DOI 10.7868/S0023476116030139
- Comparative Stability, Toxicity and Anti-Leishmanial Activity of Triphenyl Antimony(V) and Bismuth(V) a-Hydroxy Carboxylato Complexes / R.N. Duffin, V.L. Blai, L. Kedzierski et al. // Dalton Trans. - 2018. - V. 47, no. 3. - P. 971-980. DOI: 10.1039/C7DT04171C
- Синтез и молекулярные структуры бис(2-метилкарборанилкарбоксилатов) трифенилсурьмы и трифенилвисмута / В.В. Шарутин, О.К. Шарутина, В.С. Сенчурин и др. // Бутлеровские сообщения. - 2012. - Т. 29, № 3. - С. 51-56.
- Синтез и строение бис(фенилкарборанилкарбоксилата) три(и-толил)сурьмы / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина и др. // Бутлеровские сообщения. - 2011. - Т. 28, № 19. - С. 54-58.
- Synthesis, Characterization and Crustal Structures of Tri- and Tetraphenylantimony(V) Compounds Containing Arylcarbonyloxy Moiety / Li Quan, H. Yin, J. Cui, M. Hong, D. Wang // J. Organo-met. Chem. - 2009. - V. 694. - P. 3708-3717.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures from Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- OLEX2: Complete Structure Solution, Refinement and Analysis Program / O.V. Dolomanov, L.J. Bourhis, R.J. Gildea et al. // J. Appl. Cryst. - 2009. - V. 42. - P. 339-341. DOI: 10.1107/S0021889808042726
- https://sdbs.db.aist.go.jp/sdbs/cgi-bin/direct_frame_top.cgi
- Тарасевич, Б.Н. ИК-спектры основных классов органических соединений / Б.Н. Тарасевич. - М.: МГУ, 2012. - 54 с.
- Инфракрасная спектроскопия органических и природных соединений: учебное пособие / А.В. Васильев, Е В. Гриненко, А О. Щукин и др. - СПб.: СПбГЛТА, 2007. - 54 с.
- Бацанов, С.С. Атомные радиусы элементов / С.С. Бацанов // Журн. неорган. химии. -1991. - Т. 36, № 12. - С. 3015-3037.

![Исследование строения дикарбоксилатов трис(4-фторфенил) (4-FC6H4)3Sb[OC(O)R]2(R=C6H3F2-2,3, C6H3(NO2)2-3,5, C6H4OMe-2,CF2Br, CH=CHPh,CH3, C?CH) Исследование строения дикарбоксилатов трис(4-фторфенил) (4-FC6H4)3Sb[OC(O)R]2(R=C6H3F2-2,3, C6H3(NO2)2-3,5, C6H4OMe-2,CF2Br, CH=CHPh,CH3, C?CH)](/file/cover/147236609/issledovanie-stroenija-dikarboksilatov-tris-4-ftorfenil-4-fc6h4-3sb-oc-o-r-2.png)
