Исследование технологии производства экстрактов чёрного и зелёного чая с антиоксидантной активностью: определение влияния температуры экстракции
Автор: Карпова М. О., Макарова Н. В., Игнатова Д. Ф., Лашманова Л. А.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Пищевая биотехнология
Статья в выпуске: 3 (93), 2022 года.
Бесплатный доступ
Многие факторы могут влиять на эффективность экстракции антиоксидантов из растений. Наиболее важные параметры, которые влияют на эффективность экстракции с точки зрения выхода и качества, включают температуру, время экстракции, размер частиц. Целью нашего исследования был подбор оптимальной температуры экстракции для двух видов чая, для получения экстрактов с высокими значениями общего содержания фенолов, флавоноидов, антирадикальной активности по методу DPPH, восстанавливающей силы по методу FRAP и танинов. Объектами исследования выступали экстракты двух видов чая, полученные с использованием одного вида растворителя - воды, степенью измельчения 0.5 мм и тремя температурами экстракции 20-25 °C, 40-50 °C и температурой кипения растворителя. Большее количество фенолов экстрагируется из экстрактов чёрного чая (493 мг (ГК)/100 г) с температурой равной температуре кипения растворителя, зелёный чай (936 мг (ГК)/100 г) показывает высокие значения содержания фенолов при температуре экстракции 40-50 (С. Высокие значения общего содержания флавоноидов наблюдались при температуре равной температуре кипения растворителя как у чёрного (456 мг (К)/100 г), так и у зелёного (502 мг (К)/100 г) чая. Танинов больше всего содержалось в экстрактах чёрного (98.3 мг катехина/100 г) и зелёного (224.9 мг катехина/100 г) чая при температуре 40-50 (С. Наименьшая антирадикальная активность была обнаружена в экстрактах чёрного (Ec50= 1.6 мг/см3)и зелёного (Ec50=4.0 мг/см3) чая с температурой экстракции 40-50 (С. Наибольший показатель восстанавливающей силы был у экстрактов чёрного (14.04 ммоль Fe2+/кг) чая с температурой экстракции равной температуре кипения растворителя, а у зелёного (12.15 ммоль Fe2+/кг) чая при температуре 40-50 (С.
Чай чёрный, чай зелёный, фенолы, танины, свободные радикалы, температура экстракции
Короткий адрес: https://sciup.org/140297680
IDR: 140297680 | УДК: 663.958.8 | DOI: 10.20914/2310-1202-2022-3-74-81
Research of the technology of production of black and green tea extracts with antioxidant activity: determination of the effect of the extraction temperature
Many factors can influence the efficiency of the extraction of antioxidants from plants. The most important parameters that affect extraction efficiency in terms of yield and quality include temperature, extraction time, and particle size. The aim of our study was to select the optimal extraction temperature for two types of tea, to obtain extracts with high values of total phenols, flavonoids, antiradical activity according to the DPPH method, restoring strength according to the FRAP method and tannins. The objects of the study were extracts of two types of tea, obtained using one type of solvent - water, a grinding degree of 0.5 mm and three extraction temperatures of 20-25 °C, 40-50 °C and the boiling point of the solvent. A large amount of phenols is extracted from black tea extracts (493 mg (HA) / 100 g) with a temperature equal to the boiling point of the solvent, green tea (936 mg (HA) / 100 g) shows high values of phenol content at an extraction temperature of 40-50 (С. High values of the total content of flavonoids were observed at a temperature equal to the boiling point of the solvent in both black (456 mg (K) / 100 g) and green (502 mg (K) / 100 g) tea. The most tannins were found in extracts of black (98.3 mg catechin / 100 g) and green (224.9 mg catechin / 100 g) tea at a temperature of 40-50 °C. The lowest antiradical activity was found in extracts of black (Ec50 = 1.6 mg / cm3) and green (Ec50 = 4.0 mg / cm3) tea with an extraction temperature of 40-50 °C. The highest index of restorative power was in extracts of black (14.04 mmol Fe2+ / kg) tea with an extraction temperature equal to the boiling point of the solvent, and in green (12.15 mmol Fe2+ / kg) tea at a temperature of 40-50 (С.
Текст научной статьи Исследование технологии производства экстрактов чёрного и зелёного чая с антиоксидантной активностью: определение влияния температуры экстракции
This is an open access article distributed under the terms of the Creative Commons Attribution 4.0 International License
Карпова М.О. и др. Вестник ВГУИТ, 2021, Т. 83, №. 3, С. 74-81 Введение
Чай, традиционный напиток родом из Китая, является самым старым, самым популярным безалкогольным кофеинсодержащим напитком в мире. Его готовят путем варки обработанных листьев чайного растения Camellia sinensis . Чай является вторым, наиболее широко потребляемым напитком в мире после воды [1]. Он содержит до 30% растворимых веществ, которые могут варьироваться в зависимости от сорта, климатических условий, генетического штамма, региона производства, сезона сбора урожая, положения листа, а также операций обработки [2].
Экстракция – это метод отделения определенных компонентов от жидкости или смеси твердых веществ в другой растворитель или фазу. Этот метод применяется, например, для получения природных веществ из растительных материалов, таких как кора дерева, листья, стебли или даже цветы. Растущий спрос на натуральные продукты, наблюдаемый в фармацевтической, косметической и, что наиболее важно, пищевой промышленности, привел к быстрому росту интереса к нетрадиционным методам экстракции как средству повышения эффективности процесса [3]. Экстракция биологически активных веществ из лекарственных растений часто плохо контролируется и зависит от большого числа факторов, таких как температура экстракции, время экстракции, размер частиц сухого растения, а также количество и природа растения, введенного в экстракционный растворитель [4].
Подбор оптимальной температуры экстракции являлось целью работы [5]. На примере пяти образцов белого и зеленого чая из Китая и Малавии было изучено влияние температуры (70 и 90 ° С), а также размера листьев на антиоксидантную активность и сенсорные свойства чая. Пять образцов белого и зеленого чая из Китая и Африки, подвергались экстракции методом настаивания в горячей (70 °C и 90 °C; 7 мин) или холодной воде (комнатная температура: 15, 30, 60 или 120 мин) в виде целых листьев и в виде измельченных. Измерялись такие показатели, как содержание фенолов и флавоноидов, а также антиоксидантная способность (метод ABTS). Результаты показывают, что максимальная эффективность экстракции достигается в холодной воде в течение 120 мин из измельченных листьев.
В исследовании [6] было изучено влияние условий заваривания зеленого чая при 60 и 95 °С в течение 5–300 мин на антиоксидантную активность. Антиоксидантные свойства чайных настоек, которые оценивались по активности поглощения радикалов 2,2 –
В работе [7] определялись оптимальные условия экстрагирования турецкого зеленого чая на основе количества экстрагированных катехинов и сенсорных признаков. Настои зеленого чая изготавливали при 75, 85 и 95 ° С со временем 1; 2; 3; 5; 10; 20; 30 и 45 мин.
Был определен уровень количества эпиструктури-рованных катехинов, неэпиструктурированных катехинов и кофеина в образцах чая. Было установлено, что выход эпиструктурированных катехинов увеличивался в течение первых 3–5 мин варки при 85 °C. Увеличение времени варки приводило к снижению выхода эпиструкту-рированных катехинов, количество неструктурированных катехинов продолжало увеличиваться с увеличением времени экстракции.
Работа китайских учёных [8] была направлена на увеличение биологической активности чайных полифенолов. Для этого исследовали изменение чайных полифенолов с различным рН (3; 4; 5; 6 и 7) при различных температурах (4, 25 и 100 °C). Результаты показали, что чайные полифенолы с рН 3–6 оставались стабильными при 4 и 25 °С. Когда температура нагревания составляла 100 °С, наблюдалось значительное снижение содержания общих катехинов. Чайные полифенолы чувствительны к рН: чем ниже рН, тем стабильнее чайные полифенолы при хранении. Хранение при низких температурах и кислых условиях рН не оказало существенного влияния на характеристики полифенолов чая.
Целью работы [9] является определение влияния различных условий экстракции (температуры, концентрации этанола и соотношения образец / растворитель) на фенольный состав и антиоксидантную способность экстрактов стебля винограда. Исследовали влияние трех параметров процесса (каждый из которых варьируется на разных уровнях) на извлечение фенольных соединений из стеблей винограда. Этими параметрами были концентрация этанола (0; 25; 50; 75 и 100%, об. / об.), соотношение твердое вещество / растворитель (1:50 и 1:100, вес / объем) и температура экстракции (25 °C и 40 °C). Результаты показали, что концентрация этанола в экстракционном растворителе была фактором, который оказал наибольшее влияние на уровень извлечения различных биологически активных соединений. Наибольшее содержание общих фенольных соединений и наибольшая антиоксидантная активность экстрактов стебля винограда были получены с 50% этанолом и при 40 °С.
Таким образом, на основании данных проанализированных литературных источников, можно сделать вывод о решающем влиянии используемой температуры в процессе экстракции растительного сырья на выход антиоксидантных веществ.
Цель работы – подбор оптимальной температуры экстракции для двух видов чая ( Camellia sinensis ), для получения экстрактов с высокими значениями общего содержания фенолов, флавоноидов, антирадикальной активности по методу DPPH, восстанавливающей силы по методу FRAP и танинов.
Материалы и методы
Проводилось исследование на двух видах чая (Camellia sinensis) , для которых в качестве растворителя использовалась вода, т. к. по результатам исследований этот тип растворителя извлекает наибольшее количество антиоксидантных веществ и степенью измельчения 0.5 мм. Таким образом, на испытания было представлено по 3 образца экстрактов с температурой экстракции 40–50 °C, 20–25 °C, температурой кипения растворителя, в которых определяли показатели:
─ Общее содержание фенольных веществ;
─ содержание флавоноидов;
─ Содержание танинов;
─ Антирадикальную активность по методу DPPH;
─ Восстанавливающую силу по методу FRAP.
Получение сырья с необходимой степенью измельчения: чай измельчали в кофемолке, измельченное сырье просеивали через сито с размером 0.5 мм.
Получение экстракта с температурой 40–50 °C: 2 г исследуемого чая переносят в стеклянную колбу с притертой крышкой и заливают 20 мл растворителя (для каждого растворителя 3 колбы). Экстракция чая продолжается 2 ч в термостате при температуре 40–50 °C. Полученный экстракт центрифугируют 15 мин при скорости 5000 об./мин.
Получение экстракта с температурой 20–25 °C: 2 г исследуемого чая переносят в стеклянную колбу с притертой крышкой и заливают 20 мл растворителя (для каждого растворителя 3 колбы). Экстракция чая продолжается 2 ч при температуре 20–25 °C. Полученный экстракт центрифугируют 15 мин при скорости 5000 об./мин.
Получение экстракта с температурой кипения растворителя: 2 г исследуемого чая переносят в стеклянную колбу и заливают 20 мл растворителя (для каждого растворителя 3 колбы).
Экстракция чая продолжается 2 ч в обратном холодильнике при температуре кипения растворителя. Полученный экстракт центрифугируют 15 мин при скорости 5000 об./мин.
Определение общего содержания фенольных веществ в экстрактах чая проводилось на основе методики [10] с актуализацией для экстрактов чая. В экстракт чая на основе выбранного растворителя в количестве 0,25 см3 добавляют воду в количестве 4 см3, 0,25 см3 водного раствора реактива Фолина-Чокалтеу (в соотношении 1:1), 0,25 см3 раствора насыщенного карбоната натрия. Полученную смесь оставляют на 30 мин, оптическую плотность проб измеряют на спектрофотометре (КФК-3–01 «3ОМЗ») при длине волны 725 нм. По полученным значениям оптической плотности, используя калибровочную кривую, находят значения общего содержания фенольных веществ в мг галловой кислоты/100 г. исходного сырья. В качестве стандартного вещества для построения калибровочной кривой использована галловая кислота ХЧ (химически чистая).
Общее содержание флавоноидов в экстрактах чая исследуют фотометрическим методом. Измерения оптической плотности раствора на спектрофотометре проводят при длине световой волны 510 нм. Для обработки результатов измерений в качестве исходной методики была взята [11] с изменениями для экстрактов чая. В исследуемый экстракт чая объёмом 0,5 см3 добавляют 2,5 см3 дистиллированной воды, затем 0,15 см3 раствора нитрита натрия с концентрацией 5%, экспозиция 5 мин, прибавляют 0,3 см3 10%-го раствора хлорида алюминия, оставляют на 5 мин. Результаты общего содержания флавоноидов определяют по калибровочной кривой и выражают в мг катехина / 100 г. исходного сырья. В качестве стандартного вещества для построения калибровочной кривой использован катехин.
Определение общего содержания танинов проводилось на основе методики [12] приготовления реагента ванилина: навеску ванилина растворяли в 4%-ой соляной кислоте (0,5 г на 1 мл соответственно). Смешивают 1 мл экстракта чая и 5 мл раствора ванилина. Образцы и контроль (без ванилина) оставляют на 20 мин в темном месте, а затем измеряют оптическую плотность при длине волны 500 нм. Результаты общего содержания танинов определяют по калибровочной кривой и выражают в мг катехина/ 100 г. исходного сырья.
Определение антирадикальной активности по методу DPPH экстрактов чая в изучаемых растворителях проводилось с использованием раствора 2,2–дифенил-1-пикрилгидразила (DPPH)
в этаноле, имеющего насыщенную пурпурносинюю окраску. Методика [13] была взята за базу и доработана для экстрактов чая. Из экстрактов на основе каждого типа растворителя для каждого образца чая приготавливают растворы различной концентрации, из которых наливают в пробирку 0,2 см3, добавляют 2 см3 дистиллированной воды, 2 см3 раствора DPPH. Готовые растворы оставляют в затемненном месте на 30 мин. На спектрофотометре измеряется оптическая плотность полученных растворов при длине световой волны 517 нм. Определение антирадикальной активности по методу DPPH ведется по показателю Ес 50 , как концентрации экстракта чая, необходимой для поглощения 50% свободных радикалов DPPH.
В качестве исходной методики для определения восстанавливающей силы по методу FRAP используют метод [14] с модификацией для экстрактов чая. Смешивают в пробирке 0,1 см3 экстракта чая, 3 см3 дистиллированной воды, 1 см3 раствора реагента FRAP и выдерживают 4 мин в термостате при температуре 37 °C. Измерение оптической плотности полученного раствора измеряют на спектрофотометре при длине световой волны 593 нм. Результаты восстанавливающей силы по методу FRAP рассчитывают по калибровочному графику в ммоль Fе2+/1 кг исходного сырья. В качестве стандартного вещества для построения калибровочной кривой использован сульфат железа.
Результаты и обсуждения
Фенольные соединения обладают многими видами биологической активности, включая биохимические, такие как антимутагенные, антиоксидантные и антиканцерогенные, в дополнение к способности изменять экспрессию генов. Фенольные соединения широко распространены в растениях, которые в совокупности синтезируют несколько тысяч различных химических структур, характеризующихся гидроксилированным ароматическим кольцом (кольцами). Эти соединения играют несколько важных функций в растениях. Они представляют собой яркий пример метаболической пластичности, позволяющей растениям приспосабливаться к изменяющимся биотическим и абиотическим условиям, и дают растительным продуктам цвет, вкус, технологические свойства и предполагаемую пользу для здоровья [15].
Результаты испытаний определения общего содержания фенольных веществ в экстрактах двух видов чая (Camellia sinensis) , с различной температурой экстракции представлены на рисунке 1.
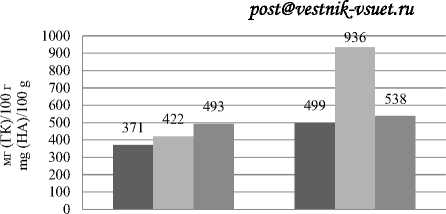
Чай чёрный Чай зелёный
Black tea Green tea
20-25°С 40-50°С t кип.
Рисунок 1. Результаты исследования общего содержания фенольных веществ в различных экстрактах чёрного и зелёного чая со степенью измельчения 0.5 мм и температурой экстракции 20–25 °C, 40–50 °C и температурой кипения растворителя Figure 1. Results of a study of the total content of phenolic substances in various extracts of black and green tea with a grinding degree of 0.5 mm and an extraction temperature of 20–25° C, 40–50° C and a boiling point of the solvent
Таким образом, максимальное количество фенольных веществ из чёрного чая экстрагируется при температуре экстракции равной температуре кипения растворителя, для зелёного при температуре - 40-50 ° С.
Флавоноиды, класс полифенольных соединений, которые в большом количестве содержатся в пищевых продуктах и напитках растительного происхождения, таких как фрукты, овощи, темный шоколад, чай и красное вино. Флавоноиды подразделяются на шесть основных подклассов в зависимости от их химической структуры: флавонолы, флаван-3-олы, флаваноны, флавоны, антоцианы и изофлавоны. Структурные различия приводят к различиям в метаболизме и биологической активности, что может привести к различным воздействиям на здоровье человека [16]. Флавоноиды проявляют широкий спектр положительных эффектов, таких как сильное антиоксидантное, противовоспалительное и антитромбоцитарное действие. Они могут способствовать профилактике хронических заболеваний, включая нарушения обмена веществ, диабет и сердечно-сосудистые заболевания, из-за их благотворного влияния на липиды крови, кровяное давление, уровень глюкозы в плазме, а также стабилизацию атетосклеротических бляшек. Кроме того, данные эпидемиологических исследований, исследований на животных подтверждают защитные эффекты пищевых продуктов и пищевых добавок, богатых флавоноидами, против некоторых видов рака, болезни Альцгеймера, болезни Паркинсона, некоторых вирусных инфекций, катаракты, эректильной дисфункции и воспалительных заболеваний кишечника [17].
Полученные результаты определения общего содержания флавоноидов в экстрактах чёрного и зелёного чая (Camellia sinensis) с тем- пературой экстракции 20–25 °C, 40–50 °C и температурой кипения растворителя представлены на рисунке 2.
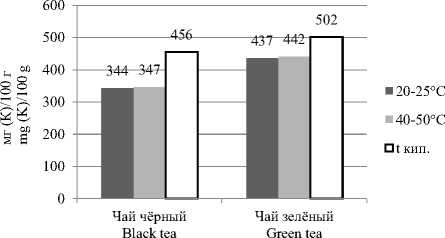
Рисунок 2. Результаты исследования общего содержания флавоноидов в различных экстрактах чёрного и зелёного чая со степенью измельчения 0.5 мм и температурой экстракции 20–25 °C, 40– 50 °C и температурой кипения растворителя
Figure 2. Results of a study of the total content of flavonoids in various extracts of black and green tea with a grinding degree of 0.5 mm and an extraction temperature of 20–25 °C, 40–50 °C and a boiling point of the solvent
Таким образом, при температуре экстракции равной температуре кипения растворителя, как из черного, так и из зелёного чая извлекается наибольшее количество флавоноидов.
Термин «танин» обозначает широкий класс соединений, которые могут быть далее классифицированы на гидролизуемые танины или более часто потребляемые конденсированные танины (также известные как проантоциани-дины). Способность танинов осаждать белки связана с вяжущей способностью, а содержание растительных танинов связано с устойчивостью растений к неблагоприятному влиянию насекомых, животных и плесени. Для продуктов богатых танинами, таких как вино и чай, наблюдается воздействие на организм человека и активизации защитных механизмов по борьбе с раком и сердечно-сосудистыми заболеваниями. Принимая во внимание как потенциальные вредные, так и полезные свойства танинов, существует дихотомия между ограничением потребления танинов лицами с риском развития ЖДА (желе-зодефициитная анемиия) и потенциальной пользой для здоровья, получаемой из богатых танинами диет. [18].
Результаты испытаний определения содержания танинов в экстрактах 2-x видов чая ( Camellia sinensis ) с различной температурой экстракции представлены на рисунке 3.
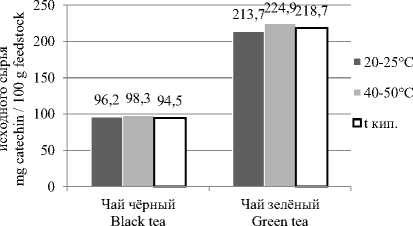
Рисунок 3. Результаты исследования содержания танинов в различных экстрактах чёрного и зелёного чая со степенью измельчения 0.5 мм и температурой экстракции 20–25 °C, 40–50 °C и температурой кипения растворителя
Figure 3. Results of studying the content of tannins in various extracts of black and green tea with a grinding degree of 0.5 mm and an extraction temperature of 20–25 °C, 40–50 °C and a boiling point of the solvent
Из экстрактов чёрного и зелёного чая при температуре экстракции 40-50 ° С извлекается наибольшее количество танинов.
Свободный радикал – это любая частица, обладающая способностью к независимому существованию, содержащая один или несколько неспаренных электронов, которые реагируют с другой молекулой, принимая или жертвуя электроны. Свободные радикалы в организме человека вызывают повышенный риск сердечнососудистых заболеваний, рака и других хронических заболеваний [19]. Свободные радикалы являются одной из причин, которые могут вызвать преждевременное старение и дегенеративные заболевания. Чтобы преодолеть эту проблему, организму необходим прием антиоксидантов [20].
Результаты исследования антирадикальной активности в экстрактах чёрного и зелёного чая ( Camellia sinensis ) с температурой экстракции 20–25 °C, 40–50 °C и температурой кипения растворителя представлены на рисунке 4.
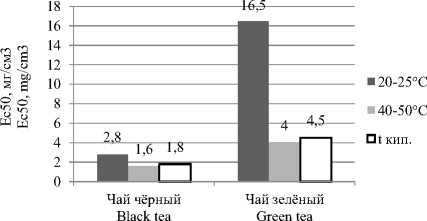
Рисунок 4. Результаты исследования антирадикальной активности по методу DPPH в различных экстрактах чёрного и зелёного чая со степенью измельчения 0.5 мм и температурой экстракции 20–25 °C, 40–50 °C и температурой кипения растворителя
Figure 4. Results of the study of antiradical activity by the DPPH method in various extracts of black and green tea with a grinding degree of 0.5 mm and an extraction temperature of 20–25° C, 40–50° C and a boiling point of the solvent
Для получения минимальных показателей по улавливанию свободного радикала 2,2 – дифенил-1-пикрилгидразила у экстрактов чёрного и зелёного чая лучше всего подойдет температура экстракции 40–50 °C.
Окислительно-восстановительное состояние основных переходных металлов, таких как Fe (II / III), делает их биологически важными, а также токсичными в процессе окислительного стресса. Железо (Fe) в организме здорового человека присутствует в основном в гемоглобине. Оно служит важным кофактором для множества ферментов, сигнальных молекул и регулирует различные биологические пути, включая выработку митохондриальной энергии, репликацию / транскрипцию ДНК и синтез нейротрансмиттеров. В присутствии перекиси водорода эти ионы железа генерируют токсичные гидроксильные радикалы посредством реакций Фентона. Редокс-активное железо (Fe) индуцирует как повреждение генома, так и ингибирует ключевые ферменты в механизмах окислительного повреждения генома, изменяя их структуру и обратимо окисляя остатки цистеина в этих белках. Для борьбы с окислительным стрессом и окислительноопосредованным повреждением человеческая система имеет эндогенные антиоксиданты (молекулы, способные стабилизировать или деактивировать свободные радикалы до того, как они атакуют клетки), которые играют решающую роль в поддержании оптимальных клеточных функций, системного здоровья и благополучия [21]. Одним из методов оценки способности к окислительно-восстановительным процессам является определение восстанавливающей силы для антиоксидантов.
Результаты испытаний определения значения восстанавливающей силы в экстрактах двух видов чая ( Camellia sinensis ) с различной температурой экстракции представлены на рисунке 5.
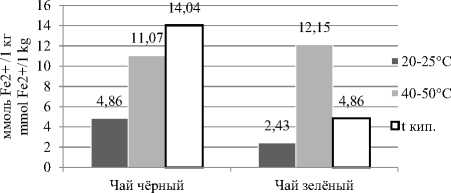
Black tea Green tea
Рисунок 5. Результаты исследования восстанавливающей силы по методу FRAP в различных экстрактах чёрного и зелёного чая со степенью измельчения 0.5 мм и температурой экстракции 20–25 °C, 40–50 °C и температурой кипения растворителя
Figure 5. Results of the study of the restoring force by the FRAP method in various extracts of black and green tea with a grinding degree of 0.5 mm and an extraction temperature of 20–25° C, 40–50° C and a boiling point of the solvent
Для увеличения показателя восстанавливающей силы для чёрного чая наиболее оптимально использовать в качестве температуры экстракции – температуру кипения растворителя, а для зелёного чая – 40–50 ° C.
Заключение
В результате проведения исследования технологических параметров производства экстрактов чёрного и зелёного чая на основе воды и степенью измельчения 0.5 мм, отличающихся температурой экстракции были получены следующие результаты:
-
• большее количетво фенолов экстрагируется из экстрактов черного чая с температурой равной температуре кипения растворителя, зелёный чай показывает высокие значения содержания фенолов при температуре экстракции 40-50 ° С;
-
• высокие значения общего содержания флавоноидов наблюдались при температуре равной температуре кипения растворителя как у черного, так и у зеленого чая;
-
• танинов больше всего содержалось в экстрактах черного и зеленого чая при температуре экстракции 40-50 ° С;
-
• наименьшая антирадикальная активность была обнаружена в экстрактах черного и зеленого чая с температурой экстракции 40-50 ° С.
-
• наибольший показатель восстанавливающей силы был у экстрактов черного чая с температурой экстракции равной температуре кипения растворителя, а у зеленого чая при температуре 40-50 ° С.
В ходе исследования было обнаружено, что температура экстракции является важным фактором, влияющим на степень извлечения антиоксидантных веществ из водных экстрактов чёрного и зелёного чая. Таким образом, с точки зрения экономии материальных ресурсов, повышения качества и свойств экстрактов чая температура экстракции 40–50 °C для чёрного и зелёного чая будет являться оптимальной.
Работа выполнена в рамках государственного задания на фундаментальные исследования Самарского государственного технического университета № 0778–2020–000.
Список литературы Исследование технологии производства экстрактов чёрного и зелёного чая с антиоксидантной активностью: определение влияния температуры экстракции
- Soni R.P., Katoch M., Kumar A., Ladohiya R. et al. Tea: production, composition, consumption and its potentialan antioxidant and antimicrobial agent // Intl. J. Food. Ferment. Technol. 2015. V. 5. P. 95-106. https://doi.org/10.5958/2277-9396.2016.00002.7
- Tong T., Liu Y., Kang J., Zhang C. et al. Antioxidant activity and main chemical components of a novel fermented tea // Molecules. 2019. V. 24. P. 1-14. https://doi.org/10.3390/molecules24162917
- Zaguła G., Bajcar M., Puchalski C., Kapusta I. et al. Comparison of the Effectiveness of water-based extraction of substances from dry tea leaves with the use of magnetic field assisted extraction techniques // Molecules. 2017. V. 22. P.1-12. https://doi.org/10.3390/molecules22101656
- Ngoc P.C., Leclercq L., Rossi J., Desvignes I. et al. Optimizing water-based extraction of bioactive principles of hawthorn: from experimental laboratory research to homemade preparations // Molecules. 2019. V. 24. P. 1-32. https://doi.org/10.3390/molecules24234420
- Castiglioni S., Damiani E., Astolfi P., Carloni P. Influence of steeping conditions (time, temperature, and particle size) on antioxidant properties and sensory attributes of some white and green teas // Int. J. Food Sci. Nutr. 2015. V. 66. P. 491-497. https://doi.org/10.3109/09637486.2015.1042842
- Jin Y., Zhao J., Kim E.M., Kim K.H. et al. Comprehensive investigation of the effects of brewing conditions in sample preparation of green tea infusions // Molecules. 2019. V. 24. P. 1-12. https://doi.org/10.3390/molecules24091735
- Saklar S., Ertas E., Ozdemir I.S., Karadeniz B. Effects of different brewing conditions on catechin content and sensory acceptance in Turkish green tea infusions // J. Food Sci. Technol. 2015. V. 52. P. 6639-6646. https://doi.org/10.1007/s13197-015-1746y
- Zeng L., Ma M., Li C., Luo L. Stability of tea polyphenols solution with different pH at different temperatures // Int. J. Food Prop. 2017. V. 20. P. 1-18. https://doi.org/10.1080/10942912.2014.983605
- Jiménez-Moreno N., Volpe F., Moler J.A., Esparza I. et al. Impact of extraction conditions on the phenolic composition and antioxidant capacity of grape stem extracts // Antioxidants. 2019. V. 8. P. 1-17. https://doi.org/10.3390/antiox8120597
- Molina Cortés A., Sánchez Motta T., Tobar Tosse F., Quimbaya M. Spectrophotometric estimation of total phenolic content and antioxidant capacity of molasses and vinasses generated from the sugarcane industry // Waste and Biomass Valorization. 2019. V. 1. P. 1-11. https://doi.org/10.1007/s12649-019-00690-1
- Silva L., Pezzini B.R., Soares L. Spectrophotometric determination of the total flavonoid content in Ocimum basilicum L. (Lamiaceae) leaves // Pharmacogn Mag. 2015. V. 11. P. 96-101. https://doi.org/10.4103/0973-1296.149721.
- Rebaya A., Belghith S.I., Baghdikian B., Leddet V.M. Phenolic, total flavonoid, tannin content, and antioxidant capacity of Halimium halimifolium (Cistaceae) // J. App. Pharm. Sci. 2015. V. 5. P. 52-57. https://doi.org/10.7324/JAPS.2015.50110
- Johari M.A., Khong H.Y. Total phenolic content and antioxidant and antibacterial activities of Pereskia bleo // Adv. Pharmacol. Sci. 2019. V. 2019. P. 1-4. https://doi.org/10.1155 / 2019/7428593
- Rubio C.P., Hernández-Ruiz J., Martinez-Subiela S., Tvarijonaviciute A. et al. Spectrophotometric assays for total antioxidant capacity (TAC) in dog serum: an update // BMC Vet Res. 2016. V. 12. P. 1-7. https://doi.org/10.1186/s12917-016-0792-7
- Augšpole I., Dūma M., Cinkmanis I, Ozola B. Herbal teas as a rich source of phenolic compounds // Chemija. 2018. V. 29. P. 257-262. https://doi.org/10.6001/chemija.v29i4.3841
- Bondonno N.P., Dalgaard F., Kyrø C., Murray K. Flavonoid intake is associated with lower mortality in the danish diet cancer and health cohort // Nature communications. 2019. V. 10. P. 1-10. https://doi.org/10.1038/s41467-019-11622x
- Kozłowska A., Szostak-Węgierek D. Flavonoids - food sources, health benefits, and mechanisms involved // Bioactive Molecules Food. 2017. V. 68. P. 79-85. https://doi.org/10.1007 / 978-3-319-54528-8_54-1
- Delimont N.M., Haub M.D., Lindshield B.L. The impact of tannin consumption on iron bioavailability and status: a narrative review // Current Developments Nutrition. 2017. V. 1. P. 1-12. https://doi.org/10.3945/cdn.116.000042
- Kiliç C., Can Z., Yilmaz A., Yildiz S. et al. Antioxidant properties of some herbal teas (green tea, senna, corn silk, rosemary) brewed at different temperatures // Int. J. Sec. Metabolite. 2017. V. 4. P. 142-148. https://doi.org/10.21448/ijsm.369273
- Indarti K., Apriani E.F., Wibowo A.E., Simanjuntak P. Antioxidant activity of ethanolic extract and various fractions from green tea (Camellia sinensis L.) leaves // Pharmacognosy J. 2019. V. 11. P. 771-776. https://doi.org/10.5530/pj.2019.11.122
- Moukette B.M., Pieme A.C., Biapa P.C.N. In vitro ion chelating, antioxidative mechanism of extracts from fruits and barks of tetrapleura tetraptera and their protective effects against fenton mediated toxicity of metal ions on liver homogenates // Evid. Based Complement. Alternat. Med. 2015. V. 2015. P. 1-14. https://doi.org/10.1155/2015/423689


