Исследование тканевой активности металлопротеиназ при гетерогенных формах аденомиоза
Автор: Леваков Сергей Александрович, Коробейников Алексей Петрович, Демура Т.А.
Журнал: Клиническая практика @clinpractice
Рубрика: Оригинальные исследования
Статья в выпуске: 3 (3), 2010 года.
Бесплатный доступ
Изучали ферментативную активность матриксных металлопротеиназ (ММР) 2 и 9 в операционном материале (ампутированные матки) по поводу диффузной и узловой формах аденомиоза у женщин в позднем репродуктивном периоде. Исследование проводили с использованием иммуногистохимического метода на парафиновых срезах. Результаты иммуногистохимической реакции оценивали полуколичественным методом в баллах по числу позитивно окрашенных клеток. Показано усиление активации и экспрессии желатиназ ММР2 и ММР9 при диффузной и узловой формах аденомиоза и различных степенях поражения миометрия. Также установлено, что при диффузной и узловой формах аденомиоза в строме и миометрии экспрессия желатиназы ММР9 была интенсивнее.
Матриксные металлопротеиназы, желатиназы, аденомиоз, миома матки, эндометрий
Короткий адрес: https://sciup.org/14338335
IDR: 14338335
Research of tissue activity of metalloproteinases at various forms of an adenomyosis
Enzymatic activity matrix metalloproteinase's 2 and 9 in an operational material (the amputated uteruses) concerning diffusive and nodal forms of an adenomyosis at women in the late genesial period was studied. Research was spent with use of an immunohistochemical method on paraffinic sections. Results of immunohistochemical reaction were estimated by a semiquantitative method in points by quantity of positively painted cells. Activation and expression intensifying gelatinase ММР2 and ММР9 has been shown at diffusive and nodal forms of an adenomyosis and their various degrees of a lesion of a myometrium. Also it has been shown, that in a stroma and myometriums at diffusive and nodal forms of an adenomyosis the expression gelatinanases ММР9 was more intensively.
Текст научной статьи Исследование тканевой активности металлопротеиназ при гетерогенных формах аденомиоза
Среди значительных достижений нашего времени особое место занимает открытие универсальной роли процессов протеолиза в регуляции различных сторон жизнедеятельности организма. Протеолитические ферменты являются одним из механизмов контроля функций органов и тканей. Эти ферменты имеют регуляторное значение для молекулярных механизмов тонких биологических процессов, таких как деление клеток, дифференцировка и морфогенез.
Семейство матриксных металлопротеиназ – это группа родственных по структуре цинк-содержащих эндопептидаз, разрушающих базальные мембраны и внеклеточ- ный матрикс при физиологических и патологических условиях [1].
В гинекологической практике одним из наиболее часто встречающихся заболеваний, связанных с перестройкой соединительной ткани, является эндометриоз [2]. Эктопический рост эндометрия при эндометриозе представляет собой инвазивное событие, при котором происходит деградация базальных мембран и экстрацеллюлярного матрикса. Роль желатиназ в патофизиологии эндометриоза еще недостаточно изучена. Некоторыми исследованиями установлено их участие в прогрессировании этого заболевания [3, 4].
Раннее показано, что экспрессия ММП-2 в эктопических тканях эндометрия значительно повышается по сравнению с нормальными тканями.
Форма генитального эндометриоза, когда гетеротопии эндометриоидной ткани обнаруживаются в миометрии, называется аденомиозом [5].
Аденомиоз представляет одну из наиболее острых проблем современной гинекологии, занимая третье место после воспалительных процессов и миомы матки. Отмечается рост этого заболевания в структуре гинекологической патологии [6].
Макроскопически аденомиоз проявляется увеличением тела матки и гиперплазией эндометрия. В зоне эндометриоза возможно также образование кистозных полостей с геморрагическим содержимым или формирование узловых элементов с преобладанием стромальной эндометриоидной ткани. Наиболее распространенными видами аденомиоза на данный момент являются диффузный и узловой.
На основании имеющихся сведений можно полагать, что в развитии и прогрессировании аденомиоза определенную роль играет измененная в силу различных обстоятельств протеолитическая активность тканей. Все изложенные факты позволили нам предположить, что при аденомиозе также возможно изменение тканевой активности матриксных металлопротеиназ (ММР-2 и ММР-9) [7].
Целью исследования явилось изучение тканевой активности матриксных металлопротеиназ (ММР-2 и ММР-9) при различных формах аденомиоза.
Материалы и методы
Исследование выполнено на операционном материале (ампутированные матки), полученном от 45 пациенток позднего репродуктивного возраста с верифицированным диагнозом диффузной и узловой форм аденомиоза. Средний возраст пациенток – 45,5 ± 3,3 года.
Контрольную группу составили 18 наблюдений – женщин позднего репродуктивного возраста (средний возраст – 43,5 ± 3,3
года) с миомой матки. Исследован операционный материал – удаленные матки. Во всех наблюдениях оценивали ферментативную активность ММР-2 и ММР-9, активность равнялась 0,35 и 1,05 соответственно.
Иммуногистохимическое исследование (ИГХ) выполнено на операционном материале от пациенток с аденомиозом, отобранном по результатам изучения морфологии. В исследование включены 20 пациенток преимущественно с узловой формой аденомиоза высокой степени активности и 25 больных – с диффузной формой аденомиоза.
В настоящей работе из всего многообразия ММР объектом для исследования выбраны ММР-9 и ММР-2. Это связанно с тем, что желатиназа ММР-9 имеет наибольшую протеолитическую активность в отношении разных типов коллагена (включая коллаген IV типа, ламинин и эластин), а также компонентов базальных мембран [8].
Послеоперационный материал окрашивался для иммуногистохимического метода.
Демаскировку антигенов для ИГХ проводили в микроволновой печи. Стекла погружали в цитратный буфер (рН 6,0) и нагревали в микроволновой печи в течение 15 мин при мощности 600 Вт.
После этого стекла остывали 20 мин при комнатной температуре. Остывшие стекла перемещали во влажные камеры (для предотвращения высыхания срезов) и инкубировали 15 мин с 3% раствором Н2О2. После обработки перекисью стекла ополаскивали в фосфатном буфере (рН 7,0-7,6). Далее стекла инкубировали с 1% раствором альбумина во влажных камерах в течение 30 мин. По окончании инкубации излишки альбумина аккуратно стряхивали со стекол и раскапывали первичные антитела. В качестве первичных антител использовали моноклональные антитела к ММП-2 и ММП-9 (Lab Vision, Ready-to-use 7 ml). Срезы инкубировали с первичными антителами 30 мин. Затем стекла отмывали в фосфатном буфере (рН 7,0-7,6) от первичных антител, не связавшихся с эпитопами, и обрабатывали вторичными антителами
(Ultra V HRP polymer KIT Lab Vision). Для визуализации места связывания антигена с антителом использовали метку – пероксидазу хрена в присутствии субстрата пероксида водорода и колориметрического реактива с 3,3-диаминобензидином (DAB sub-strate+chromogen Lab Vision). В результате образовывался нерастворимый в органических растворителях конечный продукт реакции, который обнаруживался в виде коричневого окрашивания. Для облегчения определения локализации антигенов в тканях проводили доокраску ядер гематоксилином. Ставили положительные контрольные реакции на срезах от фирмы-производителя антитела с известным распределением маркера и отрицательные контрольные реакции – на срезах исследуемых тканей без специфических первичных антител.
Результаты иммуногистохимической реакции оценивали полуколичественным методом в баллах по количеству позитивно окрашенных клеток. Оценку интенсивности реакции для ММП-2 и ММП-9 проводили по 6-балльной системе: 2 балла – до 20% окрашенных клеток; 4 балла – от 20 до 40% окрашенных клеток; 6 баллов – более 40% окрашенных клеток.
Результаты исследования и их обсуждение
Результаты иммуногистохимических реакций показали, что активность экспрессии ММР-2 в биоптатах миометрия в наблюдениях с диффузной формой аденомиоза достоверно отличалась (р < 0,03) от активности в эпителии (3,5 балла) и строме (2,4 балла). Активность ММР-2 при узловой форме была оценена в 3,1 балла в эпителии и 2,3 балла в строме. Аналогичная активность ММР-2 наблюдалась в эндотелии (4,1 балла) и в миометрии 1,1 балл, против 4,4 баллов в эндотелии и 1,3 баллов в миометриии (рис.1).
Активность экспрессии ММР-9 в эндотелии, в эпителии, в миометрии была выражена как при диффузной (в разной степени), так и при узловой формах во всех наблюдениях; средний балл составил 5,2, достовер-
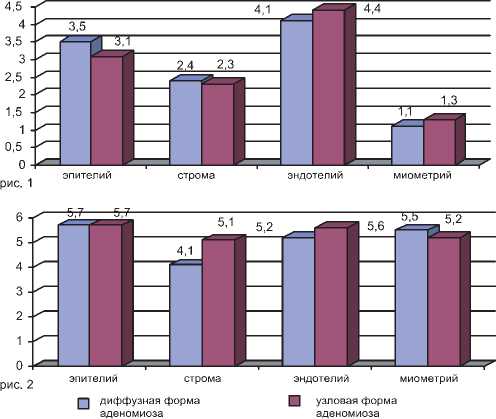
Рис. 1. Активность экспрессии ММР-2 в тканях матки при аденомиозе
Рис. 2. Активность экспрессии ММР-9 в тканях матки при аденомиозе ных различий не отмечено (р > 0,05). Уровень экспрессии ММР-9 был выше в строме биоптатов с узловым аденомиозом (5,1 ± 0,5 баллов), чем при диффузной форме (4,1 ± 0,7 баллов) и достоверно различались между собой (р < 0,02) (рис. 2).
Проведенное иммуногистохимическое исследование активности экспрессии протеолитических ферментов в тканях матки при различных формах и степенях аденомиоза свидетельствует о том, что ММР-2 и ММР-9 активно участвуют в патогенезе как при диффузных, так и узловых формах аденомиоза. Однако активность экспрессии ММР-9 была выше (р < 0,02) и в стромальном компоненте, и в миометрии при диффузной и узловой формах аденомиоза (табл. 1).
Заключение
По результатам проведенного иммуногистохимического исследования тканей матки можно сделать выводы, что усиление активности металлопротеиназ (ММР-2 и ММР-9) в тканях коррелирует с усилением патологической трансформации стромального компонента и миометрия.
Активация экспрессии желатиназ (ММР-2 и ММР-9) при диффузной и узловой формах аденомиоза и их различных степенях поражения миометрия достоверно не различались (р < 0,05). Следует
Тканевая активность матриксных металлопротеиназ в матке при различных формах аденомиоза в баллах, M±m
Таблица 1
|
Группы |
Эпителий |
Строма |
Эндотелий |
Миометрий |
||||
|
ММР-2 |
ММР-9 |
ММР-2 |
ММР-9 |
ММР-2 |
ММР-9 |
ММР-2 |
ММР-9 |
|
|
Диффузная форма аденомиоза (n=25) |
3,5 |
5,7 |
2,4 |
4,0 |
4,1 |
5,2 |
1,1 |
5,5 |
|
Узловая форма аденомиоза (n=20) |
3,1 |
5,7 |
2,7 |
5,1 |
4,4 |
5,6 |
1,3 |
5,2 |
|
Контрольная группа (n=18) |
0,35 |
1,05 |
0,35 |
1,05 |
0,35 |
1,05 |
– |
– |
отметить, что в строме и миометрии при диффузной и узловой формах аденомиоза экспрессия желатиназы ММР-9 была более выраженной и достоверно отличалась от экспрессии ММР-2: 5 и 2 балла соответственно (р < 0,02).
Таким образом, отработка кривой алгоритма активации экспрессии ММР-9 в биоптатах миометрия при различных формах аденомиоза может служить ранним маркером трансформации стромы и миометрия при аденомиозе.
Список литературы Исследование тканевой активности металлопротеиназ при гетерогенных формах аденомиоза
- Newby AC. Studying mechanisms underlying shedding of endothelial membrane proteins could help patients at risk for myocardial infarction//Cardiovasc Res. 2005 Jul 1;67(1):45.
- Баскаков В.П., Цвелев Ю.В. Кира Е.Ф. Эндометриоидная болезнь. СПб: ООО "Издательство НЛ", 2002. С 136-141.
- Борзенкова И.П. Экспрессия матриксных металлопротеиназ в эндометрии при генитальном эндометриозе//XXX Юбилейная итоговая конф. молодых учёных. 2008. С. 50-52.
- Стрижов Н.В., Сухих Г.Т., Соболева Г.М. и соавт. Сравнение сывороточной активности матриксной металлопротеиназы у больных с железистой и железистокистозной гиперплазиями эндометрия в перименопаузе//Проблемы репродукции. Спец. выпуск. 2008. С. 312-13.
- Адамян Л.В., Кулаков В.И. Эндометриозы. Руководство для врачей. М: Медицина, 1998. 380 с.
- Бурлев В.А., Лец Н.И. Роль брюшины в патогенезе наружного генитального эндометриоза: обзор литературы//Проблемы репродукции. 2000. № 1. С. 25-29.
- Волощук И.Н., Ромаданова Ю.А., Ищенко А.И., Бахвалова А.А. Молекулярнобиологические аспекты патогенеза аденомиоза//Архив патологии. 2007. № 3. С. 56-60.
- Newby AC. Matrix metalloproteinases regulate migration, proliferation, and death of vascular smooth muscle cells by degrading matrix and nonmatrix substrates//Cardiovasc Res. 2006 Feb 15;69(3):614-24.


