Исследование влияния новых производных 3-гидроксипиридина и препаратов сравнения на выживаемость и некоторые биохимические показатели крови белых крыс при экспериментальном диабете
Автор: Уланова Татьяна Вячеславовна, Инчина Вера Ивановна, Русейкин Николай Сергеевич, Худойкина Светлана Вячеславовна, Романова Элла Викторовна
Журнал: Инженерные технологии и системы @vestnik-mrsu
Рубрика: Медицинские науки
Статья в выпуске: 2, 2016 года.
Бесплатный доступ
Введение. В связи с высоким риском развития серьезных осложнений, приводящих к ранней инвалидизации и преждевременной смерти, а также высокой стоимостью лечения и реабилитации больных, сахарный диабет (СД) в недалеком будущем может стать главной медико-социальной проблемой во всех странах мира. Смертность больных СД в несколько раз выше смертности в общей популяции. Стоимость лекарственного обеспечения больного с СД 1 типа составляет в среднем 715 долл., а 2 типа - около 200 долл. в год. Лечение пациента с тяжелыми осложнениями, с учетом лекарственного обеспечения и стоимости амбулаторной и стационарной помощи, обходится в 1,5 млн долл. в год. Применяемые в настоящее время лекарственные препараты не решают проблему, поэтому актуален поиск новых лекарственных соединений. Материалы и методы. В статье рассматриваются возможности лечения сахарного диабета и его осложнений препаратами метаболического типа на экспериментальной модели аллоксанового диабета с экзогенной гиперхолестеринемией. Исследуемые соединения фумарат 3-гидроксипиридина и никотинат 3-гидрок-сипиридина синтезированы на кафедре органической химии ФГБОУ ВО «МГУ им. Н. П. Огарёва» доцентом Семеновым А. В. Результаты исследования. В результате проведенного исследования была выявлена гипогликемическая и гиполипидемическая активность фумарата 3-гидроксипи-ридина и никотината 3-гидроксипиридина. Обсуждение и заключения. Полученные нами данные свидетельствуют о дальнейшем перспективном изучении новых соединений из группы 3-гидроксипиридина в качестве корректоров метаболических нарушений при СД.
Диабет, фумарат, никотинат, метаболическая активность, гипер-холестеринемия
Короткий адрес: https://sciup.org/14720206
IDR: 14720206 | УДК: 615.27:612.12:599.323.45 | DOI: 10.15507/0236-2910.026.201602.180-191
Investigation of the effect of new derivatives of 3-hydroxypyridine and reference drugs on the survival and some biochemical parameters of blood of white rats with experimental diabetes
Introduction. Due to the high risk of serious complications leading to early disability and premature death, and the high cost of treatment and rehabilitation of patients with diabetes in the near future may become a major health and social problem worldwide mortality of diabetic patients is several times higher mortality rate in the total cost of drug supply a patient with diabetes of the first type is an average of $ 715, and the second type - about $ 200 a year. Treatment of patients with severe complications, taking into account drug supply and cost of outpatient and inpatient care costs of 1,500 thousands dollars per year. Currently used drugs do not solve the problem, so a search of new drug compounds is relevant. Materials and Methods. The possibility of the treatment of diabetes and its complications such as metabolic drugs in an experimental model of alloxan diabetes with exogenous hypercholesterolemia. Test compounds fumarate 3-hydroxypyridine and 3-hydroxypyridine nicotinate were synthesized at the Organic Chemistry Chair Mordovia State University by associate professor Semenov A.V. Results. The study was revealed hypoglycemic and lipid-lowering activity of fumarate of 3-hydroxypyridine and nicotinate 3-hydroxypyridine. Discussion and Conclusions. Our data indicate a further study of new promising compounds from the group of 3-hydroxypyridine as correctors metabolic disorders diabetes.
Текст научной статьи Исследование влияния новых производных 3-гидроксипиридина и препаратов сравнения на выживаемость и некоторые биохимические показатели крови белых крыс при экспериментальном диабете
Сахарный диабет (СД) 2 типа является самой распространенной эндокринной патологией. Несмотря на про-тиводиабетическую терапию, ежегодно увеличивается число лиц, имеющих осложнения. Применяемые в настоящее время лекарственные препараты не решают данную проблему, поэтому актуален поиск новых противодиабетических соединений.
Обзор литературы
По определению экспертов ВОЗ, «сахарный диабет – проблема всех возрастов и народов» [1]. Распространенность СД среди населения различных стран колеблется от 2 до 6 %. В Российской Федерации на официальном учете Medical sciences состоит около 8 млн больных диабетом. В 2000 г. в мире насчитывалось 175 млн больных СД, в 2010 г. – уже 239,3 млн, или 3 % населения Земли.
Смертность больных СД в несколько раз выше смертности в общей популяции [2–4]. В большинстве случаев причиной смерти больных СД являются ангиопатии, а именно кардиоваскулярные и цереброваскулярные расстройства [5]. Повышенным АД страдают до 80 % больных СД [6–8]. У лиц, имеющих другой отягощающий фактор СД – артериальную гипертензию, значительно снижается качество жизни (и на 1/3 – продолжительность), повышается риск преждевременной смерти [9]. Также среди больных СД в 2–4 раза выше риск развития ишемической болезни сердца; в 6–10 раз – острого инфаркта миокарда (ИМ); 4–7 раз – мозговых инсультов [10–11].
Стоимость лекарственного обеспечения больного с СД 1 типа составляет в среднем 715 долл., а 2 типа – около 200 долл. в год. Лечение пациента с тяжелыми осложнениями, с учетом лекарственного обеспечения и стоимости амбулаторной и стационарной помощи, обходится в 1,5 млн долл. в год. В связи с высоким риском развития серьезных осложнений, приводящих к ранней инвалидизации и преждевременной смерти, а также высокой стоимостью лечения и реабилитации больных, СД в недалеком будущем может стать главной медико-социальной проблемой во всех странах мира [12].
Значимым фактором, участвующим в формировании осложнений при СД, являются нарушения липидного обмена – дислипидемии [13].
В свою очередь гиперхолестеринемия (в сочетании с гипергликемией) способствует повышению уровня окислительного стресса при снижении активности антиоксидантной защиты. Возникающий при СД окислительный стресс способствует нарушению эндотелиальной функции сосудов, приводя к ухудшению их релаксации и тканевой перфузии, развитию гипоксии. Таким образом, метаболические нарушения и активация перекисного окисления липидов и обуславливают развитие диабетических осложнений (нефропатий, ретинопатий, нейропатий и др.) [14].
Учитывая важную роль активации перекисного окисления липидов в патогенезе СД и его осложнений, важным компонентом комбинированной терапии данной патологии являются препараты с антиоксидантной активностью. В ходе ряда клинических исследований был установлен положительный эффект препаратов такого типа действия, в частности производных 3-гидроксипиридина (3-ГП) – мексидола и эмоксипина [5; 15–19].
Фармакологические эффекты новых соединений из группы 3-ГП (фумарата 3-ГП и никотината 3-ГП) изучены недостаточно, что и послужило стимулом для проведения данного исследования.
Материалы и методы
С целью моделирования экспериментального диабета белым нелинейным крысам вводили однократно внутрибрюшинно аллоксан в дозе 135 мг/кг. Аллоксановый диабет отягощали ежедневным введением холестерина в дозе 40 мг/кг и витамина D в дозе 7 500 ЕД/кг per os в течение 14 дней. Летальность при моделировании аллоксанового диабета с экзогенной гиперхолестеринемией составила 38 %. Спустя 14 дней после введения аллоксана, с ежедневным отягощением экзогенным холестерина и эргокальциферорола, подопытные животные были разделены на 10 групп по 5–6 крыс в каждой. Первую группу составили интактные крысы; 2-я являлась контрольной (крысы с моделированным диабетом и гиперхолестеринемией, которым перорально в течение 14 дней вводили 0,9 % раствор NaCl в дозе 0,1 мл); крысы 3-й группы получали первое исследуемое соединение (фумарат 3-ГП) в дозе 25 мг/кг per os (5 % от ЛД50 ); крысам 4-й группы вводили фумарат 3-ГП в дозе 50 мг/кг per os (10 % от ЛД50 ); крысы 5-й группы получали первый препарат сравнения (мексидол) в дозе 25 мг/кг в/м; 6-й – мексидол в большей дозе (50 мг/кг) в/м; 7-й – второе исследуемое соединение (никотинат 3-ГП) в дозе 50 мг/кг per os; 8-й – второй препарат сравнения (симвастатин) в дозе 1 мг/кг per os; 9-й – никотинат 3-ГП в дозе 50 мг/кг per os в комбинации с симвастатином в дозе 1 мг/кг per os; 10-й – третий препарат сравнения (никотиновую кислоту) в дозе 25 мг/кг per os.
Исследуемые соединения фумарат 3-ГП и никотинат 3-ГП были синтезированы на кафедре органической химии ФГБОУ ВО «МГУ им. Н. П. Огарёва» доцентом А. В. Семеновым. Препараты сравнения были приобретены в аптечной сети.
Все манипуляции с использованием лабораторных животных проводились с соблюдением «Правил проведения работ с использованием экспериментальных животных».
Содержание глюкозы в сыворотке крови белых крыс определялось глю-козоксидазным методом с помощью стандартных наборов реактивов. Исследование показателей липидного обмена проводилось на электронном фотоэлектроколориметре ERMA, также с использованием стандартных наборов реактивов.
Результаты исследования
Летальность лабораторных животных в группах существенно отличалась: в контрольной группе она составила 40 %; в группе, получавшей никотиновую кислоту, – 50 %; в группе, получавшей симвастатин, – 20 %; в группах, получавших никотинат 3-ГП, никотинат 3-ГП + симвастатин,
MORDOVIA UNIVERSITY BULLETIN фумарат3-ГП, мексидол, и среди интактных животных – 0 %.
Моделирование экспериментального диабета введением аллоксана, экзогенного холестерина и витамина D сопровождалось достоверным повышением уровня глюкозы: 4,33 ± 0,42 ммоль/л – у интактных крыс и 17,9 ± 2,19 ммоль/л – в группе контроля. Достоверное снижение уровня глюкозы в сыворотке крови наблюдалось в нескольких группах: в группе крыс, получавших фумарат 3-ГП в дозе 50 мг/кг per os, уровень глюкозы составил 8,4 ± 0,4 ммоль/л; в группе получавших комбинацию симвастатин + никотинат 3-ГП – 9,04 ± 2,11 ммоль/л; в группе получавших никотинат 3-ГП – 10,36 ± 1,31 ммоль/л; в группах получавших никотиновую кислоту, симвастатин и мексидол, наблюдалось снижение уровня глюкозы, однако изменения носили недостоверный характер (рис. 1)
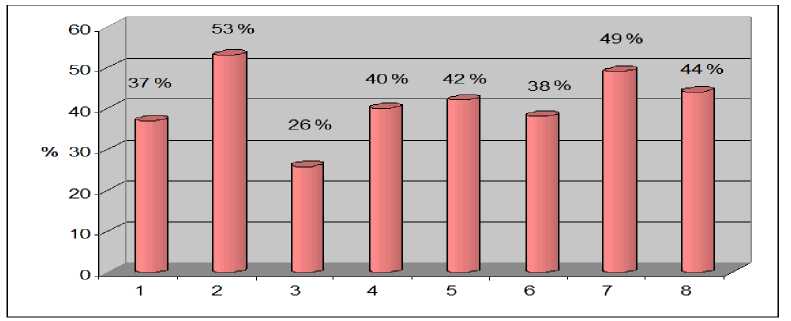
1 – Фумарат 3-ГП 25 мг/кг per os / Fumarate 3-HP 25 mg/kg per os
2 – Фумарат 3-ГП 50 мг/кг per os / Fumarate 3-HP 50 mg/kg per os
3 – Мексидол 25 мг/кг в/м / Mexidol 25 mg/kg intramuscularly
4 – Мексидол 50 мг/кг в/м / Mexidol 50 mg/kg intramuscularly
5 – Никотинат 3-ГП 50 мг/кг per os / Nicotinate 3-HP 50 mg/kg per os
6 – Симвастатин 1 мг/кг per os / Simvastatin 1 mg/kg per os
7 – Никотинат 3-ГП 50 мг/кг per os + симвастатин 1 мг/кг per os / Nicotinate 3-HP 50 mg/kg per os + simvastatin 1 mg/kg per os
8 – Никотиновая кислота 50 мг/кг per os / Nicotinic acid 50 mg/kg per os
Р и с. 1. Уровень снижения гликемии исследуемыми соединениями и препаратами сравнения по отношению к контрольной группе животных
F i g. 1. Lowering blood glucose level test compounds and reference drug in relation to the control group
На фоне формирования аллоксанового диабета с экзогенной гиперхолестеринемией + витамин D наблюдался устойчивый рост уровня ОХ сыворотки крови животных из группы контроля. Рост составил 148 % по отношению к интактным крысам. Наибольшее достоверное снижение уровня ОХ наблю-
Том 26, № 2. 2016 далось на фоне монотерапии никотинатом 3-ГП и на фоне введения комбинации симвастатина и никотината 3-ГП (на 38 и 30 % соответственно), причем последняя приводила к более эффективному снижению ОХ. На фоне введения фумарата 3-ГП уровень ОХ также достоверно снижался на 32 % (табл. 1).
Т а б л и ц а 1
T a b l e 1
Уровень общего холестерина в сыворотке крови подопытных животных при экспериментальном аллоксановом диабете с экзогенной гиперхолестеринемией + витамин D
The level of total cholesterol in the blood serum of test animals
|
Серия / Series |
Средний уровень ОХ, ммоль/л / Mean levels of total cholesterol, mmol/l (M ± m) |
Степень достоверности (* – по отношению к интактным животным; ** – по отношению к контрольной группе) / The degree of veracity (*– with respect to intact animals; ** – relative to control) |
|
Интактные крысы / Intact animals |
1,44 ± 0,70 |
|
|
Контрольная группа / Сontrol |
2,13 ± 0,50 |
р* < 0,05 |
|
Фумарат 3-ГП 25 мг/кг per os / Fumarate 3-HP 25 mg/kg per os |
1,52 ± 0,10 |
р** < 0,05 |
|
Фумарат 3-ГП 50 мг/кг per os / Fumarate 3-HP 50 mg/kg per os |
1,45 ± 0,02 |
р** < 0,05 |
|
Мексидол 25 мг/кг в/м / Mexidol 25 mg/kg intramuscularly |
1,73 ± 0,20 |
р** > 0,05 |
|
Мексидол 50 мг/кг в/м / Mexidol 50 mg/kg intramuscularly |
1,37 ± 0,15 |
р** > 0,05 |
|
Никотинат 3-ГП 50 мг/кг per os / Nicotinate 3-HP 50 mg/kg per os |
1,32 ± 0,30 |
р** < 0,05 |
|
Симвастатин 1 мг/кг per os / Simvastatin 1 mg/kg per os |
1,65 ± 0,20 |
р** < 0,05 |
|
Никотинат 3-ГП 50 мг/кг per os + симвастатин 1 мг/кг per os / Nicotinate 3-HP 50 mg/kg per os + simvastatin 1 mg/kg per os |
1,50 ± 0,14 |
р** < 0,05 |
|
Никотиновая кислота 50 мг/кг per os / Nicotinic acid 50 mg/kg per os |
1,60 ± 0,30 |
р** > 0,05 |
Уровень ТГ в сыворотке крови крыс на фоне экспериментального диабета был достоверно выше, чем у интактных крыс на 45 %. Наибольшее снижение ТГ происходило на фоне терапии никотиновой кислотой – на 42 % по отношению к контрольной группе. На фоне монотерапии симвастатином
уровень ТГ снижался на 21 % по отношению к контролю. Исследуемые соединения (никотинат 3-ГП, никотинат 3-ГП в комбинации с симвастатином и фумарат 3-ГП) привели к сопоставимому с симвастатином снижению уровня ТГ на 22, 15 и 26 % соответственно (табл. 2).
Т а б л и ц а 2
T a b l e 2
Уровень ТГ в сыворотке крови белых крыс при аллоксановом диабете с экзогенной гиперхолестеринемией + витамин D на фоне терапии исследуемыми соединениями и препаратами сравнения
The level of triacylglycerols in the blood serum of white rats with experimental diabetes
|
Серия / Series |
Средний уровень ТГ, ммоль/л / Mean levels of triacylglycerols, mmol /l (M ± m) |
Степень достоверности (*– по отношению к интактным животным; ** – по отношению к контролю; # – по отношению к группе мексидола в дозе 50 мг/кг; ^ – по отношению к группе симвастатина; & – по отношению к группе никотиновой кислоты) / The degree of veracity (*– with respect to intact animals; ** – relative to control; # – relative to mexidol 50 mg/kg; ^ – relative to simvastatin; & – relative to nicotinic acid) |
|
1 |
2 |
3 |
|
Интактные крысы / Intact animals |
0,56 ± 0,20 |
|
|
Контрольная группа / Сontrol |
0,81 ± 0,30 |
р* < 0,001 |
|
Фумарат 3-ГП 25 мг/кг per os / Fumarate 3-HP 25 mg/kg per os |
0,76 ± 0,04 |
р** < 0,05; p# > 0,05; p^ > 0,05; p& < 0,05 |
|
Фумарат 3-ГП 50 мг/кг per os / Fumarate 3-HP 50 mg/kg per os |
0,60 ± 0,02 |
р** < 0,05; p# < 0,05; p^ > 0,05; p& < 0,05 |
|
Мексидол 25 мг/кг в/м / Mexidol 25 mg/kg intramuscularly |
0,66 ± 0,05 |
р** > 0,05; p# > 0,05; p^ > 0,05; p& < 0,05 |
Oкончание табл. 2
End of table 2
|
1 |
2 |
3 |
|
Мексидол 50 мг/кг в/м / Mexidol 50 mg/kg intramuscularly |
0,74 ± 0,07 |
р** > 0,05; p^ > 0,05; p& < 0,05 |
|
Никотинат 3-ГП 50 мг/кг per os / Nicotinate 3-HP 50 mg/kg per os |
0,63 ± 0,03 |
р**<0,05; p# < 0,05; p^ < 0,05; p& < 0,05 |
|
Симвастатин 1 мг/кг per os / Simvastatin 1 mg/kg per os |
0,64 ± 0,03 |
р** < 0,05; p# > 0,05; p& < 0,05 |
|
Никотинат 3-ГП 50 мг/кг per os + симвастатин 1 мг/кг per os / Nicotinate 3-HP 50 mg/kg per os + simvastatin 1 mg/kg per os |
0,69 ± 0,05 |
р**<0,05; p# > 0,05; p^ < 0,05; p& < 0,05 |
|
Никотиновая кислота 50 мг/кг per os / Nicotinic acid 50 mg/kg per os |
0,47 ± 0,07 |
р** < 0,05; p# > 0,05; p^ > 0,05 |
-
1 – Интактные животные / Intact animals
-
2 – Контрольная группа / Control
-
3 – Фумарат 3-ГП 25 мг/кг per os / Fumarate 3-HP 25 mg/kg per os
-
4 – Фумарат 3-ГП 50 мг/кг per os / Fumarate 3-HP 50 mg/kg per os
-
5 – Мексидол 25 мг/кг в/м / Mexidol 25 mg/kg intramuscularly
-
6 – Мексидол 50 мг/кг в/м / Mexidol 50 mg/kg intramuscularly
-
7 – Никотинат 3-ГП 50 мг/кг per os / Nicotinate 3-HP 50 mg/kg per os
-
8 – Симвастатин 1 мг/кг per os / Simvastatin 1 mg/kg per os
-
9 – Никотинат 3-ГП 50 мг/кг per os + симвастатин 1 мг/кг per os / Nicotinate 3-HP 50 mg/kg per os + simvastatin 1 mg/kg per os
-
10 – Никотиновая кислота 50 мг/кг per os / Nicotinic acid 50 mg/kg per os
Примечание: * – степень достоверности по отношению к интактным животным; ** – степень достоверности по отношению к группе контроля / Note: *– degree of veracity with respect to intact animals; ** – degree of veracity relative to control)
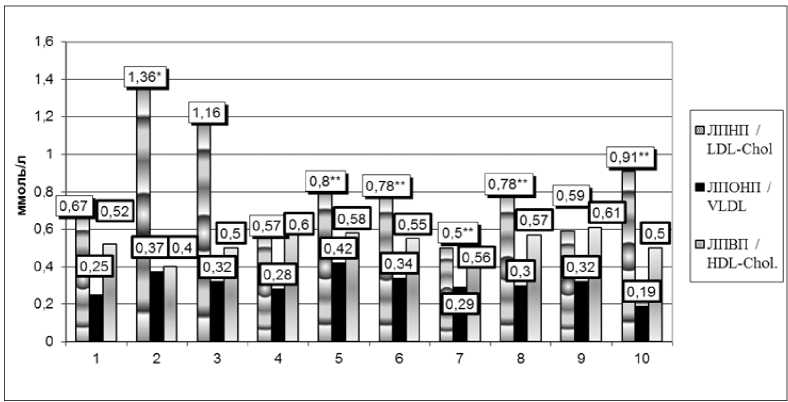
Р и с. 2. Влияние новых производных 3-ГП и препаратов сравнения на уровень ЛПНП, ЛПОНП и ЛПВП в сыворотке крови белых крыс при аллоксановом сахарном диабете и экзогенной гиперхолестеринемии
F i g. 2. Impact of new derivatives 3-HP and comparator drugs on LDL-CHOL, VLDL, HDL-CHOL in the blood serum of white rats with experimental diabetes
Новые производные 3-ГП (никотинат 3-ГП, никотинат 3-ГП в комбинации с симвастатином, а также фумарат 3-ГП) вызвали достоверное снижение холестерина ЛПНП на 63, 57 и 58 % соответственно. В группе животных, получавших монотерапию симвастатином, наблюдалось снижение уровня холестерина ЛПНП на 43 % по отношению к контрольной группе. Уровень холестерина ЛПНП в сыворотке крови белых крыс, получавших никотиновую кислоту, был ниже, чем в контрольной группе, на 33 %.
Данные по изменению уровней холестерина ЛПВП и ЛПОНП в группах отличались и были недостоверны (рис. 2).
Обсуждение и заключения
Таким образом, исследуемые нами соединения (фумарат 3-ГП и никотинат 3-ГП в дозах 50 мг/кг) проявляют выраженную метаболическую активность, достоверно снижая уровень глюкозы, ОХ, ТГ и холестерина ЛПНП. Именно этот факт, очевидно, обуславливает отсутствие летальности в группах крыс, получавших исследуемые соединения на модели аллоксанового диабета с экзогенной гиперхолестеринемией. В связи с этим перспективным представляется дальнейшее изучение новых соединений из группы 3-ГП в качестве корректоров метаболических нарушений при СД.
Поступила 18.01.2016; принята к публикации 10.03.2016; опубликована онлайн 20.06.2016
S ubmitted 18.01.2016; accepted for publication 10.03.2016; published online 20.06.2016
Список литературы Исследование влияния новых производных 3-гидроксипиридина и препаратов сравнения на выживаемость и некоторые биохимические показатели крови белых крыс при экспериментальном диабете
- Kannel W. Fifty years of Framingham Study contributions to understanding hypertension//J. Hum. Hypertens. 2000. Vol. 14, No. 2. P. 83-90. URL: http://ajh.oxfordjournals.org/content/by/year/2000.
- Дугин И. Н. Новые противодиабетические препараты//Фармацевтический вестник. 2004. № 36. С. 34-35. URL: http://www.pharmvestnik.ru/archive/1/270565.html.
- Джанашия П. Х., Мирина Е. Ю. Лечение сахарного диабета 2 типа//Русский медицинский журнал. 2005. Т. 13, № 26. С. 1761-1766. URL: http://www.rmj.ru/archive/yubileynyy_vypusk.
- Смирнов Л. Д., Донцов А. Е., Островский М. А. Ингибирование фотоиндуцированного липофусциновыми гранулами из клеток пигментного эпителия глаза человека окисление липидов с помощью гетероароматических антиоксидантов из класса 3-оксипиридинов//Молекулярная медицина. 2007. С. 56-59. URL http://elibrary.ru/contents.asp?issueid=437489.
- Изучение метаболической активности нового производного никотиновой кислоты при сахарном диабете у крыс: мат-лы Всерос. науч.-практ. конф. молодых ученых и специалистов «Актуальные проблемы современной эндокринологии»/Е. В. Семенова . М., 2008. С. 32. URL: http://www. enc.su/kgrs/Tezisi.pdf.
- Дедов И. И., Шестакова М В. Максимова М. А. Федеральная целевая программа сахарный диабет. М, 2002. С. 10-12. URL: http://www.voed.ru/fcp_sd.htm.
- Angiotensin II receptor gene polymorphism in human essential Hypertension/A. Bonnardeaux //Hypertension. 1994. Vol. 24. P. 63-69. URL: http://humbio.ru/humbio/car_g/000070b8.htm.
- Katsuyuki A., Hiroshi O., Shynya U. Anti-albuminuric effect of the aldosterone blocker eplerenone in non-diabetic hypertensive patients with albuminuria: a double-blind, randomised, placebo-controlled trial//The Lancet Diabetes & Endocrinology. 2014. Vol. 2, No. 12. P. 944-953. URL: http://www.thelancet.com/journals/landia/article/PIIS2213-8587(14)70194-9/abstract.
- Шостак Н. А., Аничков Д. А. К вопросу о диагностических критериях метаболического синдрома//Русский медицинский журнал. 2002. № 27. С. 1255-1257. URL: http://www.rmj.ru/archive/metabolicheskiy_sindrom_kardiologiya_novosti_farmkompaniy_istoriya_meditsiny.
- Возможность коррекции структурных изменений в миокарде при реперфуизионном повреждении с помощью 3-оксипиридина сукцината и 3-оксипиридина адипината/М. Н. Замотаева //Фундаментальные исследования. 2014. № 10-6. С. 1103-1106. URL: http://www.fundamental-research.ru/ru/article/view?id=35996.
- Association of the Renin-Sodium Profile with the risk of Myocardial Infarction in Patients with Hypertension/M. N. Alderman //Engl. J. Med. 1991. Vol. 324. P. 1098-1104. URL: http://www. academia.edu/17834492/Association_of_the_Renin-Sodium_Profile_with_the_Risk_of_Myocardial_Infarc-tion_in_Patients_with_Hypertension.
- Ruggenenti P., Perna A., Gerardi G. Renal function and requirement for dialysis in chronic nephropathy patients on long-term ramipril: REIN follow-up trial//The Lancet. 1998. Vol. 352, No. 9136. P. 1252-1256. URL: http://www.thelancet.com/journals/lancet/article/PIIS0140-6736(98)04433-X/abstract.
- Effect of perindopril on 24-hours ambulatory blood pressure monitoring, carbohydrates and lipids metabolism in patients with mild and moderate arterial hypertension and metabolic syndrome/V. Mychka //J. Hypertens. 2001. Suppl. P. 19-283. URL: http://ajh.oxfordjournals.org/content/by/year/2001.
- Eberhardt W., Pfeilschifter J. Nitric oxide and vascular remodeling: spotlight on the kidney//Kidney Int. 2007. Suppl P. 9-16. URL: http://2hlth.com/index.php?option=com_content&view=article&i d=88%3Anitric-oxide-and-restenosis&catid=44&Itemid=67.
- Семенова Е. В., Инчина В. И., Семенов А. В. Синтез и исследование фармакологической активности нового экспериментального препарата -фумарата 3-оксипиридина: мат-лы I Междунар. (X Всерос.) Пироговской студенч. науч. мед. конф (16 марта 2006 г)//Вестник РГМУ 2006. № 2 (49). С. 359. URL: http://vestnik.rsmu.ru/fileadmin/rsmu/img/about_rsmu/departments/red_izdat_otdel/vestnik_2_2006.pdi.
- Семенова Е. В. Возможности фармакологической коррекции гепатопатии печени и нарушений жирового обмена при сахарном диабете 1-го типа//Экспериментальная и клиническая гастроэнтерология. 2009. № 6. С. 138-142. URL: http://elibrary.ru/contents.asp?issueid=871531.
- Семенова Е. В., Инчина В. И., Семенов А. В. Изучение антигипоксической активности новых производных 3-гидроксипиридина//Журнал российской ассоциации по спортивной медицине и реабилитации больных и инвалидов. 2007. Т. 22, № 2. С. 52. URL: http://sportmed.ru/files/files/literature/journals_RASMIRBI/2007/Журнал_РАСМИРБИ_2007_N22.pdf.
- Использование новых производных 3-гидроксипиридина с целью метаболических нарушений при диабете/Т. В. Уланова //Известия Самар. науч. центра РАН. 2009. Т. 11, № 1 (6). С. 1315-1317. URL: http://www.ssc.smr.ru/media/journals/izvestia/2009/2009_1_1315_1317.pdf.
- Модификация гиполипидемической активности симвастатина никотинатом 3-гидроксипи-ридина в эксперименте/Т. В. Уланова //Современные проблемы науки и образования. 2014. № 5. URL: http://www.science-education.ru/119-14972.


