История исследования юкстагломерулярного аппарата
Автор: Арав Владимир Ильич, Слесарева Елена Васильевна, Попов Василий Васильевич, Кучина Кристина Андреевна, Уренева Регина Валерьевна
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Краткие сообщения
Статья в выпуске: 2, 2014 года.
Бесплатный доступ
История исследования юкстагломерулярного аппарата почки началась в конце XIX в. с открытия ренина. Это стимулировало открытие структур, осуществляющих синтез ренина, изучение регуляции его выделения и функционального значения ренина и юкстагломерулярного аппарата. Эти вопросы были в основном изучены в середине XX столетия, что привело к пониманию решающей роли юкстагломерулярного аппарата в сохранении водно-солевого гомеостаза. Выяснение роли ренина в патогенезе гипертонической болезни стимулировало в начале 80-х гг. XX столетия изучение механизмов его продукции и внутриклеточных механизмов его выделения. Исследование этих вопросов продолжается и в настоящее время, и они все еще далеки от окончательного разрешения.
Юкстагломерулярный аппарат, плотное пятно, ренин
Короткий адрес: https://sciup.org/14112977
IDR: 14112977 | УДК: 611-018:616.61:616.12-008.331.1
The history of juxtaglomerular apparatus of the kidney research
The history of juxtaglomerular apparatus of the kidney researching began in the end of 19th century from the renin discovery. This fact stimulated the opening of structures engaged synthesis of renin and study of the regulation and functional significance of renin and juxtaglomerular apparatus. These issues have been in the main resolved in the mid-20th century, which led to an understanding of the crucial role of the juxtaglomerular apparatus in the water and salt homeostasis preservation. In the early 80-ies of the 20th century the elucidation of the renin role in the pathogenesis of hypertension stimulated the study of its production mechanisms and intracellular mechanisms of its isolation. The examining of these issues continues now, and it is still far from the final solution.
Текст краткого сообщения История исследования юкстагломерулярного аппарата
Юкстагломерулярный аппарат – основная структура, обеспечивающая поддержание артериального давления и водно-солевого гомеостаза. Если принять во внимание, что биологическая жизнь организма представляет собой постоянный процесс поддержания постоянства внутренней среды организма, то становится понятным, что без функций юкстагломерулярного аппарата жизнь не возможна.
Юкстагломерулярный аппарат почки состоит из 3 компонентов и располагается возле почечного тельца, большую часть которого занимает капиллярный клубочек. В состав юкстагломерулярного аппарата входят:
-
1. Юкстагломерулярные (околоклубочковые) клетки, находящиеся в стенке приносящей артериолы, где они занимают среднюю оболочку, образованную у всех артерий гладкомышечными клетками. Иногда эти клетки могут располагаться и в стенке выносящей артериолы (рис. 1).
-
2. Плотное пятно (мacula densa) – это участок дистального канальца нефрона, расположенный между приносящей и выносящей артериолами (рис. 1). На данном участке клетки лежат плотно, их ядра располагаются близко друг к другу, что и определило название этого участка.
-
3. Юкставаскулярные (околососудистые) клетки, или клетки Гурмагтига (рис. 1). Это группа клеток, расположенных в треугольнике, стенки которого образуют приносящая и выносящая артериолы и плотное пятно.
Началом изучения юкстагломерулярного аппарата послужило открытие Тигерштедта в 1898 г., заключавшееся в том, что введение кролику водного экстракта почки другого кролика вызывает повышение артериального давления [16]. Поскольку почка по латыни renis, то действующее начало экстракта было названо ренином. Это послужило толчком к поиску в почке структур, ответственных за синтез и выделение ренина.
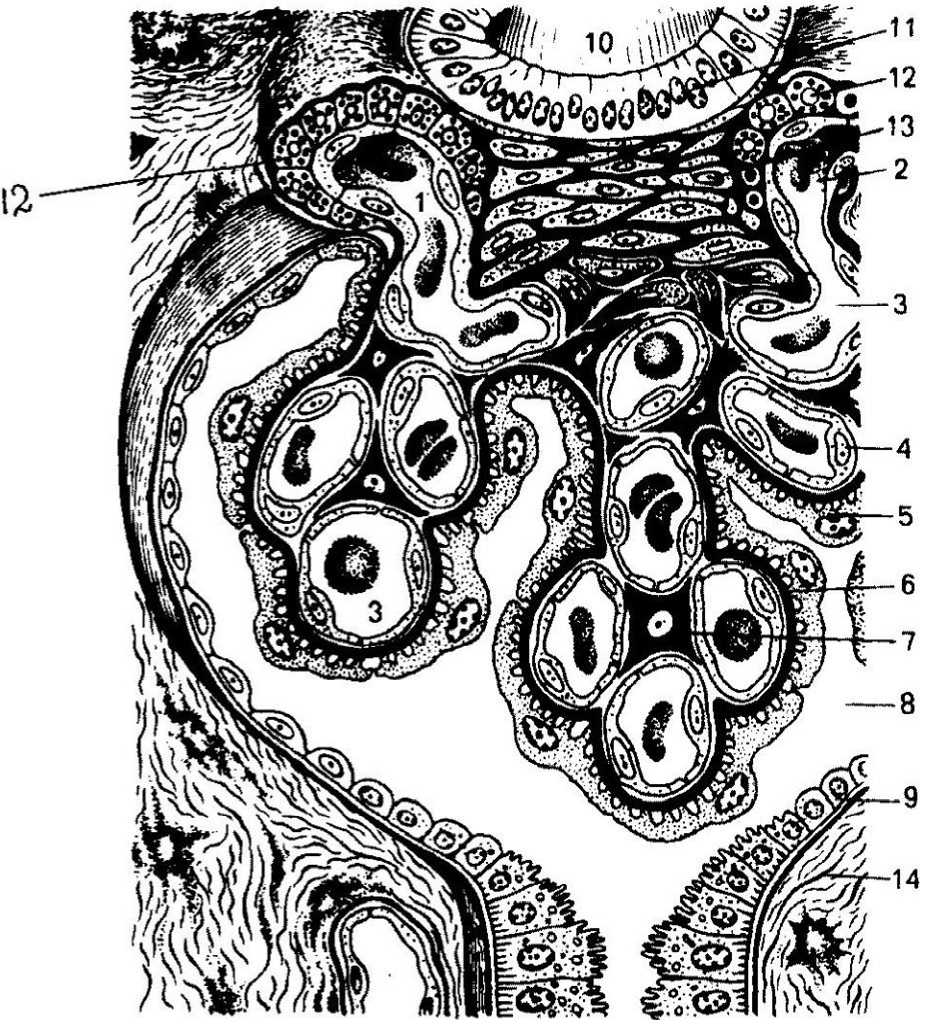
Рис. 1. Строение почечного тельца с юкстагломерулярным аппаратом:
-
1 – приносящая клубочковая артериола; 2 – выносящая клубочковая артериола; 3 – капилляры сосудистого клубочка; 4 – эндотелиоциты; 5 – подоциты внутреннего листка капсулы клубочка;
-
6 – базальная мембрана; 7 – мезангиальные клетки; 8 – полость капсулы клубочка; 9 – наружный листок капсулы клубочка; 10 – дистальный каналец нефрона; 11 – плотное пятно; 12 – эндокрино-циты (юкстагломерулярные клетки); 13 – юкставаскулярные клетки; 14 – строма почки
Паренхима почки состоит из нефронов – по 1 млн в каждой почке (рис. 2); капиллярных клубочков – по одному на каждый нефрон и сосудов. Капиллярный клубочек и канальцы нефрона – структуры, осуществляющие образование мочи. Поэтому внимание исследователей привлекли структуры, не имеющие прямого отношения к образованию мочи, которые впоследствии и вошли в состав юкстагломерулярного аппарата. Тем не менее выяснение истины не обошлось без борьбы мнений.
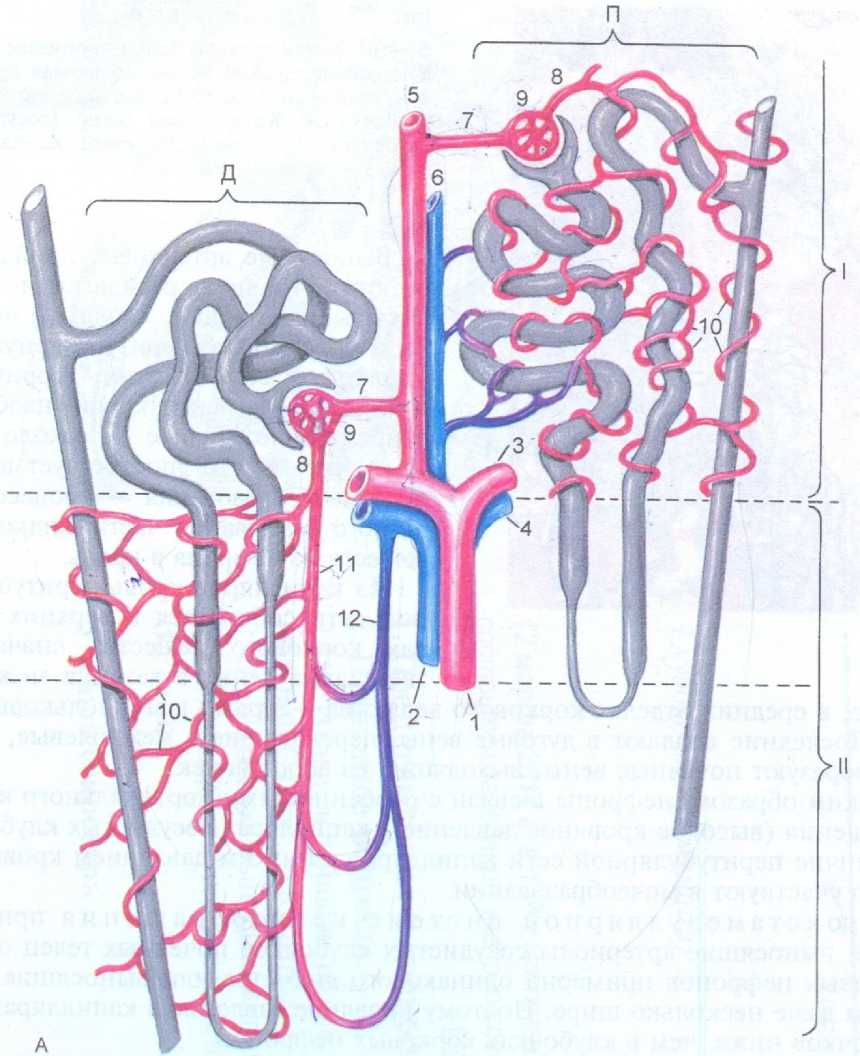
Рис. 2. Кровоснабжение нефронов: А – схема:
I – корковое вещество; II – мозговое вещество (околомозговой нефрон); Д – длинный (околомозго-вой) нефрон; П – промежуточный нефрон; 1, 2 – междолевые артерии и вена; 3, 4 – дуговая артерия и вена; 5, 6 – междольковая артерия и вена; 7 – приносящая клубочковая артериола; 8 – выносящая клубочковая артериола; 9 – клубочковая капиллярная сеть (сосудистый клубочек); 10 – перитубулярная капиллярная сеть; 11 – прямая артериола; 12 – прямая венула
Первые исследования почки как эндокринного органа провел в конце XIX – начале XX в. Роберт Тигерштедт (1853–1923), профессор физиологии Каролинского института. Рудольф Гейденгайн (1834–1891) – известный анатом и физиолог – был сторонником секреторной функции клубочка [7]. Однако Карл Людвиг (1816–1895) отстаивал то, что клубочек является простым фильтром [26]. Эта точка зрения впоследствии нашла общее признание. Франц Вольхард и Теодор Фар в 1914 г. опубликовали классификацию болез- ни Брайта и атеросклеротических изменений почек и показали, что повышенное артериальное давление может быть причиной заболевания почек [6].
В первой половине XX в. основной вклад в изучение функции почек и открытие юкстагломерулярного аппарата сделал Норберт Гурмагтиг (1890–1960). В начале 1940-х гг. он опубликовал свои первые работы по влиянию гипертензии на почечные сосуды [9, 12]. В 1925 г. Руйтер открыл у мышей клетки, залегающие в стенке артерий возле капиллярного клубочка [1, 2]. Руйтер обнаружил, что гладкомышечные клетки афферентных артерий теряют фибриллы и заменяются слоем больших гранулированных клеток. Чарльз Оберлинг в 1927 г. открыл подобные клетки в почке человека [18]. В 1932 г. Гурмагтиг описал афибриллярные клетки юкстагломерулярных артериол у 8-летней девочки, умершей от скарлатины [11]. Он посчитал их сходными с теми клетками, которые описал Руйтер, и назвал эту группу клеток «сегментами нейромиоартериального юкстагломерулярного ренина».
В 1929 г. Карл Циммерман (1861–1935), профессор Бернского университета, описал эпителиальные клетки дистальных канальцев, проходящих в области клубочка [27]. Он показал, что в этом месте наблюдается увеличение числа ядер эпителиальных клеток, и впоследствии назвал это место «макула ден-са», т.е. плотное пятно. В 1933 г. Циммерман описал группу агранулярных (незернистых) клеток, прилегающих к клубочку и расположенных между приносящей и выносящей артериолами [20]. В последующем эти клетки стали приравнивать к гранулированным клеткам, описанным Гурмагтигом, и они даже получили название клетки Гурмагтига. Гурмагтиг тоже их изучал, но с самого начала был уверен, что гранулированные клетки, которые располагаются в стенке афферентной артериолы, отличаются от негранулирован-ных клеток, расположенных в сосудистом поле клубочка. Эти клетки получили название юкставаскулярных.
Исследователи того времени: Руйтер, который открыл юкстагломерулярные клетки, Хоральд Оккельс из Копенгагена и амери- канский ученый Ричардс – считали, что юкстагломерулярные клетки представляют собой сфинктер [7]. Эти клетки могут набухать, уменьшать свой объем и тем самым регулировать приток крови к капиллярам клубочка. Гурмагтиг, продолжая изучать юкстагломерулярные клетки и плотное пятно, объединил их в один орган, который назвал юкстагломерулярным аппаратом [10]. Гурмагтиг предположил, что афферентная артериола является эндокринным органом, который выделяет вазоактивное вещество ренин [3]. Гурмагтиг считал, что юкстагломерулярный аппарат имеет большое значение в патогенезе артериальной гипертонии, что в дальнейшем получило свое подтверждение. Изучая плотное пятно («макула денса»), Гурмагтиг пришел к выводу, что его эпителиальные клетки представляют собой сенсорное поле, которое контролирует изменение объема или физикохимический состав жидкости, протекающей в канальце нефрона, и влияет на клубочковую циркуляцию крови [10]. Выводы Гурмагтига о функции юкстагломерулярных клеток и плотного пятна можно считать гениальным озарением, определившим направление будущих исследований юкстагломерулярного аппарата, сформировавшим современное представление о его функции.
Юкстагломерулярные клетки, локализованные в средней оболочке приносящей артериолы у места ее впадения в клубочек, вырабатывают ренин [13]. Клетки плотного пятна являются рецепторами ионов Na. При уменьшении концентрации натрия в жидкости, протекающей через дистальный каналец нефрона, клетки плотного пятна выделяют фактор, который стимулирует выделение ренина из юкстагломерулярных клеток [3, 20]. Ренин является начальным звеном системы «ренин – ангиотензин – альдостерон», которое определяет активность этой системы. Под влиянием ренина в конечном итоге образуется ангиотензин 2, вызывающий повышение артериального давления. Следствием этого является увеличение фильтрации в клубочке и количества натрия в жидкости в канальцах нефрона. Это в свою очередь подавляет плотное пятно и выделение ренина юкстагломерулярными клетками.
Стойкое повышение уровня ренина в плазме крови приводит к стойкому повышению артериального давления. Начальные причины этого могут быть разными. Высокое артериальное давление – основной признак гипертонической болезни, и существующее в настоящее время лечение направлено на его нормализацию. В этом вопросе достигнуты существенные успехи, и у подавляющего большинства больных удается поддерживать нормальное артериальное давление. Однако лечение не влияет на функцию системы «ренин – ангиотензин – альдостерон». Продукция ренина и активность системы остаются высокими. Поэтому в последние 30–40 лет усилия исследователей направлены на изучение механизмов увеличения продукции ренина и внутриклеточных механизмов регуляции синтеза и выделения ренина. Решение этих вопросов создаст основу для лечения гипертонической болезни, а не ее симптомов.
Каким образом происходит увеличение продукции ренина? В других железах, и экскреторных и эндокринных, увеличение продукции секрета происходит за счет усиления функции секреторных клеток. Увеличение продукции ренина осуществляется принципиально другим способом. В раннем эмбриональном периоде ренинпродуцирующие клетки имеются не только в почке, но и в других органах [1, 20]. В процессе эмбрионального развития ренинпродуцирующие клетки превращаются в клетки других типов, в частности в гладкомышечные клетки мелких и крупных почечных артерий, в клетки, располагающиеся между капиллярами клубочка, в клетки передней доли гипофиза, в эндокринные клетки семенников и яичника и клетки других органов [21]. Однако эти клетки сохраняют способность возвращаться к эмбриональному состоянию. При возникновении угрозы постоянству артериального давления или водно-солевого гомеостаза эти клетки возвращаются в эмбриональное состояние и становятся ренинпродуцирующими клетками. Этот процесс называется метаплазией. Типичной является метаплазия гладкомышечных клеток почечных артериол и мелких артерий, что приводит к увеличению количества ренинпродуцирующих клеток [14,
-
24]. Таким образом, увеличение продукции ренина происходит не за счет усиления функции ренинпродуцирующих клеток, а за счет увеличения их количества. Однако стимулы, вызывающие метаплазию гладкомышечных клеток почечных артерий в ренин-продуцирующие, остаются неизвестны.
Большое количество работ посвящено изучению внутриклеточных механизмов регуляции синтеза и выделения ренина. Определена фундаментальная роль циклического аденозинмонофосфата (ц-АМФ) в стимуляции синтеза и выделения ренина [24]. Выявлены изоформы (модификации) фермента аденилатциклазы, свойственные ренинпро-дуцирующим клеткам [14]. Установлена роль кальция в процессах синтеза и выделения ренина. Кальций – прямой стимулятор большинства секреторных клеток. Но в юкстагломерулярных клетках он подавляет и синтез, и выделение ренина [2, 22]. Это явление получило название «парадокс кальция».
Юкстагломерулярные клетки связаны между собой с помощью щелевидных контактов, которые образованы белком конекси-ном, имеющим разные изоформы. Нарушение щелевидных контактов или утрата конек-сина увеличивает секрецию ренина и повышает артериальное давление, а также приводит к атипичной локализации юкстагломерулярных клеток [4, 5, 15].
Классическое представление о клетках плотного пятна как солевых рецепторах, генерирующих паракринный сигнал выделения ренина, претерпело изменения. В настоящее время сформировалось представление, что клетки плотного пятна являются метаболическими индикаторами и хеморецепторами, реагирующими на изменение химического состава канальцевой жидкости, который зависит от тканевого обмена веществ [19, 25].
В заключение необходимо сказать, что выяснение внутриклеточных механизмов регуляции синтеза и выделения ренина, механизма метаплазии гладкомышечных клеток в юкстагломерулярные создаст условия для разработки в ближайшие 30–50 лет технологий, позволяющих управлять этими процессами и регулировать уровень синтеза и выделения ренина в условиях патологии.
-
1. A protease processing site is essential for prorenin sorting to the regulated secretary pathway / V. Brechle [et al.] // J. Biol. Chem. – 1996. – Vol. 271. – P. 636–640.
-
2. Beierwaltes W. H. The role of calcium in the regulation of rennin secretion / W. H. Beierwaltes // Am. J. Physiol. Renal Physiol. – 2009. – Vol. 29.
-
3. Celoria G. C. Role of the macula densa in relation to the granulation ot the renal juxtaglomerular cells / G. C. Сeloria, R. Puche // Acta Physiol lat Am. – 1967. – Vol. 17 (1). – P. 6–14.
-
4. Connekcin 40 regulates renin production and blood pressure / N. Krattinger [et al.] // Kidney Int. – 2007. – Vol. 72. – P. 814–822.
-
5. Connexin 40 is essential for the pressure control of renin synthesis and secretion / C. Wagner [et al.] // Circ. Res. – 2007. – Vol. 100. – P. 556–563.
-
6. Eknoyan G. On the central role of the kidney in the recognition, conceptual evolution, and understanding of hypertention / G. Eknoyan // Adv. Chronic Kidney Dis. – 2004. – Vol. 11. – P. 192–196.
-
7. Eknoyan G. The Juxtaglomerular apparatus of Norbert Goormaghtigh – a critical appraisal / G. Eknoyan, R. Ruben, N. Lameire // Nephrol. Dial Transplant. – 2009. – Vol. 24. – P. 3876–3881.
-
8. Goormaghtigh N. Existance of an endocrine gland in the media of renal arterioles / N. Goormaghtigh // Proc. Soc. Exp. Biol. Med. – 1939. – Vol. 42. – P. 688–689.
-
9. Goormaghtigh N. La scrlerose vasculaire renale experimentale du apin / N. Goormaghtigh // Ann. Anat Pathol. – 1931. – Vol. 8. – P. 587–604.
-
10. Goormaghtigh N. L'appareil neuro-myoarterial juxtaglomerulaire du rein: ses reactions en pathologic et ses rapports avec le tube urinifere / N. Goormaghtigh // Compt. Rend. Soc. Biol. – 1937. – Vol. 129. – P. 293–296.
-
11. Goormaghtigh N. Les segments neuro-myoarteriels juxtaglomerulaires du renin / N. Goormaghtigh // Arch. Biol. – 1932. – Vol. 43. – P. 575–591.
-
12. Goormaghtigh N. Sclerose vasculaire du rein apres denervation des sinus carotidience et section des nerfs depresseurs / N. Goormaghtigh // Compt. Rend. Soc. Biol. – 1931. – Vol. 106. – P. 1254–1257.
-
13. Guilan R. A. The juxtaglomerular complex / R. A. Guilan, S. Zelman, F. J. Murphy // Arch. Pathol. – 1967. – Vol. 84 (6). – P. 598–600.
-
14. Kurtz A. Renin release: sites, mechanisms and control / A. Kurtz // Ann. Rew. Physiol. – 2011. – Vol. 73. – P. 377–390.
-
15. Lack of connexin 40 causes displacement of renin-producing cells from afferent arterioles to the exxraglomerular mesangium / L. Kurtz [et al.] // J. Am. Soc. Nephrol. – 2007. – Vol. 18. – P. 1103–1111.
-
16. Marks L. S. Tigerstedt and the discowery of renin. A historical note / L. S. Marks, M. H. Maxwell // Hypertension. – 1979. – Vol. 1. – P. 384–388.
-
17. Metaplasia of smoth muscle cells into juxtaglomerular cells in the juxtaglomerular apparatus, arteries and arterioles of the ischemic kidney
/ M. Cantin [et al.] // Am. J. Pathol. – 1977. – Vol. 87, № 3. – P. 581–592.
-
18. Oberling C. R. L'existense d'une housse neuromusculaire au niveau des arteres glomerulaires de s'Homme / C. R. Oberling // Compt. Rend. Acad. Sci. – 1927. – Vol. 184. – P. 1200–1202.
-
19. Peti-Peterdi J. Macula densa sensing and signaling mechanisms of rennin release / I. Peti-Peterdi, R. C. Harris // J. Am. Soc. Nephrol. – 2010. – Vol. 21 (7). – P. 1093–1096.
-
20. Reeves G. Sensitivity of the renal macula densa to urinary sodium proc. / G. Reeves, S. C. Sommers // Soc. Exp. Biol. Med. – 1965. – Vol. 120 (2). – P. 324–326.
-
21. Renin cells are precursors, for multiple cell types that switch to the renin phenotype when homestasis is threatened / Sequeira Lopez M. L. [et al.] // Dev. cell. – 2004. – Vol. 6. – P. 719–728.
-
22. Renin release / F. Schweda [et al.] // Physiology. – 2007. – Vol. 22. – P. 310–319.
-
23. Ruyter J. H. C. Uber einen Merkwurdigen abscnitt der Vas Afferentiv in der Mauseniere / J. H. C. Ruyter // Ztschr Mikrosk Anal Forsch. – 1925. – Vol. 2. – P. 242–248.
-
24. Sequeira Lopez M. L. Novel mechanisms for the control of renin synthesis and release / Sequeira Lopez M. L., R. A. Gomez // Curr. Hypertens Rep. – 2010. – Vol. 12 (1). – P. 26–32.
-
25. Succinate receptor (GPR 91) activation in macula densa cells causes renin release / S. L. Vargas [et al.] // J. Am. Soc. Nephrol. – 2009. – Vol. 20. – P. 1002–1011.
-
26. Turau K. Renal blood fiow and dynamics of glomerular filtration: Evolution of a concept from Carl Ludwig to the present day / K. Turau, J. M. Davis, D. A. Häberle // Renal Physiology. People and Jdeas / Carl W. Gottschalk, Robert W. Berliner, Gerhard H. Giebish (eds.). – Bethesda, MD : American Physiological Society, 1987. – P. 31–61.
-
27. Zimermann K. W. Uber den Bau des Glomerulus der menschlichen / K. W. Zimermann // Niere Z. Mikr. Anat. Forsch. – 1929. – Vol. 19. – P. 520–552.
-
28. Zimermann K. W. Uber der Bau des Glomerulus der Saugerniere: Weittere Mitteilunger / K. W. Zimermann // Niere Z. Mikr. Anat. Forsch. – 1933. – Vol. 32. – P. 176–278.
THE HISTORY OF JUXTAGLOMERULAR APPARATUS OF THE KIDNEY RESEARCH
V.I. Arav1, E.V. Slesareva1, V.V. Popov2, K.A. Kuchina1, R.V. Ureneva1
1Ulyanovsk State University, 2Ulyanovsk Region Children’s Hospital
Список литературы История исследования юкстагломерулярного аппарата
- A protease processing site is essential for prorenin sorting to the regulated secretary pathway/V. Brechle [et al.]//J. Biol. Chem. -1996. -Vol. 271. -P. 636-640.
- Beierwaltes W. H. The role of calcium in the regulation of rennin secretion/W. H. Beierwaltes//Am. J. Physiol. Renal Physiol. -2009. -Vol. 29.
- Celoria G. C. Role of the macula densa in relation to the granulation ot the renal juxtaglomerular cells/G. C. Сeloria, R. Puche//Acta Physiol lat Am. -1967. -Vol. 17 (1). -P. 6-14.
- Connekcin 40 regulates renin production and blood pressure/N. Krattinger [et al.]//Kidney Int. -2007. -Vol. 72. -P. 814-822.
- Connexin 40 is essential for the pressure control of renin synthesis and secretion/C. Wagner [et al.]//Circ. Res. -2007. -Vol. 100. -P. 556-563.
- Eknoyan G. On the central role of the kidney in the recognition, conceptual evolution, and understanding of hypertention/G. Eknoyan//Adv. Chronic Kidney Dis. -2004. -Vol. 11. -P. 192-196.
- Eknoyan G. The Juxtaglomerular apparatus of Norbert Goormaghtigh -a critical appraisal/G. Eknoyan, R. Ruben, N. Lameire//Nephrol. Dial Transplant. -2009. -Vol. 24. -P. 3876-3881.
- Goormaghtigh N. Existance of an endocrine gland in the media of renal arterioles/N. Goormaghtigh//Proc. Soc. Exp. Biol. Med. -1939. -Vol. 42. -P. 688-689.
- Goormaghtigh N. La scrlerose vasculaire renale experimentale du apin/N. Goormaghtigh//Ann. Anat Pathol. -1931. -Vol. 8. -P. 587-604.
- Goormaghtigh N. L'appareil neuro-myo-arterial juxtaglomerulaire du rein: ses reactions en pathologic et ses rapports avec le tube urinifere/N. Goormaghtigh//Compt. Rend. Soc. Biol. -1937. -Vol. 129. -P. 293-296.
- Goormaghtigh N. Les segments neuro-myo-arteriels juxtaglomerulaires du renin/N. Goormaghtigh//Arch. Biol. -1932. -Vol. 43. -P. 575-591.
- Goormaghtigh N. Sclerose vasculaire du rein apres denervation des sinus carotidience et section des nerfs depresseurs/N. Goormaghtigh//Compt. Rend. Soc. Biol. -1931. -Vol. 106. -P. 1254-1257.
- Guilan R. A. The juxtaglomerular complex/R. A. Guilan, S. Zelman, F. J. Murphy//Arch. Pathol. -1967. -Vol. 84 (6). -P. 598-600.
- Kurtz A. Renin release: sites, mechanisms and control/A. Kurtz//Ann. Rew. Physiol. -2011. -Vol. 73. -P. 377-390.
- Lack of connexin 40 causes displacement of renin-producing cells from afferent arterioles to the exxraglomerular mesangium/L. Kurtz [et al.]//J. Am. Soc. Nephrol. -2007. -Vol. 18. -P. 1103-1111.
- Marks L. S. Tigerstedt and the discowery of renin. A historical note/L. S. Marks, M. H. Maxwell//Hypertension. -1979. -Vol. 1. -P. 384-388.
- Metaplasia of smoth muscle cells into juxtaglomerular cells in the juxtaglomerular apparatus, arteries and arterioles of the ischemic kidney/M. Cantin [et al.]//Am. J. Pathol. -1977. -Vol. 87, № 3. -P. 581-592.
- Oberling C. R. L'existense d'une housse neuromusculaire au niveau des arteres glomerulaires de s'Homme/C. R. Oberling//Compt. Rend. Acad. Sci. -1927. -Vol. 184. -P. 1200-1202.
- Peti-Peterdi J. Macula densa sensing and signaling mechanisms of rennin release/I. Peti-Peterdi, R. C. Harris//J. Am. Soc. Nephrol. -2010. -Vol. 21 (7). -P. 1093-1096.
- Reeves G. Sensitivity of the renal macula densa to urinary sodium proc./G. Reeves, S. C. Som-mers//Soc. Exp. Biol. Med. -1965. -Vol. 120 (2). -P. 324-326.
- Renin cells are precursors, for multiple cell types that switch to the renin phenotype when homestasis is threatened/Sequeira Lopez M. L. [et al.]//Dev. cell. -2004. -Vol. 6. -P. 719-728.
- Renin release/F. Schweda [et al.]//Physiology. -2007. -Vol. 22. -P. 310-319.
- Ruyter J. H. C. Uber einen Merkwurdigen abscnitt der Vas Afferentiv in der Mauseniere/J. H. C. Ruyter//Ztschr Mikrosk Anal Forsch. -1925. -Vol. 2. -P. 242-248.
- Sequeira Lopez M. L. Novel mechanisms for the control of renin synthesis and release/Sequeira Lopez M. L., R. A. Gomez//Curr. Hypertens Rep. -2010. -Vol. 12 (1). -P. 26-32.
- Succinate receptor (GPR 91) activation in macula densa cells causes renin release/S. L. Vargas [et al.]//J. Am. Soc. Nephrol. -2009. -Vol. 20. -P. 1002-1011.
- Turau K. Renal blood fiow and dynamics of glomerular filtration: Evolution of a concept from Carl Ludwig to the present day/K. Turau, J. M. Davis, D. A. Häberle//Renal Physiology. People and Jdeas/Carl W. Gottschalk, Robert W. Berliner, Gerhard H. Giebish (eds.). -Bethesda, MD: American Physiological Society, 1987. -P. 31-61.
- Zimermann K. W. Uber den Bau des Glomerulus der menschlichen/K. W. Zimermann//Niere Z. Mikr. Anat. Forsch. -1929. -Vol. 19. -P. 520-552.
- Zimermann K. W. Uber der Bau des Glomerulus der Saugerniere: Weittere Mitteilunger/K. W. Zimermann//Niere Z. Mikr. Anat. Forsch. -1933. -Vol. 32. -P. 176-278.


