Избирательное вовлечение рецепторов серотонина в механизмы синаптического облегчения у нейронов сенситизируемой улитки
Автор: Никитин В.П.
Журнал: Академический журнал Западной Сибири @ajws
Рубрика: Медицина
Статья в выпуске: 2 (73) т.14, 2018 года.
Бесплатный доступ
В ранее выполненных нами исследованиях обнаружено, что выработка ноцицептивной сенситизации у виноградных улиток или аппликации серотонина на ЦНС сопровождалась долговременным облегчением ответов интернейронов оборонительного поведения ЛПл1 и ППл1 на сенсорные раздражения, которое зависело от процессов трансляции и транскрипции. В настоящей работе изучена возможность избирательного вовлечения 5-HT1A субтипов рецепторов серотонина в механизмы индукции синаптического облегчения. Обнаружено, что выработка сенситизации во время подведения к нейронам антагониста этих рецепторов NAN-190 (1-(2-methoxiphenil)-4-[4-(2phthalimido)butyl]piperasine hydrobromide) вызывала подавление синаптического облегчения в ответах нейрона ЛПл1 на тактильные раздражения головы улитки. При этом синаптическое облегчение в ответах на химические раздражения головы и тактильные раздражения ноги развивалось так же, как у нейронов контрольных сенситизированных животных. Предположено, что у сенситизированных виноградных улиток б-HT1A-подобные рецепторы избирательно вовлечены в механизмы индукции пластичности синаптических "входов" интернейронов оборонительного поведения, опосредующих возбуждения от механорецепторов головы.
Сенситизация, рецепторы серотонина, сенсорные раздражения, идентифицированные нейроны, виноградная улитка
Короткий адрес: https://sciup.org/140225947
IDR: 140225947
Selective involvement of serotonin receptors in mechanisms of synaptic facilitation in neurons of a sensitized snails
In previous studies we found that the development of nociceptive sensitization in grape snails or serotonin application on the central nervous system was accompanied by a long-term facilitation of the responses of the defensive behavior interneuron Lpl1 and Ppl1 to sensory stimuli, which depended on translation and transcription processes. In the present work, the possibility of selective involvement of 5-HT1A serotonin receptors subtypes in the mechanisms of synaptic facilitation induction has been studied. It was found that the development of sensitization in the conditions of application to the neurons of these receptors antagonist NAN-190 (1- (2-methoxiphenil) -4- [4-(2phthalimido) butyl] piperasine hydrobromide) caused suppression of synaptic facilitation in the responses of Lpl1 neuron to tactile stimulation of snails head. In this case, synaptic facilitation in responses to chemical stimulation of the head and tactile stimulation of snail's leg developed in the same way as in the neurons of control sensitized animals. It is suggested that in sensitized snails, 5-HT1A-like receptors are selectively involved in the mechanisms of induction of plasticity of the defensive behavior interneurons synaptic "inputs" mediating excitations from the head mechanoreceptors.
Текст научной статьи Избирательное вовлечение рецепторов серотонина в механизмы синаптического облегчения у нейронов сенситизируемой улитки
В исследованиях, выполненных как на нервных клетках моллюсков, так и на нейронах млекопитающих показано, что серотонин вовлечен в пластические перестройки клеток, лежащие в основе механизмов обучения [1, 2, 10, 11]. Так, например, обнаружено, что у морского моллюска аплизии выработка простой формы не ассоциативного обучения – ноцицептивной сенситизации оборонительного рефлекса - приводит к изменению эффективности синаптических связей между нейронами [5, 9]. Ключевым механизмом данного процесса является так называемое гетеросинаптическое облегчение -серотонин-индуцированная функционально - морфологическая модуляция синаптических связей.
Исследование молекулярных механизмов долговременной синаптической пластичности в нейронах аплизии показало, что в ее индукцию серотони- ном вовлечены ряд протеинкиназ, в том числе цАМФ-зависимая протеинкиназа А, протеинкиназа С и митогенактивируемая протеинкиназа (MAPK) [5, 9]. Протеинкиназы регулируют активность ряда транскрипционных факторов, которые активируют экспрессию немедленных «ранних» и «поздних» генов. Синтезируемые мРНК транспортируются в нейриты и индуцируют долговременное облегчение синаптической связи, на которую многократно апп-лицировали серотонин. Важно отметить, что выявленные эффекты серотонина были синапс - специфичными, что достигалось за счет индукции вторичными посредниками механизмов маркирования и кооптирования в стимулируемых серотонином синапсах транскрипционных продуктов и локального синтеза белков [5, 9].
В опытах на виноградных улитках, обнаружено, что серотонин имитирует эффекты ноцицептивной сенситизации на уровне интернейронов оборонительного поведения животных [2, 7]. В частности, ранее нами выявлено, что инъекции серотонина к нейронам ЛПл1 и ППл1 несенситизированных улиток вызывали избирательное облегчение синаптических связей в ответах на раздражения головы тактильными стимулами или аппликациями слабого раствора хинина [3]. Серотонин не вызывал изменения ответов нейронов на тактильные раздражения ноги улитки. В последующих опытах, используя модель выработки ноцицептивной сенситизации, мы обнаружили, что химические и тактильные сенсорные входы нейронов ЛПл1 и ППл1 регулируются разными системами вторичных посредников, разными транскрипционными факторами и генами [3]. Эти факты позволяют нам предположить, что синапс-специфические эффекты серотонина реализуются за счет активации разных типов серотониновых рецепторов, связанных с разными системами вторичных посредников.
В настоящей работе исследовано влияние антагониста 5-HT1A рецептора NAN-190 на ответы интернейронов оборонительного поведения виноградной улитки, вызванные различными сенсорными раздражениями при выработке сенситизации.
Методика.
Опыты проводили на интернейроне оборонительного поведения ЛПл1 полуинтактного препарата виноградных улиток Helix lucorum [2]. Перед операцией животное анестезировали охлаждением в смеси воды со льдом в течение 30-40 мин и введением в полость тела непосредственно перед операцией 100-150 мг MgCl2, разведенного в 2 мл физиологического раствора. У улиток удаляли раковину и рассекали по средней линии переднюю часть ноги, за исключением ее головного конца. Затем улитку помещали в ванночку, заполненную парафином, и фиксировали вокруг окологлоточного комплекса ганглиев (ЦНС) силиконовое кольцо объемом 200 мкл, в которое постоянно поступал физиологический рас- твор со скоростью 500 мкл/мин. Отведение биоэлектрической активности нейронов осуществляли стандартными электрофизиологическими методами с помощью стеклянных микроэлектродов, заполненных смесью 2 М раствора цитрата калия и 2М KCl в соотношении 1:1. Электроды имели диаметр кончика менее 1 мкм и сопротивление около 30 МОм.
Сенситизацию вырабатывали трехкратным с интервалом 15 мин нанесением 100 мкл концентрированного (10%-ного) раствора хинина гидрохлорида на кожу передней части головы. Через 2 мин после каждого сенситизирующего стимула голову улитки отмывали физиологическим раствором.
Для тестирования реакций нейронов на сенсорные раздражители применяли слабый раствор хинина (0,25%) и тактильные стимулы. Хинин в объеме 600 мкл апплицировали в течение 30 с на переднюю часть головы улитки. Через 2 мин после окончания аппликации голову животного отмывали физиологическим раствором. Тактильные раздражения наносили на голову или на среднюю часть ноги с помощью электромеханического устройства (давление 1500 г/см2) [3]. В ответах, вызванных сенсорными раздражениями, оценивали площадь (в мВ·с) характерных для интернейронов улитки медленных ВПСП (возбуждающих постсинаптических потенциалов, мВПСП). Измерение площади производили с помощью прибора Digitizer KD 4030B (фирма Graphtec, Япония) и специальной компьютерной программы. В каждом эксперименте в течение 1,5 ч перед подведением веществ, а также через 2-3 ч после начала выработки сенситизации животным наносили тестирующие сенсорные раздражения с интервалом 15-20 мин. Последовательность нанесения стимулов – химического раздражения головы, тактильного раздражения ноги и тактильного раздражения головы - меняли в каждом опыте. В работах, выполненных нами ранее [3] показано, что стабильность синаптических ответов у нейронов сохраняется на протяжении 5-6 ч эксперимента. В каждом опыте данные, полученные на 120-150=й минуте после нанесения первого сенситизирующего раздражения, выражали в процентах по отношению к исходным значениям. Ранее нами было обнаружено, что на 120-150=й минуте после начала выработки сенситизации синаптическое облегчение у нейрона ЛПл1 достигало стабильного уровня, поддерживаемого более 24 ч [3]. Так как у некоторых нейронов генерация потенциалов действия препятствовала измерению площади мВПСП, ответы на раздражители регистрировали при гиперполяризации мембраны до – 80 мВ.
В качестве антагониста 5-HT1A рецепторов серотонина использовали NAN-190 (1-(2- methoxiphenil)-4-[4-(2phthalimido)butyl]piperasine hydrobromide) («Sigma»). Антагонист предварительно растворяли в этаноле, а затем в физиологическом растворе для моллюсков.
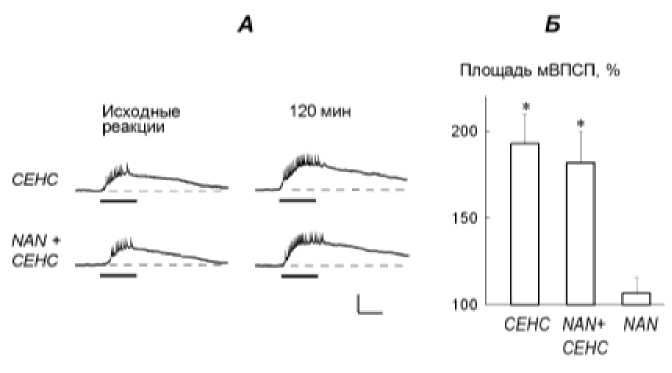
Рис. 1. Антагонист рецепторов серотонина 5-HT1A NAN-190 не влиял на индукцию синаптического облегчения ответов нейронов ЛПл1, вызванных химическими раздражениями головы виноградных улиток, при выработке ноцицептивной сенситизации. А: слева – нейронограмма исходных ответов на химические раздражения головы; справа – ответы нейронов через 120 мин после нанесения первого сенситизирующего стимула (10% раствор хинина). СЕНС - ответы нейрона контрольной сенситизируемой улитки; NAN+СЕНС – ответы нейрона животного, у которого вырабатывали сенситизацию в условиях подведения NAN-190. Утолщенная линия – время подведения слабого раствора хинина (0,25%). Калибровка – 5 мВ, 20 с. Б – Суммарный график ответов нейронов через 120-150 мин после выработки сенситизации. NAN - реакции нейронов у несенситизируемых улиток, к нейронам которых подводили NAN-190. По оси ординат – выраженные в % изменения площади мВПСП в ответах на сенсорные раздражения относительно площадей мВПСП перед выработкой сенситизации (100%). * - p<0,01, по отношению к значениям исходных реакций и ответов нейронов у несенситизируемых улиток, к которым подводили NAN-190.
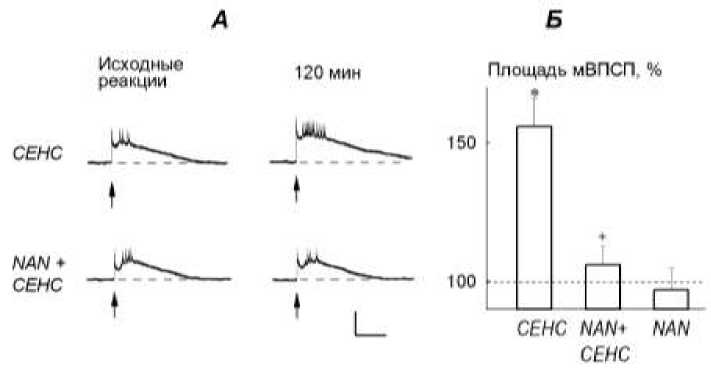
Рис. 2. NAN-190 подавлял индукцию синаптического облегчения ответов нейронов ЛПл1, вызванных тактильными раздражениями головы виноградных улиток, при выработке ноцицептивной сенситизации. * - p<0,01, по отношению к значениям исходных реакций нейронов сенситизируемых улиток, а также ответов нейронов у несенситизируемых улиток, к которым подводили NAN-190. + - p<0,01, по отношению к значениям ответов контрольных сенситизируемых улиток. Остальные обозначения как на рис. 1.
Конечная концентрация антагониста составляла 10-5 моль/л, а содержание этанола в физиологическом растворе – 0,1%. NAN-190 подводили к интернейрону под давлением сжатого воздуха через микропипетку, имевшую диаметр кончика – 20-30 мкм. Сжатый воздух (0,2 кг/см2) подавали к пипетке с помощью прибора "Neuro Phore ВН-2" (Med. Syst. Corp., США). Микроэлектрод, содержавший NAN-190, располагали на расстоянии 30-50 мкм от сомы клетки непосредственно перед началом инъекции веществ, которую начинали за 20 мин до выработки сенситизации. Сразу после выработки сенситизации инъекцию прекращали и электрод, содержавший NAN-190, удаляли из раствора. В качестве контроля использовали нейроны ЛПл1, к которым подводили 0,1% этанол в физиологическом растворе и у улиток вырабатывали сенситизацию или нейроны улиток, к которым подводили NAN-190, но сенситизирую-щих стимулов не наносили. Полученные данные усредняли, вычисляли стандартную ошибку средней. Для оценки уровня достоверности различий использовали t-критерий Стьюдента.
Результаты и обсуждение.
Аппликации 0,25%-ного раствора хинина на голову моллюска вызывали в нейроне ЛПл1 генерацию мВПСП, площадь которого составляла 346±53 мВ·с (количество нейронов, n=35). Площади мВПСП в ответах нейрона на тактильные раздражения, наносимые на голову и среднюю часть ноги, составляли соответственно 183±39 (n=35) и 118±30 мВ·с (n=35).
На 120-150-й минуте после начала выработки сенситизации во время инъекций раствора NAN-190 к нейронам ЛПл1 (n=11) площади мВПСП в ответах на химические раздражения головы были больше, чем их значения перед выработкой сенситиза-ции (рис. I, p<0,01), а также площадей мВПСП у нейронов (n=8) животных, к которым подводили NAN-190, но не вырабатывали сенситизацию (p<0,01). Вместе с тем, они не отличались от значений площадей мВПСП в ответах нейронов (n=12), сенситизируемых улиток, к которым подводили 0,1% раствор этанола (p>0,05).
На 120-150-й минуте после начала выработки сенситизации во время аппликации NAN-190 к нейронам ЛПл1 (n=13) (рис. I) площади мВПСП в ответах на тактильные раздражения головы не отличались от таковых перед выработкой сенситиза-ции (рис. 2; p>0,05) и площадей мВПСП нейронов (n=8), к которым подводили NAN-190 у несенсити-зированных животных (p>0,05). Кроме того, они были меньше площадей мВПСП в ответах нейронов (n=12) сенситизируемых улиток, которым подводили 0,1% раствор этанола (p<0,01).
В ответах на тактильные раздражения середины ноги на 120-150 мин после начала выработки сенситизации во время аппликации NAN-190 площади мВПСП у нейронов ЛПл1 (n=11) увеличились по сравнению с исходными значениями до 168±18% и они не отличались от площадей мВПСП в ответах нейронов (n=12) сенситизируемых улиток в условиях подведения 0,1% раствор этанола (p>0,05) и были больше площадей мВПСП у нейронов (n=8) животных, к которым подводили NAN-190, но не вырабатывали сенситизацию (p<0,01).
Обсуждение результатов.
Проведенные опыты показали, что во время выработки сенситизации подведение к интернейрону оборонительного поведения ЛПл1 антагониста 5-HT1A рецепторов NAN-190 приводило к избирательному подавлению облегчения ответов нейронов на раздражения механорецепторов головы улитки. Вместе с тем антагонист не оказывал влияния на синаптическое облегчение во входах нейрона ЛПл1 от хеморецепторов головы и механорецепторов ноги.
Ранее нами обнаружено [3], что в процессах индукции долговременного облегчения в сенсорных входах нейронов ЛПл1 и ППл1 от хеморецепторов головы участвуют цАМФ и зависимые от него транскрипционные факторы немедленного раннего гена С/ЕВР (CAAT/enhancer binding protein), тогда как в механизмы регуляции сенсорного входа от механорецепторов головы вовлечена протеинкиназа С и зависимый от нее транскрипционный фактор SRF (serum response factor). Исходя из этих результатов, можно предположить, что 5-HT1A-подобные рецепторы избирательно вовлечены в механизмы регуляции синаптических входов нейрона ЛПл1 от механорецепторов головы виноградной улитки за счет регуляции ими каскада молекулярных событий, включающих протеинкиназу С и SRF. Кроме того выявлено, что введение в нейрон ЛПл1 антисмысловых олигонуклеотидов к мРНК другого раннего гена zif268 (egr-1) при выработке сенсити-зации у улитки приводило к избирательному подавлению облегчения ответов в сенсорных входах как от хемо-, так и механорецепторов головы, но не механорецепторов ноги [3]. Промотер гена zif268 содержит последовательность SRE и CRE и, следовательно, его активность может регулироваться транскрипционными факторами SRF и CREB. Альтернативный вариант механизма регуляции транскрипции гена zif268 включает МАРК-семейство киназ (mitogen activated proteinkinase) [8]. В свою очередь активность МАРК может регулироваться как про-теинкиназой С и протеинкиназой А, так и независимыми от них механизмами, например, тирозинкиназными рецепторами, рецепторами глутамата, ионами кальция и др. Возможно также, что сигнальные пути от сенсорных рецепторов могут опосредоваться в нейроне ЛПл1 через другие системы вторичных посредников.
Эффекты сенситизации не ограничиваются участием в механизмах синаптической пластичности различных субтипов рецепторов серотонина и указанными системами вторичных посредников [5]. В механизмы сенситизации могут вовлекаться такие биологически активные вещества, как глутамат, ацетилхолин, опиаты, нейропептид FMRFamide, гастрин, холецистокинин и др. [2].
Полученные результаты свидетельствуют, что при выработке сенситизации 5-HT1A –подобные рецепторы избирательно вовлечены в механизмы индукции синаптического облегчения входов нейрона ЛПл1 от механорецепторов головы. Вопрос об идентификации субтипов рецепторов серотонина, вовлеченных в индукцию синаптического облечения от хеморецепторов головы, остается открытым. Как отмечено выше, синаптическое облегчение в этих входах связано с активацией аденилатциклазы. В исследованиях на нервной системе моллюска ап-лизии обнаружено, что NAN-190 незначительно влияет на активность аденилатциклазы [6]. Вместе с тем, в работе на моллюске Anodonta показано, что аденилатциклаза может активироваться через 5-НТ2А рецепторы [4]. Таким образом, одним из возможных субтипов рецепторов серотонина, опосредующих индукцию облегчения в синаптических входах нейрона ЛПл1 от хеморецепторов головы могут быть 5-НТ2А-подобные рецепторы.
Представленные результаты свидетельствуют о существовании в нейронах механизма специфической синаптической пластичности, основанного на специфичности участвующих в нем молекулярных процессов – сенситизирующие возбуждения, конвергирующие к определенным постсинаптическим рецепторам, опосредуются различными вторичными посредниками, которые активируют разные транскрипционные факторы и гены, что приводит к синтезу синапс-специфических РНК и белков избирательно регулирующих определенные синаптические связи нейронов.
Список литературы Избирательное вовлечение рецепторов серотонина в механизмы синаптического облегчения у нейронов сенситизируемой улитки
- Абрамова М.С., Нистратова В.Л., Москвитин А.А., Пивоваров А.С. Метиотепин чувствительные серотониновые рецепторы вовлечены в постсинаптический механизм сенситизации оборонительной реакции виноградной улитки//Журн. высш. нерв. деят. 2005. Т. 55, № 3. С. 385-392.
- Балабан П.М., Захаров И.С. Обучение и развитие: общая основа двух явлений. М.: Наука, 1992. 152 с.
- Никитин В.П. Новый механизм синапс-специфической нейрональной пластичности//Российский физиол. журн. им. И.М. Сеченова. 2006. Т. 92, № 4. С. 402-419.
- Шпаков А.О., Шипилов В.Н., Кузнецова Л.А., Бондарева В.М., Плеснева С.А., Перцева М.Н. Реактивность аденилатциклазной сигнальной системы нервных ганглиев моллюска Anodonta cygnea к серотонину и адренергическим агонистам//Нейрохимия. 2004. Т. 21, № 3. С. 190-197.
- Byrne J.H., Hawkins R.D. Nonassociative learning in invertebrates//Cold. Spring. Harb. Perspect. Biol. 2015. V. 7, № 5. pii: a021675.
- Cohen J.E., Onyike C.U., McElroy V.L., Lin A.H., Abrams T.W. Pharmacological characterization of an adenylyl cyclase-coupled 5-HT receptor in aplysia: comparison with mammalian 5-HT receptors//J. Neurophysiol. 2003. V. 89, № 3. P. 1440-1455.
- Golovchenko A.N., Bogodvid T.K., Muranova L.N., Gainutdinov K.L., Andrianov V.V. Serotonin modulation of premotor interneuron excitability in the snail during associative learning//BioNanoScience. 2016. V. 6, № 4. P. 450-452.
- Kharchenko O.A., Grinkevich V.V., Vorobiova O.V., Grinkevich L.N. Learning-induced lateralized activation of the MAPK/ERK cascade in identified neurons of the food-aversion network in the mollusk Helix lucorum//Neurobiol. Learn. Mem. 2010. V. 94, № 2. P. 158-166.
- Kandel E.R., Dudai Y., Mayford M.R. The molecular and systems biology of memory//Cell. 2014. V. 157, № 1. P. 163-816.
- Ogren S.O., Eriksson T.M., Elvander-Tottie E., D'Addario C., Ekström J.C., Svenningsson P., Stiedl O. The role of 5-HT(1A) receptors in learning and memory//Brain Res. 2008. V. 195. P. 54-77.
- Seyedabadi M., Fakhfouri. G., Ramezani V., Mehr S.E., Rahimian R. The role of serotonin in memory: interactions with neurotransmitters and downstream signaling//Exp. Brain Res. 2014. V. 232. P. 723-738.


