Изменение биологических свойств бактерий Staphylococcus epidermidis 33 при формировании устойчивости к ванкомицину
Автор: Кононова Людмила Ивановна, Коробов Владимир Павлович
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Биотехнология
Статья в выпуске: 5-3 т.13, 2011 года.
Бесплатный доступ
Рассмотрены некоторые биологические особенности коагулазонегативных стафилококков при формировании их устойчивости к гликопептидному антибиотику ванкомицину. Обнаружено, что селекционированный штамм Staphylococcus epidermidis 33 Vanr характеризуется снижением накопления биомассы при культивировании на богатой питательной среде, появлением множественной устойчивости к антибиотикам, значительным снижением гидрофобности клеточной поверхности, накоплением фосфолипидов в клеточных мембранах и снижением чувствительности к катионному пептиду варнерину.
Коагулазонегативные стафилококки, ванкомицин, резистентность, варнерин
Короткий адрес: https://sciup.org/148200431
IDR: 148200431 | УДК: 579.22
Alteration of bacterial biological properties of Staphylococcus epidermidis 33 as a result of vancomycin resistance formation
This work considers several biological peculiarities of coagulase-negative staphylococci occurring as a result of their resistance formation to glycopeptide antibiotic vancomycin. It was found that selected strain Staphylococcus epidermidis 33 Vanr was characterized by lowering in biomass accumulation while cultivating on rich nutrient medium, developing of multiple antibiotic resistance, marked decrease in cell surface hydrophobicity, phospholipid accumulation in cell membranes and declining in sensitivity to cationic peptide warnerin.
Текст научной статьи Изменение биологических свойств бактерий Staphylococcus epidermidis 33 при формировании устойчивости к ванкомицину
Использование гликопептидного антибиотика ванкомицина (Van) для лечения заболеваний, вызванных грамположительными микроорганизмами, введено в практику в 1958 г. и, несмотря на появление резистентных к этому антибиотику штаммов Staphylococcus epidermidis [21], а затем устойчивых к Van энтерококков [17] и золотистых стафилококков [12], он продолжает оставаться препаратом выбора для лечения инфекций, обусловленных мети-циллинрезистентными S. aureus [13], метициллин-резистентными коагулазонегативными стафилококками (КНС) [22], а также энтерококками, устойчивыми к бета-лактамным антибиотикам и аминогликозидам [1, 14].
Устойчивые к Van бактерии обладают выраженными биологическими особенностями. В частности, для штаммов S. aureus со сниженной чувствительностью к этому гликопептиду характерно существенное утолщение клеточной стенки и формирование новых мишеней действия, локализованных вдали от истинных мишеней антибиотика на плазматической мембране [9, 11]. Обнаружена также реципиентность этими штаммами детерминант резистентности к гликопептидам от энтерококков, обуславливающая возрастание уровня устойчивости стафилококков к Van до характерного для энтерококков [6, 7]. Вместе с тем, механизмы формирования устойчивости КНС к гликопептидам практически не изучены [8]. Показано лишь, что резистентные к Van КНС отличаются по некоторым свойствам от чувствительных бактерий, в частности, изменению клеточной стенки, появлению множественной устойчивости к антибактериальным препаратам, характеру сорбции антибиотика из среды культивирования. Обнаружено также, что природа устойчивости КНС к Van является гетерогенной [8], что характерно и для другого вида стафилококков – S. aureus . Для некоторых изолятов КНС, как и для S. aureus , выявлена способность к образованию биопленок в присутствии гликопептидов [10].
Несмотря на то, что штаммы КНС менее патогенны, чем штаммы S. aureus , они часто являются источником ассоциированной инфекции, а также заражения медицинских имплантатов [18]. Представленное отражает необходимость дополнительных исследований природы устойчивости КНС к Van и поиска путей ее преодоления.
В связи с этим в настоящей работе исследованы изменения физиологических характеристик коллекционного штамма S. epidermidis 33 при культивировании его на средах с возрастающими концентрациями Van с получением устойчивого к этому антибиотику варианта – S.epidermidis 33 Vanr, с оценкой чувствительности мутантного штамма к низкомолекулярному катионному пептиду варне-рину.
МАТЕРИАЛ И МЕТОДЫ
Выращивание бактерий проводили в питательной среде LB [4] на орбитальном шейкере Certomat (“Sartorius”, Германия) при 150 об/мин и температуре 370C. За динамикой роста следили по изменению оптической плотности бактериальных культур при 600 нм на спектрофотометре PD-303 (“APEL”, Япония).
Получение ванкомицинустойчивого штамма S. epidermidis 33 Vanr проведено последовательными пересевами исходного чувствительного к Van штамма S. pidermidis 33 на среду LB c повышающимися концентрациями Van. Селекцию начинали с концентрации Van в жидкой среде, близкой минимальной подавляющей концентрации (МПК) Van для данного штамма. Клеточные суспензии затем высевали на чашки с LB-агаром с той же концентрацией Van. После появления колоний их инокулировали в жидкую среду с повышенной концентрацией Van и культивировали до видимого роста. Таким образом, через 16 пассажей на жидкой среде бактерии были способны к росту в присутствии 32 мкг/мл Van.
МПК Van изучаемых штаммов определяли методом двукратных серийных разведений в 96-луночных иммунологических планшетах. В лунки, содержащие питательную среду LB, вносили бак- терии логарифмической фазы роста в конечной концентрации 105 колониеобразующих единиц/мл (КОЕ/мл). Определение чувствительности бактерий к низкомолекулярному пептиду варнерину проводили, как представлено ранее [3, 16]. Чувствительность к антибиотикам выявляли методом диффузии с дисков [5].
Степень сохранности устойчивости резистентного штамма к Van оценивали после 20 последовательных пассажей на питательной среде LB без антибиотика методом двукратных серийных разведений в иммунологических планшетах. Степень гидрофобности поверхности бактериальных клеток определи с помощью BATH-теста в двухфазной системе с гексадеканом [20].
Экстракцию и идентификацию липидов проводили по методу Блайя и Дайера [2]. Для тонкослойной хроматографии использовали пластинки Sorbfil (Россия) (сорбент – силикагель, толщина слоя 110 мкм). Разделение смеси липидов проводили в системе: хлороформ-метанол-вода (65:25:4, v/v). После разделения липидов пластинки окрашивали 10% фосфорномолибденовой кислотой в этаноле для определения общего состава липидов, 1% нингидрином в ацетоне – липидов, содержащих свободные аминогруппы, реактивом Цинцаде – фосфолипидов, α-нафтолом – гликолипидов [2].
Аутолиз исследуемых штаммов проводили в 10 mM трис HCl-буфере, pH 7.2 при 370C в течение 4 ч с перемешиванием при 150 об/мин на шейкере Cer-tomat (“Sartorius”, Германия). Для этого бактериальные культуры выращивали на среде LB до середины логарифмической фазы роста. Клетки осаждали центрифугированием (13200 об/мин, 10 мин) на центрифуге 3К30 (“Sigma”, Германия), дважды отмывали в том же режиме исходным указанным выше буфере и ресуспендировали в нем до плотности ~1.0 при 600 нм. Для активации аутолитических процессов к препаратам бактерий добавляли низкомолекулярный пептид варнерин в концентрации 1 мг/мл. Степень лизиса определяли по изменению оптической плотности клеточных суспензий при 600 нм и по количеству живых клеток постановкой теста на КОЕ, отбирая пробы ежечасно.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Обнаружено, что селекционированный в лаборатории Vanr-штамм обладал высоким уровнем устойчивости к ванкомицину (МПК ≥400 мкг/мл). Формирование Vanr-фенотипа производного штамма сопровождалось снижением интенсивности роста по сравнению с чувствительным штаммом. Сравнение динамики роста изученных штаммов представлено на рис. 1.
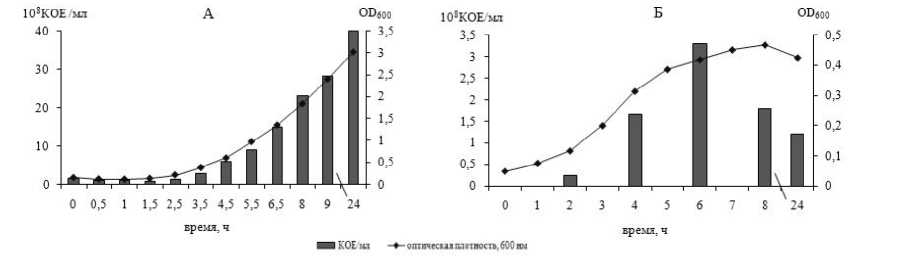
Рис. 1. Динамика роста (А) S.epidermidis 33 и (Б) S.epidermidis 33 Vanr
Важно отметить, что возрастание резистентности к Van сопровождается появлением устойчивости и к ряду других антибиотиков, обладающих различными механизмами антибактериального
Таблица. Фенотипическая резистентность исследованных штаммов
действия. Характеристика чувствительности к антибиотикам исследованных штаммов представлена в таблице.
|
Штаммы |
Антибиотики |
|||||||||||
|
Бен |
Ген |
Цеф |
Тет |
Лин |
Окс |
Риф |
Эр |
Фуз |
Лев |
Ван |
Цип |
|
|
S.epidermisis 33 |
Ч |
Ч |
Ч |
Ч |
Ч |
Ч |
Ч |
Ч |
Ч |
Ч |
Ч |
Ч |
|
S.epidermisis 33 Vanr |
У |
Ч |
Ч |
П |
У |
У |
П |
Ч |
У |
Ч |
У |
Ч |
Прим. Обозначения устойчивости к антибиотикам: У – устойчивый, П – промежуточный, Ч – чувствительный. Антибиотики: Бен – бензилпенициллин, Ген – гентамицин, Цеф – цефалексин, Тет – тетрациклин, Лин – линкомицин, Окс – оксациллин, Риф – рифампицин, Эр – эритромицин, Фуз – фузидин, Лев – левомицетин, Ван – ванкомицин, Цип – ципрофлоксацин
Большинство известных изолятов стафилококков, гетерорезистентных к Van, являются одновременно метициллин- или оксациллинрезистентны-ми, таким образом, устойчивость к Van часто связана с устойчивостью к оксациллину. Возможно, устойчивость к Van обусловлена изменениями в метаболизме клеточных стенок, что в свою очередь влияет на активность бета-лактамных антибиотиков. Экспрессия Vanr-фенотипа стафилококков не ограничивается резистентностью только к бета- лактамам, так как все они обладают различными уровнями резистентности ко многим антибиотикам [19].
После 20 последовательных пассажей на питательной среде без антибиотика Vanr-штамм сохранял высокий уровень устойчивости к Van и оставался устойчивым и к другим антибиотикам. Важно отметить, что исследования других авторов указывают на специфические особенности работы с резистентными штаммами стафилококков из-за ревертирования ванкомицинчувствительного фенотипа многих изолятов [13].
Как показало исследование поверхности клеток методом бактериальной адгезии к углеводородам, штамм S.epidermidis 33 обладает гидрофобной поверхностью. Показатель гидрофобности его поверхности составляет 45±10 %, в то же время поверхность Vanr-штамма менее гидрофобна и составляет лишь 11±4 %.
Анализ липидов клеточных мембран изучаемых штаммов выявил значительные различия в их качественном и количественном составе. Как показано на рис. 2, развитие резистентности к Van сопровождается увеличением относительного количества кардиолипина и фосфатидилглицерина в составе липидов мутантного штамма с одновременным снижением количества гликолипидов. Следует отметить появление лизилфосфатидилглицерина и лизоформ фосфолипидов, отсутствующих в составе липидов исходного штамма S.epidermidis 33. Накопление кардиолипина в клетках резистентного штамма, возможно, являясь результатом адаптации к стрессовым условиям, компенсирует нарушение жесткости клеточной стенки и ингибирует аутолиз клеток [15], а появление лизилфосфатидилглице-рина вызывает изменение заряда клеточных поверхностей, приводя к накоплению положительных зарядов на цитоплазматической мембране, что в свою очередь снижает чувствительность производного штамма к катионному пептиду варнерину. Определение МПК низкомолекулярного пептида варнерина показало возрастание устойчивости Vanr-штамма к данному антибактериальному пре- мкг/мл, что значительно превышает МПК варнери-на родительского штамма S.epidermidis 33, равную 0,25 мкг/мл.
Рис. 2. Тонкослойная хроматография полярных липи-

дов S.epidermidis 33 и S.epidermidis 33 Vanr.
Прим.: 1 – S.epidermidis 33, 2 – S.epidermidis 33 Vanr; I – моноглюкозилдиглицерид, II – кардиолипин, III – диглюкозилдиглицерид, IV - фосфатидилглицерин, V – лизилфосфа-тидилглицерин, VI – лизоформы фосфолипидов
Лизис клеток S.epidermidis 33 и S.epidermidis 33 Vanr под действием варнерина в концентрации 1 мг/мл в трис HCl-буфере, pH 7.2 в течение 4 ч показал более медленное снижение оптической плотности и количества жизнеспособных клеток в суспензии мутантного штамма (рис. 3), но несмотря на это, суспензии обоих штаммов через 24 ч не содержали живых клеток.
Таким образом, возникновение устойчивости штамма S.epidermidis 33 к Van вызвает изменение важных физиологических свойств данного микроорганизма. При этом снижение чувствительности к низкомолекулярному катионному пептиду варне-рину, возможно, происходит вследствие изменения уровня гидрофобности бактериальной поверхности, а также вследствие адаптивного накопления полярных липидов клеток.
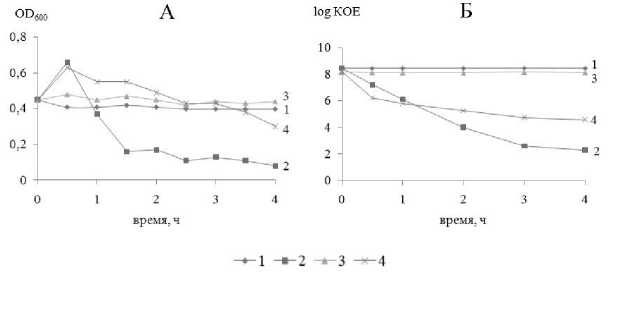
парату – МПК варнерина для него составляет ≥8
Рис. 3. Изменение оптической плотности (А) и КОЕ (Б) клеточных суспензий S.epidermidis 33 и S.epidermidis 33 Vanr под действием катионного пептида варнерина. Прим.: 1 – инкубация S.epidermidis 33 в трис-буфере, 2 – инкубация S.epidermidis
33 в присутствии варнерина в трис-буфере, 3 – инкубация S.epidermidis 33 Vanr в трис-буфере, 4 – инкубация S.epidermidis
33 Vanr в присутствии варнерина в трис-буфере
Список литературы Изменение биологических свойств бактерий Staphylococcus epidermidis 33 при формировании устойчивости к ванкомицину
- Зайцев А.А., Карпов О.И, Сидоренко С.В. Стафилококки и ванкомицин: тенденции противостояния//Антибиотики и химиотерапия. 2003. Т. 48. № 6. С. 20-26.
- Кейтс М. Техника липидологии. М.: Мир, 1975. 322с.
- Коробов В.П., Полюдова Т.В., Филатова Л.Б. и др. Активация аутолитической активности бактерий Staphylococcus epidermidis 33 низкомолекулярным катионным пептидом варнерином//Микробиология. 2010. Т. 79. № 1. С. 133-135.
- Миллер Д. Эксперименты в молекулярной генетике. М.: Мир, 1976. 394 с.
- Скала Л.З., Сидоренко С.В., Нехорошева А.Г. и др. Практические аспекты современной клинической микробиологии. М., 2004. 312 с.
- Al-Obeid S., Collatz E., Gutmann I. Mechanism of resistance to Vancomycin in Enterococcus faecium D366 and Enterococcus faecalis A256//Antimicrob. Agents Chemother. 1990. V. 34. № 2. P. 252-256.
- Arthur M., Courvalin P. Genetics and mechanisms of glycopeptide resistance in enterococci//Antimicrob. Agents Chemother. 1993. V. 37. № 8. P. 1563-1571.
- Biavasco F., Vignaroli C., Varaldo P.E. Glycopeptide resistance in coagulase-negative staphylococci//Europ. J. Clin. Microbiol. Infect. Dis. 2000. V. 19. № 6. P. 403-417.
- Cui L., Ma X., Sato K. et al. Cell wall thickening is common feature of vancomycin resistance in Staphylococcus aureus.//J. Clin. Microbiol. 2003. V. 41. № 1. P. 5-14.
- Gazolla S., Cocconcelli P.S. Vancomycin heteroresistance and biofilm formation in Staphylococcus epidermidis from food//Microbiology. 2008. V. 154. № 10. P. 3224-3231.
- Hanaki H., Kuwahara-Arai K., Boyle-Vavra S. et al. Activated cell-wall synthesis is associated with vancomycin resistance in methicillin-resistant Staphylococcus aureus clinical strains Mu3 and Mu50//J. Antimicrob. Chemother. 1998. V. 42. № 2. P. 199-209.
- Hiramatsu K., Aritaka N., Hanaki H. et al. Dissimination in Yapanese hospitals of strains Staphylococcus aureus hetero-geneously resistant to vancomycin//Lancet. 1997. V. 350. № 9092. P. 1670-1673.
- Howden B.P., Davies J.K., Johnson P.D.R. Reduced vancomycin susceptibility in Staphylococcus aureus, including vancomycin-intermediate and heterogeneous vancomycin-intermediate strains: resistance mechanisms, laboratory detection and clinical implications//Clin. Microbiol. Rev. 2010. V. 23. № 1. P. 99-138.
- Huyck M.M., Sahm D.F., Gilmore M.S. Multiple-drug resistant enterococci: The nature of the problem and an agenda for the future//Emerg. Infect. Dis. 1998. V. 4. №. 2. P. 239-249.
- Kariyama R. Increase of cardiolipin content in Staphylococcus aureus by the use of antibiotics affecting the cell wall//J. Antibiot. 1982. V. 35. № 12. P. 1700-1704.
- Korobov V.P., Lemkina L.M., Polyudova T.V. Production of a wide-spectrum antibacterial factor by Staphylococcus warneri cells//Docl. Biol. Sci. 2003. V. 390. P. 286-288.
- Leclercq R., Derlot E., Duval J., Courvalin P. Plasmidmediated resistance to vancomycin and teicoplanin in Enterococcus faecium//New Eng. J. Med. 1988. V. 319. № 3. P. 157-161.
- Livermore D.M. Antibiotic resistance in staphylococci//Intern. J. Antimicrob. Agents. 2000. V. 16. № 1. P. 3-10.
- Palazzo I.C.V., Araujo M.L.C., Darini A.L.C. First report of vancomycin-resistant staphylococci isolated from healthy carriers in Brazil//J. Clin. Microbiol. 2005. V.43. № 1. P. 179-185.
- Rosenberg M., Gutnick D., Rosenberg E. Adherence of bacteria to hydrocarbons: a simple method for measuring cell-surface hydrophobicity//FEMS Microbiol. Lett. 1980. V. 9. № 1. P. 29-33.
- Siebert W.T., Moreland N., Williams T.W.,Jr. Synergy of vancomycin plus cefazolin or cephalotin against methicillin-resistance Staphylococcus epidermidis//J. Infect. Dis. 1979. V. 139. № 4. P. 452-457.
- Sieradzki K., Roberts R.B., Serur D. et al. Heterogenously vancomycin-resistant Staphylococcus epidermidis strain causing recurrent peritonitis in a dialysis patient during vancomycin therapy//J. Clin. Microbiol. 1999. V. 37. № 1. P. 39-44.


