Изменение тактики лечения нетравматического пневмоторакса на основе применения малоинвазивных операций и термических инструментов
Автор: Шулутко А.М., Ясногородский О.О., Качикин А.С., Талдыкин М.В., Талдыкин И.М., Гандыбина Е.Г., Винарская В.А., Катанэ Ю.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 2 (36), 2014 года.
Бесплатный доступ
С 1970 по 2012 гг. в отделении торакальной хирургии ГКБ № 61 по поводу спонтанного (СП) пневмоторакса находилось на лечении 853 больных. До 1987 года единственным методом лечения пневмоторакса, принятым в клинике, было дренирование плевральной полости с активной аспирацией. Начиная с 1987 года начали применять лекарственный плевродез. Всего с 1987 по 2012 г. лекарственный плевродез выполнен 246 больным в процессе консервативного лечения пневмоторакса. С внедрением видеоэндоскопических технологий (1996) оперативная активность при лечении пневмоторакса составила 28,5%. С 1996 по 2012 г. выполнено 156 операций: 126 (80,8%) торакоскопических операций. 22-м больным (14,1%) произведена атипичная резекция легкого из мини- доступа с видеоассистенцией. В 8-ми случаях (5,1%) атипичная резекция легкого выполнена из стандартной торакотомии. 1996-2012 г. - период, когда стали внедрять малоинвазивные операции с использованием видеотехники, частота рецидива существенно снизилась. За последнее десятилетие (2003-2012 г.) наблюдалось 162 больных ятрогенным пневмотораксом (ЯП). Единственным способом лечения ЯП остается дренирование плевральной полости с активной аспирацией до полного расправления легкого и не менее 5-7 суток после расправления легкого. Ни в одном случае каких-либо осложнений, связанных с длительным дренированием плевральной полости по поводу ЯП, не наблюдали.
Спонтанный пневмоторакс, видеоторакоскопия, лекарственный плевродез, термические инструменты
Короткий адрес: https://sciup.org/142211155
IDR: 142211155 | УДК: 616-089:
Текст научной статьи Изменение тактики лечения нетравматического пневмоторакса на основе применения малоинвазивных операций и термических инструментов
Загрязнение окружающей среды, массовое курение, увеличение числа больных хроническим бронхитом ведет к росту заболеваемости буллезной эмфиземой [1]. Спонтанный пневмоторакс (СП) диагностируется у 5–7 человек на 100 тыс. населения в год, больные со СП составляют 12% от всех госпитализированных с острыми заболеваниями органов грудной полости [2]. Заболеваемость при первичном спонтанном пневмотораксе (ПСП) достигает 8,6–24 случаев на 100 тыс. человек в год [3,4]. Заболеваемость при вторичном спонтанном пневмотораксе (ВСП) составляет 8,3 случая на 100 тыс. человек [3]. ВСП наиболее часто встречается у больных хронической обструктивной болезнью легких – 26 случаев на 100 тыс. человек в год. [5]. Летальность при тяжелых клинических формах пневмоторакса достигает от 1,3% до 10,4%. [1]. Результаты лечения СП нельзя считать удовлетворительными: рецидив пневмоторакса наблюдает- ся в 20–45% случаев при лечении плевральными пункциями, после закрытого дренирования плевральной полости – в 12–18%[1]. При сочетании дренирования плевральной полости с лекарственным плевродезом рецидив СП развивается в 5,8% случаев [2]. Число рецидивов после введения тетрациклинов составляет 9–25% [6,7], талька – 8% [8]. После введения талька в плевральную полость возможны тяжелые осложнения: острый респираторный дистресс-синдром [9], эмпиема плевры [10], острая дыхательная недостаточность [10], тальк является канцерогеном [11]. Эффективность плевродеза, выполненного во время хирургических вмешательств, превосходит эффективность плевродеза, во время дренирования плевральной полости [12]. Задачами хирургического лечения пневмоторакса являются: резекция булл и субсплевральных пузырьков (blebs), ушивание дефектов легочной ткани; выполнение плевродеза[13]. Резекция булл или атипичная резекция легкого в сочетании с париетальной плеврэктомией или абразией плевры из стандртного торакотомического доступа приводит к успеху в 95% наблюдений, но сопрвождаются очевидными недостатками самой торакотомии (Getz. S., Beasly. W., 1983): частота осложнений после традиционной торакотомии по поводу СП может достигать 10,4–20%, а летальность 2,3–4,3%, что обусловлено тяжестью осложнений: эмпиема плевры, послеоперационная пневмония, тромбэмболия ветвей легочной артерии [11]. Число рецидивов после обычной торакотомии составляет от 1,5% [14] до 5,2% [11]. Развитие видеотехнологий и малоинвазивных способов оперирования открывают новые возможности при лечении СП. В последние годы стандартная торакотомия, выполняемая в связи с СП в специализированных клиниках, практически полностью вытеснена торакоскопией, а среди всех торакоскопических операций ВТС по поводу СП составляют около 45% [2]. Во многих центрах видеоассоциированная торакоскопия (ВАТ) является основным хирургическим методом терапии пневмоторакса, что связано с преимуществами метода по сравнению с открытой торакотомией: сокращение времени операции и дренирования, снижение числа постоперационных осложнений и потребности в анальгетиках, уменьшение времени госпитализации больных, менее выраженные нарушения газообмена [15–18]. По данным метаанализа Schramel и со-авт., число рецидивов пневмотораксов после ВАТ составляет 4%[14]. Другие авторы отмечают еще более низкий уровень рецидива СП после ВТС лечения – 1,3% [2], а осложнений, присущих стандартной торакотомии, не наблюдается [2]. Частота развития ятрогенных пневмотораксов: при трансторакальной игольчатой аспирации 15–37%, в среднем 10% [12, 19]; при катетеризации центральных вен – 1–10% [20, 21]; при торакоцентезе – 5–20% [22, 23]; при биопсии плевры – 10% [24]; при трансбронхиальной биопсии легких – 1–2% [25]; во время искусственной вентиляции легких – 5–15% [26].
Материалы и методы
С 1970 по 2012 гг. в отделении торакальной хирургии ГКБ № 61 по поводу пневмоторакса находилось на лечении 853 больных (1970–1986 – 144, 1987–1995 – 174, 1996–2012 – 535). До 1987 года единственным методом лечения пневмоторакса, принятым в клинике, было дренирование плевральной полости с активной аспирацией. В настоящее время для дренирования применяются силиконовые дренажи 2,5 и 3,5 мм в диаметре (рис. 1).
Для активной аспирации используются различные аппараты от ОП-1 до более современных «Элеман про 1» и «Medela» (рис. 2–5).
Начиная с 1987 года в дополнение к дренированию плевральной полости начал применяться лекарственный плевродез. Для проведения лекарственного плевродеза мы использовали тетрациклин (20 мг на 1 кг массы тела больного), морфоциклин 0,3 г (суточная доза), в последнее время – доксициклин (20 мг на 1 кг массы тела больного). Лекарственный плевродез производился как при оперативном, так и при консервативном лечении пневмоторакса. При оперативном лечении лекарственный плевродез осуществлялся введением в плевральную полость 0,8 г (максимальная суточная доза) раствора доксициклина гидрохлорида 50-ти мл 0,9% NaCl. Всего с 1987 г. по 2012 г. выполнено 246 лекарственных плевродезов в процессе консервативного лечения пневмоторакса. За период с 1987 по 1995 г. выполнено две операции – атипичные резекции легкого с использованием стандартного (традиционного) доступа – боковая торакотомия. Для атипичной резекции легкого использовались сшивающие аппараты УДО, УО, УС (рис. 6).
С внедрением видеоэндоскопических технологий (1996) оперативная активность при лечении пневмоторакса составила 28,5%. С 1996 по 2012 гг. выполнено 156 операции по поводу пневмоторакса.
Для ВТС атипичной резекции буллезно измененных участков легочной ткани применялись эндостеплеры ENDO GIA (рис. 7).
При видеоассистированных операциях из мини-доступа наиболее часто использовались сшивающие аппараты УДО – 20 и УДО – 30 как самые миниатюрные сшивающие аппараты этого ряда (рис. 8).
Для коагуляции буллезно-фиброзрно измененных участков легких и, в большей степени, для коагуляции суб-плеврпльных пузырьков (bebls) и термического плевродеза применялись следующие термические хирургические инструменты (ТХИ): СО₂-лазер «Sharplan 1080S», аппарат ар-гонусиленной коагуляции (АУК) «фотек ЕА 142», плазменная система «Plasmajet» (PJ) (рис. 9–11).
Основным оперативным пособием явилась ВТС с атипичной резекцией легкого, коагуляцией булл лазером, плазменным потоком или с помощью аргонусиленной электрокоагуляции, термической плевродеструкцией париетальной плевры этими же инструментами и лекарственным плевро-дезом раствором доксициклина гидрохлорида.
Выполнено 126 (80,8%) видеоторакоскопических операций: 100 – ВТС + атипичная резекция легкого (64,1%), 26 – ВТС + коагуляция булл и (или) деплевризированных участков легкого (16,7%).
Рисунки 12–21 демонстрируют этапы ВТС АР легкого.
Наиболее эффективна коагуляция булл и «belbs» плазменным потоком. В 2-х случаях для коагуляции использовался лазер, в 2-х – диатермокоагуляция, в 9-ти – коагуляция выполнялась с помощью АУК, в 13-ти – плазменным потоком. Цели использования ТХИ при оперативном лечении ПСП (рисунки 22–29).
22-м больным (14,1%) произведена атипичная резекция легкого из миниторакотомического доступа с видеоасси-

Рис. 1. Силиконовые дренажи 2,5 и
3,5 мм в диаметре

Рис. 2. Аспиратор ОП-1и

Рис. 3. Аспиратор
«Medela»
Рис. 4. Аспиратор «Medela»
ОП-2

Рис. 5. Аспиратор «Элма-н про 1»

Рис. 7. Эндостеплер ENDO GIA UNIVERSAL
Рис. 6. Сшивающие аппараты УДО, УО, УС

Главными причинами ЯП были: катетеризация центральной (в основном, подключичной) вены и плевральная пункция по поводу гидроторакса различного происхождения, реже баротравма при ИВЛ, еще реже при трансторакальной или трансбронхиальной пункционной биопсии легкого.
Основным поводом для перевода в отделение из других стационаров являлся «рецидив» пневмоторакса после кратковременного дренирования плевральной полости: дренаж удалялся в первые сутки (или сразу) после расправления легкого, что требовало повторного (часто многократного) дренирования плевральной полости.
Раннее удаление дренажа объяснялось опасением инфицирования плевральной полости и развитием, связанных с

Рис. 10. Аппарат аргонусиленной коагуляции «Фотек ЕА 142»

стенцией и использованием сшивающих аппаратов УДО. 8 раз (5,1%) для выполнения атипичной резекции легкого применялась традиционная торакотомия.
За последнее десятилетие (2003–2012 гг.) в торакальном отделении ГКБ № 61 наблюдалось 162 больных ятрогенным пневмотораксом (ЯП), 93 пациентов было переведено из стационаров Москвы и 69 из других отделений больницы этим осложнений – эмпиемы плевры.
Единственным способом лечения ЯП в торакальном отделении ГКБ № 61оставалось дренирование плевральной

Рис. 11. Плазменная система «Plasmajet» (PJ)
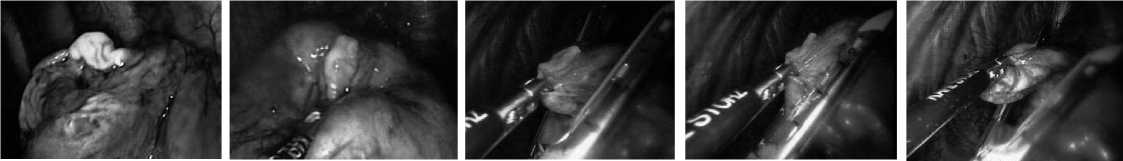
Рис. 14–16. Этапы атипичной резекции лёгкого эндостэплером ENDO GIA
Рис. 13. Фиксация (захват) верхушки лёгкого зажимом в области буллы
Рис. 12. Булла в верхушке лёгкого

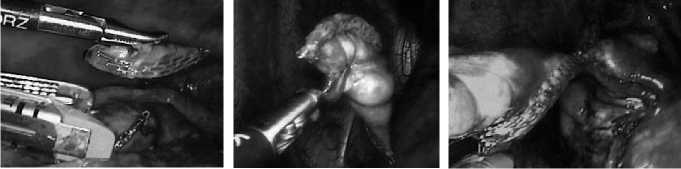
Рис. 17–19. Этапы атипичной резекции лёгкого эндостэплером ENDO GIA
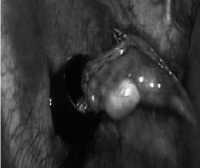
Рис. 20. Полный герметизм Рис. 21. Эвакуация резе-шва по линии резекции лёг- цированного фрагмента кого лёгкого через торако- порт

Рис. 22. Коагуляция деплеври-зированной поверхности лёгкого аппаратом аргонусиленной коагуляции «Фотек ЕА 142»

Рис. 23. Термическая плевродеструкция париеталь ной плевры аппаратом ар-гонусиленной коагуляции
«Фотек ЕА 142»
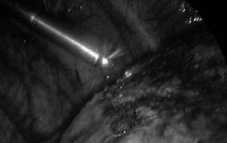

Рис. 24. Коагуляция деплев- Рис. 25. Коагуляция субплев-ризированной поверхности ральных пузырьков («belbs») лёгкого плазменной систе- «Plasmajet»
мой «Plasmajet»
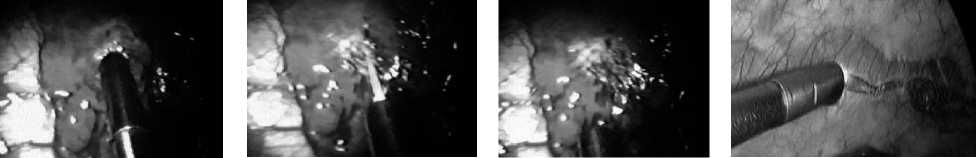
Рис. 26–29. Коагуляция субплевральных пузырьков («belbs») «Plasmajet»
полости с постоянной активной аспирацией до полного расправления легкого, и не менее 5–7 суток после расправления легкого.
Результаты
Диагностика СП основана на рентгеновских методах обследования – рентгенография легких и полипозиционная рентгеноскопия грудной клетки Рентгенологическая картина СП отличается по степени коллапса легкого (рис. 30–38).
Ограниченный СП часто приходится дифференцировать с крупными буллами (рис. 39–42).
МСКТ ОГК имеет значение не столько в диагностике пневмоторакса, сколько в выявлении его причины. На КТ ОГК хорошо видны не только крупные буллы (рис. 43), но и более мелкие (рис. 44). А также некрупные буллы при развившемся пневмотораксе в спавшемся легком (рис. 45).
Рецидивы при лечении СП методом дренирования и пункции плевральной полости наблюдались в 21,5% случаев; при дренировании с последующим лекарственным плевродезом – 5,5%, ранних рецидивов не было (после дренирования без плевродеза в ближайшие 10 дней после вы- писки рецидивный пневмоторакс развивался в 4,9% случаев). Единственное осложнение дренирования плевральной полости – подкожная эмфизема. Осложнений, связанных с выполнением лекарственного плевродеза, не наблюдалось. Для оценки непосредственных результатов оперативного лечения СП были определены критерии эффективности герметизации легкого (табл. 1).
Таблица 1
Критерии оценки непосредственных результатов оперативного лечения СП
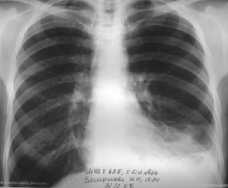
Рис. 30. Коллапс левого лёгкого I степени
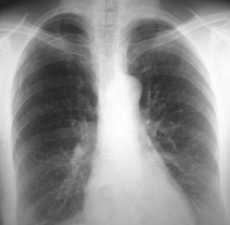
Рис. 31. Коллапс правого лёгкого I степени
|
Критерии эффективности герметизации легкого |
баллы |
|
Полное расправление легкого + отсутствие поступления воздуха |
6(4+2) хор. |
|
Полное расправление легкого + поступление воздуха по дренажам |
5(4+1) удовл. |
|
Коллапс легкого I степени + отсутствие поступления воздуха |
5(3+2) удовл. |
|
Коллапс легкого I степени + поступление воздуха по дренажам |
4(3+1) неуд. |
|
Коллапс легкого II степени + отсутствие поступления воздуха |
4(2+2) неуд. |
|
Коллапс легкого II степени + поступление воздуха по дренажам |
3(2+1) неуд. |
|
Коллапс легкого III степени + отсутствие поступления воздуха |
3(1+2) неуд. |
|
Коллапс легкого III степени + поступления воздуха по дренажам |
2(1+1) неуд. |
Результат ниже 5 баллов считается неудовлетворительным
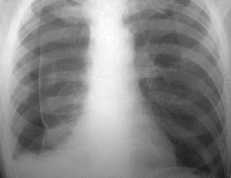
Рис. 32. Коллапс правого лёгкого II степени
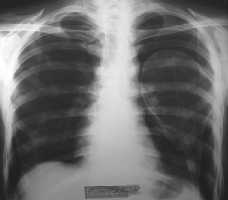
Рис. 34. Коллапс левого лёгкого II-III степени
Количество и результаты операций по поводу СП представлены в таблице 2.
Непосредственные результаты ВТС АР легкого всегда были только хорошими (6 и 5 баллов), рецидивов не на-
Количество и результаты операций по поводу СП
Таблица 2
|
Тип операции |
Количество |
Непосредственные результаты (баллы) |
Число рецидивов |
|
ВТС, атипичная резекция лёгкого |
100 |
91–6 баллов, 9–5 баллов |
0 (0%) |
|
ВТС, коагуляция булл |
26 |
15–6 баллов, 9–5 баллов, 1–4 балла, 1–3 балла |
2 (7,7%) |
|
Атипичная резекция лёгкого из минидоступа |
22 |
19–6 баллов, 2–5 баллов, 1–4 балла |
1 (4,5%) |
|
Атипичная резекция лёгкого из традиционного доступа |
10 (2 до 1996 г.) |
8–6 баллов, 2–5 баллов |
0 (0%) |
Атипичная резекция лёгкого при ВТС часто сочеталась с коагуляцией булл
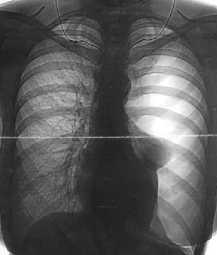
Рис. 36 Коллапс левого лёгкого III степени (цифровая флюрограмма)
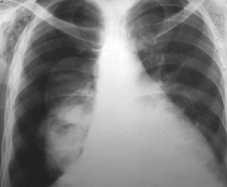
Рис. 33 Коллапс правого лёгкого II-III степени. Видна подкожная эмфизема
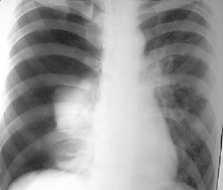
Рис. 35. Коллапс правого лёгкого III степени
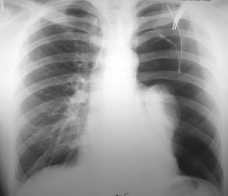
Рис. 37 Коллапс левого лёгкого III степени. Плевральная полость дренирована
блюдалось. После ВТС-коагуляции булл отмечено два неудовлетворительных непосредственных результата (4 и 3 балла), в обоих случаях коагуляция булл производилась с помощью диатермокоагуляции. Рецидивы наблюдались в 7,7%. Из 22 атипичных резекций легких неудовлетворительный результат (4 балла) зафиксирован один раз, рецидивы развивались в 4,5%
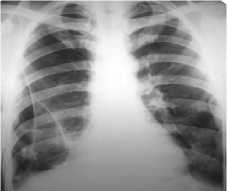
Рис. 38. Ограниченный коллапс правого лёгкого. Плевральная полость дренирована
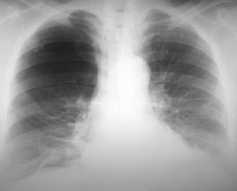
Рис. 39. Крупная булла в верхней доле правого лёгкого (прямая проекция)
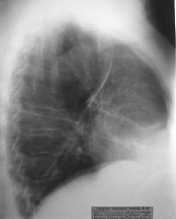
Рис. 40. Крупная булла в верхней доле правого лёгкого (боковая проекция)
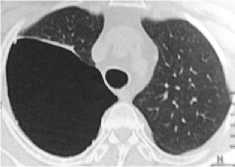
Рис. 41. Та же була (МСКТ ОГК)
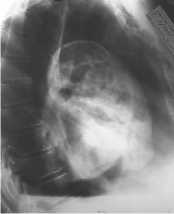
Рис. 42. Крупная булла в верхней доле в спавшемся лёгком
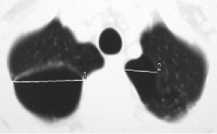
Рис. 43. Крупные буллы в лёгких
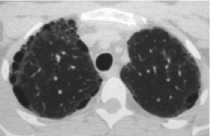
Рис. 44. Разнокалиберные буллы лёгких
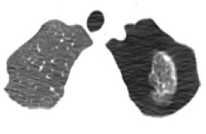
Рис. 45. Пневмоторакс слева. Мелкие буллы в верхней доле спавшегося лёгкого
случаев. После операций из традиционного доступа непосредственные результаты были хорошими, рецидивов не было. Отмечено два осложнения после ВТС-операций (1,6%): в обоих случаях после видеоторакоскопичского вмешательства сохранялся коллапс легкого при активном поступлении воздуха по плевральным дренажам (4 и 3 балла), что потребовало выполнение торакотомии и ушивание дефектов легкого в зонах электрокоагуляции. Наблюдалось одно осложнение (4,5%) после атипичной резекции легкого из мини-доступа с видеоассистенцией: продолжающееся внутриплевральное кровотечение. Осложнения после операций из традиционного доступа: в 10% случаев отмечалось нагноение послеоперационной раны, у 20% больных развилась послеоперационная пневмония. Ни в одном случае каких-либо осложнений, связанных с длительным дренированием плевральной полости по поводу ЯП при расправленном легком, не наблюдалось. Выявлено два рецидива после 126 видеоторакоскопических вмешательств, что составило 1,6%. Оба рецидива развились после ВТС-электрокоагуляции булл, в последующим диатермокоагуляция булл не применялась. С этой целью использовались плазменные потоки (ПП), СО2-лазер и АУК. Наиболее удобна и эффективна коагуляция булл ПП.
1970–1986 гг. – период, когда единственным методом лечения пневмоторакса было дренирование плевральной полости с постоянной активной аспирацией, частота рецидива составляла 21,5%;
1987–1995 гг. – период, когда дренирование плевральной полости дополнялось лекарственным плевродезом, частота рецидива составляла 5,5%; 1996–2011 гг. – период, когда стали внедряться малоинвазивные операции с использованием видеотехники, частота рецидива снизилась до 1,7%. В 2012 г., когда ВТС АР легкого с коагуляцией belbs, термическим и лекарственным плевродезом стала методом выбора, рецидивов при сроке наблюдения до нескольких месяцев не отмечено.
Обсуждение
Цели лечения СП: разрешение пневмоторакса (расправление легкого) и предотвращение повторных пневмотораксов (профилактика рецидивов).
Лекарственный плевродез при консервативном лечении СП уменьшает число рецидивов (5,5%).
ВТС с коагуляцией буллезно измененных участков легкого без атипичной резекции легкого не обеспечивает надежную профилактику рецидива пневмоторакса, частота рецидивов при этой методике достигает 7,7%, кроме того, возможны неудовлетворительные непосредственные результаты, особенно при использовании диатермокоагуляции. Оптимальным вмешательством («золотым стандартом») при ПСП можно признать ВТС АР фиброзно-буллезно измененной верхушки легкого с коагуляцией субплевральных пузырьков (belbs), в сочетании с термической плевродеструкцией и лекарственным плевродезом. При ВСП тяжесть основного легочного и сопутствующих заболеваний могут послужить противопоказанием для оперативного лечения [11]. В таких случаях, когда имеются противопоказания к проведению однолегочной вентиляции, целесообразно дренирование плевральной полости с постоянной активной аспирацией и выполнением лекарственного плевродеза, что позволяет уменьшить число рецидивов.
Для дренирования плевральной полости по поводу пневмоторакса с одинаковой эффективностью могут использоваться дренажные трубки с внутренним диаметром 2,5 и 3,5 мм, но не менее 2,5 мм. Трубки малого калибра (10– 14 F) по своей эффективности не уступают трубкам большого калибра (20–24 F) [27, 28] (1 French (F) = 1/3 мм).
Ятрогенный пневмоторакс в отличие от спонтанного, развивается на фоне здоровой легочной ткани или изменений легочной паренхимы, недостаточных для спонтанного разрыва легкого, поэтому ЯП является показанием только к консервативному лечению. При этом важно, чтобы активная аспирация продолжалась сколько угодно долго, до полного расправления легкого, и не менее 5–7 суток после расправления, до развития спаечного процесса в плевральной полости. При расправленном легком не существует опасности инфицирования плевральной полости и развития эмпиемы плевры, так как нет полости в плевре.
Для коагуляции мелких булл, деплевризированных поверхностей легкого, термической плевродеструкции ПП имеют преимущества по отношению к другим термическим факторам.
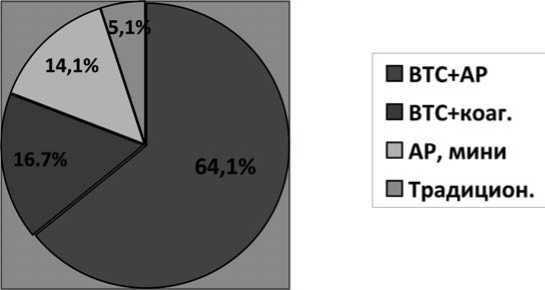
Рис. 46. Диаграмма 1. Эволюция методов оперативного лечения СП 1970–2012 гг.
За более чем 40-летний период наблюдений прослеживается существенная эволюция тактики лечения больных СП с отчетливой тенденцией к росту оперативной активности за счет внедрения и развития малоинвазивных вмешательств (технологий).
Почти 95% вмешательств приходится на малоинвазивные видеосопровождаемые операции. 80,8% составляют ВТС-вмешательства. Операцией выбора при хирургическом лечении СП становится ВТС с атипичной резекцией легкого в сочетании с коагуляцией мелких булл, термической плевродеструкцией и лекарственным плевродезом. Малоинвазивные оперативные вмешательства, рациональное выполнение лекарственного плевродеза при консервативном лечении позволили значительно улучшить результаты лечения больных СП, что проявилось уменьшением частоты и тяжести осложнений и числа рецидивов.
Выводы
-
1. С внедрением в хирургическую практику малоинвазивных технологий произошла существенная эволюция тактики лечения больных СП, выразившаяся ростом оперативной активности.
-
2. Методом выбора хирургического лечения СП становится ВТС АР фиброзно-буллезно измененной верхушки легкого с коагуляцией субплевральных пузырьков (belbs), в сочетании с термической плевродеструкцией париетальной плевры и лекарственным плевродезом.
-
3. При наличии противопоказаний к проведению однолегочной вентиляции оптимальным является дренирование плевральной полости с постоянной активной аспирацией и выполнением лекарственного плевродеза.
-
4. Для коагуляции мелких булл, деплевризированных поверхностей легкого, термической плевродеструкции париетальной плевры наиболее эффективно использование ПП.
-
5. Выбранная тактика лечения СП позволила снизить частоту осложнений и рецидивов.
-
6. При лечении ЯП важно, чтобы активная аспирация продолжалась не менее 5–7 суток после полного расправления легкого.
Тел.: 8(964) 505-67-47 (моб.), 8(499) 245-45-82 (раб).
Список литературы Изменение тактики лечения нетравматического пневмоторакса на основе применения малоинвазивных операций и термических инструментов
- Рабеджанов М.М. Роль видеоторакоскопии в диагостике и выборе метода лечения спонтанного пневмоторакса. Автореф. дис.. к.м.н. М., 2007. 25 с.
- Шулутко А.М., Овчинников А.А., Ясногородский О.О., Мотус И.Я. Эндоскопическая торакальная хирургия. М.: «Медицина», 2006, 392 с.
- Melton L.J., Hepper N.G.G., Offord K.P. Incidence of spontaneous pneumothorax in Olmsted County, Minnesota: 1950 to 1974//Am. Rev. Respir. Dis. 1979. Vol. 120. P. 1379-1382.
- Bense L., Wiman L.G., Hedenstierna G. Onset of symptoms in spontaneous pneumothorax: correlations to physical activity//Eur. J. Respir. Dis. 1987. Vol.71. P. 181-186.
- Primrose W.R. Spontaneous pneumothorax: a retrospective review of etiology, pathogenesis and management//Scott. Med. J. 1984. Vol. 29. P. 15-20.
- Light R.W., O'Hara V.S., Moritz T.E. et al. Intrapleural tetracycline for the prevention of recurrent spontaneous pneumothorax: results of a Department of Veterans Affairs Cooperative Study//JAMA. 1990. Vol.264. P. 2224-2230.
- Alfageme I., Moreno L., Heurtas C. et al. Spontaneous pneumothorax: long term results with tetracycline pleurodesis//Chest. 1994. Vol. 106. P. 347-350.
- Almind M., Lange P., Viskum K. Spontaneous pneumoThorax: comparison of simple drainage, talc pleurodesis and tetracycline pleurodesis//Thorax. 1989. Vol. 44. P. 627-630.
- Rinaldo J.E., owens G.R., Roger R.M. Adult respiratory distress syndrome following intrapleural instillation of talc//J. Thorac. Cardiovasc. Surg. 1983. Vol. 85. P. 523-526.
- Kennedy L., Rusch V.W., Strange C. et al. Pleurodesis using talc slurry//Chest. 1994. Vol. 106. P. 342-346.
- Моспанова Е.В. Лекарственный плевродез в лечении спонтанного пневмоторакса и гидроторакса. Дис..к.м.н. М., 1993. 106 с.
- Noppen M., Schramel F. Pneumothorax//Eur. Respir. Mon. 2002. Vol. 22. P. 279-296.
- Henry M., Arnold T., Harvey J. On behalf of the BTS Pleural Disease Group, a subgroup of the BTS Standards of Care Committee. BTS guidelines for the management of spontaneous pneumoThorax//Thorax. 2003. Vol. 58 (Suppl. II). ii39-ii52.
- Schramel F.M., Postmus P.E., Vanderschueren R.G. Current aspects of spontaneous pneumothorax//Eur. Resp. J. 1997. Vol. 10. P. 1372-1379.
- Atta H.M., Latouf O., Moore J.E. et al. Thoracotomy versus video-assisted thoracoscopic pleurectomy for spontaneous pneumothorax//Ann. Surg. 1997. Vol. 63. P. 209-1216.
- Radberg G., Dernevik L., Svanik J., Thune A. A comparative retrospective study of thoracoscopy versus thoracotomy for the treatment of spontaneous pneumothorax//Surg. Laparosc. Endosc. 1995. Vol.5. P. 90-93.
- Weatherford D.A., Stephenson J.E., Taylor S.M., Backhurst D. Thoracoscopy versus thoracotomy; indications and advantages//Ann. Surg. 1995. Vol. 61. P. 83-86.
- Sekine Y., Miyata Y., Yamada H. et al. Video-assisted thoracoscopic surgery does not deteriorate postoperative pulmonary gas exchange in spontaneous pneumothorax patients//Eur. J. Cardiothorac. Surg. 1999. Vol. 16. P. 48-53.
- Noppen M., De Mey J., Meysman M. et al. Percutaneous cutting biopsy of localised pulmonary, mediastinal and pleural disease with an automatic disposable guillotine soft tissue needle: preliminary results//Chest. 1995. Vol. 107. P. 1615-1620.
- Mansfield P.F., Hohn D.C., Fornage B.D. et al. Complications and failures of subclavian vein catheterization//N. Eng. J. Med. 1994. Vol. 331. P. 1735-1738.
- Lockwood A.H. Percutaneous subclavian vein catheterization. Too much of a good thing?//Arch. Intern. Med. 1984. Vol.144. P. 1407-1408.
- Collins T.R., Sahn S.A. Thoracocentesis: clinical value, complications, technical problems and patients experience//Chest. 1987. Vol. 91. P. 817-822.
- Grogan D.R., Irwin R.S., Channick R. et al. Complications associated with thoracocentesis. A prospective, randomized study comparing three different methods//Arch. Intern. Med. 1990. Vol. 150. P. 873-877.
- Blasco L.H., Hernandez I.M.S., Garrido V.V. et al. Safety of transbronchial biopsy in outpatients//Chest. 1991. Vol. 99. P. 562-565.
- Poe R.H. Sensitivity, specificity, and predictive values of closed pleural biopsy//Arch. Intern. Med. 1984. Vol. 144. P. 325-328.
- Gammon R.B., Shin M.S., Buchalter S.E. Pulmonary barotrauma in mechanical ventilation. Patterns and risk factors//Chest. 1992. Vol. 102. P. 568-572.
- Minami H., Saka H., Senda K. et al. Small calibre catheter drainage for spontaneous pneumothorax//Am. J. Med. Sci. 1992. Vol. 304. P. 345-347.
- Conces Jr. D.J., Tarrer R.D., Cory Gray W. et al. Treatment of pneumothoraces utilising small calibre Chest tubes//Chest. 1988. Vol. 94. P. 55-57.


