Изменения спектра поглощения никотинамида в водном растворе
Автор: Конькова Е.П., Затрудина Р.Ш.
Журнал: Математическая физика и компьютерное моделирование @mpcm-jvolsu
Рубрика: Химическая физика
Статья в выпуске: 13, 2010 года.
Бесплатный доступ
Рассматривается влияние растворителя на спектр поглощения никотинамида. Спектр погло- щения вычисляется полуэмпирическими методами. Представлены результаты для никотинамида в вакууме и водном растворе. Результаты для раствора с различной концентрацией сравнивают- ся с доступными экспериментальными данными. Изменения спектра поглощения никотинамида связываются со структурными особенностями молекулы.
Органические молекулы, сольватация, полуэмпирические методы, спектр поглощения
Короткий адрес: https://sciup.org/14968657
IDR: 14968657 | УДК: 53.047
Changes of nicotinamid absorption spectrum in water solution
The solvent influence on nicotinamid absorption spectrum is considered. Nicotinamid absorption spectrum is calculated by semi-empirical methods. Results for nicotinamid in vacuo and water solution are presented. Comparison is made between results for solution with various concentration and available experimental data. Changes of nicotinamid absorption spectrum are connected with the structural features of this molecule.
Текст научной статьи Изменения спектра поглощения никотинамида в водном растворе
Витамин В5, чаще называемый витамином РР (от англ. pellagra preventing factor – антипелларги-ческий фактор), химически представляет собой два вещества, обладающие одинаковой витаминной активностью: никотиновую кислоту и никотинамид. Никотиновая кислота и ее амид стали известны еще в прошлом веке в связи с исследованиями никотина. Однако связь тяжелого заболевания – пеллагры с недостатком в диете витамина РР была установлена позднее. Биохимическую роль витамин В5 играет в форме кофермента никотинамидадениндинуклеотида. Этот кофермент входит в многочисленную группу дегидрогеназ, принимающих участие почти в 150 различных биохимических реакциях дегидрирования, окисления, N-алкилирования, изомеризации, в восстановлении нитрата до нитрита и далее до аммиака, фотосинтезе, дыхании, энергетическом обмене, анаэробном расщеплении углеводов и т. д. [5]. На рисунке 1 представлена структурная формула никотинамида.
Рис. 1. Структурная формула никотинамида [5]
Большинство органических реакций протекает в жидкой фазе. Очень часто растворитель изменяет не только выходы конечных продуктов, но и механизм реакции [3]. Роль воды в клетках определяется ее химическими и структурными свойствами. Эти свойства связаны с малыми размерами молекул, их полярностью и способностью соединяться друг с другом водородными связями. Вода в клетке присутствует в двух формах: свободная и связанная. Свободная составляет 95 % всей воды в клетке, используется как растворитель и дисперсионная среда для коллоидной системы стратоплазмы. На долю связанной воды приходится 4–5 % от всей воды в клетке. Из-за симметричного распределения зарядов молекула воды действует как диполь. Дипольный момент обусловливает способность воды активно вступать во взаимодействие с различными веществами.
1. Расчет спектра поглощения никотинамида
Для расчета спектра поглощения были использованы полуэмпирические версии метода Хартри-Фока, с которыми подобные задачи решаются достаточно надежно [3; 6; 8]. Методом PM3 осуществлялась оптимизация геометрии, проводился расчет колебательного спектра. Метод РМ3 является версией метода INDO (частичное пренебрежение дифференциальным перекрыванием), параметризованной для расчета органических молекул. В работе [8] показано, что метод РМ3 позволяет получать результаты, наиболее близкие к экспериментальным. Методом Zindo/S вычислялись электронные переходы никотинамида. Метод Zindo/S является версией метода INDO, параметры которой специально подобраны для воспроизведения УФ и видимых оптических переходов.
Методом РМ3 проводилась оптимизация геометрии никотинамида, затем для найденной конфигурации выполнялся расчет частот колебаний в гармоническом приближении. Структуре оптимизированной молекулы отвечал набор положительных частот нормальных колебаний и, следовательно, точка минимума на поверхности потенциальной энергии системы.
Методом Zindo/S с учетом конфигурационного взаимодействия вычислялся электронный спектр никотинамида. Электронно-колебательный спектр никотинамида аппроксимировался гауссовой кривой, ширина которой оценивалась по разности между верхней и нижней частотами колебательного спектра [1; 2; 4].
Для определения влияния воды на спектр поглощения никотинамида моделировались непрерывные с постоянной плотностью макроскопические условия, то есть создавались периодические граничные условия. Оптимизированная молекула никотинамида помещалась в периодический ящик, линейные размеры которого полагались равными удвоенным линейным размерам исследуемой молекулы. Затем, при данной начальной концентрации раствора, проводилась оптимизация геометрии и расчет электронного спектра. В процессе дальнейшего уменьшения концентрации раствора, путем пропорционального увеличения размеров периодического ящика, были рассчитаны длины волн электронных переходов никотинамида в растворе с различной концентрацией. Перед расчетом электронного перехода никотинамида в растворе с различной концентрацией проводилась предварительная оптимизация геометрии системы.
2. Результаты и обсуждение
Зависимость длины волны электронного перехода из основного состояния в первое возбужденное никотинамида от концентрации раствора приведена на рисунке 2.
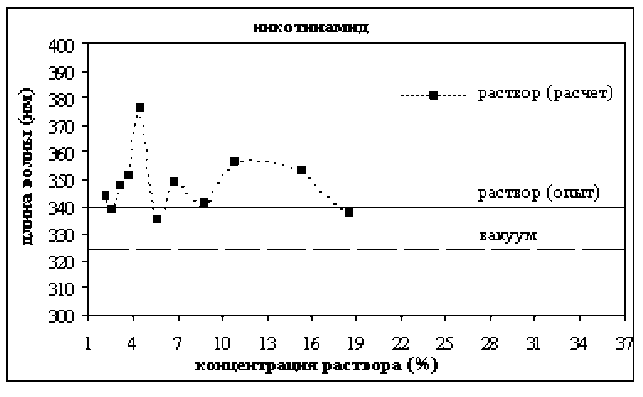
Рис. 2. Зависимость длины волны электронного перехода никотинамида от концентрации раствора
Из рисунка 2 видно, что максимальный сдвиг длины волны составляет 51 нм (концентрация 4,5 %), минимальный сдвиг длины волны составляет 11 нм (концентрация 5,6 %).
Спектры поглощения никотинамида в вакууме и реальном растворе [7] представлены на рисунке 3. Электронные переходы обозначены вертикальными линиями.
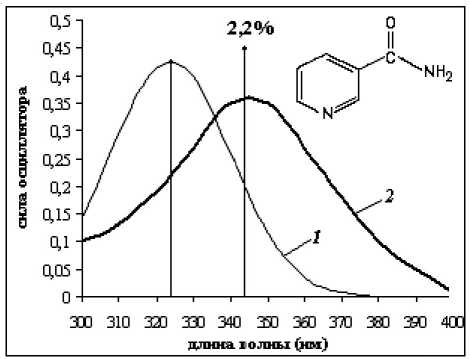
Рис. 3. Спектры поглощения никотинамида и электронные переходы: 1 – в вакууме; 2 – в растворе (опыт [7])
Обычно для описания взаимодействия растворенного соединения с растворителем рассматривают дискретные системы, содержащие 200–300 молекул растворителя [3]. Из рисунка 3 видно, что при концентрации раствора 2,2 % (300 молекул воды) для длины волны электронного перехода никотинамида наблюдается наилучшее согласие с экспериментом. Длинноволновый сдвиг электронного перехода никотинамида при данной концентрации составил 19 нм по сравнению с вакуумом. Расчет при концентрации раствора менее 2,2 % не был реализован в связи с недостатком вычислительных ресурсов.
На рисунке 4 представлена трехмерная модель молекулы никотинамида в периодическом ящике при концентрации раствора 2,2 % и комплекс, образованный молекулой никотинамида и связанными с ней водородными связями молекулами воды.
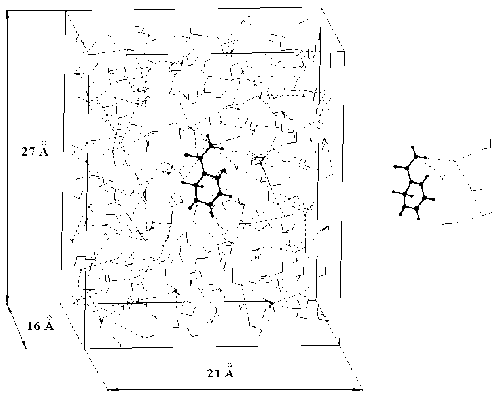
Рис. 4. Трехмерная модель молекулы никотинамида в периодическом ящике при концентрации раствора 2,2 % и комплекс, образованный молекулой никотинамида и связанными с ней водородными связями молекулами воды
100 Е.П. Конькова, Р.Ш. Затрудина. Изменения спектра поглощения никотинамида в водном растворе
Из рисунка 4 видно, что общее число молекул воды, принявших участие в образовании комплекса, равно 6. Четыре молекулы воды образуют незамкнутую цепочку, в которой атом кислорода одной молекулы связан водородной связью с атомом водорода другой. Непосредственно с молекулой никотинамида связаны водородной связью 2 молекулы воды. Одиночная молекула воды связана с атомом азота карбонильной группы никотинамида.
В зависимости от концентрации раствора в образовании водородных связей с никотинамидом принимало участие разное количество молекул воды. Однако во всех случаях образования комплекса присутствовала также связь молекулы воды с атомом азота карбонильной группы никотинамида.
Существование связи между атомом азота молекулы никотинамида и атомом водорода молекулы воды свидетельствует о перераспределении заряда внутри молекулы никотинамида в растворе, в результате которого в области карбонильной группы образовалась повышенная плотность отрицательного заряда, а в районе пиридинового кольца – повышенная плотность положительного заряда. Такое распределение заряда внутри молекулы никотинамида привело к повышению энергии электронного перехода, локализованного преимущественно на связи N=С пиридинового кольца. Этим обусловливается длинноволновой сдвиг спектра поглощения никотинамида в растворе.
3. Выводы
Длинноволновой сдвиг спектра поглощения никотинамида в растворе связан с образованием повышенной плотности положительного заряда в районе пиридинового кольца молекулы, что приводит к повышению энергии электронного перехода, локализованного преимущественно на связи N=С пиридинового кольца.
Список литературы Изменения спектра поглощения никотинамида в водном растворе
- Баранов, В./В. Баранов, Л. Грибов//Оптика и спектроскопия. -1978. -Т. 45. -С. 463-471.
- Баранов, В./В. Баранов, Л. Грибов//Журнал прикладной спектроскопии. -1979. -Т. 31. -С. 476-479.
- Бурштейн, К. Я. Квантово-химические расчеты в органической химии и молекулярной спектроскопии/К. Я. Бурштейн, П. П. Шорыгин. -М.: Наука, 1989. -98 с.
- Грибов, Л. Методы расчета электронно-колебательных спектров многоатомных молекул/Л. Грибов, В. Баранов, Б. Новосадов. -М.: Наука, 1984. -325 с.
- Калоус, В. Биофизическая химия: пер. с чеш./В. Калоус, З. Павличек. -М.: Мир, 1985. -466 с.
- Немухин, А. В./А. В. Немухин, И. М. Колесников, В. А. Винокуров//Журн. структур. химии. -1995. -Т. 36, № 3. -С. 410-417.
- Carrie, K./K. Carrie, G. Staerkel//Lasers in Surgery and Medicine. -1999. -V. 24. -P. 29.
- Seeger, D./D. Seeger, C. Korzeniewski, W. Kowalchyk//Phys. Chem. -1991. -V. 95. -P. 68.


