Изменения спектра производных фибринопептида в плазме крови при действии о-изобутил-s-(2-диэтиламиноэтил) метилтиофосфоната
Автор: Краснов И.А., Подольская Е.П., Гончаров Н.В., Бабаков В.Н., Глашкина Л.М., Ермолаева Е.Е., Дубровский Я.А., Прокофьева Д.С., Войтенко Н.Г., Смолихина Т.И., Поляков Н.Б., Радилов А.С., Краснов Н.В.
Журнал: Научное приборостроение @nauchnoe-priborostroenie
Рубрика: Масс-спектрометрия для биотехнологии. Интерпретация данных, методология, применение
Статья в выпуске: 4 т.18, 2008 года.
Бесплатный доступ
Известно, что при воздействии фосфорорганических соединений (ФОС) на организм происходит подавление активности ряда ключевых ферментов, что подтверждается простыми методами лабораторной и клинической биохимии. Однако диагностика при хроническом действии малых доз ФОС или в отдаленные сроки после острой интоксикации затруднена вследствие отсутствия подавления или восстановления активности этих ферментов. Определение пептидного спектра плазмы или сыворотки крови может служить альтернативным и более чувствительным методом диагностики интоксикации. В данной работе приведены пептидные спектры плазмы и сыворотки крови крыс и человека, полученные при субхроническом воздействии российского VX (RVX) на крыс in vivo или однократном воздействии на кровь человека in vitro. Показано, что основной пептидный фон в плазме крови или сыворотки человека и крысы после воздействия RVX составляют производные фибринопептида А, что свидетельствует об инактивации экзопептидаз при воздействии RVX.
Короткий адрес: https://sciup.org/14264569
IDR: 14264569 | УДК: 577.112.6
Differences in spectra of fibrinopeptide derivatives in blood plasma after exposure to o-isobutyl-s-2-diethylaminoethyl methylphosphonothiolate
It is a well-known fact that organophosphates (OP) inhibit several major enzymes, and this fact can be easily proved by simple laboratory and clinical biochemistry methods. On the other hand, diagnostics of low dosed chronic OP action, or their delayed effects after subacute intoxication is a serious problem because of lack of inhibition or recovery of the enzymes activity. Determination of peptide or serum blood plasma spectrum can serve an alternative and more sensitive method for intoxication diagnostics. In this paper, we demonstrate data on peptide spectra of rat plasma or serum after subchronic intoxication with Russian VX (RVX) in vivo, and that of human plasma or serum after human blood exposure to RVX in vitro. It is shown that the principal peptide plasma or serum component after RVX exposure is peptides derivatives of fibrinopeptide A, thus showing inactivation of exopeptidases under RVX exposure.
Текст научной статьи Изменения спектра производных фибринопептида в плазме крови при действии о-изобутил-s-(2-диэтиламиноэтил) метилтиофосфоната
В настоящее время уничтожение химического оружия в соответствии с федеральной целевой программой "Уничтожение запасов химического оружия в Российской Федерации" является одной из приоритетных технологических задач. Однако существует опасность для персонала, участвующего в выполнении работ, которая может быть связана как с однократным острым поражением в аварийных ситуациях, так и с хроническим отравлением малыми дозами отравляющих веществ (ОВ) [1]. Доказательством поражения ОВ может служить изменение биохимической активности определенных ферментов, так называемых биомаркеров интоксикации. Так, известными биомаркерами острой и подострой интоксикации организма фосфорорганическими соединениями (ФОС) являются ферменты ацетилхолинэстераза (АХЭ) и бутирилхолинэстераза (БХЭ), активность которых снижается. Из перечня ФОС наиболее токсичным считается О-изобутил-S-(2-диэтил-аминоэтил)метилтиофосфонат — российский VХ (RVX). Как и другие ФОС, RVX обладает цитотоксическим действием на клетки нервной системы, печени, системы крови, а также вызывает неблагоприятные эффекты при длительном воздействии субтоксических концентраций [2]. Однако диагностика при действии малых доз ФОС вообще и RVX в частности затруднена отсутствием подавления активности АХЭ или БХЭ.
В последние годы активно развивается область протеомики, которая получила название пептидо-мика [3–5]. Это направление достаточно перспективно при поиске биомаркеров различных патологических состояний, в том числе и при интоксикации. Воздействие ОВ на организм приводит к появлению нехарактерных для здорового состояния соединений, которые могут быть детектированы тем или иным способом. К таким соединениям в первую очередь относятся белки и пептиды крови. Набор низкомолекулярных пептидов можно рассматривать как "молекулярный отпечаток" состояния биологических систем, или "роспись" (signature). Состояние пептидного спектра ("пептидом", "деградом") отражает состояние определенных белков-ферментов, активность или сам факт существования которых чрезвычайно сложно измерить прямыми биохимическими методами [6, 7]. С точки зрения специфичности и чувствительности наиболее удобным методом для анализа пептидов является масс-спектрометрия (МS), а применительно к массовому анализу наиболее подходящим методом представляется масс-спектрометрия с ионизацией лазерной десорбцией в присутствии матрицы (MALDI).
Целью данной работы было изучение пептидного спектра низкомолекулярной фракции плазмы крови крыс при интоксикации RVX, а также пептидного спектра плазмы крови человека при взаимодействии с RVX in vitro.
МАТЕРИАЛЫ И МЕТОДЫ
Субхроническую интоксикацию крыс обеспечивали добавлением RVX в питьевую воду животных в течение трех недель, из расчета ежедневного потребления вещества в дозе 1/100 ЛД50. Низкомолекулярную фракцию пептидов плазмы крови крыс получали путем осаждения белков плазмы ацетонитрилом с 2 % уксусной кислоты в соотношении 1 : 2 в течение 30 мин при 4 °С с последующим центрифугированием при 10 000 g в течение 30 мин. Затем осадок перерастворяли в 0.1 % растворе трифторуксусной кислоты (ТФУ), а не-растворившуюся фракцию из неосажденных на предыдущей стадии белков удаляли центрифугированием при 10000 g в течение 10 мин. Пробу обессоливали с помощью мембраны с привитой фазой С-18, помещенной в микроколонку, после чего пептиды, которые связались с мембраной, смывали на мишень 60 %-м раствором ацетонитрила в 0.1 %-м ТФУ, содержащим а-циано-4-гидрокси-коричную кислоту в концентрации 10 мг/мл.
Цельную венозную кровь от здоровых доноров отбирали в вакуумные пробирки, содержащие ЭДТА (Becton Dickinson). Цельную кровь инкубировали с RVX в конечной концентрации 0.1 мг/мл при 37 °С в течение 1 часа. Затем кровь центрифугировали при 1000 g 10 мин. Низкомолекулярную фракцию пептидов плазмы крови человека получали путем осаждения белков плазмы ацетонитрилом с 2 % уксусной кислоты в соотношении 1 : 2 в течение 30 мин при 4°С и последующим центрифугированием при 10000 g в течение 30 мин.
Масс-спектрометрический анализ пептидов проводили на времяпролетном масс-спектрометре Ultraflex-TOF-TOF (Bruker Daltonics, Bremen, Germany) с источником MALDI, оснащенном УФ-лазером (337 нм) в режиме детектирования положительных ионов с использованием рефлектрона при следующих настройках ионного источника. Напряжение на IS1 — 25 кВ, IS2 — 21.75 кВ, напряжение на линзах (Lens) 9.5 кВ, напряжения на рефлектроне (Ref) — 26.99 и 13.80 кВ (Ref 2). Ионы детектировали в диапазоне m / z от 700 до 2000.
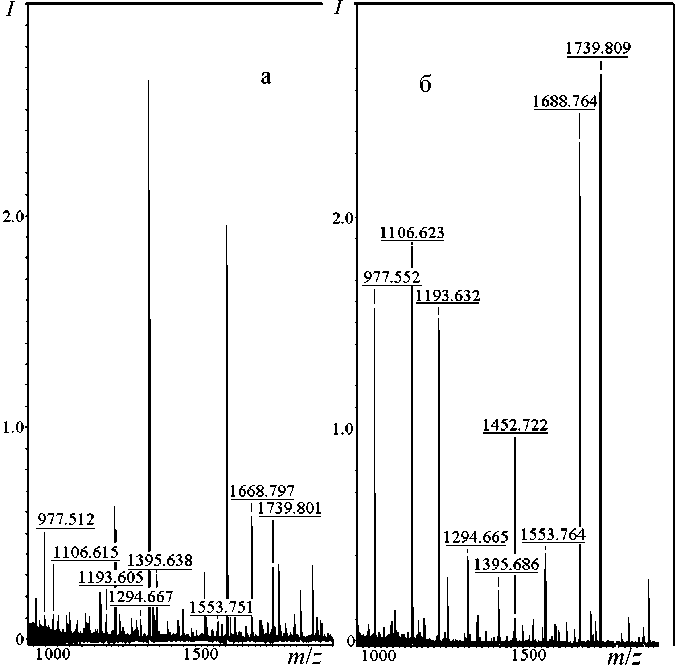
Рис. 1. Масс-спектры пептидной фракции плазмы крови контрольных крыс (а) и крыс после субхронической интоксикации RVX (б)
Обработку спектров, полученных при помощи масс-спектрометра MALDI-TOF-TOF проводили при помощи программного обеспечения Flex Analysis 2.4 (Bruker Daltonics, Bremen, Germany). К спектрам применяли сглаживание по алгоритму Savizky Golay (ширина 0.1 m / z , 1 цикл), и вычитание базовой линии согласно алгоритму Convex Hull. Использовали следующие параметры детекции пиков: алгоритм детекции пиков SNAP; соотношение сигнал/шум 2; порог качества спектра 100). Поиск в базе SwisProt осуществляли с помощью программного комплекса MASCOT (Matrix Science, Великобритания). Точная моноизотопная масса и форма изотопного распределения вычислялись при помощи программы MassPro (ИАнП РАН). Данные MS-MS анализа представлялись с помощью программы Sequence Viewer 2.0 (ИАнП РАН).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
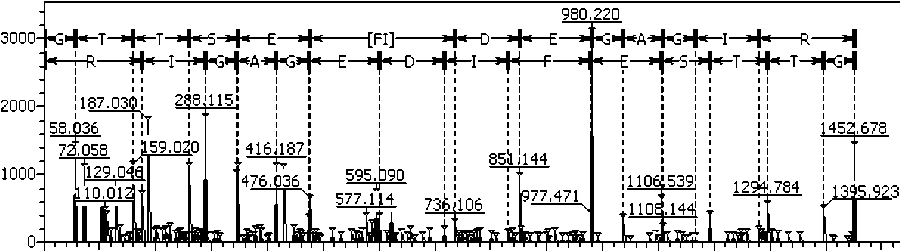
Основной целью данной работы было выявление и идентификация пептидных маркеров влияния RVX на низкомолекулярную фракцию плазмы крови крыс и человека. На первом этапе проводился масс-спектрометрический анализ проб, по- лученных от крыс, подвергнутых воздействию RVX in vivo, и контрольных проб из плазмы крови здоровых крыс. При сравнении спектров значительного различия между пептидными пулами по качественному составу в диапазоне масс 700– 2000 Да не было обнаружено. Но ряд сигналов, не выделяющихся по интенсивности из общего пула в спектрах контрольной группы, становятся мажорными в спектрах образцов экспериментальной группы (рис. 1, б). Кроме того, в этих спектрах появляется сигнал с MH+ 1452.77 Да, который отсутствует в контроле. Для каждого из пептидов, которым соответствуют указанные сигналы, был проведен MS-MS анализ, результат которого показал, что все они относятся к фибринопептиду А, который является частью фибриногена, и характеризуются потерей одной аминокислоты с N-конца (рис. 2, б). На рис. 3 приведен фрагментный спектр пептида с MH+ 1452.77 Да с указанием b- и y-фрагментных серий. Как показано на рисунке, данный спектр принадлежит пептиду с аминокислотной последовательностью GTTSEFIDEGAGIR, являющемуся частью фибринопептида А ADTGTTSEFIDEGAGIR с потерей трех аминокислот с N-конца.
1266 646
1060.482
1.0
б
TSEFIEAGGDIR
1294.665
'TSEFIEAGGDIR
1395.686
1553.764
а
1324.761
TSEFIEAGGDIR
1294.675
1688.764
EFIEAGGDIR
1106.623
TGTTSEFIEAGGDIR
GTTSEFIEAGGDIR
1452.722
1584.879
1193.612
TGTTSEFIE-
1553.712
DTGTTSEFIEAGGDIR
1211.630
FIEAGGDIR
1387.731 1514.797
1161.622
977.366
^i.QVi
|----1 α ul^laJj^JUd^
1668.880175998g
1000 1100 1200 1300
1L. m / z
1870.949
1782.961 |
1830.975
ADTGTTSEFIEAGGDIR
1739.809
DTGTTSEFIEAGGDIR
SEFIEAGGDIR
1193.632
1000 1100 1200
SEFIEAGGDIR
FIEAGGDIR
977.552
1300 1400 1500
1600 1700
1901.837
1830.805
EFIEAGGDIR 1106.554
TTSEFIEAGGDIR
1395.647
α
.1V.vWJaWWW
1450 1460
1800 m / z
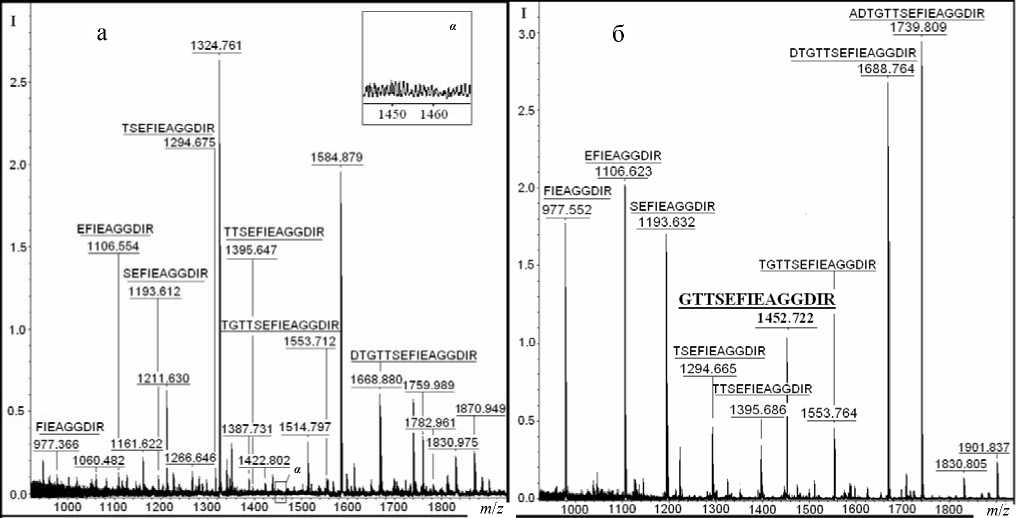
Рис. 2. Масс-спектры пептидной фракции плазмы крови контрольных крыс (а) и крыс после субхронической интоксикации RVX (б). Показано отсутствие пептида с MH+ 1452.77 Да в плазме крови контрольных животных (а)
а
3000-
ы
Ь2
ЬЗ Ь4
у4
Ь5
уб
Ь7
Ь8
980.220
Ь9 .
2000-
У1
у2 уЗ
У5
у7
у8
У У
187.0311
2(8
: 58, )36
ЫО Ы1 yll
| Ы2 уЮ
ЫЗ
у12
1 DOO-
^129^
159.02
е
У13
452.678
110.012
595. )90
577.1 .4
73 i
977.471
1106.539
б
Ш 73 >106 s wk wЦ itwkw, м р.w^w
110Е
t , к ^W
лЖ pwgTTj ,
1395.92.3
100 200 300 400 500 600 700 800 900 1000 1100 1200 1300 1400 1500
О 100 200 300 400 500 600 700 800 900 1000 1100 1200 1300 1400 1500
Mass/Charge
Рис. 3. Масс-спектр пептида GTTSEFIDEGAGIR с MH+ 1452.77 Да, полученный тандемной масс-спектрометрией (а), и определение его последовательности (б)
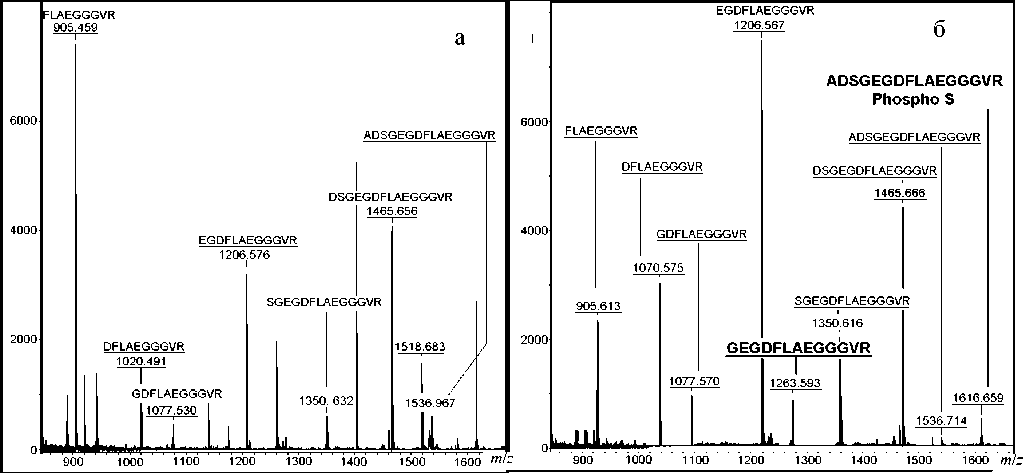
Рис. 4. Масс-спектры пептидной фракции плазмы крови человека (а) и плазмы крови человека после инкубации с RVX in vitro (б)
Таким образом, в низкомолекулярной фракции плазмы крови крыс, подвергнутых субхронической интоксикации RVX, обнаружен пептид фибриногеновой природы; этот факт наряду с характерным изменением пептидного спектра в целом может служить молекулярным свидетельством интоксикации RVX.
В следующем эксперименте мы добавляли RVX в кровь человека in vitro (см. раздел "Материалы и методы"), после чего исследовали пептидную фракцию плазмы крови. Как и в эксперименте с крысами in vivo, некоторые компоненты спектра становятся мажорными (рис. 4, б). Более того, все мажорные сигналы в процессе идентификации были отнесены к фибринопептиду А, лишенного аминокислот с N-конца. Масс-спектрометрический анализ образцов контрольной плазмы и плазмы с добавлением RVX показал определенное сходство полученных результатов с теми, что были получены в эксперименте in vivo с кровью крыс. В образцах появляется пептид GEGDFLAEGGGVR, MH+ 1263.6 Да, также имеющий фибриногеновую природу и характеризующийся отсутствием трех аминокислот по сравнению с фибринопептидом человека (ADSGEGDFLAEGGGVR). MS-MS спектр пептида GEGDFLAEGGGVR приводится на рис. 5.
Таким образом, в обоих экспериментах обнаружен фрагмент фибринопептида, отсутствующий в контрольных пробах и имеющий разницу с родительским пептидом в три аминокислоты, отщепленные с N-конца. Фрагменты фибринопептидов крысы и человека начинаются с глицина с N-конца, а предшествующая отщепленная аминокислота является нейтральной и имеет гидроксильную группу (треонин в фибринопептиде крысы и серин в фибринопептиде человека) (см. таблицу).
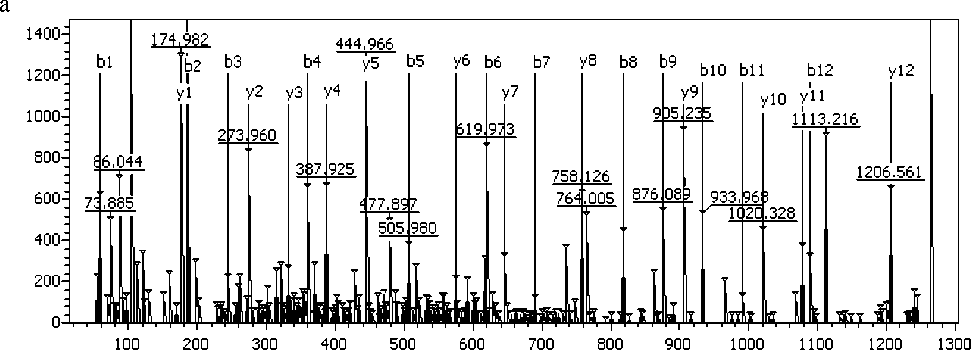
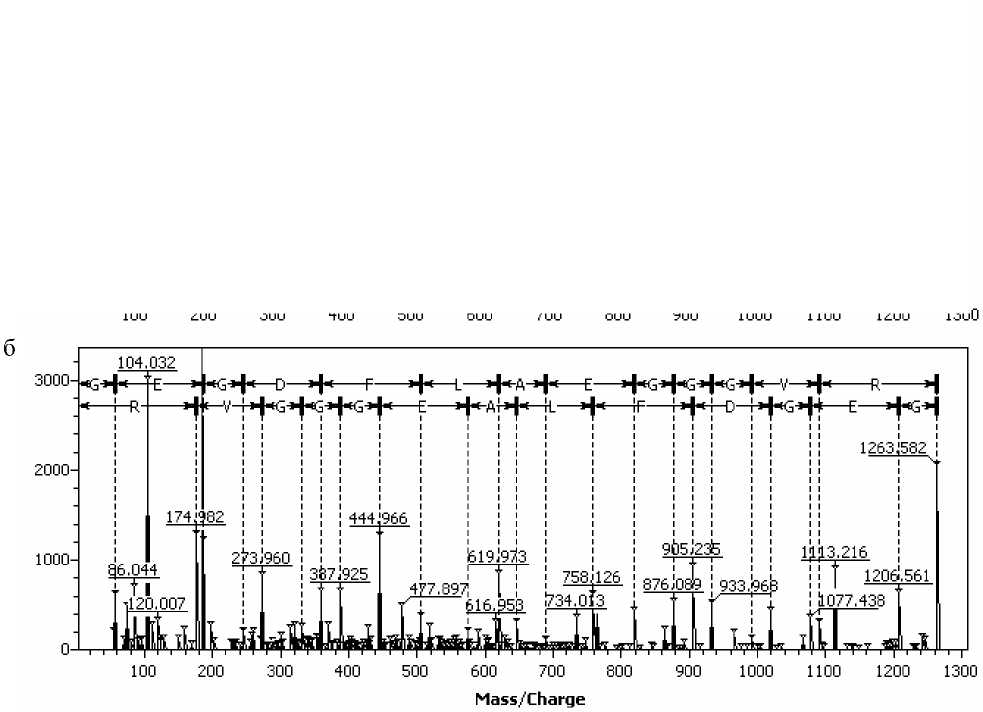
Рис. 5. Масс-спектр (а) пептида GEGDFLAEGGGVR MH+ 1263.6 Да, полученный тандемной масс-спектрометрией, и определение его последовательности (б)
Пептиды, относящиеся к фибринопептиду А, выявленные в плазме крови крысы и человека, в контроле и при действии RVX
|
№ п/п |
Крыса |
Человек |
||||
|
Пептид (MH + Да) |
Контроль |
VX |
Пептид (MH + Да) |
Контроль |
VX |
|
|
1 |
ADTGTTSEFIDEGAGIR + Phospho ST |
– |
– |
ADSGEGDFLAEGGGVR + Phospho ST (1616.6515) |
– |
+ |
|
2 |
ADTGTTSEFIDEGAGIR (1739.809) |
+ |
+ |
ADSGEGDFLAEGGGVR (1536.6912) |
+ |
+ |
|
3 |
DTGTTSEFIDEGAGIR (1668.772) |
+ |
+ |
DSGEGDFLAEGGGVR (1465.6481) |
+ |
+ |
|
4 |
TGTTSEFIDEGAGIR (1553.745) |
+ |
+ |
SGEGDFLAEGGGVR (1350.6212) |
+ |
+ |
|
5 |
GTTSEFIDEGAGIR (1452.697) |
– |
+ |
GEGDFLAEGGGVR (1263.5891) |
– |
+ |
|
6 |
TTSEFIDEGAGIR (1395.676) |
+ |
+ |
EGDFLAEGGGVR (1206.5677) |
+ |
+ |
|
7 |
TSEFIDEGAGIR (1294.628) |
+ |
+ |
GDFLAEGGGVR (1077.5251) |
+ |
+ |
|
8 |
SEFIDEGAGIR (1193.580) |
+ |
+ |
DFLAEGGGVR (1020.5036) |
+ |
+ |
|
9 |
EFIDEGAGIR (1106.548) |
+ |
+ |
FLAEGGGVR (905.4767) |
+ |
+ |
По-видимому, при действии RVX происходит ингибирование ряда экзопептидаз (N-аминопептидаз), в результате чего изменяется количественное соотношение компонентов низкомолекулярной фракции плазмы крови, в частности наблюдается значительное усиление сигналов фиб-ринопептидных фрагментов по отношению к остальным сигналам в спектре, а также появляются другие пептиды, имеющие фибриногеновую природу. С другой стороны, возможно ингибирование антитромбина, что приводит к усиленному расщеплению фибриногена и повышению уровня фиб-ринопептида А. Так, помимо вышеназванного пептида с MH+ 1263.6 Да в пробах плазмы человека с добавлением RVX появляется еще один пептид c MH+ 1616.6 Да. По результатам анализа методом тандемной масс-спектрометрии, данный сигнал был также отнесен к фибринопептиду А, фосфорилированному по серину (рис. 6). Фибри-нопептид А — это пептид, отщепляемый тромбином от фибриногена при активации системы свертывания крови. Тромбин гидролизует 4 пептидные связи Arg–Gly в фибриногене, в результате чего образуются фибринопептиды А и В [8]. Функциональное значение отщепленных фибринопептидов и их фрагментов остается неясным.
Таким образом, на основе полученных результатов можно сделать следующие выводы.
-
• Основной пептидный фон в плазме крови человека и крысы после воздействия RVX составляют пептиды, принадлежащие к фибриногену, в частности к фибринопептиду А.
-
• Пептиды, входящие в состав низкомолекулярной фракции сыворотки крови (GTTSEFIDEGAGIR) и (GEGDFLAEGGGVR) соответственно крысы и человека, могут появляться в результате инактивации экзопептидаз при воздействии RVX [7].
-
• Два пептида, имеющие фибриногеновую природу в сыворотке крови человека, а именно ADSGEGDFLAEGGGVR + Phospho (ST) и GEGDFLAEGGGVR, могут свидетельствовать о воздействии RVX на организм, в частности на систему гуморального гемостаза.
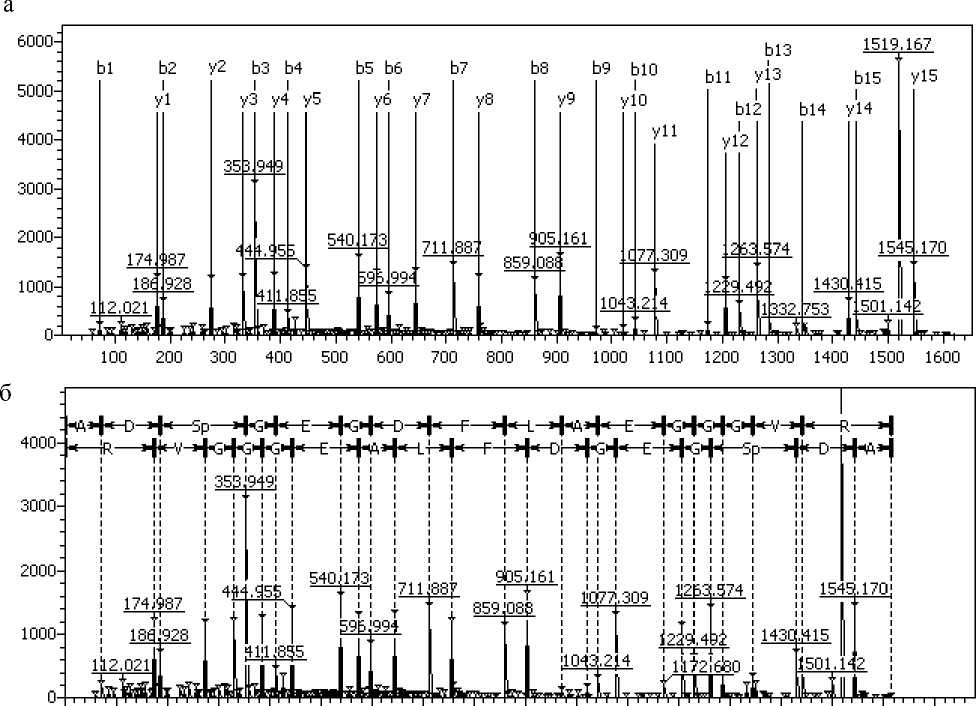
О 100 200 300 400 500 600 700 800 900 1000 1100 1200 1300 1400 1500 1600 1700
Mass/Charge
Рис. 6. Масс-спектр (а) пептида ADSGEGDFLAEGGGVR , фосфорилированного по серину с MH+ 1616.6 Да, полученный тандемной масс-спектрометрией, и определение его последовательности (б)


