Измерения и анализ локальной церебральной гемодинамики у больных с сосудистыми мальформациями головного мозга
Автор: Чупахин Александр Павлович, Черевко Александр Александрович, Хе Александр Канчерович, Телегина Надежда Юрьевна, Кривошапкин Алексей Леонидович, Орлов Кирилл Юрьевич, Панарин Вячеслав Александрович, Баранов Виктор Ильич
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Ангионеврология и нейрохирургия
Статья в выпуске: 4 т.16, 2012 года.
Бесплатный доступ
Впервые проведены измерения скорости и давления крови в артериях головного мозга до четвертых сегментов при наличии артериовенозных мальформаций и артериальных аневризм. Разработан и внедрен аппарат диаграмм «давление - скорость» и «расход - поток энергии», позволяющий характеризовать тип сосудистой аномалии по гемодинамическим параметрам и отслеживать эффективность операции. На основании вейвлет-анализа локальных гемодинамических параметров в пораженных и здоровых ветвях артерий обнаружено изменение низкочастотной части спектра кровотока после операции. Полученные результаты дают качественные и количественные признаки аномалии сосудов головного мозга и позволяют оценить эффективность эмболизации в процессе операции.
Артериовенозные мальформации, артериальные аневризмы, гемодинамические параметры
Короткий адрес: https://sciup.org/142140502
IDR: 142140502 | УДК: 616.1
Measurement and analysis of cerebral hemodynamic parameters in the presence of brain vascular anomalies
Hemodynamic parameters of the blood flow in human cerebral vessels up to the 4th branch levels were measured. A framework based on "Pressure - Velocity" and "Discharge - Energy flow rate" regimen was designed and implemented. This framework makes it possible to detect brain vascular anomalies like arteriovenous malformations and arterial aneurysms depending on hemodynamic parameters, and to monitor the efficiency of the operation. Modification in the low-frequency spectrum of the cerebral blood flow following the operation was detected by the wavelet analysis of the hemodynamic parameters. The results obtained give qualitative and quantitative characteristics of the presence of cerebral blood vessels anomalies and makes it possible to estimate the efficiency of their embolization at operation.
Текст научной статьи Измерения и анализ локальной церебральной гемодинамики у больных с сосудистыми мальформациями головного мозга
ВАК 14.01.18
Поступила в редакцию 10 августа 2012 г.
А.А. Черевко,
А.К. Хе,
Н.Ю. Телегина,
А.Л. Кривошапкин,
К.Ю. Орлов,
В.А. Панарин,
В.И. Баранов, 2012
Впервые проведены измерения скорости и давления крови в артериях головного мозга до четвертых сегментов при наличии артериовенозных мальформаций и артериальных аневризм. Разработан и внедрен аппарат диаграмм «давление – скорость» и «расход – поток энергии», позволяющий характеризовать тип сосудистой аномалии по гемодинамическим параметрам и отслеживать эффективность операции. На основании вейвлет-анализа локальных гемодинамических параметров в пораженных и здоровых ветвях артерий обнаружено изменение низкочастотной части спектра кровотока после операции. Полученные результаты дают качественные и количественные признаки аномалии сосудов головного мозга и позволяют оценить эффективность эмболизации в процессе операции. Ключевые слова: артериовенозные мальформации; артериальные аневризмы; гемодинамические параметры.
Сосудистые заболевания центральной нервной системы являются одной из основных причин смертности и инвалидизации населения России. Особенно неблагоприятные условия складываются в регионе Сибири. Одной из частых причин геморрагического инсульта является разрыв артериальных аневризм (АА) сосудов головного мозга. По статистике, ежегодно разрыв аневризм происходит от 8 до 21 случаев на 100 000 человек. Приблизительно 15% пациентов с аневризматическим субарахноидальным кровоизлиянием погибает, не достигнув больницы. Около 50% пациентов в течение ближайших шести месяцев повторяют кровоизлияние, с летальностью до 70%. Сосудистый спазм увеличивает риск развития летальных исходов после субарахноидального кровоизлияния в 2,3 раза и снижает число хороших исходов более чем на 1/3 [12]. Единственный выход для таких пациентов – оперативное лечение: микрохирургическое или эндоваскулярное.
С появлением неинвазивных методов обследования возрастает количество случайно выявленных, неразорвавшихся аневризм. Остается до конца неясным, какие из этих аневризм должны подвергаться оперативному лечению. Очевидно, что в определении показаний для хирургического лечения неразорвавшейся аневризмы следует учиты- вать совокупность факторов риска ее потенциального разрыва. Гемодинамическим факторам здесь отводится ведущая роль.
Другой причиной внутричерепных кровоизлияний являются артериовенозные мальформации (АВМ). В последнее десятилетие значительные успехи достигнуты в эндоваскулярном лечении АВМ. Использование нового эмболизирующего материала Onyx позволило добиться тотального выключения АВМ только эндоваскулярным методом более чем у половины пациентов; в то же время остается достаточно высоким процент осложнений, приводящих к стойкой инвалидизации и смерти. В самой крупной опубликованной моноцентровой серии из 350 пациентов эти показатели составили 7,1 и 1,4% [15]. Наиболее тяжкие осложнения связаны с перипроцедуральными кровоизлияниями, частота которых, по разным данным, варьирует от 2 до 16,7% [16]. Для предупреждения такого рода осложнений возникает потребность в моделировании возможных интраоперационных изменений гемодинамики в АВМ и окружающем мозге.
Последние десятилетия характеризуются революцией в нейрохирургии, связанной с появлением нового приборного и медицинского обеспечения (томография различных типов, оборудование для внутрисосу- дистой хирургии). Это оборудование позволяет получать и использовать информацию о кровотоке непосредственно во время операции. Ставится задача виртуального моделирования хода операции и активного использования результатов моделирования в реальном режиме времени. Исследование гемодинамики головного мозга человека в норме и при патологии является комплексной проблемой, требующей описания общих физиологических закономерностей мозгового кровообращения, получения экспериментальной информации о гемодинамике мозга методами магнитно-резонансной томографии (МРТ), компьютерной рентгеновской томографии (КТ), допплерографии, математического моделирования на основе этих данных. Это позволяет создавать компьютерные модели аномалий (артериовенозные мальформации, артериальные аневризмы) для использования в медицинской практике.
Исключительная сложность сосудистой системы мозга, физиологических механизмов в регуляции мозгового кровообращения, отсутствие полных и надежных экспериментальных данных о мозговом кровотоке объясняют отсутствие в настоящее время единой модели, описывающей течение крови в сосудах мозга. Различные геометрические параметры и механические свойства сосудов (артерий, вен, капилляров), учет влияния на течение форменных элементов крови, высокая вариабельность кровотока в различных структурах мозга вносят существенные сложности в создание адекватных гемодинамических моделей [1, 2, 4, 5, 7–9, 11, 13, 14].
Моделирование гемодинамики головного мозга – это моделирование нестационарного, пульсирующего течения крови по сети сосудов вариативной геометрии с активно реагирующими на пульсации потока стенками. Эта сеть погружена в субстанцию мозга, которая, в свою очередь, находится в твердой черепной коробке. Для создания моделей, которые могут использоваться в реальном режиме времени, необходимо совершенствовать глобальные модели кровотока в мозге в целом. Эти модели должны основываться на данных эксперимента. Данная работа выполнена в рамках проекта комплексного исследования патологических изменений сосудов головного мозга человека, включающего: клинико-физиологический анализ, математическое и компьютерное моделирование, предназначенного для разработки новых подходов к диагностике, прогнозированию и лечению.
В общем виде задачи исследования могут быть сформулированы так. Имеются две операции, схожие по своим визуальным результатам (ангиограммам), но с различными клиническими исходами. Определить гемодинамические причины возникших осложнений и показания к хирургическому лечению у пациентов со случайно выявленными аномалиями сосудов головного мозга.
Глобальная цель исследования – нахождение признаков, параметров, которые качественно и количественно определяют безопасность хирургического лече- ния. Достижение этой цели невозможно без глубокого и всестороннего экспериментального и теоретического исследования гемодинамики сосудов головного мозга.
МАТЕРИАЛ И МЕТОДЫ
В нейрохирургическом центре ННИИПК с помощью прибора Volcano ComboMap проводились измерения давления и скорости кровотока в сосудах головного мозга при наличии аномалий: АВМ и АА. Датчик прибора имеет диаметр 0,36 мм и позволяет измерять с высокой точностью одновременно давление и скорость потока крови в сосудах диаметром более 1,5 мм. Скорость измеряется ультразвуковым допплеровским методом (12 МГц).
Измерения проводили в нескольких точках сосуда, расположенных на различных расстояниях от аномалии. Особый интерес представляют измерения, проводимые в одной и той же точке сосуда до и после операции по устранению сосудистой аномалии. Они позволяют описать качественные свойства и количественные параметры кровотока, сопутствующие аномалии. Полученную информацию (цифровые массивы значений давления и скорости кровотока) обрабатывали, очищали от шумов, в ней выделяли значимые фрагменты и проводили ее компьютерный анализ. Цифровая запись данных велась во время операции непрерывно, графики давления и скорости выводились на экран монитора прибора в реальном режиме времени. В этих цифровых массивах имелись различные шумы, возникающие при передвижении датчика, установлении его в позицию, обеспечивающую устойчивую запись данных. Вследствие этого окончательные данные представлены в виде фрагментов длительностью от 10–15 до 150–200 с.
Карта операции включает в себя: клинические данные (дата, вид и локализация аномалии, результат операции); первичные графики давления и скорости потока крови в различных точках сосудов головного мозга на протяжении всей операции; набор фрагментов, соответствующий отрезкам времени, в течение которых проводились измерения в различных точках сосудов. Эти фрагменты содержат очищенные от шумов отрезки графиков давления и скорости, на основании которых выполняются качественный и количественный анализ кровотока. В каждом из фрагментов выполнен вейвлет-анализ цифровых массивов (сигналов) давления и скорости кровотока, на основании которого строились вейвлет-скейлограммы – динамические, нестационарные спектральные портреты.
В период с октября 2011 по апрель 2012 г. в нейрохирургическом центре ННИИПК были проведены 16 операций, во время которых измеряли давление и скорость кровотока, из них в 13 снималась цифровая информация с последующей обработкой и составлением карт операций. Из этих 13 операций внутрисосудистая эмболизация АВМ осуществлялась в шести, АА – в шести, каро-тидо-кавернозного соустья (ККС) в одном случае.
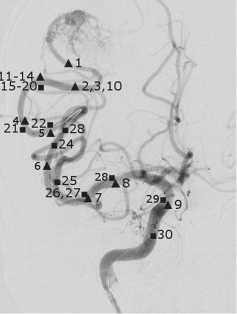
Рис. 1.
Ангиограмма сосудов с отмеченными положениями датчика.
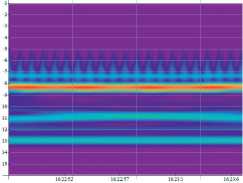
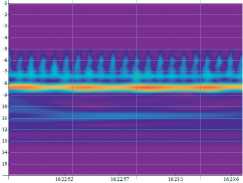
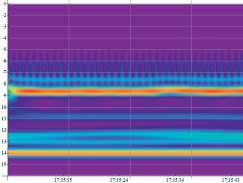
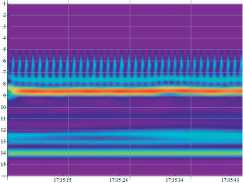
Рис. 2.
Скейлограммы давления и скорости в афференте до операции (а) и после нее (б).
РЕЗУЛЬТАТЫ
Рассмотрим подробнее результаты измерений на примере типичной операции по внутрисосудистой эмболизации АВМ. На рис. 1 приведена ангиограмма сосудов головного мозга в районе АВМ (левый угол снимка) с отмеченными положениями датчика, в которых проводились измерения. Для некоторых позиций проводилось несколько измерений – например, с 15 по 20. Проводник с датчиком виден как светлая кривая в позициях 5, 22. Номера отметок возрастают со временем, положения датчика в моменты до эмболизации отмечены треугольником, после нее – квадратом.
Вейвлет-скейлограммы сигналов, соответствующих этим значениям давления и скорости, показаны на рис. 2. Вейвлет-преобразование одномерного сигнала позволяет анализировать свойства сигнала одновременно в частотном и физическом пространствах. Разложение сигнала производится по специальным локализованным вейв-лет-функциям, зависящим от времени. Результатом вейв-лет-преобразования является двумерный массив амплитуд-значений коэффициентов разложения этого сигнала по базису из вейвлет-функций. В отличие от Фурье-анализа вейвлет-анализ дает динамику спектра нестационарного процесса [1]. Спектр сигнала – это поверхность в трехмерном пространстве, на рис. 2 представлена ее проекция на плоскость (время – частота), при этом частота измеряется в логарифмических переменных.
На скейлограммах хорошо видны линии спектра, отвечающие сердечным сокращениям (частота 1 Гц) и дыхательному циклу. Эти спектральные линии отвечают высоким частотам и не изменяются в процессе операции. Сильнее меняется картина в области низких частот, при этом наблюдаются как расщепления спектральных линий, так и изменение интенсивности сиг- нала на выделенных частотах. Изменение спектра интракраниального кровотока в терминах Фурье-анализа изучалось отечественными нейрохирургами [3].
Диаграмма Dp, u давление – скорость (рис. 3, а, в ) представляет собой построенную на плоскости ( p, u ) кривую зависимости p = p (u) , которая соответствует временным зависимостям p = p (t), u = u (t) . При возрастании времени точка пробегает диаграмму против часовой стрелки. Диаграмма DQ E расход – поток энергии (рис. 3, б, г ) строится по данным давления и скорости в сосуде сечением S . Величины Q и E вычисляются по формулам:
,
Е = £(||м|2 -v—^pu-ndS, где ρ, p, й – плотность, давление, скорость потока крови, п – нормаль к сечению сосуда S.
Диаграммы Dp, u и DQ, E сохраняют свою форму вдоль сосуда. Они имеют характерную геометрию, различную для разных аномалий. Эти диаграммы меняют свой размер и положение после операции.
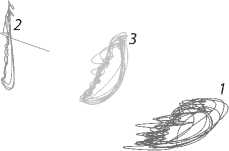
Диаграмма Dp, u для АВМ меняет свое положение на плоскости ( p, u ), переходя из правой нижней части в левую верхнюю. Это объясняется тем, что при эмболизации АВМ аномально высокая скорость в афференте понижается, давление повышается до нормального. Диаграмма DQ, E сохраняет характерную форму пера, но резко уменьшается в размере и перемещается к началу координат на плоскости ( Q, E ). При введении эмболизата диаграмма DQ, E плавно уменьшается в размере и монотонно
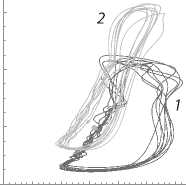
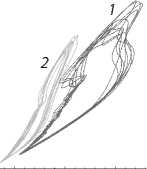
Рис. 3.
Фазовые диаграммы D p, u
(слева) и DQ, E (справа) до операции (1), после нее (2) и при частичной (более 90%) эмболизации (3): а, б – АВМ; в, г – АА.
CL s s
в
0,8
g 0,6
0,4
0,2
20 40
V, cм/c
60 80
б
1,0


1,5
o.
s
s
10 20 30 40 50 60
V, cм/c
0,5 1,0
Q, cм3/c
1,5
3 1,0
0,5
0,5 1,0 1,5
Q, cм3/c
сдвигается к началу координат. Это происходит до введения большей части эмболизата (80–90%). Затем, после введения оставшейся части, она резко смещается к началу координат и уменьшается в размере (рис. 3, б ).
При наличии в сосуде АА диаграммы Dp, u и DQ, E имеют характерную S-образную форму. Эта форма сохраняется после эмболизации аневризмы, но сами диаграммы существенно уменьшаются в размерах (рис. 3, в, г ).
Наличие аномалий в сосудистой сети изменяет как гемодинамические (скорость, давление потока), так и прочностные параметры этой сети. АВМ и АА по-разному влияют на прочностные, упругие свойства церебральных сосудов. Диаграмма Dp, u дает своеобразное уравнение состояния аномалии, характеризуя различные механические свойства сети сосудов с аномалией в процессе ее разгрузки ускоряющимся потоком крови и нагрузки – при торможении потока.
Измерения проведены в большом числе сосудов, имеющих диаметры от 1,5 мм до 5 мм. Получены значения для скорости потока 10–150 см/с, давления 20–180 мм рт. ст., при этом скорости свыше 60–80 см/с характеризуют наличие АВМ. Эти данные согласуются со значениями давления и скорости кровотока, получаемыми при транскраниальной допплерографии в проксимальных сегментах артерий виллизиева круга [3].
Обнаружены качественные различия скейлограммы до и после операции. Построены и проанализированы диа- граммы Dp, u (давление – скорость) и DQ, E (расход – поток энергии). Обнаружены качественные различия этих диаграмм для разных видов аномалии (АВМ и АА), установлены качественные и количественные изменения этих диаграмм в процессе операции. Показано, что они наглядно характеризуют степень эмболизации аномалии, в частности, позволяют определить момент полного закрытия артериовенозного шунта еще до ангиографического подтверждения данного события.
ВЫВОДЫ
-
1. Впервые проведено измерение гемодинамических параметров в дистальных церебральных сосудах при различных видах сосудистых аномалий.
-
2. Разработан и внедрен аппарат диаграмм «давление – скорость» и «расход – поток энергии», позволяющий характеризовать тип сосудистой аномалии (АВМ и АА) по гемодинамическим параметрам и отслеживать эффективность операции.
-
3. Создано программное обеспечение, позволяющее визуализировать фазовые диаграммы «давление – скорость» и «расход – поток энергии» в ходе операции, что уже на данном этапе исследования дало возможность хирургу определять момент полного выключения АВМ. Представляется, что правильная интерпретация изменений этих диаграмм в ходе операции позволит выработать критерии прекращения эмболизации и снизить число перипроцеду-ральных кровоизлияний.
-
4. Отмечено качественное изменение спектра вейв-лет-скейлограмм после эмболизации. Более детальный анализ, как качественный, так и количественный, требует дальнейшего всестороннего изучения.
Список литературы Измерения и анализ локальной церебральной гемодинамики у больных с сосудистыми мальформациями головного мозга
- Aстафьева Н.М.//УФН. 1996. Т. 166, № 11. С. 1145-1170.
- Aшметов И.В., Буничева A.Я., Мухин С.И. и др. Компьютер и мозг. Новые технологии. М., 2005.
- Гайдар Б.В., Семенютин В.Б., Парфенов В.Е. и др. Транскраниальная допплерография в нейрохирургии. СПб., 2008.
- Левтов В.А., Регирер С.А., Шадрина Н.Х. Реология крови. М., 1982.
- Медицина в зеркале информатики. М., 2008.
- Мозг: фундаментальные и прикладные проблемы//Вест. РAH. № 5-6. 2010. С. 397-520.
- Парашин В.Б., Иткин Г.П. Биомеханика кровообращения. М., 2005.
- Педли Т. Гидродинамика крупных кровеносных сосудов. М., 1983.
- Петров И.Б.//Труды МФТИ. 2009. Т. 1, № 1. С. 5-16.
- Сибирский международный нейрохирургич. форум: Сб. науч. материалов. Новосибирск, 2012.
- Система кровообращения и артериальная гипертония: биофизические и генетико-физиологические механизмы, математическое и компьютерное моделирование. Новосибирск, 2008.
- Хирургия аневризм головного мозга. Т. I-III.
- Quarteroni A., Tuveri M., Venezani A.//Comput. Visual. Sci. 2000. V. 2. P. 163-197.
- Sforza D.M., Putman C.M., Cebral J.R.//Fluid Mech. 2009. V. 41. P. 91-107.
- Saatci I., Geyik S., Cekirge H.S. et al.//J. Neurosurg. 2011. V. 115 (1). P. 78-88.
- Liu L., Jiang C., He H. et al.//Interv. Neuroradiol. 2010. V. 16 (1). P. 47-57.


