Изолированная гипоплазия верхушки левого желудочка, редкая врожденная кардиомиопатия
Автор: Скидан Виктория Игоревна, Павлюкова Елена Николаевна, Нарциссова Галина Петровна
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Обзоры и лекции
Статья в выпуске: 1 т.33, 2018 года.
Бесплатный доступ
Представлен обзор научных публикаций, касающихся описания клинических случаев изолированной гипоплазии верхушки левого желудочка у 42 пациентов. Для гипоплазии верхушки левого желудочка характерны: 1) сферическая форма левого желудочка со срезанной верхушкой и выбуханием межжелудочковой перегородки вправо в сочетании с нарушением систолической функции левого желудочка; 2) замещение миокарда верхушки левого желудочка жировой тканью; 3) локализация папиллярных мышц на уплощенной верхушке левого желудочка; 4) удлиненный правый желудочек, обтекающий контур верхушки левого желудочка. Течение данного состояния может быть бессимптомным либо проявляться клиникой бивентрикулярной сердечной недостаточности с высокой легочной гитпертензией и нарушениями ритма сердца.
Изолированная гипоплазия верхушки левого желудочка, врожденная кардиомиопатия
Короткий адрес: https://sciup.org/149125195
IDR: 149125195 | УДК: 616.124.2: | DOI: 10.29001/2073-8552-2018-33-1-21-26
Isolated left ventricular apical hypoplasia, rare inborn cardiomyopathy
The review of data of literature concerning the description of clinical cases of isolated left ventricular apical hypoplasia (LVAH) in 42 patients are presented. left ventricular apical hypoplasia is characterized by 1) a spherical left ventricular with a cut-off tip and a swelling of the interventricular septum to the right in combination with systolic dysfunction of left ventricular; 2) replacement of the myocardium of the upper limb with fat tissue; 3) localization of papillary muscles on the flattened apex of the left ventricular; 4) elongated right ventricle (RV), flowing around the top of the upper left vertex. The course of this condition may be asymptomatic, or manifest as a clinic of biventricular heart failure with high pulmonary hypertension and heart rhythm disturbances.
Текст обзорной статьи Изолированная гипоплазия верхушки левого желудочка, редкая врожденная кардиомиопатия
Fernandez-Valls M. и соавт. (США) на основании сходных данных компьютерной и магнитно-резонансной томографии (МРТ) трех пациентов впервые описали врожденную изолированную гипоплазию верхушки левого желудочка (ИГВЛЖ) [1]. Для ИГЛЖ характерны: 1) сферическая форма ЛЖ со срезанной верхушкой и выбуханием межжелудочковой перегородки (МЖП) вправо в сочетании с нарушением систолической функции ЛЖ; 2) замещение миокарда верхушки ЛЖ жировой тканью; 3) локализация папиллярных мышц на уплощенной верхушке ЛЖ; 4) удлиненный правый желудочек (ПЖ), обтекающий контур верхушки ЛЖ [1–5]. Patrianakos A.P. и соавт. предложили ИГВЛЖ относить к неклассифици-руемым кардиомиопатиям [6]. В научной литературе пока приведено описание ИГВЛЖ только у 42 пациентов. При этом в ряде публикаций описано сочетание ИГВЛЖ с различными другими анатомическими аномалиями строения сердца и нарушениями электрофизиологических свойств миокарда [7–9]. Это, в свою очередь, может определять как бессимптомное течение заболевания [10], развитие внезапной смерти [11], так и клиническую картину сердечной недостаточности [10–15]. По мнению Wang Т.
и соавт. [16], этиология и патогенез ИГВЛЖ не изучены, а основные клинические симптомы у большинства пациентов связаны с различными нарушениями ритма сердца, развитием легочной гипертензии и прогрессированием хронической сердечной недостаточности.
Со времени первого сообщения в 2004 г. [1] и по настоящий момент опубликовано всего 26 сообщений, из них 24 англоязычные и 2 русскоязычные статьи, в которых в основном представлены единичные клинические наблюдения или анализ диагностических и клинических находок у небольшой группы пациентов с ИГВЛЖ.
С точки зрения эпидемиологической географии, в настоящий момент ИГВЛЖ описана на трех континентах, исключая Африку, в основном среди представителей евразийского, азиатского и североамериканского населения, в меньшей степени — на территориях проживания мексиканского и испанского населения [11–13, 15]. Наибольшее число больных ИГВЛЖ выявлено в Китае — 8 человек, России — 5 наблюдений, США — 6 пациентов, странах Евросоюза — 6 больных, Великобритании и странах Британского содружества — 7 случаев, в Корее — трое пациентов.
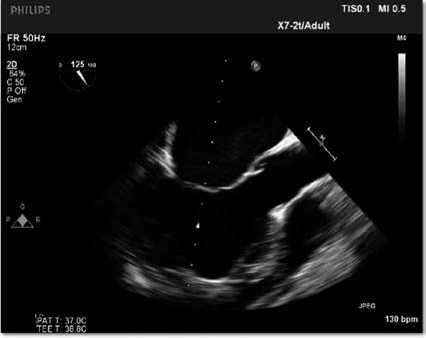
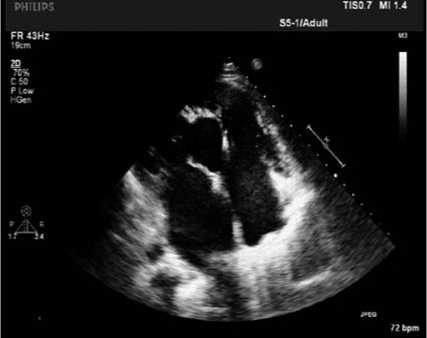
Рис. 1а
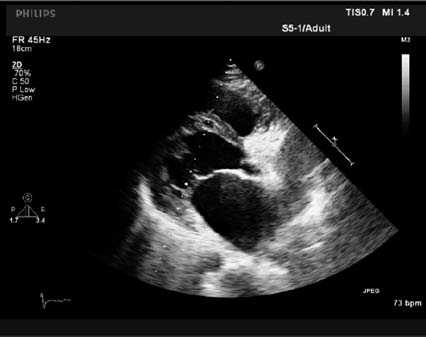
Рис. 1б
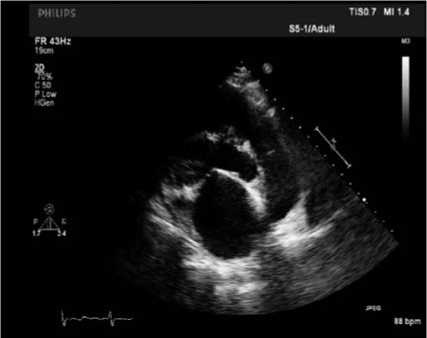
Рис. 1в
Рис. 1г
Рис. 1. Основные критерии ИГВЛЖ при ЭхоКГ, пациент Г., 32 года (ФЦССХ, г. Хабаровск): а, б — 1-й признак, ЛЖ шаровидной формы с аневризмоподобным выбуханием МЖП; в — 3-й признак: аномальное расположение основания папиллярных мышц на уровне уплощенной верхушки ЛЖ; г — 4-й признак: удлиненная полость ПЖ, «бананоподобная» форма
Врожденный характер ИГВЛЖ на данный момент не оспаривается, поскольку у одного ребенка ИГВЛЖ была заподозрена внутриутробно при стандартном акушерском скрининге [16]. Средний возраст пациентов составляет 29 лет, возрастной диапазон колеблется от 3 мес. до 66 лет [15].
Дискутабельным остается обсуждение вопроса об этиологии и патогенетическом механизме возникновения этой аномалии ЛЖ. Мутация гена Lamin A/C выявлена в семье с двумя случаями ИГВЛЖ [15, 17]. Современные представления о структуре и функциях ядерных белков ламинов и патологических механизмах генных ламиновых мутаций тесно связаны с проблемами ламин-ассоциированных форм кардиомиопатий, ассоциированных с различными скелетно-мышечными расстройствами, а также развитием блокад и/или фатальных желудочковых аритмий.
В диагностике ИГВЛЖ определяющая роль отводится МРТ сердца с использованием парамагнетиков [1, 11–13, 16–19]. Возможности ультразвуковой визуализации выявления ИГВЛЖ были подтверждены несколько позже. Причем подчеркивается доступность и экономическая целесообразность эхокардиографического (ЭхоКГ) ис- следования при первичном выявлении этой аномалии ЛЖ [2, 3, 7, 14, 18]. Вероятно, в скором времени будет доказана целесообразность использования эхоконтрастов в диагностике ИГВЛЖ [7, 18].
Коронаронарная ангиография выполняется больным старшей возрастной группы для исключения аномалий развития или стенотического повреждения коронарного русла. Целесообразно проводить вентрикулографию и ангиопульмонографию для детализации формы ЛЖ с целью выявления дивертикулов в ЛЖ и определения давления в легочной артерии [19]. В ряде случаев показана биопсия эндомиокарда ПЖ для выявления очагов некроза, признаков воспаления в миокарде, замещения миокарда фиброзно-жировой тканью, а также для исключения воспалительно-дистрофических изменений не-кробиотического характера, наблюдаемых при болезни Чагаса (трипаносомоз) и гранулематозном процессе при саркоидозе [19].
Подавляющим большинством авторов [1–3, 13, 14, 16, 18, 21] при описании ИГВЛЖ подтверждаются четыре основных диагностических признака заболевания (рис. 1 и 2):
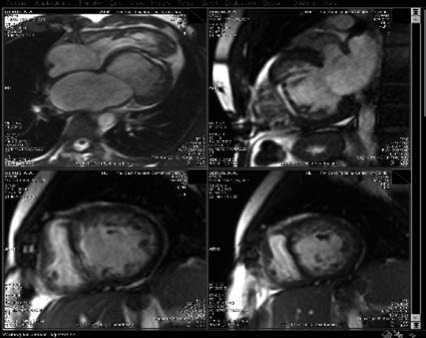
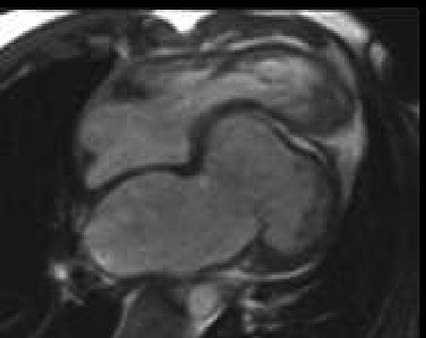
Рис. 2а
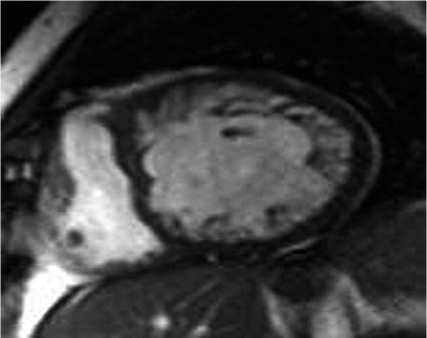
Рис. 2б
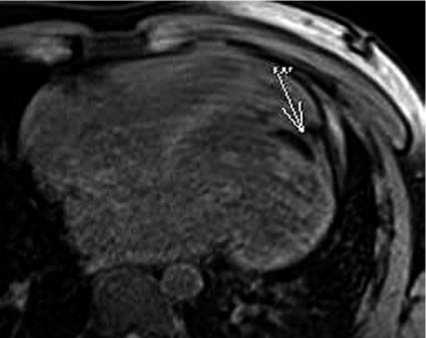
Рис. 2в
Рис. 2г
Рис. 2. Основные критерии ИГВЛЖ при МРТ, пациент Г., 32 года (ФЦССХ, г. Хабаровск): а — изолированная гипоплазия верхушки; б — 1-й и 2-й признаки, 4-камерная проекция (режим кинопетли, диастола); в — 3-й признак: короткая ось (режим кинопетли, диастола); г — 4-й признак, 4-камерная проекция (Т1-FatSat)
-
1) закругленный ЛЖ шаровидной формы за счет выбухающей в полость ПЖ МЖП — нарушение анатомического взаимоотношения с усеченной формой ЛЖ и срезанной верхушкой формирует увеличение ЛЖ в ширину и выраженное уменьшение продольного размера, в результате чего желудочек имеет форму подковы. МЖП выбухает вправо, создавая впечатление аневризмы, однако кинез ее сохранен;
-
2) замещение миокарда верхушки ЛЖ эпикардиальным жиром — с помощью ЭхоКГ выявляется не всегда, может визуализироваться как гиперэхогенное включение или гиперэхогенный участок акинеза в области верхушки ЛЖ овальной или треугольной формы. В высокоинформативном режиме подавления сигнала от жировой ткани (fatsat) при МРТ сердца данные участки гипоинтенсивны;
-
3) аномальное расположение основания папиллярных мышц на уровне уплощенной верхушки ЛЖ — выраженность изменений папиллярных мышц и подклапанных структур митрального клапана может различаться. В некоторых случаях длина папиллярных мышц удовлетворительная или укорочена, в свою очередь, головки папиллярных мышц могут быть гипоплазированы, а хорды — удлиненными;
-
4) удлиненная полость ПЖ, «окутывающая» верхушку ЛЖ, представленную эпикардиальным жиром, — «бананоподобная форма» ПЖ, когда ПЖ заворачивается вокруг гипоплазированной верхушки ЛЖ, выполняет всю верхушку сердца, создавая эффект «обтекания».
Опубликованные данные литературы свидетельствуют об отсутствии поражения коронарных артерий, отсутствии признаков атрезии митрального и/или аортального клапанов, характерных для синдрома гипоплазии левых отделов сердца [4, 6]. Обращает на себя внимание отсутствие у этих больных ИГВЛЖ межпредсердного и межжелудочкового сообщения [20]. Описываемая врожденная аномалия верхушки ЛЖ чаще встречается при изолированном варианте [21–23]. Однако у трети пациентов данная патология сочетается с другими врожденными пороками сердца, такими как открытый артериальный проток [7], корригированная транспозиция магистральных артерий [9], стеноз аорты и инфундибулярный стеноз легочной артерии [7]. Из сопутствующих аномалий описаны обструкция выводного тракта ПЖ [5], дивертикул ЛЖ [11], некомпактный миокард ЛЖ [4].
Дифференциальная диагностика ИГВЛЖ проводится с дилатационной кардиомиопатией, аритмогенной дисплазией ПЖ, аневризмой ЛЖ, синдромом гипоплазии ЛЖ и некомпактным миокардом [9, 22].
ИГВЛЖ может длительное время протекать бессимптомно, и в большинстве представленных случаев у детей и подростков клинические проявления были незначительными [2, 6, 11–13, 19]. Пациенты молодого возраста и старшей возрастной группы чаще всего предъявляют жалобы на одышку и повышенную утомляемость, имеют низкую толерантность к физической нагрузке. Нарушается систолическая функция ЛЖ и диастолическая дисфункция ЛЖ, чаще всего по рестриктивному типу [2, 3, 16, 18, 20].
A. P. Patrianakos и соавт. [6] описали пятилетнее наблюдение за асимптомным ребенком 11 лет и взрослой пациенткой 35 лет с клиникой отека легких и симптомами хронической сердечной недостаточности, соответствующей функциональному классу II по NYHA на момент госпитализации. За время наблюдения и успешного медикаментозного лечения сердечной недостаточности у пациентки в возрасте 40 лет впервые была зарегистрирована пароксизмальная форма фибрилляции предсердий [6].
Развитие бивентрикулярной сердечной недостаточности с высокой легочной гипертензией сочетается с синкопальными состояниями при ИГВЛЖ [17, 23, 24]. В ряде случаев на первый план клинической картины заболевания выступают нарушения ритма сердца (суправентрикулярные тахикардии, фибрилляция предсердий, пароксизмальные желудочковые тахиаритмии) [1, 5, 6, 11, 13, 14, 18, 19].
Нами проведен анализ доступных для нас публикаций, касающихся клинического течения заболевания у 42 пациентов с ИГВЛЖ. При этом бессимптомное течение заболевания описано в 12 случаях (7 — дети и подростки, 5 — взрослые пациенты); в одном случае наблюдался летальный исход [10, 24], хроническая сердечная недостаточность функциональных классов I–III по NYHA описана у 20 больных, из них у троих пациентов — отек легких, а в шести случаях — фибрилляция предсердий. Сочетание ИГВЛЖ с различными другими аномалиями сердца определяет степень тяжести заболевания от бессимптомного течения в детстве до манифестации бивен-трикулярной хронической сердечной недостаточности с высокой легочной гипертензией у взрослых пациентов, часто с отеком легких и тахиаритмиями, вплоть до летального исхода [2, 13, 22, 24–26]. В ряде работ отмечен хороший ответ на стандартную медикаментозную терапию хронической сердечной недостаточности [26]. Вместе с тем Irving C. A. и соавт. [27] описали летальный случай у подростка, когда после физической нагрузки развившийся пароксизм фибрилляции желудочков осложнился острой декомпенсированной сердечной недостаточностью, отеком легких и высокой легочной гипертензией, рефрактерной к терапии, которая и стала причиной смерти, что было подтверждено данными аутопсии.
Хирургическая тактика ведения ИГВЛЖ впервые применена в России (ФЦССХ, г. Хабаровск) у пациента с ИГВЛЖ в возрасте 32 лет в сочетании с некомпактным миокардом, клиническими проявлениями прогрессирования сердечной недостаточности. Первым этапом была выполнена имплантация двухкамерного кардиовертера дефибриллятора (ИКД) с целью профилактики внезапной смерти. Положительная динамика изменений внутрисердечной гемодинамики, объема левого предсердия, повышение систолической функции ПЖ была отмечена уже после имплантации ИКД. Вторым этапом выполнена радиочастотная абляция (РЧА) ФП с использованием навигационной системы Carto III с последующим наблюдением в течение 6 мес. В результате был восстановлен синусовый ритм, наблюдалось уменьшение объема пред- сердий, улучшение сократительной способности миокарда ЛЖ, сохранялись умеренная легочная гипертензия и диастолическая дисфункция ЛЖ по рестриктивному типу. Наблюдалось увеличение времени теста шестиминутной ходьбы.
Принимая во внимание отсутствие проспективного наблюдения и небольшое число больных ИГВЛЖ, описанных в литературе, прогноз заболевания остается неизвестен, что диктует необходимость рекомендовать более тщательное наблюдение пациентами, формирование регистров, разработку стандартов медикаментозного и хирургического лечения, включающих в тяжелых случаях возможность трансплантации сердца.
Заключение
Таким образом, анализ накопленного в настоящее время материала наблюдений за пациентами с ИГВЛЖ дает основание относить ИГВЛЖ к неклассифицируемым кардиомиопатиям. Клиническое течение данной патологии сердца требует пристального динамического наблюдения даже у бессимптомных пациентов, разработки тактики хирургического лечения, а при неблагоприятном течении заболевания должен рассматриваться вопрос о трансплантации сердца.
Список литературы Изолированная гипоплазия верхушки левого желудочка, редкая врожденная кардиомиопатия
- Fernandez-Valls M., Srichai M.B., Stillman A.E., White R. D. Isolated left ventricular apical hypoplasia: a new congenital anomaly described with cardiac tomography. Heart. 2004; 90(5): 552-555.
- Подзолков В. П., Плахова В. В., Александрова С. А., Тюкина Н. С., Шляппо М. А. Изолированная гипоплазия верхушки левого желудочка -редкая врожденная патология сердца. Детские болезни сердца и сосудов. 2016; 13(3): 117-120
- Сугак А. Б., Сильнова И. В., Басаргина Е. Н., Дворяковский И. В., Барский В. И., Филинов И. В., Дегтярева Т. Д., Архипов Е. Н. Новый диагноз: гипоплазия верхушки левого желудочка сердца. Ультразвуковая и функциональная диагностика. 2013; 3: 79-87 (In Russ).
- Orsborne C., Schmitt M. Isolated left ventricular apical hypoplasia, characterized by cardiac magnetic resonance imaging. Eur. Heart J. 2014; 35: 3303.
- Zhao Y., Zhang J., Zhang J. Isolated Left Ventricular Apical Hypoplasia with Right Ventricular Outflow Tract Obstruction: A Rare Combination. Ann. Noninvasive Electrocardiol. 2015; 20: 502-505.
- Patrianakos A. P., Protonotarios N., Zacharaki A., Tsatsopoulou A., Parthenakis F. I., Vardas P. S. Isolated left ventricular apical hypoplasia: a newly recognized unclassified cardiomyopathy. J. Am. Soc. Echocardiogr. 2010; 3(12): 1336.
- Moon J. I., Jeong Y. J., Lee G., Choi J. H., Lee J. W. Isolated Left Ventricular Apical Hypoplasia with Infundibular Pulmonary and Aortic Stenosis: a Rare Combination. Korean J. Radiol. 2013; 14: 874-877.
- Haffajee J. A., Finley J. J., Brooks E. L., Kuvin J. T., Patel A. R. Echocardiographic characterization of left ventricular apical hypoplasia accompanied by a patent ductus arteriosus. Eur. J. Echocardiogr. 2011; 12(3): E17.
- Chaowu Y., Xin S., Shihua Z., Jianrong L., Hao W. Complete transposition of the atrioventricular valves associated with left ventricular apical hypoplasia. Circulation. 2011; 124: 538-539.
- Melendez G., Munoz L., Meave A. Isolated left ventricular apical hypoplasia. Rev. Esp. Cardiol. 2010; 63(8): 984.
- Sani Z. A., Vojdanparast M., Rezaeian N., Seifi A., Tehrani S. O., Nezafati P. Left ventricular apical hypoplasia: Case report on cardiomyopathy and a history of sudden cardiac death. ARYA Atheroscler. 2016; 12: 50-54.
- Fridon R. M. Black M. D., Benson L. N. Hypoplastic left heart syndrome. In: Allen H. D., Driscol D., Shaddy R., Felles T. F. Moss&Adams' heart Disease in infant, children, and adolescents: including the fetus and young adult. Philadelphia: PA, Lippincott Williams & Wilkins; 2001: 1011-2106.
- Yan C. W., Li J. R., Zhao S. H. Meng H. Sun X. Clinical and cardiac imaging characteristics of patients with left ventricular apical hypoplasia. Zhonghua Xin Xue Guan Bing Za Zhi. 2012; 40(12): 1012-1015.
- Vanhecke T. E., Decker J., Leonowicz N., Chinnaiyan K. M. Isolated left ventricular apical hypoplasia. Congenit. Heart Dis. 2011; 6: 646-649.
- Wang T., Chen H., Ma X., Wang Zh. F. Isolated Left Ventricular Apical Hypoplasia: A Case Report and Literature Review. J. Gen. Pract. (Los Angel). 2016; 4: 4.
- DOI: 10.4172/2329-9126.1000267
- Marin C., Sanchez M. L., Maroto E. Silvia Ossaba Ruiz Y. Zabala J. MR imaging of isolated left ventricular apical hypoplasia. Pediatr. Radiol. 2007; 37(7): 703-705.
- Pica S., Ghio S., Raineri C., Scelsi L., Turco A. Mutation of the lamin A/C gene associated with left ventricular apical hypoplasia: a new phenotype for laminopathies? G. Ital. Cardiol. 2014; 15: 717-719.
- Motwani M., Witte K. K., Plein S., Greenwood J. P. Isolated left ventricular apical hypoplasia evaluated by cardiovascular magnetic resonance and gadolinium enhancement techniques. J. Am. Coll. Cardiol. 2011; 58(22): 2355.
- Starmer G., Younger J. F., Stewart P. Multimodality imaging of isolated left ventricular apical hypoplasia. Eur. Heart J. 2011; 33: 675.
- Mirdamadi А., Ashrafi S. Isolated Left Ventricular Apical Hypoplasia: manifestations and different echocardiography features. Iran. Red. Crescent. Med. J. 2016; 18(8): 260-265.
- Braga C. G., Silva P., Magalhaes S., Bettencourt N., Themudo R. Isolated left ventricular apical hypoplasia. Eur. Heart J. 2014; 15: 1399.
- Ong C. C., Hia C. P., Lim T. C., Teo L. L. Isolated leftventricular apical hypoplasia presenting as a leftventricular mass on echocardiography. Pediatr. Cardiol. 2012; 33(8): 1456-1457.
- Ding W. Y., Meah M., Rao A., Fairbairn T., Hasleton J. Isolated Left Ventricular Hypoplasia in a Postpartum Patient. Can. J. Cardiol. 2016; 32(829): e17.
- Tumabiene K. D., Magpali A. E. Jr., Chiong L. A plump and fatty heart: isolated left ventricular apical hypoplasia. Echocardiography. 2012; 29(8): E193-E196.
- Hong S. A., Kim Y. M., Lee H. J. Three-Dimensional Endo-Cardiovascular Volume-Rendered Cine Computed Tomography of Isolated Left Ventricular Apical Hypoplasia: A Case Report and Literature Review. Korean J. Radiol. 2016; 17(79): 82.
- Flett A. S., Elliott P. M., Moon J. C. Images in cardiovascular medicine. Cardiovascular magnetic resonance of isolated left ventricular apical hypoplasia. Circulation. 2008; 117(25): 504-505.
- Irving C. A., Chaudhari M. P. Fatal presentation of congenital isolated left ventricular apical hypoplasia. Eur. J. Cardiothorac. Surg. 2009; 35(2): 368-369.


