Изучение анксиолитической активности в ряду новых производных диазепинобензимидазола на установке «Приподнятый крестообразный лабиринт»
Автор: Таран А.С., Мальцев Д.В., Яковлев Д.С., Караваева Т.В., Ткаченко Ю.О., Диваева Л.Н., Морковник А.С., Кузьменко Т.А.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Фармакология токсикология
Статья в выпуске: 1 (53), 2017 года.
Бесплатный доступ
В статье приводятся данные по изучению анксиолитической активности соединений, представляющих собой новые производные диазепинобензимидазола - комбинации двух привилегированных структур. В результате тестирования на установке «Приподнятый крестообразный лабиринт» было показано, что соединения ДАБ-7 и ДАБ-19 по изучаемым показателям - латентному времени выхода в открытый рукав, количеству выходов и общему времени нахождения в нем - не уступают показателям препарата сравнения диазепама, что свидетельствует о наличии высокой анксиолитической активности.
Бензодиазепин, бензимидазол, диазепинобензимидазол, анксиолитик, приподнятый крестообразный лабиринт
Короткий адрес: https://sciup.org/142149207
IDR: 142149207 | УДК: 615.214.22:547.785.5
A study of anxiolytic activity of new diazepinobenzimidazoles in the elevated plus maze test
This article provides the data on anxiolytic activity of new diazepinobenzimidazoles - a combination of two privileged structures. We have shown that have the studied parameters of DAB-7 and DAB-19 (latency to enter the open arms, entries in open arms and time spent in open arms) show no significant differences as compared to Diazepam as a reference anxiolytic drug. Therefore, we can conclude the high level of anxiolytic activity of these compounds.
Текст научной статьи Изучение анксиолитической активности в ряду новых производных диазепинобензимидазола на установке «Приподнятый крестообразный лабиринт»
Фармакологическая коррекция тревожнодепрессивных расстройств имеет неоспоримое значение для современной медицины [3], которая располагает большим количеством разнообразных препаратов для предупреждения и лечения нервно-психических заболеваний. В клинической практике чаще всего используют производные бензодиазепинов (диазепам, фе-назепам, лоразепам, медазепам, нитразепам и др.) [5], но большинство таких препаратов обладает неблагоприятными побочными эффектами, заключающимися в угнетении ЦНС: сонливость в дневное время, вялость, мышечная слабость, притупление эмоций, головная боль, головокружение, атаксия и др., возможно, нарушение когнитивных функций, а при длительном применении – привыкание и лекарственная зависимость [2].
В настоящее время активно ведется поиск новых препаратов с анксиолитической активностью и низким риском развития побочных эффектов среди производных пиримидина, пиразола [9–13].
Экспериментальные исследования, проведенные ранее на базе Волгоградского государственного медицинского университета, позволили выявить у производных бензимидазола различные виды активностей: противодиабети-ческую [10], антиагрегантную [4], антиоксидантную [7], противоэпилептическую [6], а также анксиолитическую [14, 15] наряду с низким риском проявления нежелательных эффектов. В связи с этим перспективным является исследование новых соединений с комбинированной структурой, содержащих диазепиновый и бен-зимидазольный фрагменты в рамках поиска и разработки потенциальных анксиолитиков.
ЦЕЛЬ РАБОТЫ
Изучение анксиолитической активности новых производных диазепинобензимидазола.
МЕТОДИКА ИССЛЕДОВАНИЯ
Эксперименты проводили на половозрелых мышах-самцах массой 18–23 г. Животные содержались в условиях вивария с естествен- ным световым режимом на стандартной диете лабораторных животных, без ограничения доступа к еде и воде (ГОСТ Р 50258-92) с соблюдением Международных рекомендаций по защите позвоночных животных, используемых при экспериментальных исследованиях (1997). Животных разделили на группы по 10 животных в каждой.
Изучаемые вещества внутрибрюшинно вводили за 30 минут до начала теста. Контрольным группам мышей вводили изотонический раствор хлорида натрия, животным группы препарата сравнения – диазепам (Реланиум, «Польфа», Польша) в дозе 2 мг/кг, а опытным группам вводили исследуемые вещества в эквимолярных препарату сравнения дозах.
Метод изучения анксиолитической активности в тесте «Приподнятый крестообразный лабиринт» (ПКЛ) был основан на естественном предпочтении грызунами темных нор, а также на страхе нахождения на открытых площадках и падения с высоты [1].
Животных помещали в приподнятый крестообразный лабиринт и в течение 3 минут регистрировали следующие показатели анксиолитической активности: латентное время выхода в открытый рукав (с), количество выходов в открытый рукав и суммарное время, проведенное в открытых рукавах лабиринта (с) [14, 15].
Статистическая обработка результатов исследования проводилась с использованием теста Вилкоксона, критерия Краскела-Уолиса с постобработкой тестом Данна.
Обсчет реализован в программе GraphPad Prism 5.0.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯИ ИХ ОБСУЖДЕНИЕ
В результате исследования было выявлено, что у животных, которым вводили соединение ДАБ-4, сохранялось чувство страха открытого пространства, поэтому латентное время выхода животных в открытый рукав ПКЛ (рис. 1) не отличается от значений контрольной группы.
В опытных группах, которым вводили соединения ДАБ-5, ДАБ-15 и ДАБ-16 снижался показатель латентного времени выхода в светлый рукав – в 2 раза относительно контрольной группы и не уступал показателю в группе диазепама, что свидетельствует о подавлении тревоги у животных.
Соединения ДАБ-7 и ДАБ-19 после введения животным приводили к достоверному снижению латентного времени выхода в светлый рукав в 5 раз относительно контроля, превосходя эффект диазепама.
Также было изучено общее количество выходов животных в светлый рукав ПКЛ.
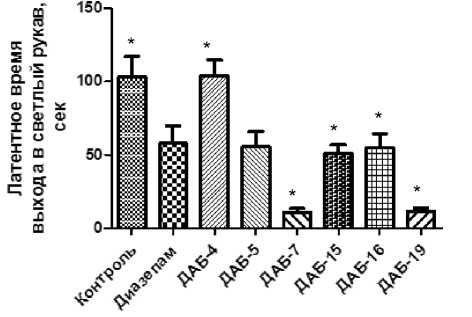
Рис. 1. Влияние диазепама, ДАБ-4, ДАБ-5, ДАБ-7, ДАБ-15, ДАБ-16 и ДАБ-19 на латентное время выхода мышей в открытый рукав в установке ПКЛ
Примечание: * – отличия статистически достоверны по отношению к группе контроля (р < 0,05, по критерию Краскела-Уолиса с посттестом Данна).
Данный параметр можно интерпретировать в как совокупный показатель двух видов активности – исследовательской (изучение нового пространства) и анксиолитической (отсутствие страха выхода из темного рукава). По полученным результатам (рис. 2) при введении соединений ДАБ-4, ДАБ-15 и ДАБ-16 количество выходов в открытый рукав не имело достоверных отличий от такового группы контроля. У животных, которым вводили соединения ДАБ-5, ДАБ-7 и ДАБ-19, достоверно в 2– 2,5 раза увеличивалось количество выходов в светлый рукав и исследуемые показатели не уступали группе препарата сравнения.
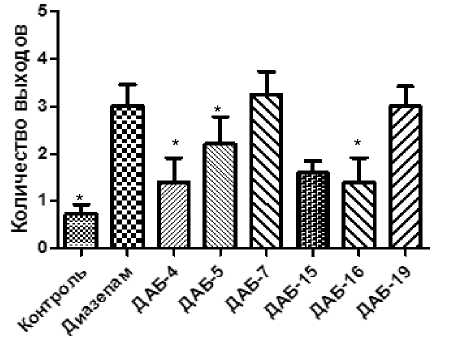
Рис. 2. Влияние диазепама, ДАБ-4, ДАБ-5, ДАБ-7, ДАБ-15, ДАБ-16 и ДАБ-19 на количество выходов в светлый рукав мышей в установке ПКЛ
Примечание: * – отличия статистически достоверны по отношению к группе контроля (р < 0,05, по критерию Краскела-Уолиса с посттестом Данна).
Одним из наиболее значимых критериев оценки при изучении анксиолитической актив- ности в установке ПКЛ является время нахождения животных в открытом рукаве, что указывает на наличие или отсутствие естественных фобий открытых и освещенных пространств у лабораторных животных [8].
Так, при введении животным соединений ДАБ-4, ДАБ-5, ДАБ-7, ДАБ-15 и ДАБ-16 показатель времени нахождения в открытом рукаве достоверно не отличался от показателей контрольных животных (рис. 3). При введении ДАБ-7 и ДАБ-19 проявление тревожности у животных снижалось. Так, время нахождения в открытом рукаве достоверно увеличивалось в 2,5 раза относительно контрольной группы, не уступая показателям группы препарата сравнения – диазепама в дозе 2 мг/кг.
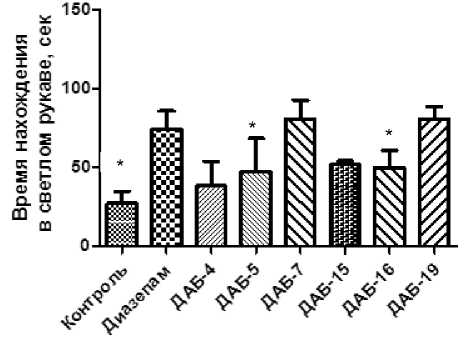
Рис. 3. Влияние диазепама, ДАБ-4, ДАБ-5, ДАБ-7, ДАБ-15, ДАБ-16 и ДАБ-19 на время нахождения мышей в светлом рукаве в установке ПКЛ
Примечание: * – отличия статистически достоверны по отношению к группе контроля (р < 0,05, по критерию Краскела-Уолиса с посттестом Данна).
Изученные производные диазепинобензи-мидазола можно разделить по анксиолитической активности на группы: неактивные, низкоактивные и высокоактивные. Для соединения ДАБ-4 анксиолитической активности не выявлено. Соединения ДАБ-5, ДАБ-15 и ДАБ-16 можно отнести к веществам, проявляющим среднюю по выраженности анксиолитическую активность, так как они снижают латентное время выхода в светлый рукав, увеличивают количество выходов, но не влияют на время нахождения в открытом рукаве. Наиболее значимые эффекты отмечались в группах животных, которым вводили соединения ДАБ-7 и ДАБ-19, достоверно снижающие ощущения страха и тревоги. Так, вещества значительно снижали латентное время выхода в открытый рукав, количество выходов и время пребывания в нём, не уступая по уровню проявления проти- вотревожного действия препарату сравнения диазепаму.
ЗАКЛЮЧЕНИЕ
Таким образом, среди новых производных диазепинобензимидазола обнаружены соединения, проявляющие анксиолитичские свойства. Для изученных соединений выявлен различный уровень антифобического действия. Наиболее активными являются соединения ДАБ-7 и ДАБ-19, которые не уступают эффектам диазепама.
Список литературы Изучение анксиолитической активности в ряду новых производных диазепинобензимидазола на установке «Приподнятый крестообразный лабиринт»
- Багметова В. В., Бородкина Л. Е., Тюренков И. Н, с соавт. ПОИСК АНКСИОЛИТИЧЕСКИХ СРЕДСТВ В РЯДУ НОВЫХ ПРОИЗВОДНЫХ ГАМК И ГЛУТАМИНОВОЙ КИСЛОТЫ//Современные проблемы химической науки и фармации. -2014. -С. 131-132.
- Воронина Т. А.//Руководство по проведению доклинических исследований лекарственных средств: под ред. А. Н. Миронова. -2012. -Ч. 1. -С. 264-275.
- Гурович И. Я., Шмуклер А. Б.//Социальная и клиническая психиатрия. -2011. -Т. 21, № 4. -С. 51-57.
- Морковин Е. И., Тарасов А. С., Степанова В. В., Неделько Е. А.//Международный журнал прикладных и фундаментальных исследований. -2014. -№ 12. -С. 115-118.
- Морковник А. С., Спасов А. А., Кузьменко Т. А, с соавт.//Известия Академии наук. Серия химическая. -2015. -№ 11. -С. 2622.
- Спасов А. А, Анисимова В. А, Гоечко О. Ю., Калитин К. Ю.//Бюллетень экспериментальной биологии и медицины. -2015. -№ 9. -С. 53-56.
- Спасов А. А., Анисимова В. А., Косолапов В. А., Сороцкий Д. В.//Бюллетень экспериментальной биологии и медицины. -2015. -№ 3. -С. 90-93.
- Тюлькова Е. И. Механизмы формирования патологических состояний мозга в ответ на воздействие гипоксии в пренатальном онтогенезе: автореф. дис.. д-ра биол. наук. -СПб., 2015. -C. 19.
- Чепляева Н. И., Кузнецова В. А., Спасов А. А, с соавт.//Волгоградский научно-медицинский журнал. -2014. -№ 3 (43). -С. 21-24.
- Шавловская О. А.//Медицинский алфавит. -2015. -№ 12. -С. 12-16.
- Fitzpatrick C. M., Larsen M., Madsen L. H.//Behav Pharmacol. -2016. -Vol. 27 (6). -P. 549-555.
- Ivachtchenko A. V., Lavrovsky Y., Okun I.//J Alzheimers Dis. -2016. -Vol. 53 (2). -P. 583-620.
- Kaczor A. A., Targowska-Duda K. M., Budzynska B., et al.//Neurochem Int. -2016. -Vol. 96. -P. 84-99.
- Maltsev D. V., Yakovlev D. S., Matokhin D. G., et al.//European neuropsychopharmacology. -2013. -Vol. 23, Sup. 2. -P. S519-S520.
- Yakovlev D., Kolobrodova N., Spasov A., et al. P.4.005 ANXIOLYTIC PROFILE OF 5-HT3-ANTAGONIST RU 1204 VERSUS TROPISETRON AND DIAZEPAM//European neuropsychopharmacology. -2011. -Vol. 21, Sup. 2. -P. S147.


