Изучение генов, контролирующих реакцию дегалогенирования, бактерий-деструкторов 4-хлорбензоата
Автор: Шумковa Е.С., Лобова И.В., Ананьина Л.Н., Плотникова Е.Г.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 5, 2007 года.
Бесплатный доступ
Методом полимеразной цепной реакции проведен скрининг бактерий-деструкторов 4-хлорбензойной кислоты на наличие fcb-генов, контролирующих реакцию дегалогенирования 4-хлорбензоата. Установлено, что Arthrobacter sp. H4, H5, Pseudomonas fluorescens H2, Micrococcus sp. G120 и Rhodococcus ruber Р25 содержат fcbA и fcbB гены, кодирующие 4ХБК-СоА-лигазу и 4ХБК-СоА-дегалогеназу, соответственно. Уровень сходства fcb-генов штамма R. ruber Р25 с деструкторами 4ХБК рода Arthrobacter cjcnfdkztn 95-99%.
Короткий адрес: https://sciup.org/147204393
IDR: 147204393 | УДК: 579.25
Study of genes controlling dehalogenation in bacteria-destructors of 4-chlorbenzoate
Screening of bacteria-destructors of 4-chlorobenzoic acid for fcb-genes controlling the initial stage of 4CBA destruction (dehalogenation) has been made by polymerase chain reaction. It was revealed that strains Arthrobacter sp. H4, H5, Pseudomonas fluorescens H2, Micrococcus sp. G120, and Rhodococcus ruber P25 comprised fcbA and fcbB genes encoding 4CBA-CoA-ligase and 4CBA-CoA-dehalogenase, respectively. The analysis of restriction fragment length polymorphism and comparing of sequenced regions of fcb-genes of Rhodococcus ruber P25 with similar sequences showed 95-99% affinity to fcb-genes of strains-destructors of 4CBA from genus Arthrobacter
Текст научной статьи Изучение генов, контролирующих реакцию дегалогенирования, бактерий-деструкторов 4-хлорбензоата
-
a Институт экологии и генетики микроорганизмов, 614081, Пермь, ул. Голева, 13
-
b Пермский государственный университет, 614990, Пермь, ул. Букирева, 15
Методом полимеразной цепной реакции проведен скрининг бактерий-деструкторов 4-хлор-бензойной кислоты на наличие fcb -генов, контролирующих реакцию дегалогенирования 4-хлорбензоата. Установлено, что Arthrobacter sp. H4, H5, Pseudomonas fluorescens H2, Micrococcus sp . G120 и Rhodococcus ruber Р25 содержат fcb A и fcb B гены, кодирующие 4ХБК-СоА-лигазу и 4ХБК-СоА-дегалогеназу, соответственно. Уровень сходства fcb- генов штамма R. ruber Р25 с деструкторами 4ХБК рода Arthrobacter cjcnfdkztn 95–99%.
К наиболее распространенным и экологически значимым загрязнителям окружающей среды относятся галогенированные ароматические соединения, в том числе полихлорированные бифенилы (ПХБ) и хлорбензойные кислоты (ХБК). Данные ксенобиотики являются высокотоксичными веществами, способными вызывать серьезные нарушения нервной, репродуктивной и иммунной систем животных и человека (Кулинский, 1999). Они характеризуются высокой устойчивостью к физическим и химическим воздействиям, способны накапливаться в значительных количествах в объектах окружающей среды. Известно, что основная роль в трансформации ПХБ и ХБК в природной среде принадлежит микроорганизмам (Dua et al., 1991; Hickey et al., 1993; Abraham et al., 2002). Изучение процессов разложения этих соединений микроорганизмами приобретает все большую актуальность и является основой для разработки методов биоремедиации загрязненных почв и водных объектов.
Микробная деструкция ПХБ в большинстве случаев идет до стадии образования хлорбензойной и пентадиеновой кислот. Полное разложение хлорированных бифенилов осуществляется смешанными культурами бактерий, в состав которых входят деструкторы ХБК (Hickey et al., 1993; Fava et al., 1994; Fava et al. 1996; Abraham et al., 2002). О природных бактериях, способных утилизировать моно- и дихлорированные бифенилы, имеются лишь единичные публикации (Arensdorf, Focht, 1995; Kim, Picardal, 2000). Однако, появляются работы по созданию рекомбинантных штаммов, осуществляющих полную деструкцию хлорбифе- нилов (Havel, Reineke, 1991; Hrywna et al., 1999; Dua et al., 2002; Rodrigues et al., 2006). При конструировании таких микроорганизмов используются клонированные гены, контролирующие реакцию дегалогенирования ХБК. Отщепление галогена от молекулы хлорбензойной кислоты проводит к резкому снижению ее биологической устойчивости и делает это соединение доступным в качестве источника питания для большинства микроорганизмов (Карасевич, 1982).
Реакция дехлорирования 4ХБК, в результате которой происходит замещение иона хлора в пара положении на гидроксильную группу воды и образование пара -оксибензойной кислоты, катализируется ферментной системой, включающей 3 компонента: 4ХБК-СоА-лигазу ( ген fcbA), 4ХБК-СоА-дегалогеназу (ген fcbB ) и пара -оксибензоат-СоА-тиоэстеразу (ген fcbC ) (рис. 1). Подобные ферментные системы обнаружены у ряда деструкторов 4ХБК, в том числе у Arthrobacter globiformis КЗТ1 (Tsoi et al., 1991), Arthrobacter sp. SU (Schmitz et al., 1992), Arthrobacter sp. TM1 (Garte-mann, Eichenlaub, 2001), Pseudomonas sp. DJ-12 (Chae et al., 2000).
Из почв, загрязненных отходами производства галогенированных соединений (ОАО «Галоген», Пермь), выделены бактериальные штаммы, способные использовать в качестве единственного источника углерода разнообразные ароматические соединения (бифенил, нафталин, толуол, бензол, фенол), а также моно- и дихлорированные бензойные кислоты. Изолированные биодеструкторы отнесены к родам Arthrobacter, Micrococcus, Pseudo-
monas , Planococcus и Rhodococcus (Рыбкина, 2003;
Рыбкина и др., 2005). Наиболее интересный из изолированных бактерий штамм Rhodococcus ruber P25 является эффективным деструктором ряда ксенобиотиков, в том числе орто- и пара-замещенных моно- и полихлорированных бифенилов, и он обладает ферментативными системами, отвечающими за деградацию 2ХБК и 4ХБК (Рыб- кина, 2003).
OCoA
АТФ, KoA
O OH
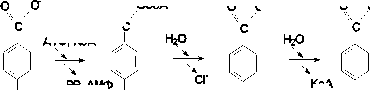
O OСoA
C
Cl 4ХБК fcbC
4ХБК-КоА тиоэстераза
PP, АМФ
Cl
4ХБК-КоА
KoA
OH 4ОБК
OH 4ОБК-КоА fcbB
4ХБК-КоА дегалогеназа
fcbA
4ХБК:КоА лигаза
Рис. 1. Схема гидролитического дегалогенирования 4ХБК штаммом A. globidformis КЗТ1 (Tsoi et al., 1991)
Цель настоящей работы – поиск и изучение fcb -генов, контролирующих реакцию дегалогенирования, бактерий-деструкторов 4ХБК.
Материалы и методы
Рабочая коллекция. В работе использованы бактериальные штаммы, выделенные ранее из образцов почв, отобранных на территории предприятия ОАО «Галоген» (Пермь): Arthrobacter sp. H4, H5, Micrococus sp . G126, G120, Planococcus sp. G110, P. fluorescens H2, P. putida G107, R. ruber P25 (Рыбкина, 2003; Рыбкина и др., 2005), а также биодеструктор 4ХБК A. globiformis КЗТ1 (Tsoi et al., 1991).
Среды и условия культивирования. Для культивирования бактериальных культур использовали минеральную среду К1 следующего состава (г/л): K 2 HPO 4 x 3H 2 O – 4, NaH 2 PO 4 x 2H 2 O – 0,4, (NH 4 ) 2 SO 4 – 0,5, Ca(NO 3 ) 2 – 10, MgSO 4 х 7H 2 O – 0,15, дополненную раствором витаминов (мкг/л): биотин – 0.02, тиамин – 0.5, рибофлавин – 0.5, инозитол – 0.5, рН среды 7.3 (Zaitsev et al., 1991). В качестве ростового субстрата использовали химически чистую 4ХБК (1 г/л) (Fluka, США), которую добавляли в виде водного раствора. Культивирование микроорганизмов проводили в колбах объемом 250 мл в 100 мл среды при 28°С с аэрацией на шейкере (100 об/мин).
Молекулярно-генетические методы. Выделение тотальной ДНК у исследуемых штаммов проводили по стандартной методике (Ausbel et al., 1995). Плазмидную ДНК выделяли модифицированным методом щелочного лизиса (Marko et al., 1982).
Для проведения полимеразной цепной реакции (ПЦР) и определения нуклеотидных последовательностей исследуемых генов были использованы праймеры, сконструированные на основе известных последовательностей fcb-генов штаммов Arthrobac- ter sp. SU и A. globiformis КЗТ1 (GenBank). Праймеры к гену fcbA:
f:5’-AACTGATCCGCCGAGACAACATTC-3’, r:5’-AGGCATTTTTCGAGACGCTTCA-3’;
fcbB : f:5’-GGTCCAGCGAGCGAAATCCAGTC-3’, r:5’-CCCCCGCACACCGCATCAAG-3’.
ПЦР осуществляли на приборе MyCycler (BioRad, США) по стандартной методике (Ausbel et al., 1995). Условия проведения ПЦР: 5 мин. при 95°С, далее 30 циклов: 30 сек. при 94°С, 30 сек. при 60°С, 2 мин. 10 сек. при 72°С.
Для обнаружения ДНК и ПЦР-продуктов применяли электрофорез в горизонтальном агарозном геле (1%) при напряжении 60–90 В в трис-ацетатном буфере (89 мМ Трис, 12.5 мМ Na 2 ЭДТА, 89 мМ ацетата Na, рН 8,0). Агарозные гели окрашивали раствором бромистого этидия (2 мкг/мл) в течение 20 мин. и фотографировали в УФ-свете с помощью системы гель-документирования Gel DocTM XR (BioRad, США). В качестве метчиков использовали ДНК λ / Hind III и молекулярный маркер IX (Sigma, Германия). Размер плазмидной ДНК оценивали сравнивая ее электрофоретическую подвижность с подвижностью плазмидной ДНК известного размера. В качестве маркерной плазмиды использовали pКЗТ1 (110 т.п.н.).
Анализ полиморфизма длин рестрикционных фрагментов (ПДРФ) исследуемых участков fcb -генов осуществляли с помощью эндонуклеаз рестрикции Hha I , Hae III , Eco RI , Eco RV , Bam HI , Pvu II , Mse I (Sigma, Германия). Реакцию проводили при 37°С в течение 1–2 часов в объеме реакционной смеси 20 мкл. Построение карт сайтов рестрикции для участков исследуемых генов осуществляли с помощью программы Vector NTI.
Секвенирование продуктов амплификации проводили по методу Сэнгера с помощью набора CEQ Cycle Sequencing kit на автоматическом секвенаторе CEQ 2000XL DNA Analysis System (Beckman Coulter, США) согласно инструкциям производителя. Полученные нуклеотидные последовательности анализировали с использованием программы Chro-mas 1.45. Нуклеотидные последовательности были выровнены с соответствующими последовательностями других бактерий-деструкторов с помощью программы CLUSTALX 1.83. Построение дендрограмм сходства исследуемых участков ДНК проводили с помощью метода «neighbor-joining», реализованного в пакете программ TREECONW и PHY-LIP. Показатель достоверности порядка ветвления определяли на основании «butstrap»-анализа 100 альтернативных деревьев. Для поиска гомологичных нуклеотидных последовательностей в международных базах данных GenBank/EMBL/DDBJ использовали программу BLAST.
Результаты и обсуждение
Характеристика штаммов-деструкторов
Для настоящей работы были отобраны восемь штаммов, способных использовать в качестве единственного источника углерода и энергии 4-хлорбензоат: Arthrobacter sp. H4, Arthrobacter sp. H5 , Micrococcus sp. G120, Micrococcus sp. G126 , Planococcus sp. G110, P. fluorescens H2, P. putida G107 и R. ruber P25.
Показано, что все бактерии-деструкторы способны к росту на возможных продуктах разложения 4ХБК: пара- оксибензойной и протокатеховой кислотах. Исследуемые штаммы проявляют широкую субстратную специфичность по отношению к различным ароматическим соединениям, способны к росту на феноле, орто -фталате, бензоле и толуоле. Кроме того, изоляты разлагают 2-хлорбензоат (штаммы G120, G126, H2, G107, G110), 3-хлорбензоат и 2,4-дихлорбензоат (штаммы G120, G126, G107, G110) (Рыбкина, 2003; Рыбкина, Гусев, Плотникова, 2005).
Rhodococcus ruber P25 является активным деструктором хлорбифенилов (ХБ): способен утилизировать 2-моноХБ, 4-моноХБ, 2,4-диХБ, 2,2’-диХБ и 4,4’-диХБ, осуществляет 2,3-диоксигенирование ди( орто-пара )хлорированного кольца молекулы 2,4,2’-триХБ и окисляет моно( пара )хлорированное кольцо 2,4,4’-триХБ. Штамм способен к росту на 2ХБК, 4ХБК и 2,4ДХБК, используя данные субстраты в качестве единственного источника углерода и энергии (Рыбкина, 2003).
Известно, что способность к деструкции различных ксенобиотиков, в том числе ХБК, часто определяется генами, расположенными в плазмидах. Исследуемые нами штаммы были проверены на наличие плазмидной ДНК. Плазмиды большого размера были обнаружены в штаммах Arthrobacter sp. Н4 (120 т.п.н.) и P.fluorencens H2 (100 т.п.н.). Ранее было показано, что штамм R. ruber P25 содержит три плазмиды, размеры которых - 110, 90 и 80 т.п.н. Результаты экспериментов по элиминации плазмид позволили предположить, что гены, ответственные за деструкцию 2ХБК и 4ХБК расположены в плазмиде размером 110 т.п.н., гены деструкции бифенила – в плазмиде размером 90 т.п.н., а гены, контролирующие деструкцию нафталина, – в плазмиде размером 80 т.п.н. (Рыбкина, 2003). Таким образом, размер обнаруженных плазмид (100– 120 т.п.н.), предположительно содержащих гены деградации 4ХБК, сопоставим с размером плазмид известных биодеструкторов 4ХБК (Gartemann, Eichen-laub, 2001; Zaitsev et al., 1991). Кроме того, в плазмид-ных ДНК штаммов A.globiformis КЗТ1, Arthrobacter sp. SU были обнаружены fcb -гены, контролирующие первый этап разложения 4ХБК до 4-оксибензоата, дальнейшее разложение которого контролируется хромосомальными генами (Zaitsev et al., 1991; Schmitz et al., 1992).
Скрининг штаммов на наличие fcb-генов методом полимеразной цепной реакции
На матрице ДНК исследуемых штаммов была проведена амплификация нуклеотидных последовательностей, соответствующих участкам fcb- генов, контролирующих первый этап разложения 4ХБК (дегалогенрование) у бактерий. Для выявления генов fcbA и fcbB, кодирующих 4-хлоробензоат-СоА-лигазу и 4-хлоробензоат-СоА-дегалогеназу соответственно, были использованы праймеры, разработанные на основе известных последовательностей fcb- генов штаммов Arthrobacter sp. SU и A. globi-formis КЗТ1 (GenBank).
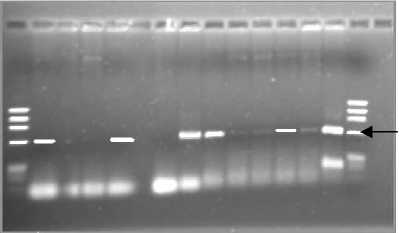
500 п.н.
1 2 3 4 5 6 7 8 9 10 11 12 13 14
Рис. 2. Гель-электрофорез продуктов ПЦР-амп-лификации генов fcb из препаратов ДНК штаммов: H2 ( 2 – fcbA , 8 – fcbB ), G107 ( 3 – fcbA , 9 – fcbB ), G110 ( 4 – fcbA , 10 - fcbB ), G120 ( 5 – fcbA , 11 – fcbB ), G126 ( 6 – fcbA , 12 – fcbB ), КЗТ1 ( 7 – fcbA , 13 – fcbB ), маркер IX ( 1 , 14 )
У пяти из восьми изучаемых штаммов (H4, H5, H2, G120 и Р25) обнаружены ПЦР-продукты длиной около 600 п.н., соответствующие фрагменту гена fcbA. Ампликоны такого же размера, соответствующие участку гена fcbB, получены для всех исследуемых штаммов (рис. 2, 3). Размер гена fcbA у A. globi-formis КЗТ1 (GenBank) составляет 1556 п.н. (позиции 277–1833 секвенированной последовательности ДНК), а гена fcbB – 830 п.н. (позиции 1843–2673 сек-венированной последовательности ДНК). Амплифи-цируемая область гена fcbA , располагающаяся в районе 568–1157 нуклеотидов, соответствует участку около 1/3 длины гена и находится в его центральной части. Амплифицируемый фрагмент гена fcbB располагается в районе 2068–2666 нуклеотидов. Этот участок соответствует большей части гена, за исключением первых 200 п.н. Длина амплифицирован-ных фрагментов fcb -генов с матриц ДНК исследуемых штаммов совпадала с ожидаемой. Полученные данные позволяют предположить наличие у штаммов H4, H5, H2, G120 и Р25 генов, контролирующих дегалогенирование 4ХБК.
Более подробно были исследованы нуклеотидные последовательности фрагментов fcbA и fcbB генов, амплифицированных с матрицы тотальной ДНК R. ruber P25 и Arthrobacter sp. Н4.
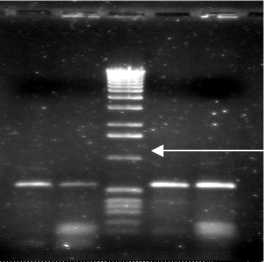
1000 п.н.
1 2 3 4 5
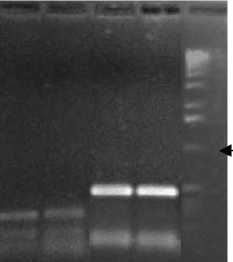
Рис. 3. Гель-электрофорез продуктов ПЦР-амплификации fcb -генов штамма КЗТ1 ( 1, 4 ) и штамма Р25 ( 2,5 ): 1,2 – fcbA , 4,5 – fcbB, 3 – маркер мол. масс 1000 п.н.
галогенирование 4ХБК у штаммов P25 и КЗТ1.
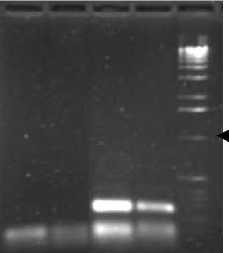
1000 п.н.
1 2 3 4 5
Рис. 5. Электрофореграмма рестрикционных фрагментов, полученных в результате обработки продуктов ПЦР fcbA и fcbB штамма P25 ( 1, 3 ) и штамма КЗТ1 ( 2, 4 ) эндонуклеазой Hha I: 1, 2 – fcbA ; 3, 4 – fcbB ; 5 – маркер мол. масс 1000 п.н.
ПДРФ-анализ fcb -генов штамма R. ruber 25
Для подбора эндонуклеаз рестрикции с помощью программы VectorNTI были построены рестрикционные карты генов fcbA и fcbВ штамма A. glo-biformis КЗТ1. ПЦР-продукты fcb -генов исследуемого штамма P25 и контрольного штамма КЗТ1 обработали следующими рестриктазами: ДНК fcbA - Hha I, Hae III, Eco RV, Bam HI, Mse I, а ДНК fcbB -Hha I, Hae III, Bam HI, Pvu II, Mse I. Картины гидролиза перечисленными выше ферментами ампликонов fcb генов обоих штаммов совпадали (рис. 4, 5) и согласовывались с предполагаемыми результа-
1000 п.н.
1 2 3 4 5
Рис. 4. Электрофореграмма реестрикци-онных фрагментов, полученных в результате обработки продуктов ПЦР fcbA и fcbB штамма P25 ( 1, 3 ) и штамма КЗТ1 ( 2, 4 ) эндонуклеазой Hae III: 1,2 – fcbA , 3,4 – fcbB ; 5 – маркер мол. масс 1000 п.н.
тами построенных рестрикционных карт. Таким образом, полученные результаты говорят о сходстве амплифицированных нуклеотидных последовательностей штаммов, что является дополнительным свидетельством в пользу предположения о сходстве генов/ферментов, осуществляющих де-
Анализ нуклеотидных последовательностей fcb -генов штаммов-деструкторов 4ХБК
На следующем этапе исследования были определены нуклеотидные последовательности ампли-фицированных фрагментов fcbA и fcbB генов штаммов R. ruber P25 и Arthrobacter sp . H4. Для проведения сравнительного анализа полученных нуклеотидных последовательностей с уже имеющимися в международных базах данных Gen-Bank/EMBL/DDBJ последовательностями fcb генов штаммов-деструкторов 4ХБК была использована программа BLAST. Для участка гена fcbA штамма Arthrobacter sp . H4 обнаружено 100% сходство с гомологичными последовательностями штаммов рода Arthrobacter : КЗТ1, FG1, SU, TM1. Уровень гомологии секвенированного участка гена fcbA штамма R. ruber P25 с перечисленными выше штаммами составил 98-99% и 95% – со штаммом Arthrobacter sp . FHP1 (рис. 6).
В результате проведения сравнительного анализа гомологичных нуклеотидных последовательностей, соответствующих участку гена fcbB, обнаружено 100% сходство штамма Arthrobacter sp . Н4 и 98–99% штамма R. ruber P25 со всеми исследованными штаммами рода Arthrobacter (рис. 6).
Уровень гомологии нуклеотидных последовательностей грамотрицательных штаммов ( Pseudomonas sp. DJ-12, Alcaligenes sp. AL3007) с грампо-ложительными штаммами бактерий-деструкторов 4ХБК составил около 60% для обоих исследуемых fcb- генов.
Заключение
Шесть грамположительных и два грамотрица-тельных штамма-деструктора 4-хлорбензоата были
а)
0,1
A. globiformis КЗТ-1 (pCA31 1)
Arthrobacter sp. TM 1 4
Arthrobacter ramosus FG1
Arthrobacter sp. SU (pASU1)
Arthrobacter sp. FHP1
Rhodococcus ruber P25
Pseudomonas sp. DJ-12
Alcaligenes sp. AL3007 (pss70)
б)
0,1
A. globiformis КЗТ-1 (pCA31 1)
Arthrobacter sp. TM 1 4
Arthrobacter ramosus FG1
Arthrobacter sp. SU (pASU1)
Arthrobacter sp. FHP1 [2]
Arthrobacter sp. FHP1 [1]
Rhodococcus ruber P25
Alcaligenes sp. AL3007 (pss70)
Pseudomonas sp. DJ-12
Рис. 6. Древо сходства нуклеотидных последовательностей, гомологичных исследуемым участкам генов fcbА (а) и fcbB (б) R. ruber P25. Масштаб соответствует 10 нуклеотидным заменам на каждые 100 нуклеотидов. “Bootstrap”-анализ проведен на 100 повторностях исследованы на наличие генов, контролирующих начальный этап разложения 4ХБК – гидролитическое дегалогенирование. Скрининг исследуемых бактериальных культур методом полимеразной цепной реакции установил наличие у штаммов Arthrobacter sp. H4, H5, P. fluorescens H2, Microcoсcus sp. G120 и R. ruber P25 генов fcbA и fcbB, кодирующих 4ХБК-СоА-лигазу и 4ХБК-СоА-дегалогеназу соответственно. Данные белки являются компонентами ферментной системы, осуществляющей реакциию дегалогенирования 4ХБК по гидролитическому пути. У штаммов P. fluorescens H2, Arthrobacter sp. Н4 и R. ruber Р25 гены fcb, возможно, локализованы в плазмидах.
ПЦР-анализ ДНК бактериальных культур Micrococcus sp. G126, Planococcus sp. G110, P. putida G107 показал лишь наличие гена fcbB . Можно предположить, что нуклеотидные последовательности fcbA -генов этих деструкторов отличаются от последовательности генов, на основе которых были синтезированы праймеры. Изучение таких генов представляет интерес и будет продолжено.
Гены fcbA и fcbB грамположительных штаммов R. ruber P25 и Arthrobacter sp. H4 были исследованы более детально. ПДРФ-анализ ПЦР-продуктов и сравнительный анализ нуклеотидных последовательностей fcb-генов штамма P25 с гомологичны- ми последовательностями показали их значительное сходство со штаммами рода Arthrobacter.
Таким образом, исследуемые биодеструкторы обладают существенным потенциалом в виде генетических систем деградации пара хлорбензоатов, который в перспективе может быть использован в биотехнологиях по очистке почв и водных объектов, загрязненных галогенсодержащими ксенобиотиками.
Работа поддержана грантом РФФИ-Урал №0404-96042.
Список литературы Изучение генов, контролирующих реакцию дегалогенирования, бактерий-деструкторов 4-хлорбензоата
- Карасевич Ю.Н. Основы селекции микроорганизмов, утилизирующих синтетические органические соединения. М.: Наука, 1982. 144 с.
- Кулинский В.И. Обезвреживание ксенобиотиков.//Соросов. образов. журн. 1999. № 1. C. 8-12.
- Рыбкина Д.О. Исследование аэробных бактерий, разлагающих полихлорированные бифенилы и хлорбензойные кислоты: Дис. …канд. биол. наук. Пермь, 2003. 181 с.
- Рыбкина Д.О., Гусев В.А., Плотникова Е.Г. Почвенные микроорганизмы, разлагающие ароматические углеводороды и карбоновые кислоты.//Вестн. Перм. ун-та. 2005. № 6. Биология. С. 115-122.
- Abraham W.R. et al. Polychlorinated biphenyldegrading microbial communities in soils and sediments.//Curr. Opin. Microbiol. 2002. Vol. 5. P. 246-253.
- Arensdorf J.J., Focht D.D. A meta cleavage pathway for 4-chlorobenzoate, an intermediate in the metabolism of 4-chlorobiphenyl by Pseudomonas cepacia P166.//Appl. Environ. Microbiol. 1995. Vol. 61. P. 443-447.
- Ausbel F.M. et al. Short protocols in molecular biology. Third edition. 1995. 450 p.
- Chae J.C. et al. Genetic structure and functional implication of the fcb gene cluster for hydrolytic dechlorination of 4-chlorobenzoate from Pseudomonas sp. DJ-12.//Gene. 2000. Vol. 258. P. 109-116.
- Dua M. et al. Biotechnology and bioremediation: successes and limitations.//Appl. Microbiol. Biothechnol. 2002. Vol. 59. P. 143-152.
- Fava F. et al. Degradation and dechlorination of lowchlorinated biphenyls by a three-membered bacterial co-culture.//Appl. Microbiol. Biotechnol. 1994. Vol. 41. P. 117 -123.
- Fava F. et al. Aerobic dechlorination of lowchlorinated biphenyls by bactterial biofilms in packed-bed batch bioreactors.//Appl. Microbiol. Biotechnol. 1996. Vol. 45. P. 562-568.
- Gartemann K.H. and Eichenlaub R. Isolation and characterization of IS1409, an insertion element of 4-chlorobenzoate-degrading Arthrobacter sp. strain TM1, and development of a system for transposon mutagenesis//J. Bacteriol. 2001. Vol. 183. P. 3729-3736.
- Havel J., Reineke W. Total degradation of various chlorobiphenyls by cocultures and in vivo constructed hybrid pseudomonads.//FEMS Microbiol. Lett. 1991. Vol. 78. P. 163-170.
- Hickey W.J., Searles D.B., Focht D.D. Enhanced mineralization of polychlorinated biphenyls in soil inoculated with chlorobenzoate-degradin bacteria.//Appl. Environ. Microbiol. 1993. Vol. 59. P. 1194-1200.
- Hrywna Y. et al. Construction and characterization of two recombinant bacteria that grow on ortho-and para-substituted chlorobiphenyls.//Appl. Environ. Microbiol. 1999. Vol. 65. P. 2163-2169.
- Kim S., Picardal F.W. A novel bacterium that utilizes monochlorobiphenyls and 4-chlorobenzoate as a growth substrates.//FEMS Microb. Letters. 2000. V.185. P. 225-229.
- Marko M.A., Chipperfield R., Birnboim H.C. A procedure for the large-scale isolation of highly purified plasmid DNA using alkaline extraction and binding to glass powder.//Analit. Biochem. 1982. Vol. 121. P. 382-388.
- Rodrigues J.L. et al. Degradation of aroclor 1242 dechlorination products in sediments by Burkholderia xenovorans LB400 (ohb) and Rhodococcus sp. strain RHA1 (fcb).//Appl Environ Microbiol. 2006. Vol. 72. P. 2476-2482.
- Schmitz A. et al. Cloning and sequence analysis of genes for dehalogenation of 4-chlorobenzoate from Arthrobacter sp. strain SU.//Appl. Environ. Microbiol. 1992. Vol.58. P. 4068-4071.
- Tsoi T.V. et al. Cloning and expression of the Arthrobacter globiformis KZT-1 fcb gene encoding dehalogenase (4-chlorobenzoatehydroxylase) in E. coli.//FEMS Microbiol. Lett. 1991. Vol. 81. P. 165-170.
- Zaitsev G.M. et al. Genetic control of degradation of chlorinated benzoic acids in Arthrobacter globiformis, Corynebacterium sepedonicum and Pseudomonas cepacia strains.//FEMS Microbiol. Lett. 1991. Vol. 81. P. 171-176.


