Изучение хронической токсичности трифенилфосфония
Автор: Петров М.С.
Статья в выпуске: 1 т.261, 2025 года.
Бесплатный доступ
В эксперименте in vivo у лабораторных крыс определяли хроническую токсичность. Целью данного эксперимента было выявление воздействия трифенилфосфония на организм подопытных животных в течение его длительного применения. Установлено, что у крыс, которым перорально вводили соль фосфония в разных дозах, большинство морфологических показателей крови не имели значимых различий с контролем и находились в пределах референтных значений. В результате длительного введения трифенилфосфония у крыс опытных групп не выявлено значимых различий в макроскопической картине наиболее реактивных внутренних органов по сравнению с таковыми показателями контрольных животных.
Трифенилфосфоний, иммуностимуляция, хроническая токсичность, введение, крысы
Короткий адрес: https://sciup.org/142244547
IDR: 142244547 | УДК: 619:615.917 | DOI: 10.31588/2413_4201_1883_1_261_194
Study of chronic toxicity of triphenylphosphonium
Chronic toxicity was determined in laboratory rats in an in vivo experiment. The purpose of this experiment was to reveal the effect of triphenylphosphonium on the organism of experimental animals during its long-term administration. It was found that in rats orally administered the phosphonium salt in different doses, most morphological blood parameters had no significant differences with the control and were within the reference values. As a result of long-term administration of triphenylphosphonium in rats of the experimental groups, no significant differences in the macroscopic picture of the most reactive internal organs were found compared with those of control animals.
Текст научной статьи Изучение хронической токсичности трифенилфосфония
Устойчивость бактерий к антимикробным препаратам – серьезный вызов для современного здравоохранения и ветеринарии. Систематическое злоупотребление антибиотиками в медицине, в ветеринарии и пищевой промышленности ставит под угрозу население всех стран [9]. Вот почему необходимо рассмотреть альтернативные пути для сохранения иммунного статуса у животных.
Иммуностимуляторы – это соединения, которые могут усиливать клеточный иммунный ответ различными способами, а именно увеличивать количество и активность Т-клеток, NK-клеток и макрофагов и высвобождать интерфероны и интерлейкин. Иммунодефициты развиваются в результате нарушений функциональной активности клеток неспецифической (моноциты, макрофаги, и нейтрофилы) и/или специфической (T- и B-лимфоциты) иммунной системы [1, 2, 3, 5].
Конструирование новых эффективных лекарственных средств, обладающих высокой физиологической активностью и минимальной токсичностью является фундаментальной задачей биомолекулярной, фармацевтической и медицинской химии [4, 6].
В арсенале синтетических биологически активных веществ занимают важнейшее место фосфорорганические соединения, которые нашли широкое применение в сельском хозяйстве в качестве пестицидов, гербицидов и рострегуляторов, а также в ветеринарии и медицине – в качестве лекарственных препаратов. Наибольшее распространение получили соли фосфония на основе трифенилфосфина или линейных фосфинов (три-н-гексилфосфина и три-н-бутилфосфина), что обусловлено, в первую очередь, их доступностью. Варьирование строения соли фосфония и, в частности, увеличение стерического объема заместителей у атома фосфора, может существенно расширить перспективы их использования в качестве реакционной среды и коатирующего реагента для стабилизации наночастиц палладия -высокоэффективных катализаторов реакций кросс-сочетания [9].
Цель работы заключалась в выявлении воздействии трифенилфосфония на организм подопытных животных в течение его длительного применения.
Материал и методы исследований. Проводили определение хронической токсичности трифенилфосфония на белых крысах живой массой от 70 г обоих полов при пероральном введении в соответствии с руководствами по определению доклинических исследований лекарственных средств [7, 8, 10].
Для опыта брали четыре группы лабораторных животных по шесть крыс в каждой. Животным опытных групп трифенилфосфоний вводили перорально в дозе 1/2, 1/3, 1/4 от максимально вводимой (5200 мг/кг) дозы (первая, вторая, третья группы соответственно). Также была создана контрольная группа животных (четвёртая группа), которым вводили только дистиллированную воду. Введение вещества продолжалось ежедневно в течение 21 дня совместно с измерением массы тела подопытных. Вещество измерялось при помощи весов и растворялось в дистиллированной воде для дальнейшего введения его в желудок при помощи пищеводного зонда с оливой на конце и присоединённого шприца. Об общем действии препарата судили по изменению поведения животных, появлению у них после введения препарата тех или иных признаков, не наблюдавшихся в параллельном контроле после применения плацебо.
Также у испытуемых каждые семь дней отбирали кровь из хвостовой вены для проведения её морфологического анализа. Гематологические показатели определяли на автоматическом геманализаторе «URIT-3020».
По окончании опыта животные всех групп были подвергнуты эвтаназии с помощью эфира диэтилового для макроскопического исследования внутренних органов. Исследованию подвергались печень, почки, желудок, селезёнка, поджелудочная железа, сердце, лёгкие.
Проводили статистическую обработку полученных данных методом вариационной статистики посредством сравнения средних по критерию t-Стьюдента.
Доклинические исследования были проведены при строгом соблюдении всех требований Европейской конвенции «О защите позвоночных животных, используемых для экспериментальных или иных целей».
Результат исследований. Все животные содержались в помещении вивария на территории Казанской ГАВМ. Животных не ограничивали в воде и корме, но за 8 часов перед введением трифенилфосфония прекращали кормить. Внешний осмотр животных показал, что подопытные как до, так и после введения вещества имели хороший аппетит, умеренную жажду, их суточная активность была свойственна животным контрольной группы, которым вводили дистиллированную воду. Слизистые оболочки ротовой полости у опытных животных имели бледно-розовый цвет, умеренную влажность, сохранили свою целостность. Кожа не имела внешних признаков воспаления, шёрстный покров был сохранён.
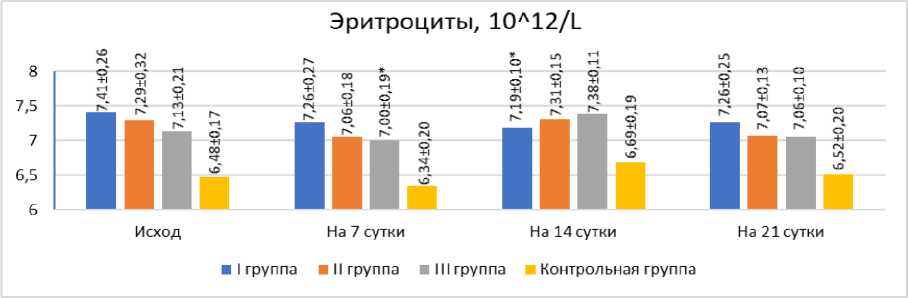
Рисунок 1 – Количество эритроцитов в крови крыс после применения трифенилфосфония
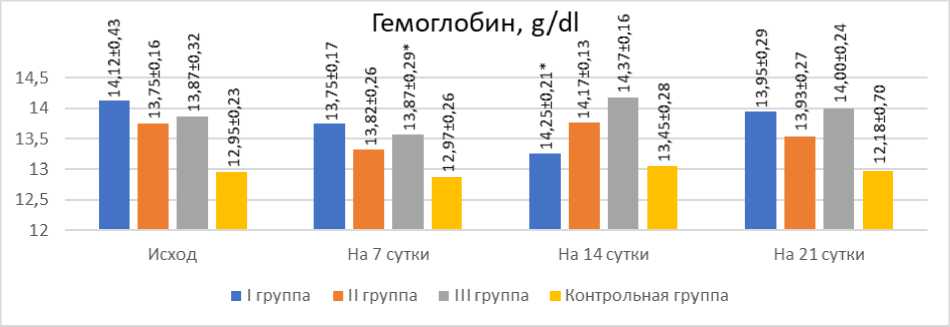
Рисунок 2 – Уровень гемоглобина в крови крыс после применения трифенилфосфония
Еженедельный анализ крови показал, что между значениями эритроцитов и гемоглобина при длительном применении препарата была прямая зависимость (Рисунок 1, 2).
На 7 сутки исследования в третьей и на 14 сутки в первой группе была выявлена достоверная разница в содержании эритроцитов и гемоглобина в крови испытуемых по сравнению с контролем (p≤0,05). Через 7 суток применения (Таблица 1) трифенилфосфония количество лейкоцитов в первой группе было больше на 2,42*10^9/L, во второй на 2,09 и в третьей на 2,04 по сравнению с контрольными животными (p≤0,05). Такая разница сохранилась и в другие сроки исследования. Гранулоциты крови, играющие важную роль в развитии воспаления и иммунной защите, превышали показатели контрольных крыс на 14 сутки введения в третьей группе и на 21 сутки во второй группе (p≤0,05).
Уровень гематокрита в опытных группах животных во все сроки исследования был выше, чем у контрольных, но достоверные значения были только в первой группе. Все эти изменения не выходили за пределы физиологической нормы и, видимо, являются ответной реакцией организма на введение трифенилфосфония.
Результаты вскрытия показали, что в исследуемых органах не было замечено макроскопических патологических изменений. Органы имели сохранённый рисунок. Печень в своих размерах не увеличена, тёмно-красного цвета, имела однородную структуру на разрезе, острые края. Почки имели бобовидную форму, внешне были примерно одинакового размера, рисунок строения на месте разреза сохранён. Почечные лоханки не были подвержены петрификации, не имели отложений в своих полостях. Поджелудочная железа имела сохранённую конфигурацию, была бледного цвета. Желудок внешне имел сохранённую целостность, имел ненарушенную слоистость. Лёгкие были полновоздушными, структура их сохранена. Сердце имело округлую форму, было кровенаполнено. Селезёнка была тёмно-вишнёвого цвета, имела в продольном сечении треугольную форму, острые края, однородную структуру.
Заключение. При многократном пероральном введении трифенилфосфоний хорошо переносится крысами, не было выявлено токсических эффектов. В результате проведённого после эвтаназии патологоанатомического вскрытия экспериментальных животных макроскопическая картина наиболее реактивных внутренних органов крыс опытных групп, получавших испытуемый препарат в дозах 1/2, 1/3/, 1/4 от максимально вводимой разовой дозы 5200 мг/кг, была идентичной таковой, наблюдаемой у контрольных животных, получавших дистиллированную воду.
Таблица 1 – Морфологические показатели крови крыс после применения трифенилфосфония
|
Показатель |
Опытная группа |
Контрольная группа |
||
|
I группа |
II группа |
III группа |
||
|
Исходные показатели |
||||
|
Лейкоциты, 10^9/L |
8,07±0,72 |
7,93±0,62 |
7,63±0,29 |
5,45±0,92 |
|
Лимфоциты, 10^9/L |
5,30±0,28 |
3,35±0,23 |
3,33±0,18 |
4,25±0,31 |
|
Базофилы, эозинофилы, моноциты, 10^9/L |
0,2±0,04 |
0,22±0,05 |
0,18±0,03 |
0,07±0,04 |
|
Гранулоциты, 10^9/L |
2,08±0,33 |
1,72±0,16 |
1,82±0,23 |
1,20±0,14 |
|
Гематокрит, % |
40,37±0,60 |
41,50±1,1 |
41,03±0,71 |
38,32±0,70 |
|
Тромбоциты, 10^9/L |
734,83±22,45 |
791,50±32,13 |
755,50±36,78 |
644,33±29,14 |
|
На 7 сутки применения трифенилфосфония |
||||
|
Лейкоциты, 10^9/L |
9,05±0,61* |
8,72±0,26* |
8,67±0,24* |
6,63±0,61 |
|
Лимфоциты, 10^9/L |
5,48±0,23 |
4,78±0,41 |
4,27±0,28 |
5,37±0,67 |
|
Базофилы, эозинофилы, моноциты, 10^9/L |
0,43±0,10* |
0,33±0,05 |
0,47±0,10* |
0,18±0,03 |
|
Гранулоциты, 10^9/L |
2,53±0,16 |
2,57±0,16 |
2,58±0,16 |
1,68±0,33 |
|
Гематокрит, % |
42,13±0,37 |
42,87±0,9 |
42,62±0,78 |
39,63±0,99 |
|
Тромбоциты, 10^9/L |
716,67±20,58 |
717,33±21,32 |
717,17±27,60* |
614,67±34,44 |
|
На 14 сутки применения трифенилфосфония |
||||
|
Лейкоциты, 10^9/L |
11,28±1,13** |
9,77±1,06* |
8,28±0,57* |
5,73±0,81 |
|
Лимфоциты, 10^9/L |
7,65±0,60 |
6,75±0,41 |
6,40±0,28 |
5,07±0,43 |
|
Базофилы, эозинофилы, моноциты, 10^9/L |
0,30±0,04 |
0,35±0,05 |
0,33±0,07 |
0,15±0,05 |
|
Гранулоциты, 10^9/L |
2,37±0,19 |
2,27±0,21 |
2,25±0,24* |
1,45±0,26 |
|
Гематокрит, % |
42,17±0,47* |
42,20±0,37 |
42,62±0,85 |
39,30±1,14 |
|
Тромбоциты, 10^9/L |
780,83±9,28* |
789,50±21,59 |
814,50±42,85 |
653,33±56,19 |
|
На 21 сутки применения трифенилфосфония |
||||
|
Лейкоциты, 10^9/L |
15,12±0,45** |
13,17±0,6 |
12,93±0,49 |
10,13±1,13 |
|
Лимфоциты, 10^9/L |
9,50±0,26 |
7,38±0,31 |
6,92±0,23 |
5,48±0,48 |
|
Базофилы, эозинофилы, моноциты, 10^9/L |
0,30±0,04 |
0,33±0,06 |
0,33±0,05 |
0,15±0,05 |
|
Гранулоциты, 10^9/L |
2,58±0,16 |
2,48±0,13* |
2,63±0,21 |
1,83±0,24 |
|
Гематокрит, % |
42,67±0,44* |
43,33±0,57 |
43,62±0,48 |
40,97±0,58 |
|
Тромбоциты, 10^9/L |
801,67±39,25 |
751,83±31,73* |
781,17±30,70 |
617,17±49,66 |
Примечание: * - P <0,05; ** - P <0,02
Список литературы Изучение хронической токсичности трифенилфосфония
- Агнес Ш.Х. Антимикробные улитки в качестве иммуностимулятора модификатора биологического ответа / Ш.Х. Агнес, Р. Путринингрум // Микробиология Индонезии. - 2019. - № 3. - С. 56-63.
- Алтынбеков О.М. Коррекция антител к возбудителям вирусных инфекций в крови телят применением иммуностимулирующих препаратов / О.М. Алтынбеков, А.В. Андреева // Ветеринария и кормление. - Москва, 2019. - № 4. - C. 14-17. EDN: WSUPJI
- Асрутдинова Р.А. Оценка иммунного статуса поросят в условиях свиноводческих комплексов / Р.А. Асрутдинова, Л.В. Резниченко // Достижения науки и техники АПК. -2009. - № 5. - 51 с. EDN: LURLVJ
- Камалиев А.Р. Оценка безопасности некоторых полисахаридов /А.Р. Камалиев, М.Г. Сагитова, Р.А. Асрутдинова // Ученые записки Казанской государственной академии ветеринарной медицины им. Н.Э. Баумана. - 2014. - Т. 217.- № 1. - С. 109-112. EDN: SAMJHN
- Ковзов В.В. Эффективность применения иммуностимуляторов, препаратов для коррекции обменных процессов у стельных коров и повышения устойчивости телят к обменным и желудочно-кишечным болезням / В.В. Ковзов, С.Л. Борознов // Ученые Записки УО ВГАВМ, Т. 47. - 2011. - № 1. - С. 177181.
- Маланин Л.П. Ветеринарные препараты: справочик / Л.П. Маланин, А.П. Морозов, А.С. Селиванов; под ред. А.Д. Третьякова. - М.: Агропромиздат, 1988. - 319 с.
- Миронова, А.Н. Руководство по определения доклинических исследований лекарственных средств / под ред. А.Н. Миронова. - М.: Гриф и К. - 2012. - Ч.1. -944 с.
- Першин, Г.Н. Методы экспериментальной химиотерапии / Г.Н. Першин. - М.: Медицина, 1971. - С. 171195.
- Пинто Т.К.А. Производные трифенилфосфония как альтернатива обычным антибиотикам / Т.К.А. Пинто, А. Банержи, П.А. Назаров // Вестник Российского государственного медицинского университета. - 2018. - № 5. - С. 16-21. EDN: XQWGYH
- Смирнов, А.М. Научнометодологические аспекты исследования токсических свойств фармакологических лекарственных средств для животных / А.М. Смирнов, В.И. Дорожкин // Рос. акад. с.-х. наук. - Москва, 2008. - 120 с.


