Изучение иммунореактивности ВЛКРС-инфицированных коров на основе ПЦР-ПДРФ анализа гена ENV BLV
Автор: Якупов Т.Р., Усольцев К.В., Шангараев Р.И., Зиннатов Ф.Ф., Масленников Н.Н.
Статья в выпуске: 3 т.259, 2024 года.
Бесплатный доступ
В статье описываются результаты исследования сывороток крови методом ИФА и ПЦР-ПДРФ анализа гена env BLV в целях изучения особенностей иммунореактивности, инфицированных вирусом лейкоза крупного рогатого скота. Результаты ИФА показали, что 64.1% исследованных проб сывороток крови от ВЛКРС инфицированных коров положительно реагировали на микобактериальные антигены. Результаты сравнительного изучения данных ПЦР-ПДРФ анализа ДНК изолятов и ИФА свидетельствуют о том, что антитела против антигенов 4 генотипа ВЛКРС больше склонны проявлять перекрестные реакции с антигенами M.Avium, а антитела против 7 генотипа – с антигенами M.Bovis.
Лейкоз, антитела, ИФА, ПЦР-ПДРФ анализ, ВЛКРС, микобактерии
Короткий адрес: https://sciup.org/142242508
IDR: 142242508 | УДК: 619:616.002.5-07.636.2.9 | DOI: 10.31588/2413_4201_1883_3_259_313
Studying the immunoreactivity of BLV-infected cows based on PCR-RFLP analysis of the ENV BLV gene
The results of a study of blood serum using ELISA and PCR-RFLP analysis of the BLV env gene in order to study the characteristics of the immunoreactivity of cattle infected with the leukemia virus the article described. The ELISA results showed that 64.1 % of the studied blood serum samples from BLV-infected cows reacted positively to mycobacterial antigens. The results of a comparative study of data from PCR-RFLP analysis of DNA isolates and ELISA indicate that antibodies against genotype 4 antigens of VLCRS are more likely to exhibit cross-reactions with M.Avium antigens, and antibodies against genotype 7 are more likely to cross-react with M.Bovis antigens.
Текст научной статьи Изучение иммунореактивности ВЛКРС-инфицированных коров на основе ПЦР-ПДРФ анализа гена ENV BLV
Вопросы о возможности реакций на туберкулин у скота, инфицированного с ВЛКРС и о положительной реакции в РИД у коров, инфицированных микобактериями несмотря на то, что для борьбы с этими инфекциями предлагаются самые современные высокоэффективные методики и технологии, в научной литературе остаются открытыми [1]. Встречаются утверждения разнопланового характера. Если одни выявляют прямую связь между уровнем инфицированности ВЛ КРС и реагированием животных на туберкулин, то другие утверждают, что крупный рогатый скот с диагнозом на лейкоз по гематологическим показателям, а также инфицированный ВЛ КРС, как правило, не реагируют на туберкулин [2, 3]. Причинами таких утверждений, несомненно, являются как сложная антигенная структура микобактерий, у которых выявляется множество антигенов общих для всех групп микобактерий [4, 6], так и неоднородность, перекрестная реактивность, постоянное изменение титров и спектров антител, соотношения между свободными и связанными антителами к ВЛКРС у инфицированных животных с развитием инфекционного процесса [5]. Целью данной работы было изучение иммунореактивности ВЛКРС инфицированных коров на основе ПЦР-ПДРФ анализа гена env BLV.
Материал и методы исследований. Иммуноферментный анализ ставили по стандартной методике в твердофазном неконкурентном варианте. Для обнаружения противотуберкулезных антител применяли липополисахаридные антигены M. bovis, M. avium и M. sctochromogenes.
Постановка ПЦР осуществлялась с помощью гнездовых праймеров по методике, описанной Fechner Hetal [8]. Выделение ДНК осуществлялось из осадка после центрифугирования с помощью набора «Рибо-преп» производства Интерлабсервис согласно инструкции производителя.
Для рестрикционного анализа применялись рестриктазы: PvuII, SspI, BstDEI, BamHI. Реакционная смесь на 1 реакцию – 10-ти кратный реакционный буфер – 1 мкл, рестриктаза – 1 мкл, бычий сывороточный альбумин (БСА) (100 мкг/мл) – 0,1 мкл. Программа рестрикции: для PvuII, SspI и BamHI – 37 ℃ - 1 час, 80 ℃ - 20 мин; для BstDEI – 60 ℃ - 1 час, 80 ℃ - 20 мин. Детекцию результатов проводили посредством горизонтального электрофореза в 2,5 % агарозном геле.
Результат исследований. Всего исследовано методом ИФА 300 проб сывороток крови, полученные из разных хозяйств Республики Татарстан. Все исследуемые сыворотки крови были РИД положительными 95.6 % (287) проб в ИФА на обнаружение противолейкозных антител показали положительные результаты. Все пробы положительные в
ИФА на лейкоз крупного рогатого скота были исследованы на обнаружение микобактериальных антител с использованием антигенов М. bovis, M. avium и M. sctochromogenes. В результате в 168 пробах (64,1 %) обнаружены микобактериальные антитела. В том числе 38 проб реагировали только на M. Avium, 18 – на M. Bovis и 7 – на M. Scot. Все 168 проб были в дальнейшем исследованы методом ПЦР на лейкоз (провирусная ДНК Bovine leukemia virus) и туберкулез (M. bovis). Предварительно образцы сыворотки крови были осаждены при 13000 об/мин в течение 10 мин. Выделение ДНК проводили из осадка после центрифугирования посредством набора «ДНК-сорб В» (Интерлабсервис) согласно инструкции производителя. Постановка ПЦР на лейкоз выполнялась по следующему протоколу. Приготовление ПЦР-смесей (на 1 образец) осуществляли по представленной ниже прописи: 2 мкл 10-ти кратного ПЦР-буфера, 2 мкл 2,5 мМ раствора нуклеозидтрифосфатов, 2 мкл 25 мМ раствора магния хлорида, по 1 мкл 10 рМ прямого (5’-ggcaccgggtctcgcaagtatg-3'), обратного (5'-cggttaggctggtcatgtggcc-3')
праймеров и олигонуклеотидного зонда типа TaqMan (ROX- aaacactacgacttgcaatcttacaggccgac-RTQ2) (праймеры и зонд патент RU 2644233 C2), 1 мкл Taq-полимераза (5 ед.акт./мл), 10 мкл исследуемого образца ДНК. Для идентификации M. bovis методом ПЦР-РВ были использованы праймеры
(IS1081_Forward – ggctgctctcgacgttcatc,
IS1081_Reverse - cgctgattggaccgctcat) и олигонуклеотидный зонд (IS1081_Probe – FAM-ctgaagccgacgccctgtgc-MGBNFQ), разработанные Duffy SC et al (7).
Результаты ПЦР подтвердили отсутствие в пробах генетического материала микобактерий и три пробы в ПЦР на ВЛКРС были отрицательные. Методом случайной выборки из каждой группы свороток крови отобрали по 5 проб и использовали для ПЦР-ПДРФ анализ гена envBLV. Всего 15 проб, где первые 5 – реагирующие на M.Avium, следующие 5 – на M.Bovis и на M.Scot. Детекцию результатов проводили посредством горизонтального электрофореза в 2,5 % агарозном геле (Рисунок 2 и 3).
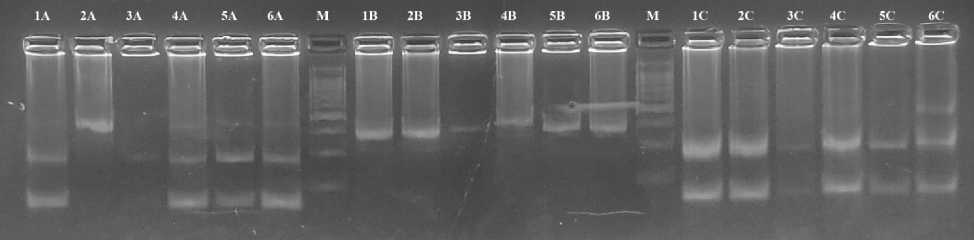
Рисунок 2 – Результаты ПЦР-ПДРФ гена env BLV . Обозначения: М – маркер молекулярного веса ДНК от 100 до 1000 пар нуклеотидов (п.н.); 1А – 6А – образцы ДНК, обработанные рестриктазой PvuII; 1B – 6B – образцы ДНК, обработанные рестриктазой SspI; 1C – 6C – образцы ДНК, обработанные рестриктазой BstDEI
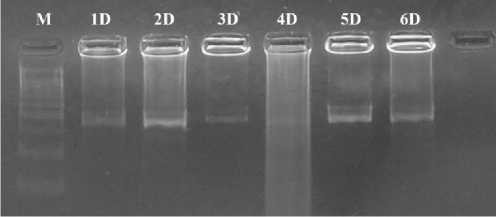
Рисунок 3 – Результаты ПЦР-ПДРФ гена env BLV . Обозначения: М – маркер молекулярного веса ДНК от 100 до 1000 пар нуклеотидов (п.н.); 1D – 6D – образцы ДНК, обработанные рестриктазой BamHI
При ПЦР-ПДРФ анализе ДНК изолятов 1-5 с использованием рестриктазы PvuI идентифицировали два паттерна размером 164 и 280 п.н., что, согласно филогенетической классификации, представленные изоляты могут иметь отношение к четвёртому генотипу. А в ДНК изолятов 6-15 обнаружен один паттерн размером 444 п.н., следовательно, данный изолят имеет отношение седьмому или восьмому генотипу.
При применении рестриктазы SspI в ДНК всех изолятов обнаруживается единичный паттерн размером от 395 до 444 п.н., что не позволяет точно определить принадлежность к тому или иному генотипу. Необходимо выполнить дополнительные исследования.
Использование рестриктазы BstDEI, которая является изошизомером эндонуклеазы DdeI, позволило определить наличие двух паттернов величиной 168 и 276 п.н. во всех исследуемых изолятах, что скорее всего относит их четвёртому или седьмому, или восьмому генотипам.
Применив рестриктазу BamHI), было обнаружено, что в первых 5 анализируемых образцах ДНК выявлен только паттерн величиной в 444 п.н., следовательно, данные изоляты вероятно всего относятся к четвёртому генотипу.
Таким образом проведенный рестрикционный анализ позволяет приблизительно заключить, что изоляты №№ 1-5 относятся к четвертому генотипу, а 6-10 к седьмому. Однако, полученные результаты желательно подтвердить дополнительными исследованиями, например, секвенированием ДНК.
Заключение. Представленные результаты исследований позволяют заключить как о возможной детерминантной общности антигенов ВЛКРС и микобактерий, так и об изменениях в иммунореактивности организма коров, инфицированных ВЛ КРС. Результаты сравнительного изучения данных ПЦР-ПДРФ анализа и ИФА ДНК изолятов свидетельствуют о том, что антитела против антигенов 4 генотипа ВЛКРС больше склонны проявлять перекрестные реакции с антигенами M. Avium, а антитела против 7 генотипа – с антигенами M. Bovis. Однако, нужно помнить, что более 100 из исследованных проб сывороток крови положительные результаты показывали в ИФА одновременно против нескольких видов микобактериальных антигенов. Причиной такой неоднородности и перекрестной реактивности безусловно, является постоянное изменение титров и спектров антител к ВЛКРС у инфицированных животных с развитием инфекционного процесса (5). А также, как отмечает Иванов О.В. (1), инфицирование организма ВЛКРС приводит к нарушению регулирования иммунной системы хозяина как на клеточном (поражение В-лимфоцитов, части Т-лимфоцитов, моноцитов), так и на гуморальном уровне (дефицит IgM, IgA).
Безусловно, для дальнейших утверждений требуются более глубокие исследования, однако, неоспоримым является то, что при проведении диагностических мероприятий на лейкоз и туберкулез крупного рогатого скота необходимо учитывать эпизоотическую ситуацию по этим инфекциям.
Список литературы Изучение иммунореактивности ВЛКРС-инфицированных коров на основе ПЦР-ПДРФ анализа гена ENV BLV
- Иванов, О. В. Качество серологической диагностики – гарантия оздоровления стада от лейкоза крупного рогатого скота / О. В. Иванов, О. Ю. Иванова // Farm Animals. – 2014. – № 3. – С. 26-29.
- Магер, С. Н. Биологическая характеристика потомства здоровых и больных лейкозом коров, и ассоциативное развитие лейкоза и туберкулеза у животных / С. Н. Магер // Автореферат дис. … док. биол. наук, Новосибирск. – 2006.
- Сорокина, А. И. Изучение влияния инфицированности вирусом лейкоза и гельминтозов на проявление аллергических туберкулиновых реакций у крупного рогатого скота / А. И. Сорокина // Автореферат дис. … канд. вет. наук, Благовещенск. – 2000.
- Якупов, Т. Р. Молекулярно- генетические и иммунохимические методы в диагностике, индикации и идентификации возбудителей туберкулеза и лейкоза крупного рогатого скота / Т. Р. Якупов // Автореферат дис. … док. вет. наук. – Казань. – 2011. – 49 с.
- Якупов, Т. Р. Новые подходы в диагностике лейкоза крупного рогатого скота / Т. Р. Якупов // Ученые записки Казанской государственной академии ветеринарной медицины им. Н.Э. Баумана. – 2010. – Т. 204. – С. 342-347.
- Alok Choudhary. Characterization of the Antigenic Heterogeneity of Lipoarabinomannan, the Major Surface Glycolipid of Mycobacterium tuberculosis and Complexity of Antibody Specificities toward This Antigen / C. Alok, P. Deendayal, H. William [et all.] // J. Immunol. – 2018. – P. 3053-3066.
- Duffy, S. C. Development of a Multiplex Real-Time PCR Assay for Mycobacterium bovis BCG and Validation in a Clinical Laboratory.MicrobiolSpectr / S. C. Duffy, M. Venkatesan, S. Chothe [et all.] // Spectrum.01098-21. Epub. – 2021.
- Fechner, H. Provirus variants of the bovine leukemia virus and their relation to the serological status of naturally infected cattle / H. Fechner, P. Blankenstein, А. Looman [et all.] // Virology. – 1997. – P. 261-9. – doi: 10.1006/viro.1997.8784. PMID: 9356338).


