Изучение кето-енольной таутомерии пептидной связи глицилглицина при комплексообразовании с ионами металлов
Автор: Кадырова Р.Г., Кабиров Г.Ф., Муллахметов Р.Р.
Статья в выпуске: 1 т.221, 2015 года.
Бесплатный доступ
Изучена кето-енольная таутомерия пептидной связи глицилглицина в зависимости от рН реакционной среды. Показано, что в кислой среде не идет превращение амидной группы в иминольную (енольную). В щелочной среде (рН 8,5) (при эквимолярном соотношении субстрата и щелочи) глицилглицин из кетоформы превращается в енольную форму мононатриевого производного. При последующем действии на реакционную смесь солями металлов (рН 5) енольная форма переходит в кетонную с образованием глицилглицинатов металлов в кетоформе. В сильно щелочной среде (рН 11-12) (соотношение субстрат: щелочь 1 : 2 моль) глицилглицин из кетоформы превращается в енольную форму динатриевого производного, при последующим действии на который сульфатом меди (II) получается двойной медный комплекс в енольной форме.
Пептиды, глицилглицин, комплексные соли марганца, железа, кобальта, цинка, меди, пептидная связь, таутомерия
Короткий адрес: https://sciup.org/14288517
IDR: 14288517 | УДК: 547.461.4
Keto-enol glycylgycine peptide bond tautomerismstudy at complexation with metal ions
Keto-enolglycylglycine peptide bond tautomerism depending on the pH of the reaction medium was studied. It has been shown that there is no conversionof theamide group into an iminol (enol) groupin an acidic environment. In an alkaline medium (pH 8.5) (at an equimolar ratio of the substrate and base) glycylglycineis converted from keto- form into monosodium enol derivative. At follow-up action on the reaction mixture with metal salts (pH 5)the enol form is converted into a ketone one to form metalsglicylglicinate in the keto- form. In a highly alkaline environment (pH 11-12) (substrateratio : alkali of 1: 2 mol) glycylglycineis converted from keto-form into the enol form of disodium derivative, followed by action on which with copper sulfate (II) double coppercomplex in the enol form isobtained.
Текст научной статьи Изучение кето-енольной таутомерии пептидной связи глицилглицина при комплексообразовании с ионами металлов
В последние годы активно развивается фармакология физиологически активных пептидов. Выделено и изучено несколько сотен природных пептидов, которые играют самостоятельную физиологическую роль. Пептидные антибиотики синтезируются микроорганизмами, например грамицидин- S , в состав которого входят остатки аминокислот – орнитина и D -изомеры фенилаланина. Регуляторные пептиды – пептидные гормоны, регулирующие многие химические реакции в клетках и тканях организма (например инсулин, вазопрессин и др.). Интенсивно развивается учение о нейропептидах. К ним относятся пентапептиды (энкефалины), выделенные из мозга животных, которые оказывают обезболивающее действие и используются как лекарственные средства [1].
В ГУНИИ фармакологии имени В.В. Закусова РАМН созданы оригинальные нейротропные глицин- и пролинсодержащие дипептидные соединения, при комплексном исследовании которых продемонстрированы их
+NH3 - CH(R1) - CO - иммунокорригирующие свойства и противовоспалительное действие [2].
Получены высокоэффективные дипептидные лекарственные препараты: ноотроп, ноопепт, антипсихотик дилепт нейропротектор KF-2 и др. [3].
Ранее нами [4] были проведены экспериментальные исследования по изучению комплексообразующей способности дипептида глицилглицина с ионами 3 d -биогенных металлов. Показано, что комплексообразование глицилглицина с ионами металлов может идти по амино-, карбоксильной и пептидной группам в зависимости от рН реакционной среды. В оптимальных условиях синтезированы комплексонаты глицилглицина с высокими выходами [4].
Комплексообразование дипептидов с ионами биогенных металлов представляет интерес, так как позволяет моделировать биологические системы, в которых свойства белка модифицированы присоединением иона металла. Дипептиды в водном растворе существуют в виде цвиттер-ионов:
NH - CH(R2) - COO-
Пептидная (амидная) группа является р,P—сопряженной системой, в которой сопряжена с кетогрупп:
электронами л -связями
неподеленная пара электронов атома азота
.. О
NH C
Делокализация электронной плотности в пептидной группе может быть представлена резонансными структурами:
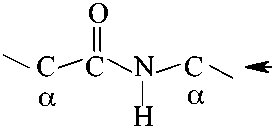
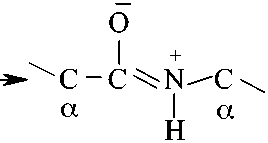
В пептидной связи за счет резонанса канонических структур простая связь С – N между углеродным атомом карбонильной группы и атомом азота NН-группы имеет характер частично двойной связи, что проявляется в уменьшении ее длины (0,132
нм) по сравнению с длиной одинарной простой связи С – N (0,147 нм). Такое сопряжение обусловливает копланарность пептидной группировки. В пептидах и белках пептидная группа находится в состоянии кето-енольной таутомерии:
_С NC = N
II II
O HOH кетоформа енольная форма
Пептидные связи очень прочны и самопроизвольно не разрываются при нормальных условиях. При нагревании с концентрированными кислотами или щелочами пептидов происходит гидролиз пептидных связей с образованием свободных аминокислот.
В сильно щелочной среде пептидные группы пептидов переходят из кетоформы в енольную (иминольную) форму. В избытке щелочи происходит диссоциация водорода енольной ОН-группы. При этом возникает отрицательный заряд на атоме кислорода и при взаимодействии с ионами металлов образуются соли [chem. msu. su л rus / teachind / kolman / 72htm.]. [Биохимия. Biochemistru. ru > biochimija-severind / B 5873 Part 4.].
С целью разработки физиологически активных дипептидных лекарственных препаратов, и учитывая свойства пептидной связи в кислой и щелочной средах, нами проведено изучение кето-енольной таутомерии пептидной связи глицилглицина при комплексообразовании с ионами металлов в зависимости от рН реакционной среды.
Материал и методы. Для изучения кето-енольной таутомерии пептидной связи глицилглицина при комплексообразовании были использованы следующие реактивы: глицилглицин (дипептид), содержание основного вещества 99,8 %, производства «АСROS Organics» (Бельгия); сульфаты: MnSO 4 > 5H 2 O; FeSO 4 • 7H 2 O; CuSO 4 • 5H 2 O; ZnSO 4 • 7H 2 O; CoCl • 6H 2 O и гидроксид натрия марки «х.ч.».
-
1. Общая методика синтеза глицилглицинатов марганца (II) (1) и железа (II) (2) в кислой среде. Раствор 0,0076 моль сульфатов Mn (II) или Fe (II) в 18 мл воды (рН 3) нагревают до 45-50 • С в течение 20 минут. К гомогенному гидролизату (рН 2) прибавляют по частям 0,0152 моль глицилглицина, нагревают 3035 минут до 45-50 О С (рН реакционного раствора 6,5), выдерживают в течение двух
-
2. Общая методика синтеза глицилглицината Cu (II) (3) в кислой среде. К раствору 0,0076 моль глицилглицина в 10 мл воды прибавляют 0,0038 моль сульфата меди (II), 0,00365 моль ацетата натрия и выдерживают при комнатной температуре в течение двух часов. Гомогенный раствор (рН 5) ярко синего цвета упаривают, кристаллический продукт промывают спиртом и сушат при комнатной температуре. Получают глицилглицинат меди (II) дигидрат (кристаллический продукт ярко голубого цвета) с выходом 96,60 % [4]. Продукт хорошо растворяется в воде, не растворяется в спирте, ацетоне.
-
3. Общие методики синтеза глицилглицинатов цинка, меди (II), кобальта (II)
-
3.1. Синтез глицилглицината цинка (4) . 1-стадия – щелочная среда. К раствору 0,0152 моль глицилглицината в 15 мл воды прибавляют 0,0152 моль гидроксида натрия. Наблюдается разогрев реакционной массы до 36 О С выдерживают 10 минут (рН 8,5) и нагревают до 50 о с.
-
-
3.2. Синтез глицилглицинат меди (II) (3). 1-стадия – щелочная среда. К раствору 0,0152 моль глицилглицина в 15 мл воды прибавляют 0,0152 моль гидроксида натрия. Наблюдается разогрев реакционной массы до 36 О С, выдерживают 10 минут (рН 8,5) и нагревают до 50 О С
2-стадия – кислая среда . К гомогенному раствору прибавляют 0,0076 моль сульфата меди (II) и перемешивают. Реакционную смесь (рН 5) нагревают в течение 25 минут при 55 О С охлаждают, выдерживают 2 часа при комнатной температуре и упаривают. Кристаллический остаток голубого цвета промывают спиртом и сушат при комнатной температуре. Получают глицилглицинат меди (II) дигидрат (кристаллический продукт голубого цвета с фиолетовым оттенком) с выходом 96,0 %. Продукт хорошо растворяется в воде, не растворяется в спирте, ацетоне.
-
3.3. Синтез глицилглицината кобальта (II) (5). 1-стадия – щелочная среда. К раствору 0,0076 моль глицилглицина в 10 мл воды прибавляют 0,0076 моль гидроксида натрия. Наблюдается разогрев реакционной массы до 36 о с выдерживают 10 минут (рН 8,5) и нагревают до 50 О С
2-стадия – кислая среда . К гомогенному раствору прибавляют 0,0038 моль хлорида кобальта (II) и перемешивают. Реакционную смесь (рН 5) выдерживают 15 минут при 55 о с и в течение двух часов при комнатной температуре. Получают глицилглицинат кобальта (II) дигидрат (кристаллический продукт темновишневого цвета) с выходом 97,72 %. Продукт хорошо растворяется в воде, не растворяется в спирте, ацетоне.
-
4. Комплексообразование в сильно щелочной среде (рН 11-12).
часов при комнатной температуре и упаривают. Остаток обрабатывают спиртом, кристаллизуют, сушат при комнатной температуре и получают целевые продукты с высокими выходами (глицилглицинат Mn (II) дигидрат – 95,0 %, глицилглицинат Fe (II) дигидрат – 98,0 %[4]). Продукты хорошо растворяются в воде, не растворяются в спирте и ацетоне.
2-стадия – кислая среда. К гомогенному раствору прибавляют по частям 0,0076 моль сульфата цинка и перемешивают. Через 10 минут выпадает белый осадок. Реакционную смесь (рН 5) выдерживают 30 минут при 50 ОС в течение одного часа при комнатной температуре и охлаждают. Осадок фильтруют, промывают водой (контроль на сульфаты с BaCl2), спиртом и сушат при комнатной температуре. Получают глицилглицинат цинка дигидрат (кристаллический продукт белого цвета) с выходом 94,5 %. Продукт не растворяется в воде, спирте, ацетоне.
Синтез двойного комплекса глицилглицината меди (II) (6). К раствору 0,0152 моля глицилглицина в 15 мл воды прибавляют 0,034 моля гидроксида натрия. Наблюдается разогрев реакционной массы до 40 ОС, выдерживают 10 минут (рН 11-12) и нагревают до 50 ос. к гомогенному раствору присыпают по частям 0,0152 моль сульфата меди (II) и перемешивают. Реакционную смесь (рН 10) нагревают в течение 30 минут при 55 ОС охлаждают, выдерживают 2 часа при комнатной температуре и упаривают. Получают двойной комплекс глицилглицината меди (II) – ди-(глицилглицинат)-дикупрат (кристаллический продукт темнофиолетового цвета) с выходом 93,75 %. Продукт с трудом растворяется в воде при комнатной температуре, не растворяется в спирте, ацетоне.
Результаты исследования. Комплексообразование глицилглицина с ионами 3 d -биогенных металлов основана на взаимодействии субстрата с гидроксидами данных металлов. Технология процесса определяется растворимостью, устойчивостью образующихся гидроксидов в реакционной среде.
Гидроксиды марганца (II), железа (II) хорошо растворяются в кислой среде и не подвергаются окислению, в щелочной среде – нерастворимы и быстро окисляются до гидроксидов металлов (III).Для образования Mn(OH) 2 и Fe(OH) 2 нами использован процесс гидролиза соответствующих сульфатов при рН 2 реакционной смеси [4]. При действии на гомогенный водный гидролизат (рН 2), содержащий гидроксиды Me(II), глицилглицином реакция комплексообразования с ионами Mn2+, Fe2+ протекает в кислой среде по амино- и карбоксильной группам и не идет по пептидной группе. Реакция глицилглицина с ионами Сu2+ (реагенты сульфат меди и ацетат натрия [5]) при рН 5 идет по аналогичной схеме:
Схема комплексообразования глицилглицина в кислой среде:
t o C
MeSO4 + 2HOH Me(OH)2 + H2SO4
2NH CH C N CH COOH +
2 2 2 рН < 7
ОН
[NH CH C N CH COO ] Ме
( H 2 O) 2 2 2 2
ОН
(1 3)
где Me2+ : Mn2+ (1); Fe2+(2) ; Cu2+(3) Комплексообразование глицилглицина с ионами Zn2+ и Со2+ проводится действием на реакционный раствор субстрата и гидроксида натрия солями соответствующих металлов. На первой стадии процесса идет взаимодействие глицилглицина с гидроксидом натрия (при эквимолярном соотношении) с образованием мононатриевой соли по карбоксильной группе субстрата при рН (8,5) [6] и превращение пептидной группы из кетоформы в енольную форму. На второй стадии при добавлении в щелочной раствор реакционной смеси солей металлов происходит образование гидроксидов Me(II) и их взаимодействие с енольной формой мононариевой соли глицилглицина при рН 5 реакционной среды.
На второй стадии в реакционной смеси протекают следующие превращения реагентов, соответственно:
ZnSO 4 ° 7H 2 O + 2NaOH • Zn(OHh + Na 2 SO 4 + 7H 2 O ZnSO 4 + 2H 2 O ^ Zn(OH) 2 + 2H+ + SO
2 -
C0CI 2 6H 2 O + 2NaOH ^ Co(OH) 2 + NaCl + 6H 2 O
C0CI 2 + 2H 2 O ^ Co(OH) 2 + 2H+ + 2
-
Ñl
В результате указанных превращений среда становится кислой (рН 5).
При переходе рН среды в кислую область (от 8,5 до 5) комплексонаты глицилглицина цинка (II) и кобальта (II) получаются в кетонной форме, т. е. протекает кето-енольная таутомерия в две стадии по схеме:
1-стадия
+ NaOH
NH2 CH2 C N CH2COOH NaO NH2 CH2 C = N CH2COONa
2 2 2 p H > 7 2 2 2
O H ( H2O) OH кетоформа енольная форма
2-стадия
+ Me(OH)2 (H+) pH < 7
2NH2 CH2 C = N CH2COONa енольная
OH форма
[NH2 CH2 C NH CH2 COO ]2Me
O кетоформа где Me2+: Zn2+ (4), Со2+ (5)
Глицилглицинат меди (II) (3), полученный указанным способом (методика 3.2) имеет фиолетовый оттенок (в отличие от продукта (3) по способу 2), что связано с наличием примеси биуретового медного комплекса.
В сильнощелочной среде (рН 11-12) комплексообразование глицилглицина с
ионами меди (II) протекает через енольную форму динатриевой соли глицилглицина [6]. В результате реакции получается двойной медный комплекс: первый – по карбоксильной и аминной группам, второй – по иминольной группе (биуретовый комплекс), ди-(глицилглицинат)-дикупрат (6).
Схема превращения
NH2 CH2 C N CH2 COOH 22 2
O H кетоформа 1-стадия
+ 2 NaOH(pH 11-12)
( 2H 2 O)
+ 2 CuSO
NH2 CH2 C = N CH2COONa 4>
I ( Na2So4)
ONa2-стадия енольная форма
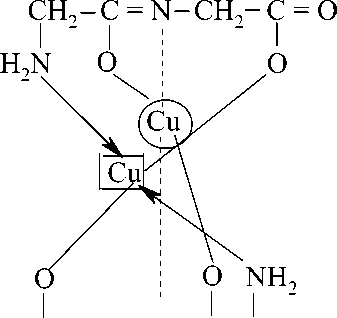
O = C CH2 N = C CH2
Двойной комплекс – кристаллический высокоплавкий продукт темно-фиолетового цвета. В водном растворе (в воде растворяется с трудом) ионы Cu2+ с К 4 [Fe(CN) 6 ] образуют осадок красно-бурого цвета Cu 2 [Fe(CN) 6 ] (качественная реакция).
Биуретовая реакция обусловлена наличием в белках и пептидах пептидной связи, которая в щелочной среде превращается из кетоформы (амидной) в иминольную форму и с сульфатом меди (II) образует биуретовый комплекс фиолетового цвета. [Studopedia ru > 1 …Biuretovaja…na peptidnuy – svuaz…v; Википедия – пептидная связь].
Глицилглицинаты меди (II) (3), цинка (4), кобальта (II) (5) дают качественную биуретовую реакцию на пептидную связь в щелочной среде (рН 8,5) с сульфатом меди (II). В этих условиях глицилглицинаты марганца (II) (1), железа (II) (2) образуют цветные осадки соответствующих гидроксидов, которые маскируют характерное фиолетовое окрашивание
ЛИТЕРАТУРА: 1. Комов В.П., Шведова В.Н. Биохимия. – М.: Дрофа, 2004. с. 26-28;
2. Щипаева Е.В. Иммунофармакологические свойства глицин- и пролинсодержащих дипептидов: Автореф…диссерт…канд. мед. наук. – Москва: ГУНИИ фармакологии им. В.В. Закусова РАМН. 2008.; 3. Гудашева Т.А. Стратегия создания дипептидных лекарств. / Инновации в современной фармакологии. Тез. докл. IV съезда фармакологов России. – Казань. 18-21.09.2012.; 4. Кадырова Р.Г., Кабиров Г.Ф., Муллахметов Р.Р. Изучение комплексообразующей способности глицилглицина с 3 d -биогенными металлами. // Ученые записки КГАВМ им. Н.Э, Баумана. – Казань, 2014. – т. 218, с. 102-110.; 5. Гранберг И.И Практические работы и семинарные занятия по органической химии. – М.: Дрофа, 2001. – 352с.; 6. Кадырова Р.Г., Кабиров Г.Ф., Муллахметов Р.Р. Изучение реакции взаимодействия глицилглицина с гидроксидами щелочных и щелочноземельных металлов. // Ученые записки КГАВМ им. Н.Э. Баумана. – Казань, 2014. – с. 110-117.
биуретового комплекса.
Заключение. Изучена кето-енольная таутомерия пептидной связи глицилглицина в зависимости от рН реакционной среды.
Показано, что в кислой среде не идет превращение амидной группы в иминольную (енольную). В щелочной среде (рН 8,5) (при эквимолярном соотношении субстрата и щелочи) глицилглицин из кетоформы превращается в енольную форму мононатриевого производного. При последующем действии на реакционную смесь солями металлов (рН 5) енольная форма переходит в кетонную с образованием глицилглицинатов металлов в кетоформе. В сильно щелочной среде (рН 11-12) (соотношение субстрат: щелочь 1 : 2 моль) глицилглицин из кетоформы превращается в енольную форму динатриевого производного, при последующим действии на который сульфатом меди (II) получается двойной медный комплекс в енольной форме.
ИЗУЧЕНИЕ КЕТО-ЕНОЛЬНОЙ ТАУТОМЕРИИ ПЕПТИДНОЙ СВЯЗИ ГЛИЦИЛГЛИЦИНА ПРИ КОМПЛЕКСООБРАЗОВАНИИ С ИОНАМИ МЕТАЛЛОВ
Кадырова Р.Г., Кабиров Г.Ф., Муллахметов Р.Р.
Резюме
Изучена кето-енольная таутомерия пептидной связи глицилглицина в зависимости от рН реакционной среды.
Показано, что в кислой среде не идет превращение амидной группы в иминольную (енольную). В щелочной среде (рН 8,5) (при эквимолярном соотношении субстрата и щелочи) глицилглицин из кетоформы превращается в енольную форму мононатриевого производного. При последующем действии на реакционную смесь солями металлов (рН 5) енольная форма переходит в кетонную с образованием глицилглицинатов металлов в кетоформе. В сильно щелочной среде (рН 11-12) (соотношение субстрат: щелочь 1 : 2 моль) глицилглицин из кетоформы превращается в енольную форму динатриевого производного, при последующим действии на который сульфатом меди (II) получается двойной медный комплекс в енольной форме.
KETO-ENOL GLYCYLGYCINE PEPTIDE BOND TAUTOMERISMSTUDY AT COMPLEXATION WITH METAL IONS
Kadyrova R.G., Kabirov G.F., Mullakhmetov R.R.
Список литературы Изучение кето-енольной таутомерии пептидной связи глицилглицина при комплексообразовании с ионами металлов
- Комов В.П., Шведова В.Н. Биохимия. -М.: Дрофа, 2004. с. 26-28;
- Щипаева Е.В. Иммунофармакологические свойства глицин-и пролинсодержащих дипептидов: Автореф…диссерт…канд. мед. наук. -Москва: ГУНИИ фармакологии им. В.В. Закусова РАМН. 2008.;
- Гудашева Т.А. Стратегия создания дипептидных лекарств.//Инновации в современной фармакологии. Тез. докл. IV съезда фармакологов России. -Казань. 18-21.09.2012.;
- Кадырова Р.Г., Кабиров Г.Ф., Муллахметов Р.Р. Изучение комплексообразующей способности глицилглицина с 3d-биогенными металлами.//Ученые записки КГАВМ им. Н.Э, Баумана. -Казань, 2014. -т. 218, с. 102-110.;
- Гранберг И.И. Практические работы и семинарные занятия по органической химии. -М.: Дрофа, 2001. -352с.;
- Кадырова Р.Г., Кабиров Г.Ф., Муллахметов Р.Р. Изучение реакции взаимодействия глицилглицина с гидроксидами щелочных и щелочноземельных металлов.//Ученые записки КГАВМ им. Н.Э. Баумана. -Казань, 2014. -с. 110-117.


