Изучение кислотно-основного равновесия 5-гидрокси-6-метилурацила в водных растворах
Автор: Валиуллина К.А., Нигматуллина А.А.
Журнал: Форум молодых ученых @forum-nauka
Статья в выпуске: 10 (38), 2019 года.
Бесплатный доступ
В работе подобраны условия для хроматографического анализа продуктов метилирования 5-гидрокси-6-метилурацила в водных щелочных растворах методом ВЭЖХ. Продукты выделены методом полупрепаративной ВЭЖХ. И идентифицированы на основании данных 1Н, 13С, 15N ЯМР спектроскопии.
Урацил, алкилирование, водные растворы, ямр, вэжх
Короткий адрес: https://sciup.org/140285109
IDR: 140285109 | УДК: 547.854.4
Study of acid-basic equilibrium 5-hydroxy-6-methyluracyl in aqueous solutions
The conditions for chromatographic analysis of methylation products of 5-hydroxy-6-methyluracil in aqueous alkaline solutions by HPLC are selected. Products were isolated by semi-preparative HPLC. And identified on the basis of data 1H, 13C, 15N NMR spectroscopy.
Текст научной статьи Изучение кислотно-основного равновесия 5-гидрокси-6-метилурацила в водных растворах
Термодинамические свойства различных замещенных производных урацила важны с точки зрения их медицинского применения. 5-гидрокси-6-метилурацил усиливает иммунитет и эффективен при лечении инфекций, он не токсичен, не вызывает побочных реакций, проявляет универсальные антисептические характеристики, ускоряет процесс заживления ран, ожогов и уменьшает вредное воздействие радиации, восстанавливает количество лейкоцитов, усиливая гуморальный и клеточный иммунитет, имеет антистрессовое, кардиостимулирующее и антитоксическое воздействие. Широкое применение ГМУ в практике требует всестороннего изучения термодинамических характеристик процессов кислотно-основного равновесия этого вещества в водном растворе.
Алкилирование 5-гидрокси-6-метилурацила диметилсульфатом в щелочной среде проводили по известной методике [1].
Исходя из цели получения максимального количества метилированных производных ГМУ, соотношение компонентов составило ГМУ:ДМС:NaOH=1:5:4 и реакция была остановлена до полного расходования исходного ГМУ. Полученная смесь была фракционирована методом полупрепаративной высокоэффективной жидкостной хроматографии. В ходе фракционирования удалось выделить соединения, соответствующие пикам 5 и 7 на хроматограмме смеси (рис.1).
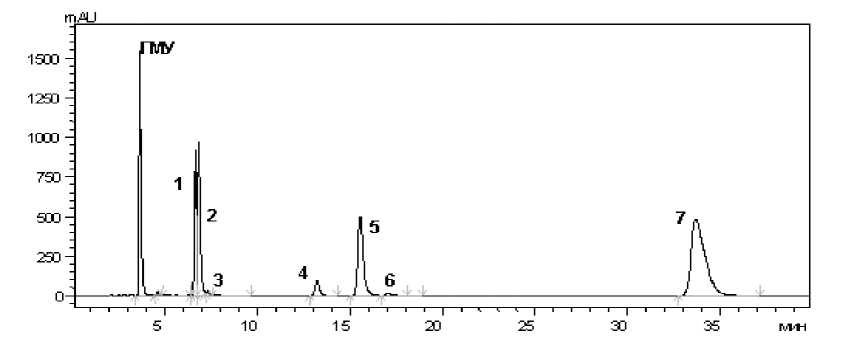
Рис. 1. Хроматограмма реакционной смеси:
5 пик – 5-метокси-3,6-диметилурацил, 7 пик – 5-метокси-1,3,6-триметилурацил
После упаривания растворителя были записаны 13С, 1H и 15N ЯМР спектры.
Cтруктура индивидуальных соединений была доказана методами 13С, 1H и 15N ЯМР спектроскопии. Потенциометрическим титрованием определены константы и термодинамические характеристики кислотноосновного равновесия ГМУ и его производных.
Таблица
Константа и термодинамические характеристики кислотно-основного равновесия ГМУ и 5-метокси-3,6-диметилурацил в водном растворе (0,1 М
KNO 3 )
|
T |
pK |
ΔH, кДж/моль |
ΔG 298 , кДж/моль |
ΔS 298 , Дж/моль·К |
|
|
о |
20 |
9,02±0,07 |
|||
|
"'N-^Y'0" |
25 |
8,85±0,05 |
27,3±1,4 |
50,92±7 |
-257±13 |
|
35 |
8,74±0,05 |
||||
|
н |
45 |
8,61±0,04 |
|||
|
O |
20 |
9,68±0,02 |
|||
|
H3Cx JJ OCH3 N |
25 |
9,62±0,07 |
9,6±0,5 |
56,60±2 |
-215±12 |
|
O N CH3 |
35 |
9,59±0,06 |
|||
|
H |
45 |
9,53±0,06 |
Из зависимости константы депротонирования от температуры для 5-метокси-3,6-диметилурацила, установлено, что процесс кислотно-основного равновесия эндотермичен, а величины изменений энергий Гиббса свидетельствует об энергетической невыгодности образования аниона N1 в нейтральной среде. Исходя из литературных данных и полученных значений рК для 5-метокси-3,6-диметилурацила, следует также, что депротонирование ГМУ по перовой ступени не идет по N1 положению.
Таким образом, алкилированием ГМУ были выделены 5-метокси-1,3,6-триметилурацил и 5-метокси-3,6-диметилурацил, для которогоопределены термодинамические характеристики кислотно-основного равновесия.
Список литературы Изучение кислотно-основного равновесия 5-гидрокси-6-метилурацила в водных растворах
- WierzchowskiK.L., LitonskaE., ShugarD. // J.Am.Chem.Soc. - 1965.- V.83, № 20. - P.4621-4629


