Изучение клинической и патоморфологической картины при остром токсическом гепатите на фоне применения биодобавки
Автор: Домбровский В.О., Матросова Л.Е., Губеева Е.Г., Танасева С.А., Тарасова Е.Ю.
Статья в выпуске: 3 т.251, 2022 года.
Бесплатный доступ
В ходе гистологического исследования крыс, получавших тетрахлорметан и «Карсил», выявлены признаки очаговой жировой дистрофии гепатоцитов, зернистой дистрофии с некробиозами, некрозами вокруг центролобулярных вен, паретическое полнокровие, эритростазы, отек стенок сосудов. У крыс, которые получали тетрахлорметан и БАД, изменения структуры были наименее выраженными.
Печень, гепатит, гепатопротекторы, тетрахлорметан, биодобавка
Короткий адрес: https://sciup.org/142235681
IDR: 142235681 | УДК: 619:616.36-002:619:615.4 | DOI: 10.31588/2413_4201_1883_3_251_102
Study of the clinical and pathomorphological picture in acute toxic hepatitis on the background of the application of bioadditive
In the course of histological examination of rats receiving carbon tetrachloride and «Karsil», signs of focal fatty degeneration of hepatocytes, granular degeneration with necrobiosis, necrosis around centrilobular veins, paretic congestion, erythrostasis, and edema of the vascular walls were revealed. In rats that received carbon tetrachloride and dietary supplements, structural changes were the least pronounced.
Текст научной статьи Изучение клинической и патоморфологической картины при остром токсическом гепатите на фоне применения биодобавки
Оптимизация процессов производства продукции на животноводческих предприятиях нашей страны принесла большое количество новых обменных патологий сельскохозяйственных животных [5]. Печень является одним из центральных органов метаболизма, который, сохраняя динамическое постоянство внутренней среды, принимает самое активное участие в устранении последствий различных заболеваний. Не существует такого звена обмена веществ в организме, которое так или иначе не было бы связано с процессами, протекающими в печени [10, 11]. Нарушение работы печени – одна из наиболее частых патологий, встречающихся на производстве. Гепатопатологии наносят колоссальный экономический ущерб, что связано с падежом животных, снижением их продуктивности, воспроизводительной способности, резистентности, развитием на этом фоне многих инфекционных и незаразных болезней [2, 3, 12].
Основной группой лекарственных препаратов для лечения болезней печени, связанных с патологией обмена веществ, являются гепатопротекторы. Данные препараты препятствуют разрушению мембран клеток и стимулируют регенерацию гепатоцитов [5]. Поэтому разработка новых гепатопротективных средств и биодобавок является перспективной целью для отечественной фармакологии [1, 8, 9, 13].
Доклинические исследования перспективных гепатопротективных лекарственных средств проводятся на классической модели токсического гепатита, вызванного внутрижелудочным или интраперитонеальным введением 50 % масляного раствора тетрахлорметана [7]. Этот гепатотоксин оказывает прямое повреждающее действие на печень посредством образования ковалентных связей с клеточными макромолекулами, что, в свою очередь, приводит к выраженному повреждению мембран гепатоцитов, активации процессов липопероксидации, дисбалансу в работе ферментативного звена антиоксидантной системы организма, нарушению метаболизма липидов, белков, углеводов [4].
Материал и методы исследований. Опытная часть исследований была выполнена на базе отделения токсикологии ФГБНУ «ФЦТРБ-ВНИВИ» (г. Казань). Для моделирования токсического гепатита печени использовали тетрахлорметан в дозе 0,4 мл/кг, вводили внутрибрюшинно. Эксперименты проведены на 24 белых крысах, разделенных по принципу аналогов на 4 группы. Биологическим контролем служили животные первой группы. Белые крысы второй, третьей и четвертой групп получали внутрибрюшинно тетрахлорметан в 50 % растворе на оливковом масле в дозе 0,4 мл/кг однократно. Подопытным животным третьей и четвертой групп на фоне затравки задавали препараты. Животные третьей группы получали коммерческий препарат «Карсил» (100 мг/кг внутрижелудочно один раз в сутки). Четвертая группа получала биодобавку на основе шрота расторопши, янтарной кислоты, бентонита, пробиотического штамма B. subtilis, витаминов А и Е. Лечение препаратами продолжалось в течение 14 суток.
По окончании лечения животные были подвергнуты декапитации под эфирным наркозом. Вскрытие проводилось по общепринятой методике. Была проведена визуальная оценка внутренних органов, а также забор материала на гистологическое исследование печени. Кусочки органов фиксировали в 10 % нейтральном формалине, проводку проводили общепринятыми в патоморфологии методами. Гистопрепараты окрашивали гематоксилин-эозином. Микрофотосъемку гистологических препаратов осуществляли в проходящем свете с помощью микроскопа Leica DM 1000, камера Leica DFC 320 («Leica Microsystems», Япония).
Результат исследований. В группе крыс, получавших тетрахлорметан без лечения, уже на третьи сутки эксперимента наблюдалось угнетение, частичный отказ от приема корма, взъерошенность кожного покрова. К концу эксперимента большая часть животных была сильно истощена, дегидратирована.
У группы, получавшей помимо тетрахлорметана «Карсил», клиническая картина проявилась на седьмые сутки угнетением и снижением тургора кожи.
У животных, получавших на фоне введения тетрахлорметана биодобавку, клиническая картина не проявлялась.
При вскрытии у всех подопытных, получавших тетрахлорметан без лечения, наблюдалась иктеричность слизистых оболочек, гепатомегалия, очаговые кровоизлияния под капсулой печени, сама печень была тестоватой консистенции. Из группы, получавшей «Карсил», только у двух из шести крыс наблюдалась желтушность слизистых оболочек, у одной наблюдались очаговые кровоизлияния под капсулой печени. В остальных группах при осмотре внутренних органов визуальные изменения не обнаружены.
Гистологическая картина печени у животных группы биологического контроля соответствовала картине нормальной печени, сохранена структура печеночных долек без деструкции гепатоцитов (Рисунок 1).
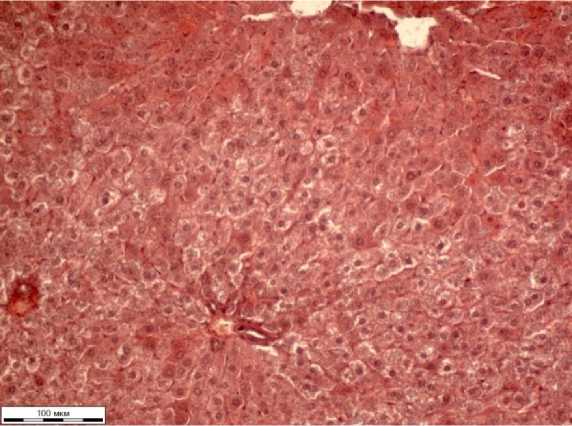
Рисунок 1 – Печень белой крысы группы биологического контроля, окраска гематоксилином
Эрлиха и эозином водным, объектив Х20
У животных четвертой группы были выявлены общие изменения в виде неравномерного кровенаполнения сосудов. Стенки венозных сосудов были тонкие.
При этом толщина стенок, как на поперечном срезе, так и на продольном срезе могла различаться, имелись еще более истонченные участки. Сами стенки были окрашены в мутноватый эозинофильный цвет. Артерии во всех препаратах имели утолщенные стенки, ядра эндотелия не на всем протяжении среза. Однако ядра, которые были видны, различались формой и цветом, некоторые были гиперхромные, округлые, другие – «сплюснутые» бледные. В перипортальных трактах определялась инфильтрация лимфоцитами, гистиоцитами. Во всех препаратах синусоиды были заполнены гомогенными эозинофильными массами неравномерно с участками скоплений, местами выглядели как сдавленные. Здесь же определялись единичные лимфоциты и деформированные, вытянутые Купферовские клетки. Гепатоциты были более крупные, чем в контроле, а некоторые почти в два раза. Цитоплазма гепатоцитов имела неравномерную эозинофильную «мутную» окраску. В некоторых клетках определялись участки пустот и фрагменты цитоплазмы в виде зерен. В других гепатоцитах определялись круглые, мелкие оптические пустотки. Также обращало на себя внимание строение ядер клеток. В некоторых они были увеличены, неравномерно окрашены, зернистые, базофильные. В отдельных гепатоцитах не определялись ядра. Наиболее выраженные изменения гепатоцитов наблюдались вокруг центральной вены. Строение балок в дольках было нарушено (Рисунок 2).
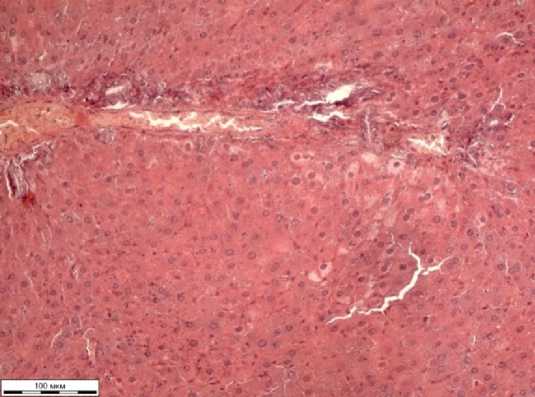
Рисунок 2 – Печень белой крысы группы токсического контроля, окраска гематоксилином Эрлиха и эозином водным, объектив Х20
В ходе гистологического исследования крыс, получавших «Карсил», наблюдались выраженные изменения структуры. Вены и артерии были расширены, заполнены эритромассами с признаками агрегации эритроцитов. Стенки артерий были неравномерно утолщены, вены тонкие. Гепатоциты неравномерно увеличенные, некоторые набухшие. В цитоплазме многих гепатоцитов определялись мелкие круглые пустоты. В других имелись просветления цитоплазмы и зернистые массы. Ядра гепатоцитов были разного размера, некоторые увеличенные, другие мельче, чем в контроле. Имелось неравномерное окрашивание ядер с гиперхромным глыбчатым хроматином. Синусоиды были сдавлены, неравномерно заполнены эозинофильными гомогенными массами. Встречались единичные лимфоциты и Купферовские клетки, которые были деформированными. Единичные гепатоциты были без ядер, располагались они преимущественно вокруг центролобулярных вен. Балочные структуры были плохо различимы (Рисунок 3).
У крыс, которые получали тетрахлорметан и БАД, также были выявлены расширенные сосуды, заполненные эритромассами. Стенки артерий были несколько утолщены, эндотелий преимущественно с круглыми ядрами. Строение долек было сходно с группой биологического контроля. В цитоплазме гепатоцитов определялись оптические пустоты и зернистые эозинофильные массы. У всех крыс определялись единичные безъядерные гепатоциты (Рисунок 4).
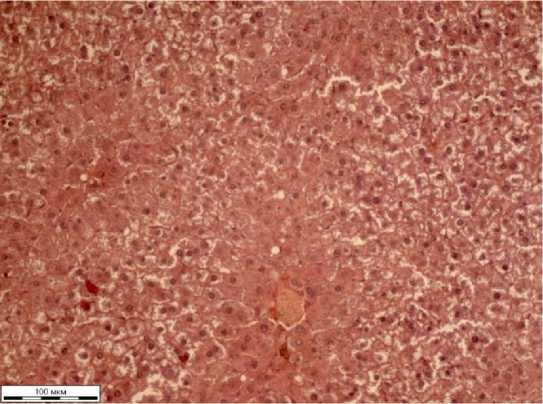
Рисунок 3 – Печень белой крысы третьей группы, окраска гематоксилином Эрлиха и эозином водным, объектив Х20
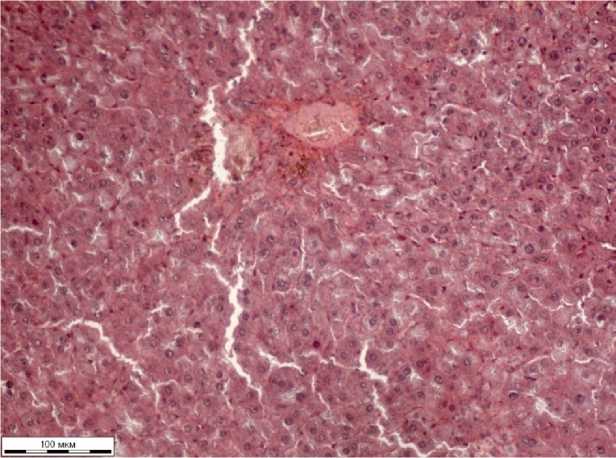
Рисунок 4 – Печень белой крысы четвертой группы, окраска гематоксилином Эрлиха и эозином водным, объектив Х20
Заключение. При гистологическом исследовании препаратов печени крыс группы токсического контроля выявлены признаки нарушения сосудистого тонуса, отек стенок сосудов, деформация эндотелия артерий и вен, слабо выраженная мелкокапельная жировая дистрофия и зернистая дистрофия с некробиозами, некрозами, сдавление синусоидов, деформация Купферовских клеток.
У крыс, получавших тетрахлорметан и «Карсил», в печени выявлены признаки очаговой жировой дистрофии гепатоцитов, зернистой дистрофии с некробиозами, некрозами вокруг центролобулярных вен, паретическое полнокровие, эритростазы, отек стенок сосудов.
У крыс, которые получали тетрахлорметан и БАД, изменения структуры печени были наименее выраженными. Наблюдались признаки очаговой зернистой дистрофии, некробиозы и некрозы единичных гепатоцитов.
Печень белых крыс из группы, получавших БАД, имела наименее значимые изменения. Это свидетельствует о достаточно высокой эффективности биодобавки.
В ходе гистологического исследования крыс, получавших тетрахлорметан и «Карсил», выявлены признаки очаговой жировой дистрофии гепатоцитов, зернистой дистрофии с некробиозами, некрозами вокруг центролобулярных вен, паретическое полнокровие, эритростазы, отек стенок сосудов. У крыс, которые получали тетрахлорметан и БАД, изменения структуры были наименее выраженными.
Список литературы Изучение клинической и патоморфологической картины при остром токсическом гепатите на фоне применения биодобавки
- Абрамов, А. А. Изучение токсических свойств нового инъекционного гепатопротектора в остром эксперименте / А. А. Абрамов, М. Н. Семененко, В. В. Меньшенин // Сборник научных трудов СКНИИЖ. -Краснодар, 2018. - С. 160.
- Абрамов, А. А. Определение гепатозащитной активности препарата филовектин на модели острой патологии печени у лабораторных животных / А. А. Абрамов // Сборник научных трудов СКНИИЖ. - Краснодар, 2021. - С. 294.
- Ермолаева, О. К. Качество мяса свиней при микотоксикозе на фоне применения энтеросорбентов / О. К. Ермолаева, С. А. Танасева, Л. Е. Матросова, Е. Ю. Тарасова, Э. И. Семенов // Ветеринарный врач. -2020. - № 4. - С. 15-20.
- Ерютин, А. В. Сравнительный анализ токсического гепатита, вызванного внутрижелудочным и интраперитонеальным введением раствора тетрахлорметана / А. В. Ерютин, М. Э. Филь, М. А. Шилова [и др.] // Journal of Siberian Medical Sciences. - 2016. - 5. -С. 8.
- Кузьминова, Е. В. Перспективы расширения спектра применения гепатопротекторов в ветеринарии / Е. В. Кузьминова, М. П. Семененко, Е. А. Старикова [и др.] // Политематический сетевой электронный научный журнал Кубанского государственного аграрного университета. - 2014. - № 102. - С. 787-797.
- Минушкин, О. Н. Гепатопротекторы в лечении некоторых заболеваний печени / О. Н. Минушкин // Медицинский совет. - 2016. - № 14. - С. 52.
- Миронов, А. Н. Руководство по проведению доклинических исследований лекарственных средств / Под ред. А. Н. Миронова. - Москва: Гриф и К, 2012. - 944 с.
- Мишина, Н. Н. Обоснование введения в рацион животных комбинации сорбентов неорганической и органической природы при Т-2 токсикозе / Н. Н. Мишина, Э. И. Семенов, К. Х. Папуниди [и др.] // Ветеринарный врач. - 2019.- № 2. - С. 3037.
- Танасева, С. А. Эффективность адсорбентов при сочетанном микотоксикозе цыплят-бройлеров / С. А. Танасева, Е. Ю. Тарасова, Л. Е. Матросова [и др.] // Международный вестник ветеринарии. - 2020. - № 4. - С. 5056.
- Тарасова, Е. Ю. Изучение сорбционной активности потенциальных средств профилактики микотоксикозов в отношении афлатоксинов / Е. Ю. Тарасова, Э. И. Семенов, Л. Е. Матросова [и др.] // В етер инарный врач - 2020. - № 2. - С. 5158.
- Тяпкина, Е. В. Влияние биологически активных соединений на метаболические функции печени / Е. В. Тяпкина, О. А. Фомин // Молодой ученый. - 2015. - № 7. - С. 1048.
- Семенов, Э. И. Методические рекомендации по диагностике, профилактике и лечению микотоксикозов животных / Э. И. Семенов, М. Я. Тремасов, К. Х. Папуниди [и др.]. -Росинформагротех, 2017. - 67 с.
- Matrosova, L. E. Enterosorbent efficiency mineral attenuation during pig mycotoxicosis / L. Е. Matrosova, N. N. Mishina, S. A. Tanaseva [et al.] // International Journal of Mechanical and Production Engineering Research and Development. - 2020. - V. 10. - P. 1851.


