Изучение реакции комплексообразования аскорбиновой кислоты с ионами цинка и меди (II)
Автор: Кадырова Р.Г., Кабиров Г.Ф., Муллахметов Р.Р.
Статья в выпуске: 2 т.222, 2015 года.
Бесплатный доступ
Изучена реакция комплексообразования аскорбиновой кислоты с ионами цинка и меди (II). Найдены оптимальные условия синтеза аскорбатов цинка и меди (II) с хорошими выходами, что позволяет исследовать их биологическую активность. Показано, что для обеспечения стабильности аскорбиновой кислоты реакцию необходимо проводить в кислой среде.
Аскорбиновая кислота, аскорбаты цинка, меди (ii)
Короткий адрес: https://sciup.org/14288524
IDR: 14288524 | УДК: 547.461.4
Ascorbic acid with zinc and copper(II) ions complex formation reaction study
The reaction of ascorbic acid complex formation with ions of zinc and copper (II) was studied. The optimal conditions for the synthesis of zinc ascorbate and copper (II) with high yields, which allow to explore their biological activity were found. It has been shown that to ensure the stability of the ascorbic acid, the reaction must be carried out in an acidic medium.
Текст научной статьи Изучение реакции комплексообразования аскорбиновой кислоты с ионами цинка и меди (II)
Природная биологически активная аскорбиновая кислота имеет L-конфигурацию и представляет собой у-лактон (белые кристаллы, т. пл. 190-192 О С, растворимые в воде).
В водных растворах аскорбиновая кислота дает кислую реакцию (для 0,1н раствора рН 2,2). Кислые свойства аскорбиновой кислоты определяются главным образом гидроксильной группой в положении 3. Частично за кислую реакцию ответственна гидроксильная группа в положении 2. Наличие в аскорбиновой кислоте двух сопряженных двойных связей обусловливает ее способность к обратимому окислению, продуктом которого является дегидроаскорбиновая кислота (ДАК – бесцветные кристаллы, т. пл. 222-225 ос, хорошо растворимые в воде). В сильно щелочных условиях лактонная связь в ДАК разрывается и она превращается в 2,3-дикето-L-гулоновую кислоту [Аскорбиновая кислота. Химические и физические свойства витамина С. Электронная медицина]. Эта реакция необратима.
-
L- аскорбиновая кислота восстанавливает окисленные формы ферментов, окисляясь в ДАК, обратимо легко регенерующуюся в аскорбиновую кислоту под действием глутатиона (трипептида) за счет его сульфогидрильной
группы. Окисление аскорбиновой кислоты катализируется ионами меди, в меньшей степени – ионами серебра и железа. [Строение и физико-химические свойства аскорбиновой кислоты – allRefs. net > Биология «17 klb / p4»].
Аскорбиновая кислота принимает участие в некоторых важных окислительных процессах, например в качестве второго донора электронов при окислении остатков пролина в проколлагене до гидроксипролина. При этом она превращается в ДАК, которая восстанавливается до аскорбата с помощью специальной редуктазы [1].
Аскорбиновая кислота (витамин С) способствует здоровому функционированию митохондрий, стимулирует иммунную систему для производства интерферона. Витамин С содействует преобразованию аминокислот в нейротрансмиттеры, снижает окислительное повреждение генов.
Аскорбиновая кислота важна для поддержания здоровья и нормального роста сельскохозяйственных животных как лекарственный препарат. Она назначается животным в профилактических и лечебных целях при гиповитаминозе С, нарушении обмена веществ, инфекционных болезнях и др. [Ветеринария].
В ветеринарийной и медицинской практике в лечебных целях используются комплексные соединения аскорбиновой кислоты с биогенными металлами.
Для лечения онкологических заболеваний разработаны нормы потребления минеральных аскорбатов, в том числе аскорбата цинка ~ 40 мг/сут., аскорбата марганца – 11 мг/сут. [Новые технологии в Германии. Лечение онкологических заболеваний. Центр Гамманож. Мюнхен].
Создан интерактивный мультивитаминный комплекс (супервитаминный) Activite (МНР), содержащий также аскорбаты кальция, магния, калия, цинка, меди, марганца, хрома [для спортсменов. Activite (МНР )– Maximum Human Performance. США. Megasila. ru > product 4403. html].
Аскорбат цинка входит в состав БАД к пище для взрослых: L-аскорбиновая кислота, L-аскорбаты натрия, калия, кальция, магния, цинка, аскорбил– пальмитат [Формы витаминов и минеральных солей для использования при производстве БАД к пище для взрослых. Приложение 10 к техническому регламенту Таможенного союза « О безопасности пищевой продукции»].
Аскорбат цинка, как биогенный препарат, рекомендован в качестве кормовой добавки для кормления сельскохозяйственных животных и птицы. Препарат способствует повышению продуктивности и сохранности поголовья [2].
Изучена фармакология и токсикология аскорбатов калия, железа, цинка, марганца, кобальта. Установлено, что препараты нетоксичные (Классификация К.К. Сидорова) и рекомендованы в качестве лечебно-профилактических средств при гипомикроэлементозах и для повышения продуктивности животных [3].
При взаимодействии аскорбата цинка с 1-этилимидазолом получен комплекс асказол (брутто формула С 16 Н 22 N 4 O 6 Zn), который повышает устойчивость организма к действию диоксида азота и обладает цитопротекторным и антигипоксическим действием.
Синтез аскорбата цинка при этом осуществляется действием водным раствором аскорбиновой кислоты на водную суспензию гидроксида цинка при 60 О С с последующим перемешиванием реакционной смеси в течение 6 часов при 50 ОС. Не вступивший в реакцию гидроксид цинка фильтруют, водный фильтрат упаривают в вакууме. Целевой продукт выделяют смесью ацетона и эфира с выходом 75,3 % в виде порошка желтого или желто-оранжевого цвета, растворимого в воде; температура плавления 104 о с [4].
Имеется сообщение об использовании аскорбата меди (II) для инактивации вирусов: простого герпеса 1-го и 2-го типа, цитомегаловируса и вируса пара-гриппа [Лечебные свойства витамина С против герпеса. hedlth-scince-report. сom. > alotek /topies 6/.].
О методиках синтеза аскорбата меди (II) сообщения в литературе малочисленны.
На форуме химиков (20.11.2013) обсуждался способ получения аскорбата меди (II) из аскорбата натрия. При этом рассматривались разные варианты синтеза:
– при постепенном приливании аскорбата натрия к купоросу будет последовательно получаться аскорбат меди (II) в смеси с основным сульфатом меди;
– при избытке аскорбата начнутся процессы комплексообразования и восстановления ионов Сu2+ до Сu1+;
– при обратном порядке слива реагентов, когда соль меди в недостатке, комплексообразование с восстановлением начнутся сразу.
В щелочной среде протекают процессы:
2CuSO 4 + С б Н 8 0 б + 4NaOH ^ C^O^ + С б Н б О б + 2Na 2 SO 4 + ЗН 2 О аскорбиновая (ДАК)
кислота
Аскорбат натрия окисляется до дегидроаскорбиновой кислоты (ДАК), а ионы меди (II) восстанавливаются до ионов меди (I) с выпаданием осадка красного цвета Cu 2 O [Аскорбат Na-CuSO 4 / Форум химиков > 20.11.2013. Chemport ru > форум химиков > viewtopic. php…].
Как следует из литературных источников, аскорбаты цинка, меди (II) являются перспективными биологически активными веществами, но технологичные способы их получения отсутствуют.
В связи с этим нами проведены экспериментальные исследования по изучению реакции комплексообразования аскорбиновой кислоты с ионами цинка и меди (II).
Материалы и методы. Для изучения реакции комплексообразования были использованы следующие реактивы: аскорбиновая кислота, имп. «ч». «Экофарм»; сульфаты: ZnSO 4 • 7H 2 O, CuSO 4 • 5H 2 O марки «хч».
-
1. Синтез аскорбата цинка . Раствор 4,07 г (0,0142 моль) сульфата цинка, ZnSO 4 • 7H 2 O в 15 мл воды (рН 3) нагревают до 4550 О С в течение 20 минут. К гомогенному раствору гидролизата (рН 2) присыпают порциями 5 г (0,0284 моль) аскорбиновой кислоты, перемешивают до полного растворения и нагревают реакционную смесь до 45-50 о с 30 минут (рН 1-2). Затем выдерживают при комнатной температуре 2 часа. Бесцветный гомогенный раствор упаривают, кристаллический продукт промывают этанолом. Проводят качественный контроль на содержание сульфат-анионов (с BaCl 2 ) и сушат при комнатной температуре.
-
2. Синтез аскорбата меди (II). а) Раствор 3,4 г (0,0142 моль) сульфата меди (II), CuSO 4 • 5H 2 O в 15 мл воды (рН 3) нагревают до 40-45 о с в течение 20 минут. К гомогенному раствору гидролизата (рН 2) присыпают по частям 5 г (0,0284 моль) аскорбиновой кислоты, перемешивают до полного растворения, нагревают реакционную смесь до 40-45 о с 30 минут (рН 1-2) и выдерживают при комнатной температуре в течение 2-3х часов. При этом реакционная смесь приобретает светлозеленый цвет и на дне колбы осаждается незначительное количество осадка красного цвета Сu 2 O. Реакционную смесь фильтруют, гомогенный раствор упаривают и получают кристаллический продукт голубого цвета с примесью зеленой густой жидкости. Сырец промывают несколько раз спиртом, голубые кристаллы сушат на воздухе. Получают 2,9 г (46,5 %) аскорбата меди (II) дигидрата, [C 6 H 7 O 6 ] 2 Cu • 2H 2 O.
Получают 6,02 г (94,2 %) аскорбата цинка дигидрата [C 6 H 7 O 6 ] 2 Zn • 2H 2 O.
Аскорбат цинка дигидрат - кристаллический продукт белого цвета (с кремовым оттенком), хорошо растворяется в воде, не растворяется в спирте. При необходимости дополнительная очистка препарата возможна методом высаживания из водного раствора спиртом. При температуре 93-94 ос продукт плавится с обугливанием. Аскорбат цинка дает качественную реакцию с раствором NaOH. При этом образуется белый гельобразный осадок Zn(OH)2. При взаимодействии водного раствора аскорбата цинка с раствором гексацианоферрат (III) калия, K3[Fe(CN)6] образуется желтый осадок Zn3[Fe(CN)6]2.
Аскорбат меди (II) дигидрат -кристаллический продукт голубого цвета, хорошо растворяется в воде, не растворяется в спирте. Легко очищается методом высаживания из водного раствора спиртом. При температуре 132-134 ОС наблюдается начало разложения (образец голубого цвета приобретает серое окрашивание).
Аскорбат меди (II) дает качественную реакцию на ионы меди (II) с гексацианоферрат (II) калия, K 4 [Fe(CN) 6 ]. При этом образуется осадок Сu 2 [Fe(CN) 6 ] красно-бурого цвета.
-
б) Раствор 3,4 (0,0142 моль) сульфата меди (II), CuSO 4 • 5H 2 O в 15 мл воды (рН 3) нагревают до 40-45 о с 20 минут. к гомогенному раствору гидролизата (рН 2) присыпают порциями 5 г (0,0284 моль) аскорбиновой кислоты при температуре 3035 о с, перемешивают до полного растворения и выдерживают при комнатной температуре в течение 3-х часов. Реакционная смесь приобретает светлозеленый цвет и на дне колбы осаждается незначительное количество Cu 2 O красного цвета. Реакционную смесь фильтруют, гомогенный раствор упаривают, остаток обрабатывают и очищают спиртом по аналогии с методикой (2а). Получают 3,27 г (51 %) аскорбата меди (II) дигидрата, [C 6 H 7 O 6 ] 2 Cu • 2H 2 O.
-
в) Раствор 1,7 г (0,0142 моль) сульфата меди (II) в 10 мл воды нагревают до 40-45 о с 20 минут. К гомогенному раствору гидролизата присыпают 2,5 г (0,028 моль) аскорбиновой кислоты при температуре 30-35 о с, перемешивают до полного растворения и выдерживают при комнатной температуре 45-50 минут. Реакционный раствор фильтруют от микропримесей Cu 2 O. Фильтрат (светлозеленого цвета) высаживают спиртом, голубые кристаллы фильтруют, промывают
спиртом, и сушат при комнатной температуре. Получают 0,7 г (22 %) аскорбата меди (II) дигидрата, [C 6 H 7 O 6 ] 2 Cu • 2H 2 O.
-
г) К гомогенному раствору 2,5 г (0,0284 моль) аскорбиновой кислоты (рН 2) приливают гидролизат, полученный из 1,7 г (0,0142 моль), CuSO 4 • 5H 2 O в 10 мл воды при температуре 40-45 о с в течение 20 минут. Реакционную смесь выдерживают 45-50 минут при комнатной температуре, фильтруют от микропримесей Cu 2 O. Фильтрат (светло-зеленого цвета) высаживают спиртом, голубые кристаллы фильтруют, промывают спиртом и сушат при комнатной температуре. Получают 0,82 г (25 %) аскорбата меди (II) дигидрата, [C 6 H 7 O 6 ] 2 Cu • 2H 2 O.
Аскорбат меди (II), полученный по методикам 2б-2г, хорошо растворяется в воде, не растворяется в спирте, имеет температуру начала разложения 132-134 о с, дают качественную реакцию с K 4 [Fe(CN) 6 ] на ионы Cu2+.
Результаты исследований . Реакция комплексообразования аскорбиновой кислоты с ионами цинка и меди (II) осуществлялась взаимодействием аскорбиновой кислоты с гидроксидами соответствующих металлов. При этом учитывалась стабильность аскорбиновой кислоты, которая неустойчива в щелочной среде, а устойчива в кислой среде. В связи с этим были использованы гидроксиды металлов, образованные в процессе гидролиза сульфатов, в виде гидролизатов, имеющих рН 2 [5].
Образование аскорбатов цинка и меди (II) протекают по схеме:
СН2ОН
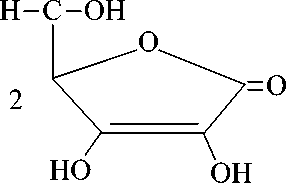
аскорбиновая кислота
to
MeSO4 + 2 HOH C Me(OH)2 + H2SO4
рН < 7
СН2ОН
( 2H2O)
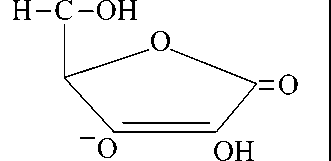
Ме
аскорбаты Ме (II)
(1,2)
где Ме: Zn2+ (1); Сu2+(2).
Из данных эксперимента следует, что комплексообразование аскорбиновой кислоты с ионами цинка протекает в гомогенной фазе в кислой среде однозначно . В оптимальных условиях реакции: температура 45-50 ОС, время 30-35 минут, аскорбат цинка получается с выходом более 90 %. При взаимодействии аскорбиновой кислоты с ионами меди (II) по данной схеме наряду с комплексообразованием протекают побочные реакции, связанные с окислительно-восстановительными процессами: окисление аскорбиновой кислоты, которое катализируется ионами Cu2+, и восстановление ионов Cu2+ до Cu1+ с образованием Cu2O. Для снижения побочных реакций нами была проведена отработка оптимальных условий реакции кмплексообразования. При этом изучалось влияние следующих факторов: температура
ЛИТЕРАТУРА: 1. Кнорре Д.Г., Мызина С.Д. Биологическая химия. М.: Высшая школа, 2003. – с. 34,157; 2. Пат. РФ 2078519.10.05.1997. Кормовая добавка. / А.Ю. Занкевич, А.И. Бойко, О.В. Мерзленко, А.А. Шапошников; 3. Мерзленко О.В. Фармакологические свойства препаратов, получаемых на основе биокоординационных соединений металлов с аскорбиновой кислотой: Автореф…диссерт…доктор. вет. наук, 1998.; 4. Пат РФ 2024514.15.12.1994. Комплекс 1-этилимидазола с аскорбатом цинка. / А.И. Скушникова, Е.С. Домнина, М.Г. Воронков и др.; 5. Кадырова Р.Г., Кабиров Г.Ф., Муллахметов Р.Р. Изучение комплексообразующей способности глицилглицина с 3 d -биогенными металлами.// Ученые записки КГАВМ им. Н.Э. Баумана. – Казань, 2014. – т. 218, с. 102-110.
реакции, время, порядок смешивания реагента и субстрата, способ обработки реакционной смеси. Из данных опытов 2а-2г следует, что наибольший выход аскорбата меди (II) (51 %) получается по методике 2б (температура реакции 30-35 о с, выдержка реакционной смеси 3 часа при комнатной температуре).
Для подтверждения структуры полученных соединений (1,2) проведены качественные реакции на Мe (II).
Заключение. Изучена реакция комплексообразования аскорбиновой кислоты с ионами цинка и меди (II). Найдены оптимальные условия синтеза аскорбатов цинка и меди (II) с хорошими выходами, что позволяет исследовать их биологическую активность. Показано, что для обеспечения стабильности аскорбиновой кислоты реакцию необходимо проводить в кислой среде.
ИЗУЧЕНИЕ РЕАКЦИИ КОМПЛЕКСООБРАЗОВАНИЯ АСКОРБИНОВОЙ КИСЛОТЫ С ИОНАМИ ЦИНКА И МЕДИ (II)
Кадырова Р.Г., Кабиров Г.Ф., Муллахметов Р.Р. Резюме
Изучена реакция комплексообразования аскорбиновой кислоты с ионами цинка и меди (II). Найдены оптимальные условия синтеза аскорбатов цинка и меди (II) с хорошими выходами, что позволяет исследовать их биологическую активность. Показано, что для обеспечения стабильности аскорбиновой кислоты реакцию необходимо проводить в кислой среде.
ASCORBIC ACID WITH ZINC AND COPPER(II) IONS COMPLEX FORMATION REACTION STUDY
Kadyrova R.G., Kabirov G.F., Mullakhmetov R.R.
Список литературы Изучение реакции комплексообразования аскорбиновой кислоты с ионами цинка и меди (II)
- Кнорре Д.Г., Мызина С.Д. Биологическая химия. М.: Высшая школа, 2003. -с. 34,157
- Пат. РФ 2078519.10.05.1997. Кормовая добавка./А.Ю. Занкевич, А.И. Бойко, О.В. Мерзленко, А.А. Шапошников
- Мерзленко О.В. Фармакологические свойства препаратов, получаемых на основе биокоординационных соединений металлов с аскорбиновой кислотой: Автореф…диссерт…доктор. вет. наук, 1998.
- Пат РФ 2024514.15.12.1994. Комплекс 1-этилимидазола с аскорбатом цинка./А.И. Скушникова, Е.С. Домнина, М.Г. Воронков и др.
- Кадырова Р.Г., Кабиров Г.Ф., Муллахметов Р.Р. Изучение комплексообразующей способности глицилглицина с 3d-биогенными металлами.//Ученые записки КГАВМ им. Н.Э. Баумана. -Казань, 2014. -т. 218, с. 102-110.


