Изучение реактогенности, безопасности инактивированной вакцины «ОспаВир» и специфической эффективности двухэтапного метода вакцинации против натуральной оспы с применением на втором этапе живой оспенной вакцины
Автор: Рузавина Е.В., Шкуратова О.В., Ставицкая Н.Х., Мальцева Г.Г., Гаврилова М.А., Чуйкова К.И., Катанахова Л.Л.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 2-2 т.24, 2009 года.
Бесплатный доступ
В НПО «Вирион» разработана инактивированная вакцина «ОспаВир», на основе высокоиммуногенно- го штамма Л-ИВП вируса вакцины. При доклиническом исследовании доказана безвредность и высокая иммунологическая эффективность. В соответствии с программой, согласованной с ГИСК им. Л.А. Тарасевича и утвержденной Комитетом медицинских иммунобиологических препаратов (МИБП) и Минздравом России на базе СиБГМУ были проведены клинические испытания вакцины «ОспаВир» с применением на втором этапе живой оспенной вакцины. Установлена низкая реактогенность и безвредность вакцины «ОспаВир». Применение ее при двухэтапном методе вакцинации против натуральной оспы сопровождается образованием грунд-иммунитета, что приводит к снижению степени проявления вакцинального процесса и не влияет на снижение общего иммунитета. На основании данных, полученных в ходе клинического исследования, была утверждена инструкция по применению. Инактивированная вакцина «Оспа- Вир» прошла регистрацию, а двухэтапный метод вакцинации против натуральной оспы рекомендован Росздравнадзором РФ для практического применения в здравоохранении.
Вакцинация, реактогенность, безвредность, специфическая активность, клинические исследования
Короткий адрес: https://sciup.org/14919058
IDR: 14919058 | УДК: 616.988.25-002.454.2
Studying reactogeneity and safety of inactivated vaccine "ОspaVir" and the analysis of specific activity of 2-stage vaccination method against variola using living variola vaccine on the 2nd stage
Inactivated vaccine ОspaVir which was created in the NPO VIRION based upon high immunogenic vaccine virus strain of L-IVP is proved to be safe and having high immunologic activity. The vaccine does not decrease total immunity.
Текст научной статьи Изучение реактогенности, безопасности инактивированной вакцины «ОспаВир» и специфической эффективности двухэтапного метода вакцинации против натуральной оспы с применением на втором этапе живой оспенной вакцины
В связи с успешной ликвидацией натуральной оспы с 80-х годов вакцинация против данного заболевания прекращена. В настоящее время лица в возрасте до 23 лет не имеют иммунитета против натуральной оспы, а среди других возрастных групп населения только 10-15% имеют остаточный иммунитет. В связи с этим доля восприимчивого населения к вирусу оспы сегодня очень высока. Быстро эволюционирующий природный резервуар ортопоксвирусов с вовлечением человеческой популяции и опасность использования возбудителей в качестве поражающего агента при биотерроризме обосновывают необходимость поддержания запаса эффективных средств массовой вакцинопрофилактики для противоэпидемических мероприятий и иммунизации лиц повышенного риска.
С учетом современных требований к производству вакцин в НПО «Вирион» усовершенствована имеющаяся технология производства инактивированной оспенной вакцины и разработана вакцина «Ос-паВир», изготовленная из высокоиммуногенного штамма Л-ИВП. При доклиническом исследовании были доказаны безвредность и высокая иммунологическая эффективность созданного препарата.
В соответствии с программой, согласованной с ГИСК им. Л.А. Тарасевича и утвержденной Комитетом медицинских иммунобиологических препаратов (МИБП) и Минздравом России, на базе СибГМУ были проведены клинические исследования инактивированной вакцины «ОспаВир» с применением на II этапе живой оспенной вакцины.
Цель и задачи исследовании – изучение реакто-генности, безопасности и иммуногенности инактивированной вакцины «ОспаВир» при двухэтапном методе вакцинации против натуральной оспы.
МАТЕРИАЛ И МЕТОДЫ
В клиническом исследовании принимали участие 204 человека обоего пола в возрасте от 18 до 23 лет, ранее не привитые против натуральной оспы, соответствующие критериям включения. Исследование относилось к двойному слепому, рандомизированному, контролированному. Методом рандоменации добровольцы были распределены на 2 группы. По рекомендации ГИСК им. Л.А. Тарасевича с целью изучения реактогенности и токсичности инактивированной вакцины и анализа отдаленных постпрививочных проявлений в условиях эпидемиологической ситуации по вирусным заболеваниям была сформирована контрольная группа из 100 человек, основная – из 104 волонтеров.
Изучение реактогенности инактивированной вакцины проводилось в два этапа.
На первом этапе вакцинации инактивированную вакцину «ОспаВир» вводили подкожно в область левого плеча. С целью изучения ее реактогенности путем регистрации общих и местных постпрививочных реакций и осложнений за привитыми было установлено медицинское наблюдение с обязательной ежедневной регистрацией постпрививочных проявлений в течение 5 дней. Лица контрольной группы на первом этапе получили референс-препарат (раствор для инъекций изотонический-0,9%), во втором этапе они участие не принимали.
На втором этапе вакцинации волонтерам, получившим вакцину «ОспаВир», ввели живую оспенную вакцину методом скарификации уменьшенной дозой (1 надрез) в область правого плеча. Учитывая, что в ответ на введение живой оспенной вакцины у привитых развивается допустимый вакцинальный процесс, был проведен учет общих и специфических местных реакций на живую вакцину, введенную на фоне вакцинации «ОспаВир».
После проведения второго этапа вакцинации медицинское наблюдение осуществлялось до полного исчезновения всех общих и местных проявлений, до образования корочки на месте вакцинации.
Оценка степени проявления реакций проводилась с учетом допустимых реакций (повышение температуры тела, увеличение регионарных лимфатических узлов и последовательное развитие вакцинального процесса) и разработанных нами критериев.
Безопасность оценивали на основании показателей общего и биохимического анализа крови, общего анализа мочи.
Иммуногенность препарата при двухэтапном методе вакцинации оценивали по данным исследования сывороток крови (процент сероконверсии, серо-протекции) в реакции биологической нейтрализации
(РБН) и реакции торможения гемагглютинации (РТГА). Концентрацию специфических вируснейт-рализующих антител (титр) в сыворотке крови иммунизированных людей определяли в РБН на хорионаллантоисной оболочке (ХАО) развивающегося куриного эмбриона, используя в качестве тест-штамма вирус вакцины ОСО серия 5 производства «НПО «Вирион» (г. Томск) и в РТГА, используя диаг-ностикум оспенный серия 3 и контрольную сыворотку, не содержащую антител к ортопоксвирусам серия 2, производства «НПО «Вирион» (г. Томск).
В ходе исследования все количественные показатели обрабатывались методом вариационной статистики. Статистическую значимость различий определяли по Т-критерию Стъюдента, при этом статистически значимыми считали различия при Р<0,05.
С целью выявления отдаленных постпрививочных проявлений и возможного нарушения иммунной защиты организма вакцинированные находились под медицинским наблюдением в течение 3 месяцев после проведенной вакцинации.
ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ
После проведения первого этапа вакцинации в 100% случаев не было зарегистрировано повышение температуры тела выше 37,5°С. Слабые температурные реакции (37,1-37,5°С) регистрировались в единичных случаях – у 6 (5,7%) человек.
Повышение температуры отмечалось кратковременно, ее нормализация происходила самостоятельно без медицинского вмешательства.
Симптомы общих реакций, такие как слабость, головная боль, регистрировались в единичных случаях в первый день наблюдения у 10 (9,6%) человек, во второй день – у 2 (1,9%) привитых. Недомогание отмечалось только в первый день наблюдения и регистрировалось у 8 (7,6%) волонтеров. Все симптомы общих реакций проходили самостоятельно к концу вторых суток. Местные реакции в виде слабой болезненности наблюдались у 10 (9,6%) вакцинированных, исчезли самостоятельно в течение 24 часов у 8 привитых и через 2 суток после введения вакцины у 2 привитых. В трех (2,8%) случаях местные реакции сопровождались небольшим кратковременным увеличением подмышечных лимфатических узлов (от 0,5 до 0,8 см), которые на третий день наблюдения сократились, стали мягкими, эластичными, безболезненными.
Гиперемии, припухлости в месте введения и других проявлений местных реакций не наблюдалось ни у одного из привитых за весь период наблюдения. В контрольной группе добровольцев были зафиксированы как местные, так и общие реакции. Местные проявления были расценены как «уколочные». Повышение температуры тела до 37,5°С у пяти человек, недомогание и головная боль в трех случаях яви-
Таблица 1
Частота основных симптомов у добровольцев, вакцинированных инактивированной вакциной «ОспаВир», и добровольцев, получивших плацебо
|
Симптомы |
Основная группа («ОспаВир») (n=104) |
Контрольная группа (натрия хлорид 0,9%) (n=100) |
|||
|
I. |
Общие реакции |
абс |
%±m |
абс |
%±m |
|
1. |
Температурная реакция |
||||
|
Нормальная (36,0-37,0)ºС |
98 |
94,3±2,2 |
95 |
95±2,1 |
|
|
Легкая степень (37,1-37,5)ºС |
6 |
5,7±2,2 |
5 |
5,0±2,1 |
|
|
Слабая степень (37,6-38,5)ºС |
0 |
0 |
0 |
0 |
|
|
Сильная степень (от 38,6ºС и выше) |
0 |
0 |
0 |
0 |
|
|
Всего лиц с повышенной температурой тела |
6 |
5,7±2,2 |
5 |
5,0±2,1 |
|
|
2. |
Нарушение общего самочувствия |
||||
|
Недомогание |
8 |
7,6±2,6 |
7 |
7,0±2,5 |
|
|
Головная боль |
10 |
9,6±2,8 |
3 |
3,0±1,7 |
|
|
Всего лиц с нарушением общего самочувствия |
18 |
17,2±3,7 |
10 |
10±3,0 |
|
|
II. |
Местные реакции |
||||
|
Боль в месте инъекции |
10 |
9,6±2,8 |
9 |
9,0±2,9 |
|
|
Гиперемия |
0 |
0 |
0 |
0 |
|
|
Припухлость |
0 |
0 |
0 |
0 |
|
|
Увеличение лимфатических узлов (шейные, подмышечные) |
3 |
2,8±1,6 |
0 |
0 |
|
|
Всего лиц с местными реакциями |
13 |
12,5±3,2 |
9 |
9,0±2,9 |
|
Плацебо – раствор натрия хлорида для инъекций изотонический 0,9%
Статистически значимых различий изучаемых величин в сравниваемых группах не выявлено.
Таблица 2
Картина периферической крови у добровольцев, принимающих участие в клинических исследованиях инактивированной вакцины «ОспаВир» при двухэтапном методе вакцинации против натуральной оспы (n=104)
|
Период наблюдения |
Изучаемые показатели |
||||||||
|
Статистические показатели |
Нb г/л |
Эритроциты х 1о12/л |
Лейкоциты х 109/л |
Сегментоядерные, % |
Эозинофилы, % |
Лимфоциты, % |
Моноциты, % |
СОЭ мм/ч |
|
|
Норма |
Х |
125 |
4,05 |
5,4 |
64 |
2,0 |
21,0 |
7,0 |
10,0 |
|
m |
5,3 |
0,25 |
1,6 |
4,0 |
1,7 |
7,0 |
0,1 |
5,0 |
|
|
До проведения |
Х |
129 |
4,19 |
5,47 |
67,98 |
2,05 |
21,0 |
7,86 |
14,2 |
|
вакцинации |
m |
1,44 |
0,03 |
0,15 |
0,49 |
0,17 |
0,39 |
0,25 |
0,75 |
|
На 7-е сутки после |
Х |
125,4 |
4,05 |
6,11 |
64,96 |
3,1 |
23,24 |
6,81 |
13,46 |
|
вакцинации |
m |
1,42 |
0,03 |
0,18 |
0,3 |
0,29 |
0,57 |
0,27 |
0,78 |
Колебания показателей периферической крови не выходят за пределы физиологической нормы.
лись, по-видимому, следствием респираторно-вирусных заболеваний.
При сравнительном анализе количества и степени проявления общих и местных реакций как в основной, так и в контрольной группах статистически значимых отличий отмечено не было.
Результаты гематологических и биохимических анализов крови после вакцинации статистически значимо не изменялись по отношению к фоновым величинам и не выходили за пределы физиологической нормы. Было установлено, что вакцинация оказывает слабое воздействие на уровень гемоглобина в крови вакцинированных. Среднее значение концентрации гемоглобина до вакцинации составляло (129,0±1,44) г/л, на 7-е сутки после вакцинации содержание гемоглобина незначительно уменьшилось до (125,4±1,42) г/л. Со стороны красной крови наблюдалось небольшое снижение количества эритроцитов на 7-е сутки после вакцинации относительно фоновых значений с (4,19±0,03) х 10 12 /л до (4,05± 0,03) х 1012/л. На 7-е сутки после вакцинации отмечалось повышение лейкоцитов с (5,47±0,15) х 109/л до (6,11±0,03) х 109/л. Наблюдались изменения со стороны сегментоядерных лейкоцитов спустя 7 дней после вакцинации. Процентное содержание сег-
(23,24±0,57)%. Количество моноцитов имело тенденцию к снижению с (7,86±0,25)% до (6,81±0,27)%. Изменений со стороны СОЭ отмечено не было, до вакцинации СОЭ соответствовала (14,2±0,75) мм/ч, после – (13,2±0,75) мм/ч. Незначительные изменения в периферической крови привитых свидетельствуют об активации системы неспецифической резистентности организма.
С целью изучения действия инактивированной вакцины «ОспаВир» на функцию печени, миокарда и почек было проведено исследование биохимических показателей крови привитых.
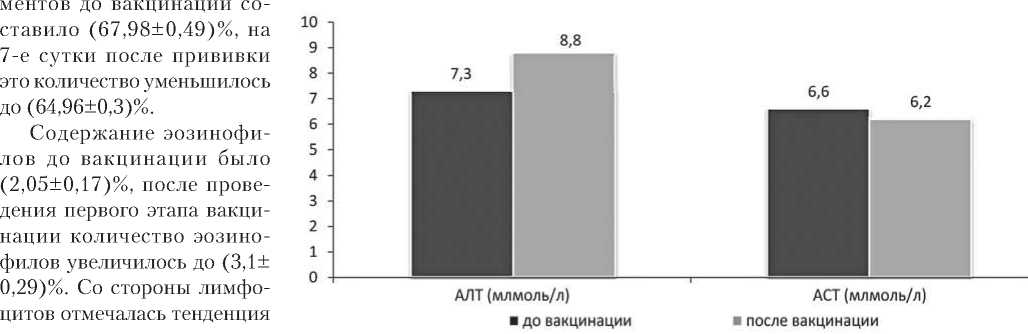
При изучении сывороточных трансаминаз – аспартатаминотрансферазы (АСТ) и аланинаминотрансферазы (АЛТ) – на 7-е сутки после вакцинации наблюдалось умеренное изменение уровня трансаминаз. Отмечалось незначительное увеличение активности АЛТ с (7,3±0,48) млмоль/л до (8,8± 0,43) млмоль/л (при норме до 11,3 млмоль/л), показатели активности АСТ на 7-е сутки фактически оставались стабильными. До вакцинации активность фермента АСТ составляла (6,6±0,39) млмоль/л, на 7-е сутки после прививки (6,2±0,41) млмоль/л (при норме до 7,5 млмоль/л) (рис. 1).
Изменения (сывороточных трансаминаз), воз-
-
- к незначительному увели чению на 7-е сутки наблю
Рис. 1. Изучение уровня АЛТ и АСТ в сыворотке крови привитых на 7-е сутки после введения инактивированной вакцины «ОспаВир».
– Показатели АЛТ и АСТ не выходят за пределы физиологической нормы
дения – с (21,0±0,39)% до
никшие в ответ на введение вакцины, не превышали физиологических норм, не приводили к нарушениям метаболизма гепатоцитов, не вызывали субклинических реакций со стороны основных, функциональных систем организма.
В ходе исследования три добровольца самостоя- тельно отказались от дальнейшего участия в качестве волонтеров, поэтому во втором этапе вакцинации принял участие 101 человек.
На 8-й день после первого этапа был проведен второй этап вакцинации – живой оспенной вакциной методом скарификации в область наружной поверхности верхней трети правого плеча (1 надрез). В ходе наблюдения у 98 (97%) привитых постпрививочная реакция протекала по типу первичной вакцинальной реакции, с ускоренным формированием и развитием кожных элементов. У трех (2,9%) вакцинированных развитие постпрививочной реакции произошло по ускоренному типу. Вакцинация двухэтапным методом с применением на втором этапе живой оспенной вакциной сопровождалась последовательным развитием клинических и местных проявлений.
Периоды течения вакцинального процесса:
-
1) скрытый;
-
2) последовательное развитие вакцинального процесса (папула, везикула, пустула, образование ореолы) с 2-го по 8-й день;
-
3) подсыхание и обратное развитие с 8-го по 12-й день;
-
4) образование рубцов на 8-й–13-й дни.
В каждом из этих периодов наблюдались характерные для них местные, общие и температурные реакции. Максимально выраженные местные и об- щие проявления постпрививочных реакций приходились в период развития оспин – с 5-го по 8-й день после вакцинации, период пустулообразования. С 9-го дня после вакцинации отмечалась регрессия всех клинических проявлений (рис. 2).
В ходе анализа и оценки реактогенности вакцины при двухэтапном методе вакцинации против натуральной оспы с использованием на первом этапе вакцинации инактивированной вакцины «ОспаВир» были выявлены допустимые реакции.
Течение вакцинального процесса с нормальной температурой (36-37)°С наблюдалось в 55 (54,5%)
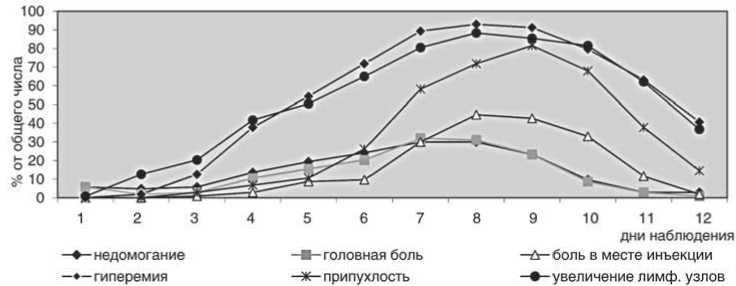
Рис. 2. Динамика клинических симптомов, наблюдаемых у волонтеров после введения живой оспенной вакцины при двухэтапном методе вакцинации против натуральной оспы
Таблица 3
Частота основных симптомов у добровольцев основной группы после проведения второго этапа вакцинации против натуральной оспы
Из местных реакций чаще других регистрировалась болезненность в месте введения вакцины, которая отмечалась у 72 (71,2%) человек. Гиперемия и припухлость в месте скарификации наблюдались у 100 (99%) и 96 (95%) привитых соответственно. Все местные реакции были расценены как легкой и средней степеней проявления и не всегда сопровождались нарушением общего состояния. Течение вакцинального процесса сопровождалось умеренным увеличением подмышечной группы лимфатических узлов справа. Наибольшее количество случаев увеличения лимфатических узлов подмышечной группы справа регистрировалось в период с 6-го по 10-й день со дня вакцинации. Реакция лимфоидной ткани была умеренно выраженной: в 98 (97%) случаях размеры лимфатических узлов не превышали 2 мм, увеличение лимфатических узлов от 2,1 и более мм отмечалось у 1 (0,9%) привитого. В ходе наблюдения каких-либо осложнений и атипичных прививочных реакций не отмечалось.
Постпрививочные реакции имели только легкую и среднюю степени выраженности. Специфическую активность препарата, обусловленную активным компонентом – антигеном вируса вакцины, оценивали по способности вызывать у вакцинированных образование вирус-нейтрализующих антител к вирусу вакцины. При исследовании сывороток крови привитых двухэтапным методом вакцинации против натуральной оспы установлено, что процент лиц, ответивших выработкой специфических антител в РБН и РТГА, составил 100, процент серопротективных волонтеров в РБН и РТГА – 98.
Так как в качестве защитного титра вируснейтра-лизующих антител в РБН был принят титр 1:40, при анализе результатов уровень образования специфических антител к ортопоксвирусам в РБН распределился следующим образом (рис. 3): только один (0,9%) вакцинированный имел уровень антител менее защитного – 1:10; в сыворотке крови еще у одного (0,9%) добровольца обнаружены антитела в титре 1:80; 10 добровольцев (9,9%) имели уровень антител в титре 1:160; 24 (23,8%) – 1:320.
Наибольшее количество – 32 (31,8%) привитых – имели титр антител 1:640, а у 25 (24,8%) добровольцев антитела определялись в разведении 1:1280. Семь человек (6,9%) в ответ на вакцинацию выработали антитела в титре 1:2560 и один (0,9%) – 1:5120. Средний геометрический титр специфических антител в РБН составил (2,804139±0,04) lg, то есть 636,99 (580,95–698,46).
При анализе результатов образования специфиче-
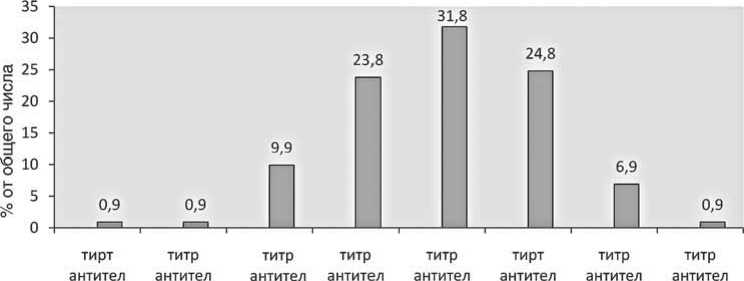
1:10 1:80 1:160 1:320 1:640 1:1280 1:2560 1:5120
Рис. 3. Анализ уровня специфических антител к ортопоксивирусам в сыворотке крови в реакции биологической нейтрализации на ХАО
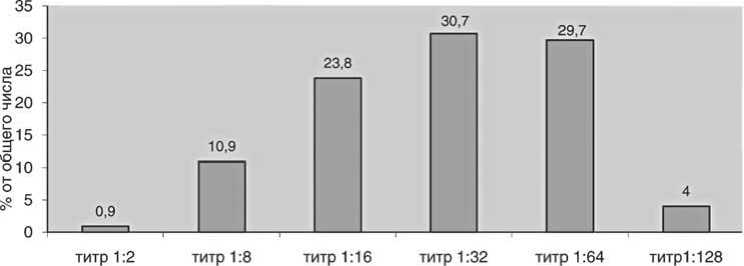
Рис. 4. Анализ уровня специфических антител к ортопоксвирусам в сыворотке крови в РТГА
ских антител к ортопоксвирусам в РТГА было установлено, что титр антител 1:2 наблюдался у 1 (0,9%) привитого, 11 (10,9%) вакцинированных имели антитела в титре 1:8; 24 (23,8%) привитых – 1:16; 31 (30,7%) человек имел титр антител 1:32 и 30 (29,7%) – 1:64. Высокий уровень специфических антител – 1:128 наблюдался у 4 (4%) привитых (рис. 4). Средний геометрический титр специфических антител в РТГА составил (1,484078±0,03) lg, то есть 30,48 (28,45-32,66).
Таблица 4
Сравнительный анализ инфекционной и соматической заболеваемости добровольцев основной и контрольной групп в течение 3 месяцев после проведения второго этапа вакцинации против натуральной оспы
|
Основная группа (n=101) |
Контрольная группа (n=100) |
|
|
Вирусные заболевания |
04.05 г. – 10 человек 05.05 г. – 3 человека 06.05 г. – 7 человек 07.05 г. – 1 человек |
04.05 г. – 12 человек 05.05 г. – 5 человек 06.05 г. – 6 человек 07.05 г. – 1 человек |
|
Всего заболевших лиц: |
21 |
24 |
|
Кожные и аллергические болезни |
0 |
1 |
При анализе полученных данных процент сероконверсии оставил 100, а процент серопротекции равнялся 98. Проведенный корреляционный анализ выявил положительную статистическую линейную взаимосвязь между данными РБН и РТГА – коэффициент корреляции r = 0,638426, с уровнем значимости Р<0,001.
Учитывая то, что вакцинация против натуральной оспы проводилась в весенний период, нами было изучено влияние вакцинации на иммунную систему организма. С целью анализа заболеваемости проводилось наблюдение за лицами основной и контрольной групп в течение трех месяцев. В ходе наблюдения было установлено, что заболеваемость среди вакцинированных была аналогична заболеваемости лиц контрольной группы (табл. 4).
ЗАКЛЮЧЕНИЕ
Результаты проведенных клинических исследований показали, что инактивированная вакцина «ОспаВир» ареактогенна и безвредна. Применение ее при двухэтапном методе вакцинации против натуральной оспы сопровождается образованием грунд-иммунитета, что приводит к снижению степени проявления вакцинального процесса и не влияет на снижение общего иммунитета.
На основании данных, полученных в ходе клинического исследования, была утверждена инструкция по применению. Вакцина «ОспаВир» прошла реги- страцию, а двухэтапный метод вакцинации против натуральной оспы рекомендован Росздравнадзором РФ для практического применения в здравоохранении.
STUDYING REACTOGENEITY AND SAFETY OF INACTIVATED VACCINE «ОSPAVIR» AND THE ANALYSIS OF SPECIFIC ACTIVITY OF 2-STAGE VACCINATION METHOD AGAINST VARIOLA USING LIVING VARIOLA VACCINE
ON THE 2-ND STAGE


