Изучение роли полиморфизма генов репарации ДНК в формировании предрасположенности к развитию тройного негативного рака молочной железы у женщин
Автор: Титов Р.А., Глушков А.Н., Торгунакова А.В., Захарова Я.А., Марущак А.В., Минина В.И.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Генетика
Статья в выпуске: 4, 2024 года.
Бесплатный доступ
Обследованы 682 женщины русской национальности, проживающие в Кемеровской обл. России, в том числе 213 больные тройным негативным раком молочной железы и 465 женщин близкого возраста, не имеющих признаков онкологических заболеваний. Проведен сравнительный анализ полиморфных вариантов генов репарации ДНК APEX1 444T>G (rs1130409), ATM 5557G >A (Ars180151), hOGGl 977C>G (rs1052133), XPD 2251T>G (rs13181), XPG 3310G>C (rs17655), ADPRT 2285 T>C (rs11610) у больных раком молочной железы и индивидов, не имеющих онкологических заболеваний, проживающих в той же местности. Анализ однолокусных эффектов показал значимую связь между риском рака молочной железы и вариантами гена XPG 3310G>C (rs17655) (OR = 0.64, CI: 0.47-0.87, p = 0.004) в общей группе и (OR = 0.68, 95% CI: 0.49-0.94; р = 0.019) в некурящей группе, и гена XPD 2251T>G (OR = 0.30, 95% CI: 0.11-0.78 ; р =0.011) в курящей группе. MDR-aнализ межгенных взаимодействий показал, что гены XPD 2251T>G и APEX1 444T>G, XPG 3310G>C и ATM 5557G >A тесно взаимодействуют и взаимно усиливают риск развития рака молочной железы.
Рак молочной железы, тройной негативный, полиморфизм генов apex1, atm, hogg1, xpd, xpg, adprt
Короткий адрес: https://sciup.org/147247249
IDR: 147247249 | УДК: 575.174.015.3 | DOI: 10.17072/1994-9952-2024-4-440-450
Study of polymorphism of DNA repair genes in the formation of presposition to the development of triple negative breast cancer in women
The study involved 682 women of Russian nationality living in Kemerovo oblast of Russia, including 213 patients with triple-negative breast cancer and 249 women of a similar age with no signs of cancer. Comparative analysis of polymorphic variants of DNA repair genes APEX1 444T>G (rs1130409), ATM5557G >A (Ars180151), hOGG1 977C>G (rs1052133), XPD 2251T>G (rs13181), XPG 3310G>C (rs17655), ADPRT 2285 T>C (rs11610) in patients with triple-negative breast cancer and individuals without cancer living in the same area was performed. Analysis of single-locus effects showed significant associations between the risk of breast cancer and variants of the XPG 3310G>C gene (rs17655) (OR = 0.64, CI: 0.47-0.87, p = 0.004) in the overall group and (OR = 0.68, 95% CI: 0.49 -0.94; p = 0.019) in the non-smoking group, and the XPD 2251T>G gene (OR = 0.30, 95% CI: 0.11-0.78; p = 0.011) in the smoking group. MDR analysis of intergenic interactions showed that the XPD 2251T>G and APEX1 444T>G, XPG 3310G>C and ATM 5557G>A genes closely interact and mutually increase the risk of developing breast cancer in women.
Текст научной статьи Изучение роли полиморфизма генов репарации ДНК в формировании предрасположенности к развитию тройного негативного рака молочной железы у женщин
Acknowledgments : the work was carried out within the framework of the state assignment AAAA-A21-121011590009-9 “Immuno-hormonal interactions in breast cancer”.
Рак молочной железы (РМЖ) — наиболее распространенная злокачественная опухоль, возникающая у женщин и занимающая второе место в мировой статистике по смертности [Siegel et al., 2021; Злокачественные…, 2021]. Благодаря новым методам профилактики и лечения смертность из-за этого заболевания постепенно снижается. Данная злокачественная патология характеризуется высокой степенью гетерогенности и дополнительно подразделяется на несколько типов. Классификация РМЖ основана на экспрессии молекулярных маркеров. Тройной негативный рак характеризуется наихудшим прогнозом. Этот тип РМЖ встречается примерно у 15% пациенток. При этом на поверхности опухолевых клеток нет рецепторов эстрогена и прогестерона, а экспрессия рецепторов эпидермального фактора роста (HER-2) нормальная. Это делает их крайне нечувствительными к терапии существующими на сегодняшний день препаратами, включая те, что целенаправленно действуют на HER-2 или гормональные препараты.
Согласно данным исследований известно, что РМЖ появляется в результате генетических и гормональных изменений, возникающих под действием факторов окружающей среды и профессиональной деятельности, тесно связан с неправильным образом жизни (употребление алкоголя и табака, лишний вес и ожирение, физическая инертность) и репродуктивной историей (возраст менархе, возраст первых родов, кормление грудью) [Sun et al., 2017; Obeagu, Obeagu, 2024]. Репарация ДНК является частью барьеров, защищающих от мутаций, увеличивающих риск онкопатологии [Torgovnick, Schumacher, 2015; Kur-furstova et al., 2016]. Репарация ДНК отвечает за поддержание целостности генома путем защиты клеток от генетических и экологически обусловленных нарушений. Гены, связанные с механизмами репарации ДНК, считаются генами-кандидатами предрасположенности к раку, поскольку нарушение механизмов поддержания целостности генома может привести к злокачественной трансформации [Rudolph, Chang-Claude, Schmidt, 2016]. Однако точные молекулярные механизмы развития рака молочной железы все еще находятся на стадии интенсивного изучения.
В нашем исследовании мы сосредоточились на оценке роли однонуклеотидных полиморфизмов генов (SNP) репарации ДНК в формировании наследственной предрасположенности к РМЖ у женщин, проживающих в промышленно развитом регионе. Основными задачами нашей работы было выявление активно изучаемых вариантов в генах репарации ДНК: APEX1 444T>G (rs1130409), ATM 5557G >A (Ars180151), hOGG1 977C>G (rs1052133), XPD 2251Т>G (rs13181), XPG 3310G>C (rs17655), ADPRT 2285 T>C (rs11610) у женщин Кемеровской обл. и оценка их эффектов относительно риска формирования онкопатологии. Результаты нашего исследования помогут наилучшим образом раскрыть молекулярную основу предрасположенности к РМЖ и лечь в основу профилактики данного типа рака.
Целью нашего исследования была оценка риска развития тройного негативного РМЖ у женщин Кемеровской обл. в соответствии с носительством полиморфных вариантов генов репарации ДНК.
Материалы и методы исследований
Были обследованы 682 женщины (русские по этнической принадлежности), проживающие на территории Кемеровской обл. РФ. От каждого человека было получено информированное согласие на участие в исследовании. Исследование выполнено в соответствии с Хельсинкской декларацией Всемирной медицинской ассоциации: этические принципы проведения медицинских исследований с участием человека с поправками 2000 г. и «Правилами клинической практики в Российской Федерации», утвержденными Министерством здравоохранения Российской Федерации 19.06.2003 г. Проведение исследования было утверждено комитетом по этике Института экологии человека Федерального исследовательского центра угля и углехимии СО РАН.
Группы формировались по принципу «случай–контроль» с учетом возраста, пола, этнической принадлежности и влияния факторов среды. Критерии включения: русские женщины, проживающие в Кемеровской обл. с момента рождения, возраст старше 40 лет. Критерии исключения: наличие наслед- ственных, аутоиммунных, аллергических, психических заболеваний, родственников с онкозаболеваниями, ранее диагностированный рак других органов. В первую группу вошли 217 впервые выявленных больных РМЖ (средний возраст 58.9±10.5). Диагноз РМЖ устанавливался по результатам клинического, эндоскопического и морфологического обследования на базе Кузбасского областного онкологического диспансера. Контрольную группу составили 465 не родственных женщин без онкозаболеваний в анамнезе, проживающих в той же местности (средний возраст 54.79±8.2). Все здоровые доноры, включенные в контрольную группу (онкопатология молочных желез была исключена по результатам маммографии и обследования у маммолога), не принимали препаратов с известным мутагенным действием и не проходили рентгенологических процедур в течение трех месяцев до участия в исследовании. ДНК выделяли из венозной крови с использованием стандартной методики фенольно-хлороформной экстракции [Sambrook, Fritsch, Maniatis, 1989]. После выделения клетки крови подвергались лизированию, белковая компонента разрушалась протеиназой К (SibEnzyme, Новосибирск, Российская Федерация). С учетом анализа данных литературы нами были выбраны полиморфные локусы генов APEX1 444T>G (rs1130409), ATM 5557G >A (Ars180151), hOGG1 977C>G (rs1052133), XPD 2251Т>G (rs13181), XPG 3310G>C (rs17655), ADPRT 2285 T>C (rs11610). Частота редкого аллеля в популяциях европеоидов учитывалась по данным доступного ресурса National Center for Biotechnology Information . Типирование полиморфных маркеров проводилось с помощью ал-лель-специфической ПЦР (ООО “Литех НПП”, Москва, Россия). Амплификацию проводили на термоциклере “Терцик” по программе, рекомендованной производителем наборов реагентов. Продукты ПЦР анализировали методом электрофореза в 3%-ном агарозном геле наличием бромистого этидия. Последующая визуализация фрагментов ДНК осуществлялась в камере с УФ-светом. Статистическую обработку результатов проводили с использованием пакетов прикладных программ: SNPstat , STATISTICA 10.0, MDR . Проводили оценку частоты аллелей и генотипов; анализировали соответствие распределения частот генотипов равновесию Харди–Вайнберга; оценивали статистическую значимость различий между группами по частотам аллелей и генотипов с учетом теста X2 на гомогенность выборок (статистически значимыми считали различия при p <0.05). Логистическую регрессию использовали для выявления ассоциации полиморфных локусов в различных моделях наследования (аддитивной, доминантной, сверхдоминантой, рецессивной, лог-аддитивной) c коррекцией на возраст, статус курения. Для выбора лучшей модели использовали информационный критерий Акайке (AIC). Исследование эффектов межгенных взаимодействий проводили в программе MDR – Multifactor Dimensionality Reduction .
Результаты
Частоты генотипов и аллелей исследованных полиморфных локусов показали соответствие равновесию Харди–Вайнберга как в группе больных РМЖ, так и в группе здоровых (табл. 1).
Таблица 1
Распределение частот генотипов и аллелей полиморфных локусов генов репарации ДНК [The genotype and allele frequency distribution at the polymorphic DNA repair gene loci]
|
Локусы и генотипы |
Генотипы и аллели |
Больные РМЖ (Case) |
Здоровые женщины (Control) |
χ2 |
p |
|
APEX1 444 T>G rs1130409 |
TT TG GG |
80 (36.9%) 108 (49.8%) 29 (13.4%) |
159 (34.3%) 232 (50.1%) 72 (15.6%) |
0.54 |
0.69 |
|
T/G |
268(0.62)/166(0.38) |
550(059)/376(0.41) |
|||
|
p HWE |
0.47 |
0.44 |
|||
|
ATM 5557G >A Ars180151 |
GG GA AA |
149 (73%) 46 (22.6%) 9 (4.4%) |
352 (75.7%) 105 (22.6%) 8 (1.7%) |
3.1 |
0.15 |
|
G/A |
344(0.84)/64(0.16) |
809(0.87)/121(0.13) |
|||
|
p HWE |
0.6 |
1 |
|||
|
hOGG1 977 C>G rs1052133 |
CC CG GG |
130 (59.9%) 79 (36.4%) 8 (3.7%) |
289 (62.8%) 147 (32%) 24 (5.2%) |
1.3 |
0.4 |
|
C/G |
339(0.78)/95(0.22) |
725(0.79)/195(0.21) |
|||
|
p HWE |
0.43 |
0.33 |
Окончание табл. 1
|
Локусы и генотипы |
Генотипы и аллели |
Больные РМЖ (Case) |
Здоровые женщины (Control) |
χ2 |
p |
|
XPD 2251 T>G rs13181 |
TT TG GG |
98 (45.2%) 93 (42.9%) 26 (12%) |
211 (45.4%) 198 (42.6%) 56 (12%) |
0.01 |
0.995 |
|
T/G |
289(0.67)/145(0.33) |
620(0.67)/310(0.33) |
|||
|
p HWE |
0.65 |
0.4 |
|||
|
XPG 3310 G>C rs17655 |
GG GC CC |
72 (47.7%) 67 (44.4%) 12 (8%) |
257 (60.8%) 147 (34.8%) 19 (4.5%) |
7.4 |
0.015 |
|
G/C |
211(0.7)/91(0.3) |
661(0.78)/185(0.22) |
|||
|
p HWE |
0.57 |
0.89 |
|||
|
ADPRT 2285 T>C rs11610 |
TT TC CC |
137 (70.6%) 50 (25.8%) 7 (3.6%) |
309 (66.6%) 144 (31%) 11 (2.4%) |
1.7 |
0.31 |
|
A/C |
324(0.84)/64(0.16) |
762(0.82)/166(0.18) |
|||
|
p HWE |
0.43 |
0.27 |
Примечание. pHWE – значимость отличий распределения частот генотипов от равновесия Харди–Вайнберга (exact test for Hardy–Weinberg equilibrium); p – значимость отличий частоты встречаемости генотипа в группе больных и здоровых, критерий χ2 с поправкой Йетса.
При сравнении изученных групп жительниц Кемеровской области больных РМЖ и здоровых было выявлено отличие частот по вариантам гена XPG3310G>C ( rs17655 ).
Расчеты соотношения шансов для различных моделей наследования (табл. 2) показали, что для полиморфного варианта XPG 3310 G>C ассоциации с риском РМЖ наиболее значимо проявлялись в сверхдоминантной модели наследования в общей группе (ORadj = 0.64, 95% CI: 0.47-0.87; рadj = 0.004, AIC 657.3) и в лог-аддитивной модели в группе некурящих (ORadj = 0.68, 95% CI: 0.49-0.94; рadj = 0.019, AIC 552.2).
Таблица 2
Результаты анализа ассоциаций полиморфных локусов генов-кандидатов с риском РМЖ [Results of the analysis of polymorphic loci associations of candidate gene with the risk of breast cancer]
|
Локусы и генотипы |
Группа |
Модель |
OR adj |
p |
AIC |
|
APEX1 |
Общая |
Лог-аддитивная |
1.11 (0.87-1.41) |
0.4 |
854.9 |
|
444 T>G |
Курящие |
Доминантная |
2.49 (0.94-6.57) |
0.064 |
111.3 |
|
rs1130409 |
Некурящие |
Лог-аддитивная |
1.20 (0.92-1.56) |
0.18 |
695.9 |
|
ATM |
Общая |
Рецессивная |
0.38 (0.14-1.00) |
0.051 |
823.5 |
|
5557G >A |
Курящие |
Сверхдоминантная |
0.76 (0.26-2.16) |
0.6 |
110.5 |
|
Ars180151 |
Некурящие |
Рецессивная |
0.35 (0.12-1.03) |
0.056 |
673.7 |
|
hOGG1 |
Общая |
Сверхдоминантная |
0.82 (0.58-1.15) |
0.25 |
852 |
|
977 C>G |
Курящие |
Сверхдоминантная |
0.61 (0.24-1.54) |
0.3 |
113.6 |
|
rs1052133 |
Некурящие |
Сверхдоминантная |
0.86 (0.59-1.25) |
0.43 |
694.5 |
|
XPD |
Общая |
Сверхдоминантная |
0.99 (0.72-1.37) |
0.96 |
857.2 |
|
2251 T>G |
Курящие |
Доминантная |
0.30 (0.11-0.78) |
0.011 |
108.2 |
|
rs13181 |
Некурящие |
Доминантная |
1.19 (0.83-1.70) |
0.33 |
698.4 |
|
XPG |
Общая |
Лог-аддитивная |
0.64 (0.47-0.87) |
0.004 |
657.3 |
|
3310 G>C |
Курящие |
Доминантная |
0.36 (0.11-1.14) |
0.08 |
75.7 |
|
rs17655 |
Некурящие |
Лог-аддитивная |
0.68 (0.49-0.94) |
0.019 |
552.2 |
|
ADPRT |
Общая |
Сверхдоминантная |
1.30 (0.89-1.89) |
0.17 |
800.2 |
|
2285 T>C |
Курящие |
Сверхдоминантная |
3.55 (1.06-11.84) |
0.27 |
97.6 |
|
rs11610 |
Некурящие |
Рецессивная |
0.61 (0.21-1.80) |
0.38 |
659.9 |
Примечание. OR adj – показатель отношения шансов для редкого аллеля с поправкой на возраст. P – значимость различий между группами. AIC – критерий Акайке.
Для гена XPD2251 T>G наиболее значимые ассоциации проявлялись в доминантной модели наследования в группе пациентов, характеризующихся употреблением табачных изделий (ORadj = 0.30, 95% CI: 0.11-0.78 ; рadj =0.011, AIC 108.2).
Связи риска развития злокачественных новообразований молочной железы с полиморфизмами других генов системы репарации ДНК выявлено не было.
В результате анализа межгенных взаимодействий методом MDR были определены две треxлокусные модели, связанные с риском развития РМЖ у женщин (табл. 3).
Таблица 3
Анализ межгенных взаимодействий при формировании РМЖ у женщин [Analysis of intergenic interactions in the formation of breast cancer in women]
|
XPD 2251Т>G* APEX1444 T>G XPG 3310G>C (курящие) |
0.8484 |
0.622 |
0.0001 |
0.9375 |
0.7381 |
10/10 |
0.5769 |
|
XPG 3310G>C* ATM5557G >A XPD 2251Т>G (некурящие) |
0.6182 |
0.509 |
0.0001 |
0.5891 |
0.6398 |
8/10 |
0.3958 |
Примечание. Tr.Bal.Acc. – тренировочная сбалансированная точность; Test.Bal.Acc. – тестируемая сбалансированная точность; Sign Test – тест на значимость; Se – чувствительность; Sp – специфичность; CVС – повторяемость результата; Pre. (Precision) – точность модели; *алгоритм полного поиска (Exhaustive search algoritm).
Первая модель включала в себя полиморфизмы XPD 2251Т>G, APEX 1444 T>G и XPG 3310G>C. Кластерный анализ позволил установить тесное взаимодействие и взаимное усиление эффектов (синергизм) между полиморфными локусами XPD 2251Т>G и APEX1444 T>G, данный кластер взаимодействует с геном XPG 3310G>C с дублирующим эффектом.
Вторая модель ген-генного взаимодействия, ассоциированная с развитием РМЖ у некурящих женщин, включала полиморфные варианты генов XPG 3310G>C, ATM 5557G>A и XPD 2251Т>G. Выявлен кластер тесно взаимодействующих генов XPG 3310G>C и ATM 5557G>A , эффекты которых синонимичны. Данный кластер образовывал единый блок с геном XPD 2251Т>G с дублирующим эффектом данных генов (рис. 1).
XPG(3310G>C)
XPD(22511>G)
APEX1 (444T>G)
Модель 1. Курящие женщины

Модель 2. Некурящие женщины
Рис. 1. Дендрограмма межгенных взаимодействий у женщин больных РМЖ.
Короткие линии указывают на сильное взаимодействие генных локусов, длинные – на слабую связь; черным цветом указывается синергизм, т.е. взаимное усиление эффектов между локусами, серым– дублирование эффектов между локусами
[Dendrogram of intergenic interactions in women with breast cancer.
Short lines indicate strong interaction of gene loci, long lines indicate weak connection; black color indicates synergism, i.e. mutual enhancement of effects between loci, gray color indicates duplication of effects between loci]
Анализ комбинаций всех возможных вариантов модели в таблицах сопряженности позволил выявить 9 благоприятных и 9 негативных эффектов у курящих женщин и 10 благоприятных и 12 негативных у некурящих женщин комбинаций для развития тройного негативного РМЖ (рис. 2 и 3).
cc
XPD(2251DG)
GG TG TT
XPG(3310G>C) GC GG
XPD(22511>G) XPD(2251DG)
GG TG TT GG TG TT
0
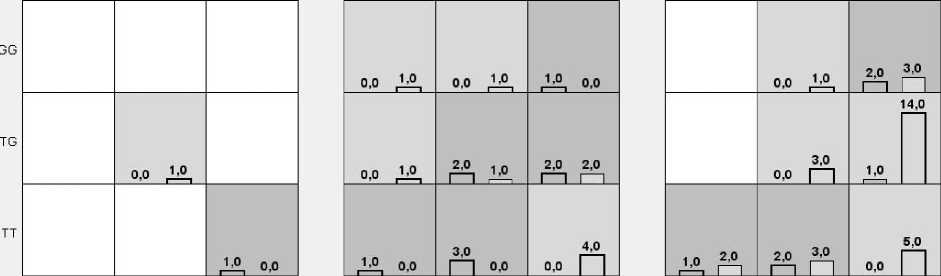
Рис. 2. Сочетания вариантов генов XPD 2251Т>G, APEX1444 T>G и XPG 3310G>C, указывающих на предрасположенность к возникновению онкозаболеваний молочной железы у курящих женщин.
Сочетания вариантов генов, указывающих на повышенный риск развития заболевания – темно-серые ячейки, на пониженный риск – светло-серые ячейки, отсутствующие сочетания генотипов – белые ячейки (столбики в ячейках слева – пациентки с РМЖ, правые – здоровые женщины)
[Combinations of gene variants XPD 2251T>G, APEX1444 T>G and XPG 3310G>C indicating a predisposition to breast cancer in women who smoke.
Combinations of gene variants indicating a high risk of developing the disease - dark gray cells, lower risk - light gray cells, missing combinations of genotypes - white cells (bars in the cells on the left - patients with breast cancer, on the right - healthy women]
AA
XPD(2251DG)
GG TG TT
ATM(5557G>A) GA GG
XPD(22511>G) XPD(2251DG)
GG TG TT GG TG TT
(□ACDO 爾 adx
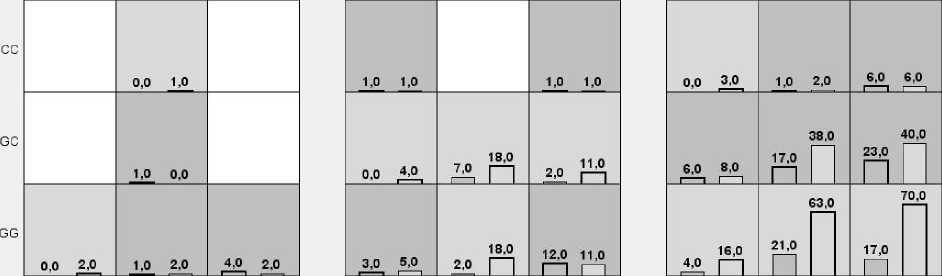
Рис. 3. Сочетания вариантов генов XPG 3310G>C, ATM 5557G >A и XPD 2251Т>G, указывающих на предрасположенность к возникновению онкозаболеваний молочной железы у некурящих женщин [Combinations of gene variants XPG 3310G>C, ATM 5557G>A and XPD 2251T>G indicating a predisposition to breast cancer in non-smoking women ]
Обсуждение
Рак молочной железы является наиболее распространенным злокачественным заболеванием у женщин. По оценкам GLOBOCAN 2020 каждая четвертая женщина страдает раком молочной железы, а каждая восьмая женщина умирает от рака молочной железы. Женщины старшего возраста имеют высокий уровень заболеваемости раком молочной железы. В 2018 г. 645 000 против 1–4 млн случаев рака молочной железы и 130 000 против 490 000 смертей были зарегистрированы в пременопаузальной и постменопаузальной группах соответственно [Sung et al., 2021]. В метааналитическом исследовании было отмече- но, что ранняя беременность и более длительное грудное вскармливание снижают ER (рецептор эстрогена) положительный и ER отрицательный риск развития рака молочной железы [Anstey et al., 2017; Fortner et al., 2019]. Поздний возраст вступления в брак и рождения ребенка приводит к недостаточной дифференциации тканей молочной железы, большему воздействию неэстрогенных мутагенов и генотоксичности эстрогенов, тем самым увеличивая риск РМЖ [Dey et al., 2009].
Кроме того, ожирение является еще одним сильным фактором риска развития рака молочной железы у женщин в постменопаузе, а также ассоциируется с плохим исходом заболевания у женщин всех возрастов [Picon‐Ruiz et al., 2017, Guo et al., 2018]. Также продолжает расти количество данных, что курение сигарет связано с повышенным риском развития рака молочной железы [Reynolds, 2013; Reiner et al., 2022]. В исследовании Gram показано, что женщины, которые курили более 5 лет до родов по сравнению с теми, кто никогда не курил, имели более высокий риск развития рака молочной железы в целом на 42% (95% CI: 1.13–1.78). [Gram et al., 2019].
Тройной негативный тип рака молочной железы представляет собой большой интерес для фундаментальных исследований генетики в виду его агрессивного течения. Его клетки характеризуются большим пролиферативным и метастатическим потенциалом в другие органы. Данный тип РМЖ может дополнительно подразделяться на другие подтипы, учитывая особенности экспрессии генов и молекул РНК, а также белков в составе опухолей. В итоге различают шесть подтипов: базальный 1-ого типа, базальный 2-ого типа, мезенхимальный, подтип подобный мезенхимальным стволовым клеткам, люминальный AR и иммунномодуляторный типы [Lehmann et al., 2011]. Тройной негативный тип возникает в 12–17% случаев у молодых женщин, которые также являются носителями мутаций в области генов BRCA . Его спорадическое формирование во многом определяется эпигенетическими изменениями в составе BRCA. В виду своего агрессивного течения, тройной негативный тип РМЖ более чувствителен к химиотерапии, что определяет наилучший прогноз лечения [Liedke et al., 2008]. В особенности наилучшую выживаемость среди пациентов обеспечивает неоадьювантная терапия.
В результате проведенного настоящего исследования были выявлены ассоциации между унаследованными вариантами ряда генов ферментов репарации ДНК и риском тройного негативного РМЖ. Была показана статистическая значимость вариантов гена XPG 3310G>C (rs17655 ) в общей и группе некурящих пациентов, и гена XPD 2251Т>G (rs13181 ) в группе курящих пациентов с риском формирования тройного негативного РМЖ у женщин, проживающих в промышленном регионе. По генам APEX1 444T>G (rs1130409), ATM 5557G >A (Ars180151), hOGG1 977C>G (rs1052133), ADPRT 2285 T>C (rs11610) статистически значимых ассоциаций выявлено не было.
Ген XPG кодирует белок, представляющий собой эндонуклеазу, которая вырезает поврежденный участок ДНК. XPG взаимодействует с комплексом TFIIH и обеспечивает прикрепление хеликаз для правильного разъединения цепей ДНК, делая их доступными для действия эндонуклеаз. Нарушение взаимодействия XPG–TFIIH приводит к диссоциации хеликаз и нарушению белкового комплекса, прерывая процесс репарации [Ito et al., 2007]. Adolf с соав. в своей работе показал, что генотип His/His XPG увеличивает риск РМЖ в 1.2 раза у молодых пациенток (<40 лет) (р = 0.028). Наличие генотипов Asp/His+His/His в 1.3 раза повышало риск развития РМЖ у пациенток с PR+ и в 1.1 раза снижало риск развития РМЖ у пациенток с люминальным-A типом РМЖ (p = 0.014, p = 0.020 соответственно) [Adolf et al., 2023]. Еще несколько ранее произведенных исследований также показали связь гена XPG с раком молочной железы [Na et al., 2015; Malik et al., 2018].
Ген XPD ( ERCC2 ) кодирует АТФ-независимую хеликазу. Это ключевой белок эксцизионной репарации нуклеотидов (NER), который узнает и исправляет различные мутации, образующиеся, например, после УФ-облучения или оксидативного стресса. В составе комплекса транскрипционных факторов (TFIIH) хеликаза XPD раскручивает цепь ДНК, обеспечивая доступ эндонуклеаз к поврежденному участку [Broughton, Steingrimsdottir, Lehmann, 1996]. Полиморфизм Lys751Gln (rs13181) является одним из наиболее широко изученных генетических маркеров XPD, и его роль в развитии рака очевидна [Ben-hamou, Sarasin, 2002]. В работах Smolarz с соав. генотип Gln/Gln гена XPD был связан с повышенным риском РМЖ и с тройным негативным РМЖ [Smolarz et al., 2014, 2019]. Samson и др. также сообщали, что генотип XPD Gln/Gln значительно связан с повышенным риском рака молочной железы у женщин Южной Индии [Samson et al., 2011]. Точно также Roberts с коллегами пришли к выводу, что варианты генов BER и NER могут влиять на риск развития рака молочной железы у человека [Roberts et al., 2011].
В рамках настоящего исследования проведено моделирование межгенных взаимодействий методом MDR. Для оценки межгенных взаимодействий с помощью MDR-анализа в отношении риска развития РМЖ у женщин использовали алгоритм всестороннего поиска (Exhaustive search algorithm), который оценивал все возможные комбинации исследованных полиморфных локусов. В результате анализа были выявлены наиболее информативные модели межгенных взаимодействий, детерминирующих формирование тройного негативного РМЖ у женщин: XPD 2251Т>G, APEX 1444 T>G, XPG 3310G>C и XPG 3310G>C, ATM 5557G>A, XPD 2251Т>G . Первая модель межгенных взаимодействий включала в себя гены XPD 2251Т>G, APEX 1444 T>G, XPG . Между генами XPD и APEX был выявлен сильный синергизм.
Ген XPG представляет собой локус с дублирующим эффектом. Вторую модель межгенных взаимодействий, связанную с развитием тройного негативного РМЖ у некурящих женщин, составили полиморфные локусы XPG 3310G>C, ATM 5557G>A, XPD 2251Т>G. Между генами XPG 3310G>C и ATM 5557G>A было выявлено взаимно усиливающее действие, а ген XPD 2251Т>G образовывал единый кластер с дублирующим эффектом данных генов.
Заключение
Подводя итог, можно сказать, что это исследование способствует раскрытию молекулярной основы тройного негативного рака молочной железы. Наши результаты указывают на гены репарации ДНК и их полиморфизмы, которые могут быть вовлечены в формирование рака молочной железы у женщин Кемеровской обл. Они могут найти практическое применение для улучшения диагностики рака на ранних стадиях развития и привести к снижению заболеваемости и смертности больных тройным негативным раком молочной железы.
Список литературы Изучение роли полиморфизма генов репарации ДНК в формировании предрасположенности к развитию тройного негативного рака молочной железы у женщин
- Злокачественные новообразования в России в 2020 году (заболеваемость и смертность) / под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М., 2021. 252 с.
- Adolf I.C. et al. The interplay between XPG-Asp1104His polymorphism and reproductive risk factors elevates risk of breast cancer in Tanzanian women: A multiple interaction analysis // Cancer Medicine. 2023. Vol. 12. P. 472-487.
- Anstey E.H. et al. Breastfeeding and breast cancer risk reduction: implications for black mothers // American journal of preventive medicine. 2017. Vol. 53, № 3. P. S40-S46.
- Benhamou S., Sarasin A. ERCC2/XPD gene polymorphisms and cancer risk // Mutagenesis. 2002. Vol. 17. P. 463-469. DOI: 10.1093/mutage/17.6.463.
- Broughton B.C., Steingrimsdottir H., Lehmann A.R. Five polymorphisms in the coding sequence of the Xeroderma pigmentosum group D gene // Mutat. Res.1996. Vol. 362. P. 209-211.
- Dey S. et al. Risk factors according to estrogen receptor status of breast cancer patients in Trivandrum, South India // International journal of cancer. 2009. Vol. 125(7). P. 1663-1670. DOI: 10.1002/ijc.24460.
- Fortner R.T. et al. Parity, breastfeeding, and breast cancer risk by hormone receptor status and molecular phenotype: results from the Nurses' Health Studies // Breast Cancer Research. 2019. Vol. 21, № 1. P. 1-9.
- Gram I.T. et al. Smoking and breast cancer risk by race/ethnicity and oestrogen and progesterone receptor status: the Multiethnic Cohort (MEC) study // Int. J. Epidemiol. 2019. Vol. 48, № 2. P. 501-511.
- Guo W. et al. Adiposity and breast cancer risk in postmenopausal women: results from the UK Biobank prospective cohort // International journal of cancer. 2018. Vol. 143, № 5. P. 1037-1046.
- Ito S. et al. XPG stabilizes TFIIH, allowing transactivation of nuclear receptors: Implications for Cockayne syndrome in XP-G/CS patients // Mol. Cell. 2007. Vol. 26. Art. 231.
- Kurfurstova D. et al. DNA damage signalling barrier, oxidative stress and treatment-relevant DNA repair factor alterations during progression of human prostate cancer // Mol. Oncol. 2016. Vol. 10. P. 879-894. DOI: 10.1016/j.molonc.2016.02.005.
- Lehmann B.D. et al. Identification of human triple-negative breast cancer subtypes and preclinical models for selection of targeted therapies // Journal of Clinical Investigation. 2011. Vol. 121, № 7. P. 2750-2767. DOI: 10.1172/jci45014.
- Liedke C. et al. Response to neoadjuvant therapy and long-term survival in patients with triple-negative breast cancer // J. Clin. Oncol. 2008. Vol. 26. P. 1275-1281.
- Malik S.S. et al. An insight into clinical outcome of XPG polymorphisms in breast cancer // Molecular Biology Reports. 2018. Vol. 45(6). P. 2369-2375. DOI: 10.1007/s11033-018-4401-7.
- Na N. et al. Association between ERCC5 gene polymorphisms and breast cancer risk // Int. J. Clin. Exp Pathol. 2015. Vol. 8, № 3. Art. 3192.
- Obeagu E.I., Obeagu G.U. Breast cancer: A review of risk factors and diagnosis // Medicine (Baltimore). 2024. Vol. 103, № 3. Art. e36905. DOI: 10.1097/MD.0000000000036905.
- Picon-Ruiz M. et al. Obesity and adverse breast cancer risk and outcome: mechanistic insights and strategies for intervention // CA: a cancer journal for clinicians. 2017. Vol. 67, № 5, P. 378-397.
- Reiner A.S. et al. Smoking, Radiation Therapy, and Contralateral Breast Cancer Risk in Young Women // JNCI: Journal of the National Cancer Institute. 2022. Vol. 114(4). P. 631-634. DOI: 10.1093/jnci/djab047.
- Reynolds P. Smoking and Breast Cancer // J. Mammary Gland. Biol. Neoplasia. 2013. Vol. 18, № 1. P. 15-23.
- Roberts M.R. et al. Singlenucleotide polymorphisms in DNA repair genes and association with breast cancer risk in the web study // Carcinogenesis. 2011. Vol. 32. P. 1223-1230.
- Rudolph A., Chang-Claude J., Schmidt M.K. Geneenvironment interaction and risk of breast cancer // Br. J. Cancer. 2016. Vol. 114, № 2. P. 125-133.
- Sambrook J., Fritsch E.F., Maniatis T. Molecular Cloning. A Laboratory Manual. N.Y.: Cold Spring Harbor Lab., 1989. 1659 p.
- Samson M. et al. XPD Lys751Gln increases the risk of breast cancer // Oncol. Lett. 2011. Vol. 2. P. 155-159.
- Siegel R.L et al. Cancer Statistics // CA Cancer J. Clin. 2021. Vol. 71, № 1. P. 7-33.
- Smolarz B. et al. Single nucleotide polymorphisms (SNPs) of ERCC2, hOGG1, and XRCC1 DNA repair genes and the risk of triple-negative breast cancer in Polish women // Tumour Biol. 2014. Vol. 35, № 4. P. 34953502.
- Smolarz B. et al. Polymorphism of DNA repair genes in breast cancer // Oncotarget. 2019. Vol. 10, № 4. DOI: 10.18632/oncotarget.265688.
- Sun Y.S. et al. Risk Factors and Preventions of Breast Cancer // Int. J. Biol. Sci. 2017. Vol. 13, № 11. P. 1387-1397. DOI: 10.7150/ijbs.21635.
- Sung H.J. et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries // CA: a cancer journal for clinicians. 2021. Vol. 71, № 3. P. 209-249.
- Torgovnick A., Schumacher B. DNA repair mechanisms in cancer development and therapy // Front Genet. 2015. Vol. 6. Art. 157. DOI: 10.3389/fgene.2015.00157.


