Изучение структуры 2-(гидроксиимино)-1-(1-нафтил)этанона методом РСА
Автор: Старновская Е.С, Гавико В.С, Рыбакова А.В, Криночкин А.П., Шабунина О.В., Красноперова К.Д., Ватолина С.Е., Юртаева А.А., Поспелова Т.А., Копчук Д.С., Зырянов Г.В.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 3 т.17, 2025 года.
Бесплатный доступ
В рамках работы изучена структура 2(гидроксиимино)1(1нафтил)этанона ме тодом РСА. Ароматическая система 2(гидроксиимино)1(1нафтил)этанона плоская и характери зуется поворотом атомов гидроксииминоацетильного фрагмента относительно плоскости цикла на 31°. Выход карбонильного атома кислорода из данной плоскости составляет 0,714 Å, тогда как вы ход гидроксильного атома кислорода – 1,237 Å. Паркетностопочная упаковка молекул в кристалле обусловлена системой межмолекулярных водородных связей типа СН…О с участием атома ки слорода гидроксильной или карбонильной групп, а также водородными связями O(2)H…O(1) и O(2)H…N(1). Результаты рентгеноструктурного анализа зарегистрированы в Кембриджской базе структурных данных под номером CCDC 2445219.
2-(гидроксиимино)-1-(1-нафтил)этанон, РСА, нитрозирование, 1-ацетилнафталин
Короткий адрес: https://sciup.org/147251992
IDR: 147251992 | УДК: 548.3 | DOI: 10.14529/chem250316
Study of the structure of 2-(hydroxyimino)-1-(1-naphthyl)ethanone by X-ray diffraction analysis
In the present study the structure of 2(hydroxyimino)1(1naphthyl)ethanone has been investigated by Xray diffraction. The aromatic system of 2(hydroxyimino)1(1naphthyl)ethanone is planar; it is characterized by rotation of the hydroxyiminoacetyl fragment atoms in relation to the plane of the ring by 31°. The deviation of the carbonyl oxygen atom from this plane is 0.714 Å, while the deviation of the hydroxyl oxygen atom is 1.237 Å. The parquetstack packing of molecules in the crystal is due to the system of intermolecular hydrogen bonds of the CH…O type with participation of the oxygen atom of the hydroxyl or carbonyl groups, as well as the O(2) H…O(1) and O(2) H…N(1) hydrogen bonds. The results of Xray diffraction analysis have been registered in the Cambridge Crystallographic Data Center under the number CCDC 2445219.
Текст научной статьи Изучение структуры 2-(гидроксиимино)-1-(1-нафтил)этанона методом РСА
Благодарности. Работа проведена с использованием оборудования Центра коллективного пользования «Спектроскопия и анализ органических соединений» (ЦКП «САОС») Института Органического Синтеза УрО РАН, а также оборудования Центра коллективного пользования «Испытательный центр нанотехнологий и перспективных материалов» Института физики металлов УрО РАН. Спектральные данные получены в Лаборатории комплексных исследований и экспертизы органических материалов Центра коллективного пользования уникальным оборудованием Уральского федерального университета,
Работа выполнена при поддержке Министерства науки и высшего образования Российской Федерации (тема № 124020200072-0).
Производные изонитрозоацетофенонов являются важными синтонами для дальнейшего построения различных гетероциклов, в частности, 1,2,4-триазинов [1–4], пиразинов [5, 6], 2 H -1,4-оксазинов [7] и др. Также представляют интерес своей биологической активностью металлоком-плексы на основе данных соединений [8]. Основным методом их получения является реакция нитрозирования соответствующих ацетильных производных (гетеро)ароматических соединений, которая может быть реализована в кислых [9] или основных [10] условиях. Что касается непосредственно объекта, рассматриваемого в данной работе (2-(гидроксиимино)-1-(нафтил)этанона), то для его синтеза ранее использовались взаимодействие (1-нафтил)глиоксаля с гидроксиламином [11], а также нитрозирование 1-ацетилнафталина в кислых условиях [12]. В данной работе нами впервые рассмотрена кристаллическая структура данного соединения.
Экспериментальная часть
Спектр ЯМР 1H записан на спектрометре Bruker Avance-400 (частота 400 МГц), внутренний стандарт – SiMe 4 . Масс-спектр (тип ионизации – электроспрей) записан на приборе Agilent 6545
Q-TOF LC-MS фирмы «Agilent Technologies» (США). Элементный анализ выполнен на CHN анализаторе РЕ 2400 II фирмы Perkin Elmer (США).
Синтез 2-(гидроксиимино)-1-(1-нафтил)этанона 1 выполнен по процедуре, описанной ранее [2] для схожих соединений. Выход продукта по двум стадиям синтеза составляет 55 %. Спектр ЯМР 1Н: 7,56–7,63 (м, 3Н, нафтил), 7,82 (дд, 1H, 3 J 7,2 Гц, 4 J 1,2 Гц, нафтил), 8,00–8,05 (м, 1H, нафтил), 8,07 (с, 1Н, Н-2), 8,08–8,16 (м, 2Н, нафтил), 12,71 (уш. с, 1Н, OH). MS ESI: m/z ( I , %): 200,07 (100) [M+H]+. Найдено, %: C 72,26; H 4,67; N 6,92. Вычислено, %: C 72,35; H 4,55; N 7,03.
Рентгеноструктурный анализ (РСА) проведен на автоматическом четырехкружном дифрактометре Rigaku XtaLAB Synergy с CCD-детектором HyPix-6000HE и источником рентгеновского излучения PhotonJet по стандартной процедуре (MoKα-излучение, графитовый монохроматор, ω-сканирование с шагом 1°) при T = 295(2) K. Была применена эмпирическая поправка на поглощение. Данные измеренных отражений проиндексированы, интегрированы и масштабированы с использованием пакета программ CrysAlisPro [13]. Структуры расшифрованы методом внутренней фазировки по программе SHELXT [14] и уточнены методом наименьших квадратов по F2 с использованием программы SHELXL [15]. Расшифровка и уточнение структуры проведены в программной оболочке Olex2 [16]. Неводородные атомы уточнены в анизотропном приближении. Атомы водорода при атомах кислорода выявлены из разностных рядов Фурье. Все остальные атомы водорода помещены в вычисленные положения в соответствии со стереохимическими критериями и уточнены по «схеме наездника». Результаты рентгеноструктурного анализа зарегистрированы в Кембриджской базе структурных данных под номером CCDC 2445219. Эти данные находятся в свободном доступе и могут быть запрошены по адресу Основные кристаллографические данные и результаты уточнения структуры 2-(гидроксиимино)-1-(нафтил)этанона приведены в табл. 1.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структуры 2-(гидроксиимино)-1-(нафталенил)этанона
|
Параметр |
Значение |
|
Формула |
C 12 H 9 NO 2 |
|
М |
199,20 |
|
Сингония |
monoclinic |
|
Пр. группа |
P 2 1 /c |
|
a , Å |
18,8114(5) |
|
b, Å |
3,87210(10) |
|
c, Å |
13,8287(3) |
|
α, град. |
90 |
|
β, град. |
109,652(3) |
|
γ, град. |
90 |
|
V , Å3 |
948,61(4) |
|
Z |
4 |
|
ρ выч , г/см3 |
1,395 |
|
µ , мм–1 |
0,096 |
|
F (000) |
416,0 |
|
Размер кристалла, мм |
0,707 × 0,261 × 0,063 |
|
Область сбора данных по 2 θ , град. |
4,598–59,166 |
|
Интервалы индексов отражений |
–25 ≤ h ≤ 25; –5 ≤ k ≤ 5; –18 ≤ l ≤ 18 |
|
Измерено отражений |
34582 |
|
Независимых отражений |
2454 [R int = 0,0592; R sigma = 0,0247] |
|
Переменных уточнения |
137 |
|
GOOF |
1,054 |
|
R -факторы по F 2 > 2 σ ( F 2) |
R 1 = 0,0388; w R 2 = 0,0979 |
|
R -факторы по всем отражениям |
R 1 = 0,0523; w R 2 = 0,1074 |
|
Остаточная электронная плотность (min/max), e /Å3 |
0,13/–0,18 |
Обсуждение результатов
Синтез 2-(гидроксиимино)-1-(1-нафтил)этанона ( 1 ) был выполнен с использованием в качестве исходного соединения коммерчески доступного 1-ацетилнафталина ( 2 ), при этом была применена описанная ранее процедура [2] (схема). Так, взаимодействие натриевой соли ацетилпро-изводного 2 как С-Н-кислоты, полученной in situ действием этилата натрия, с изопропилнитри-том приводит к натриевой соли целевого соединения ( 3 ), которая легко выделяется из реакционной массы в виде осадка. На последующей стадии взаимодействие с ледяной уксусной кислотой позволяет получить 2-(гидроксиимино)-1-(нафтил)этанон 1 ; в данной работе нами впервые представлены данные спектра ЯМР этого соединения. Его кристаллы, пригодные для РСА, были получены в результате медленного упаривания раствора в хлороформе.
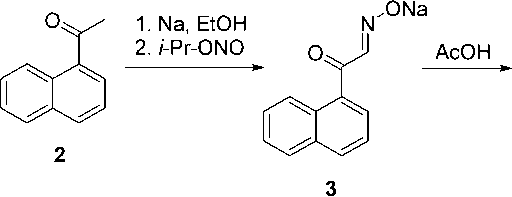
Схема синтеза 2-(гидроксиимино)-1-(1-нафтил)этанона (1)
По данным рентгеноструктурного анализа 2-(гидроксиимино)-1-(1-нафтил)этанон кристаллизуется в моноклинной сингонии с центросимметричной пространственной группой P 2 1 /c. Принятая в структурном эксперименте нумерация атомов представлена на рис. 1.
Все атомы ароматической системы ожидаемо лежат в одной плоскости, атомы гидроксииминоацетильного фрагмента повернуты относительно плоскости цикла на 31°, при этом выход карбонильного атома кислорода из данной плоскости составляет 0,714 Å, выход гидроксильного атома кислорода – 1,237 Å (рис. 2). Следует отметить, что подобная геометрия является характерной для аналогичных структур, известных в литературе [17, 18] и найденных нами в Кембриджской Структурной Базе Данных (Cambridge Structural Database . Однако, введение в ароматический цикл гидроксильной или нитро-групп, а также появление кристаллизационной молекулы воды, по-видимому, существенно влияет на межмолекулярные взаимодействия в кристалле, за счет которых атомы гидроксииминоацетильного фрагмента лежат практически в одной плоскости с циклической системой [19].
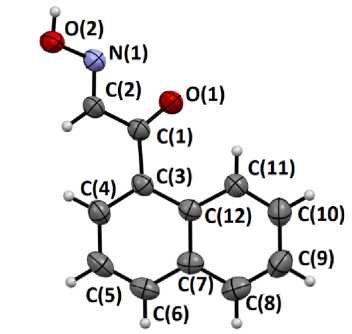
Рис. 1. Данные РСА 2-(гидроксиимино)-1-(1-нафтил)этанона в тепловых эллипсоидах 50 % вероятности и принятая в структурном эксперименте нумерация атомов
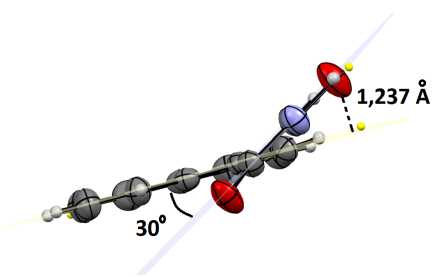
Рис. 2. Пространственное расположение атомов в молекуле 2-(гидроксиимино)-1-(1-нафтил)этанона
Структурная самоорганизация молекул в кристалле 1 обусловлена системой межмолекулярных водородных связей (табл. 2), среди которых можно выделить слабые водородные связи С-Н…О с участием атома кислорода гидроксильной или карбонильной групп.
Таблица 2
Геометрические параметры водородных связей в кристалле 2-(гидроксиимино)-1-(1-нафтил)этанона
|
D-H^A |
d D-H, А |
d H.A, А |
d D.A, А |
< D-H...A, ° |
|
С(5)-Н…О(1) |
0,93(0) |
2,46 |
3,37 |
164,0(8) |
|
С(2)-Н…О(2) |
0,93(0) |
2,49 |
3,42 |
171,5(2) |
|
O(2)-H…O(1) |
0,82(0) |
2,09 |
2,85 |
153,7(0) |
|
O(2)-H…N(1) |
0,82(0) |
2,46 |
3,07 |
131,5(9) |
При этом карбонильная группа образует одноточечный гетеросинтон, а гидроксильная группа – двухточечный гетеросинтон (рис. 3). Кроме того, водород гидроксильной группы участвует в образовании бифуркатной (трёхцентровой) водородной связи, в которой взаимодействие O(2)-H…O(1) более короткое (2,09 Å) и называется основным компонентом, а взаимодействие O(2)-H…N(1) более длинное (2,46 Å) – второстепенным компонентом связи [20]. Таким образом, за счёт системы межмолекулярных связей молекулы в кристалле 1 укладываются в стопки вдоль оси b (рис. 4), расположенные относительно друг друга под углом ~ 47 °, что приводит к их паркетно-стопочной («ёлочной») упаковке (рис. 5).
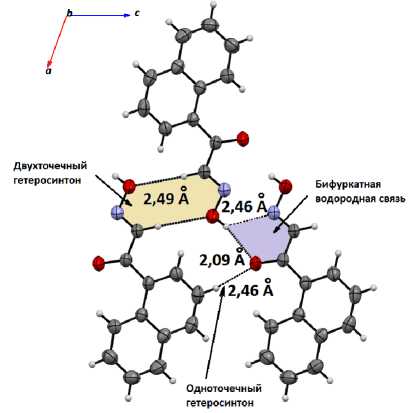
Рис. 3. Водородно-связанные мотивы в кристалле соединения 1 (проекция вдоль оси b )
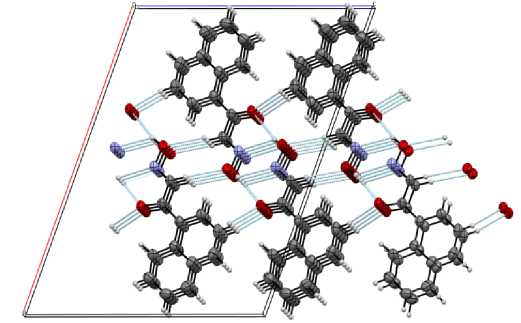
Рис. 4. Н-связанные стопки вдоль оси b в структуре 1 (водородные связи показаны пунктирными линиями)
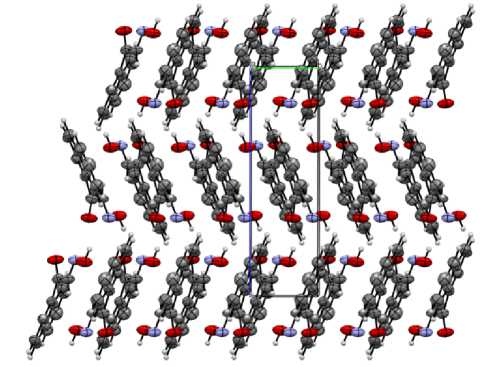
Рис. 5. Паркетно-стопочная («ёлочная») упаковка молекул в кристалле соединения 1 (проекция вдоль оси а )
Нами также замечено, что для аналогичных структур гидроксииминоарилэтанонов(пропанона), описанных в литературе, характерными также являются С-Н…О, O-H…N и O-H…O типы водородных связей [17–19], формирующих «ёлочную» или слоистую упаковку молекул в кристалле.
Заключение
Таким образом, нами изучена кристаллическая структура 2-(гидроксиимино)-1-(1-нафтил)этанона методом РСА. Супрамолекулярная структура в кристалле 1 обусловлена системой межмолекулярных водородных связей типа С-Н…О с участием атома кислорода гидроксильной или карбонильной групп, а также водородные связи O(2)-H…O(1) и O(2)-H…N(1). За счёт вышеперечисленных межмолекулярных связей молекулы укладываются в стопки вдоль оси b , формируя паркетно-стопочную упаковку.


