Изучение структуры гидрохлорида 2-фенилхиназолин-4(3h)-она методом РСА
Автор: Эмилия Владимировна Носова, Василий Семёнович Гавико, Анастасия Владимировна Рыбакова, Алексей Петрович Криночкин, Юлия Владимировна Пермякова, Алина Андреевна Юртаева, Александра Сергеевна Маркина, Анастасия Сергеевна Алексеева, Наталья Валерьевна Словеснова, Татьяна Александровна Поспелова, Дмитрий Сергеевич Копчук, Григорий Васильевич Зырянов
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 4 т.17, 2025 года.
Бесплатный доступ
В рамках работы изучена структура гидрохлорида 2-фенилхиназолин-4(3Н)-она методом РСА, в т. ч. в сравнении с таковой для соответствующей нейтральной молекулы. При этом обнаружена более сложная упаковка молекул в кристалле в случае гидрохлорида. Результаты рентгеноструктурного анализа зарегистрированы в Кембриджской базе структурных данных под номером CCDC 2448813. Для описываемого гидрохлорида следует отметить межмолекулярные водородные связи, реализующиеся в псевдослое: C(8)-H…Cl(1), C(8)-H…O(1), N(1) H…Cl(1). Кроме того, между фенильными заместителями соседних молекул наблюдается π стэкинг. Слоистая структура стабилизируется за счет слабых нецентрированных взаимодействий электронно-дефицитного атома углерода хиназолинонового цикла, связанного с двумя электроноакцепторными атомами азота, и анионом хлора (C(2)…Cl– 3,40(9) Å). Подобные нековалентные взаимодействия между электронно-дефицитными ароматическими системами и анионами согласно имеющимся в литературе теоретическим и экспериментальным научным исследованиям энергетически выгодны и получают значительное признание ввиду того, что играют важную роль для многих ключевых химических и биологических процессов.
Хиназолин-4(3Н)-он, гидрохлорид, РСА
Короткий адрес: https://sciup.org/147252519
IDR: 147252519 | УДК: 547.856.1 | DOI: 10.14529/chem250407
Study of the structure of 2-phenylquinazolin-4(3h)-one hydrochloride by X-ray diffraction analysis
The structure of 2-phenylquinazolin-4(3H)-one hydrochloride was investigated in the study context using X-ray crystallography, including the comparison to the structure of the corresponding neutral molecule., At that, more complex packing of molecules in the crystal was observed in the case of hydrochloride. The results of X-ray crystallography analysis were registered in the Cambridge Structural Data Base under the number CCDC 2448813. For the described hydrochloride, intermolecular hydrogen bonds should be noted, realized in the pseudo-layer: C(8)-H…Cl(1), C(8)-H…O(1), N(1) H…Cl(1). In addition, the π stacking was observed between the phenyl substituents of adjacent molecules. The layered structure was stabilized by weak non-centered interactions between the electron-deficient carbon atom of the quinazolinone cycle, bonded to two electron-acceptor nitrogen atoms, and the chloride anion (C(2)…Cl– 3.40(9) Å). According to theoretical and experimental studies in the literature, such non-covalent interactions between electron-deficient aromatic systems and anions are energetically favorable and have received significant recognition due to their importance in many chemical and biological key processes.
Текст научной статьи Изучение структуры гидрохлорида 2-фенилхиназолин-4(3h)-она методом РСА
Благодарности. Работа проведена с использованием оборудования Центра коллективного пользования «Спектроскопия и анализ органических соединений» Института органического синтеза УрО РАН, а также оборудования Центра коллективного пользования «Испытательный центр нанотехнологий и перспективных материалов» Института физики металлов УрО РАН. Спектральные данные получены в Лаборатории комплексных исследований и экспертизы органических материалов Центра коллективного пользования уникальным оборудованием Уральского федерального университета,
Работа выполнена при поддержке Министерства науки и высшего образования Российской Федерации (тема № 124020500044-4).
2-Арилхиназолин-4( 3H )-оны представляют собой важные реагенты для синтеза на их основе биологически активных производных и флуорофоров хиназолинового ряда [1–3]. В последние годы большое внимание уделяется разработке синтетических подходов к 4-замещенным либо [ c ]-аннелированным хиназолинам, основанных на модификации 2-арилхиназолин-4( 3H )-онов [4–6]. Имеется значительный интерес и к самим 2-арилпроизводным хиназолин-4-онов, поскольку в их ряду выявлены ингибиторы различных ферментов [7–9].
В связи с этим структурные особенности 2-фенилхиназолин-4-она и его солевых производных заслуживают внимания синтетиков, изучающих пути создания новых гетероциклических соединений бензодиазинового ряда. В данной работе нами изучена структура гидрохлорида 2-фенилхиназолин-4( 3H )-она методом РСА, в т.ч. в сравнении с таковой для соответствующей нейтральной молекулы.
Экспериментальная часть
Спектр ЯМР 1H записаны на спектрометре Bruker Avance-400 (400 МГц, внутренний стандарт – SiMe 4 ). Масс-спектр (тип ионизации – электроспрей) записан на приборе Agilent 6545 Q-TOF LC-MS фирмы «Agilent Technologies» (США). Элементный анализ выполнен на CHN анализаторе РЕ 2400 II фирмы Perkin Elmer (США). Все используемые реагенты коммерчески доступны.
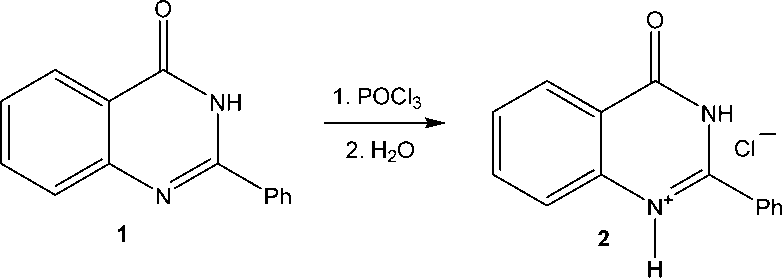
Гидрохлорид 2-фенилхиназолин-4( 3H )-она (2). К хиназолинону 1 (296 мг, 1,33 ммоль) добавляли POCl3 (1,74 мл, 18,65 ммоль). Реакционную массу кипятили 2 ч на установке с хлоркальциевой трубкой, после чего охлаждали и выливали в лёд. Смесь интенсивно перемешивали, сформировавшийся осадок отфильтровывали и сушили. Выход 70%. Спектр ЯМР 1H (400 МГц, DMSO- d 6 , м. д., J/Гц): 7,56–7,62 (м, 3Н); 7,63–7,67 (м, 1Н); 7,84–7,92 (м, 2Н); 8,15–8,20 (м, 3Н). MS ESI: m/z ( I , %): 223,09 (100) [M-Cl]+. Найдено, %: C 65,12; H 4,43; N 10,72. Вычислено, %: C 65,00; H 4,29; N 10,89.
Рентгеноструктурный анализ (РСА) проведен на автоматическом четырехкружном дифрактометре Rigaku XtaLAB Synergy с CCD-детектором HyPix-6000HE и источником рентгеновского излучения PhotonJet по стандартной процедуре (MoKα-излучение, графитовый монохроматор, ω-сканирование с шагом 1°) при T = 295(2) K. Была применена эмпирическая поправка на поглощение. Данные измеренных отражений проиндексированы, интегрированы и масштабированы с использованием пакета программ CrysAlisPro [10]. Структуры расшифрованы методом внутренней фазировки по программе SHELXT [11] и уточнены методом наименьших квадратов по F2 с использованием программы SHELXL [12]. Расшифровка и уточнение структуры проведены в программной оболочке Olex2 [13]. Неводородные атомы уточнены в анизотропном приближении. Атомы водорода при атомах кислорода выявлены из разностных рядов Фурье. Все остальные атомы водорода помещены в вычисленные положения в соответствии со стереохимическими критериями и уточнены по «схеме наездника». Результаты рентгеноструктурного анализа зарегистрированы в Кембриджской базе структурных данных под номером CCDC 2448813. Эти данные находятся в свободном доступе и могут быть запрошены по адресу Основные кристаллографические данные и результаты уточнения структуры гидрохлорида 2-фенилхиназолин-4(3H)-она приведены в табл. 1, избранные длины связей и валентные углы показаны в табл. 2.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структуры гидрохлорида 2-фенилхиназолин-4(3 H )-она
|
Параметр |
Значение |
Параметр |
Значение |
|
Формула |
C 14 H 11 ClN 2 O |
ρ (выч.), г/см3 |
1,451 |
|
М |
258,70 |
µ , мм–1 |
0,310 |
|
Сингония |
monoclinic |
F (000) |
536,0 |
|
Пр. группа |
P 2 1 /c |
Размер кристалла (мм) |
0,357 × 0,167 × 0,072 |
|
a , Å |
12,1983(2) |
Область сбора данных по 2 θ , град. |
6,112–59,158 |
|
b, Å |
7,96110(10) |
Интервалы индексов отражений |
–16 ≤ h ≤ 16; –10 ≤ k ≤ 11; –16 ≤ l ≤ 16 |
|
c, Å |
12,3156(3) |
Измерено отражений |
48410 |
|
α, град. |
90 |
Независимых отражений |
3121 [R int = 0,0539, R sigma = 0,0255] |
|
β, град. |
98,174(2) |
Переменных уточнения |
167 |
|
γ, град. |
90 |
GOOF |
1,020 |
|
V , Å3 |
1183,84(4) |
R -факторы по F 2 > 2 σ ( F 2) |
R 1 = 0,0370; wR 2 = 0,1075 |
|
Z |
4 |
R -факторы по всем отражениям |
R 1 = 0,0523; wR 2 = 0,1159 |
|
Остаточная электронная плотность (min/max), e /Å3 |
0,24/–0,20 |
Таблица 2
Длины связей и валентные углы в структурах 1 и 2
|
Связь |
d , Å |
Угол |
ω , град |
|
O1–C1 |
1,2165(16) |
C2–N2–C3 |
122,13(11) |
|
N2–C3 |
1,3971(16) |
C2–N1–C1 |
124,98(11) |
|
N2–C2 |
1,3171(16) |
C4–C3–N2 |
119,08(11) |
|
N1–C2 |
1,3381(16) |
C8–C3–N2 |
119,83(11) |
|
N1–C1 |
1,4029(16) |
C8–C3–C4 |
121,06(12) |
|
C3–C4 |
1,3955(17) |
C3–C4–C1 |
119,68(12) |
|
C3–C8 |
1,3938(18) |
C3–C4–C5 |
119,16(12) |
|
C4–C1 |
1,4577(18) |
C5–C4–C1 |
121,16(11) |
|
C4–C5 |
1,3974(19) |
N2–C2–N1 |
119,83(12) |
|
C2–C9 |
1,4698(18) |
N2–C2–C9 |
119,99(11) |
|
C9–C14 |
1,387(2) |
N1–C2–C9 |
120,13(11) |
|
C9–C10 |
1,394(2) |
O1–C1–N1 |
120,34(12) |
|
C8–C7 |
1,3791(19) |
O1–C1–C4 |
125,42(12) |
|
C5–C6 |
1,369(2) |
N1–C1–C4 |
114,24(10) |
|
C14–C13 |
1,384(2) |
C14–C9–C2 |
119,69(12) |
|
C10–C11 |
1,386(2) |
C14–C9–C10 |
120,68(14) |
|
C7–C6 |
1,388(2) |
C10–C9–C2 |
119,61(13) |
|
C13–C12 |
1,384(3) |
C7–C8–C3 |
118,26(12) |
|
C11–C12 |
1,377(3) |
C6–C5–C4 |
119,85(13) |
Обсуждение результатов
Одно из первых упоминаний о синтезе 2-фенилхиназолин-4(3H)-она (1) встречается в работе [14], структура данного соединения методом РСА была подтверждена другими авторами [15]. Супрамолекулярная структура полученного нами согласно схеме гидрохлорида 2-фенилхиназолин-4(3H)-она (2) ранее не была описана в литературе. Кроме того, представляет интерес рассмотреть её в сравнении с самоорганизацией молекул в кристалле 2-фенилхиназолин-4(3H)-она. С этой целью мы проанализировали имеющиеся в Кембриджской Структурной Базе Данных (Cambridge Structural Database рентгеноструктурные данные фенилхиназолинона (CCDC 2123836 [15]).
Как в случае нейтральной молекулы фенилхиназолинона 1, так и в случае его гидрохлорида 2 все атомы, включая атом кислорода карбонильной группы, конденсированной бициклической системы хиназолинона лежат в одной плоскости. При этом угол поворота фенильного заместителя относительно плоскости гетероцикла в рассматриваемых структурах незначительно отличается и составляет 35,8(8)° для соединения 1 и 38,1(7)° для соединения 2. Кватернизация по атому азота N-1 характеризуется образованием более длинной связи N(2)-H (0,89(6) Å), чем связь N(1)-H (0,86(0) Å для соединений 1 и 2) в 3-м положении гетероцикла.
В кристалле гидрохлорида 2 расстояние N(2)-H…Cl(1) составляет 2,24(7) Å) (рис. 1), при этом ионная пара стабилизирована слабой водородной связью C(8)-H…Cl(1) ( d H…Cl составляет 2,82(3) Å, d C(8)…Cl(1) равно 3,57(3) Å, ∠ C(8)HCl(1) 138,5°).
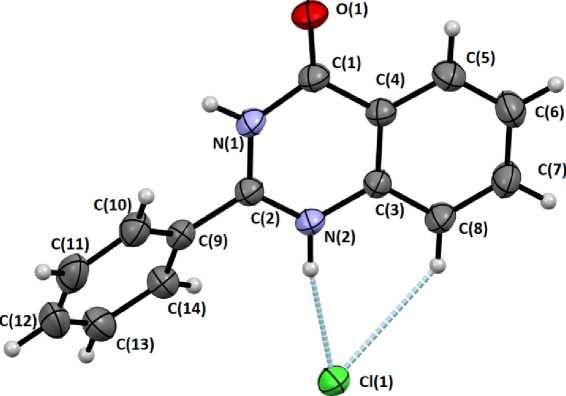
Рис. 1. Данные РСА гидрохлорида 2 в тепловых эллипсоидах 50% вероятности и принятая в структурном эксперименте нумерация атомов (пунктирными линиями показаны водородные связи в кристалле)
Молекулы соединения 2 за счет системы водородных связей (табл. 3) формируют бесконечные цепи, ориентированные вдоль кристаллографической оси b , которые посредством π-стэкинга между фенильными заместителями укладываются в псевдослои (рис. 2). При этом π-стэкинг характеризуется расстояниями С(11)…С(11) 3,24(1) Å и С(12)…С(13) 3,28(9) Å, что значительно меньше суммы ванн-дер-ваальсовых радиусов атомов углерода [16]. Расстояния между центроидами ароматических систем составляет 4,69(9) (для π-стэкинга с расстоянием С(12)…С(13)) и 5,16(8) Å (для π-стэкинга с расстоянием С(11)…С(11)), угол между нормалью к плоскости и плоскостью цикла составляет 36 и 35° соответственно.
Таблица 3
Геометрические параметры водородных связей для структуры 2
|
D-H…A |
dD-H |
dH…A, Å |
dD…A, Å |
∠ DHA, ° |
|
C(8)-H…O(1) |
0,93(0) |
2,58(8) |
3,22(6) |
126,3(0) |
|
N(1)-H…Cl(1) |
0,86(0) |
2,37(5) |
3,20(7) |
163,1(3) |
Слоистая структура в кристалле 2 создаётся посредством коротких контактов между электронно-дефицитным ароматическим атомом углерода, связанным с двумя электроноакцепторными атомами азота, и анионом хлора: расстояние C(2)…Cl– составляет 3,40(9) Å (рис. 3) при сумме радиусов Ван-дер-Ваальса соответствующих атомов 3,45 Å. Известно [17], что контакт считается взаимодействием, если расстояние между галогеном и его партнером составляет от 2,2 Å до расстояния контакта Ван-дер-Ваальса. Расстояние от аниона Cl– до центра пиримидинового цикла равно 3,62(0) Å и характеризует данный контакт как нецентрированное слабое взаимодействие (расстояние до 4 Å используется как мера возможного взаимодействия галогенида с ароматическим кольцом [18]). В работах [18–20] представлены данные по распознаванию галогенид-анион…π взаимодействий, т. е. нековалентных сил между электронно-дефицитными ароматическими системами и анионами. Согласно приведенным данным такие взаимодействия энергетически выгодны и получают высокое признание, потому что их ключевая роль отмечена для многих значимых химических и биологических процессов.
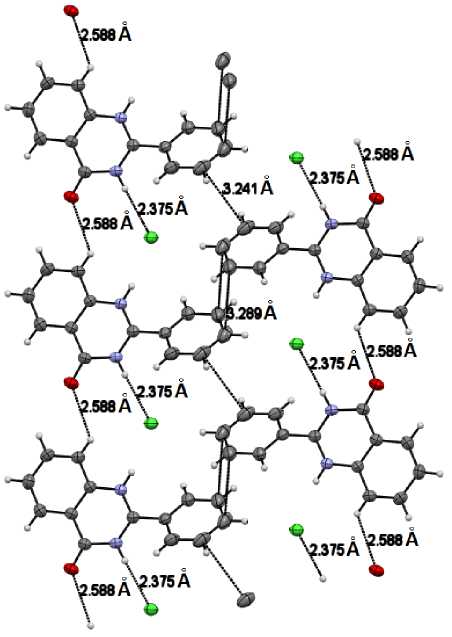
Рис. 2. Система межмолекулярных водородных связей в кристалле 2 (проекция вдоль оси с )
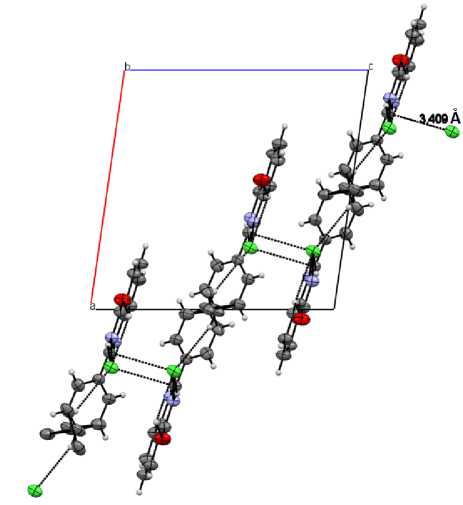
Рис. 3. Слоистая структура в кристалле 2 (проекция вдоль оси b )
В свою очередь для кристалла нейтрального соединения 1 наблюдается более простая упаковка молекул, вызванная их ассоциацией в димеры посредством межмолекулярных водородных связей N(1)-H…O(1) (1,99(8) Å) в двухточечном гетеросинтоне (рис. 4). Каждая из молекул димера участвует в образовании слабых взаимодействий С(10) Ph -H…O(1) (2,66(7) Å), формируя стопки вдоль оси а (рис. 5).
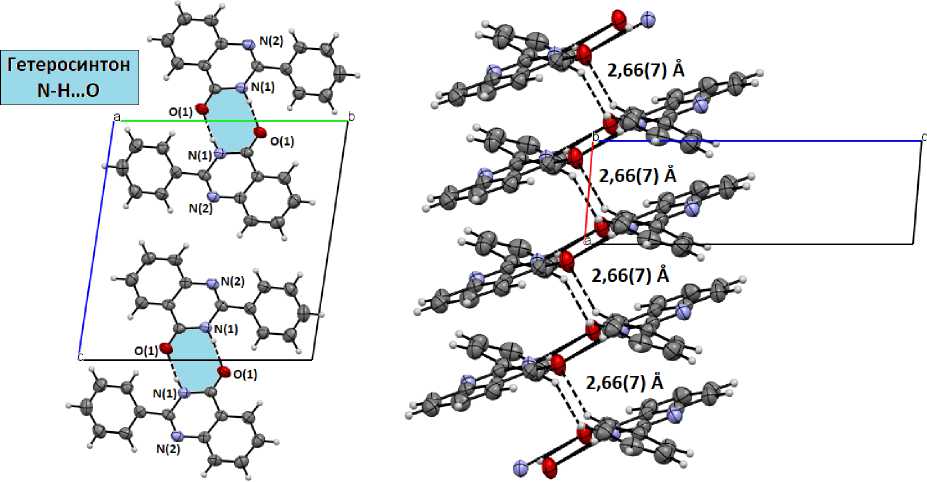
Рис. 4. Двухточечный гетеросинтон N-H…O Рис. 5. Образование слабых взаимодействий С Ph -H…O в кристалле 1 (проекция вдоль оси а ) в кристалле 1 (проекция вдоль оси b )
Заключение
Таким образом, геометрия нейтральной молекулы фенилхиназолинона 1 схожа с геометрией его гидрохлорида 2 . Что касается самоорганизации молекул в кристаллах, то в отличие от кристалла 1 для молекул кристалла 2 характерна более сложная упаковка. При этом наиболее значимыми контактами, реализующимися между молекулами соединения 2 в псевдослое, является система водородных связей C(8)-H…Cl(1), C(8)-H…O(1), N(1)-H…Cl(1), а также π-стэкинг между фенильными заместителями. Между слоями молекулы самоорганизованы за счет слабых нецен-трированных взаимодействий электронно-дефицитного атома углерода хиназолинонового цикла, связанного с двумя электроноакцепторными атомами азота, и анионом хлора (C(2)…Cl– 3,40(9) Å). Подобные взаимодействия, как показывают многие описанные в литературе теоретические и экспериментальные научные исследования, энергетически выгодны и получают значительное признание ввиду того, что играют важную роль для многих ключевых химических и биологических процессов.


